模拟酸雨对不同营养水平湖泊pH值的影响
2018-10-30陈非洲杨书运
刘 乐,蔡 敏,陈非洲①,杨书运,李 芸
(1.安徽农业大学资源与环境学院,安徽 合肥 230031;2.中国科学院南京地理与湖泊研究所湖泊与环境国家重点实验室,江苏 南京 210008)
酸雨指pH值小于5.6的雨水、冻雨、雪、雹、露等大气降水[1],它的形成主要是二氧化硫和氮氧化物在大气或水滴中转化为硫酸和硝酸所致[2]。酸雨是一种自然灾害,也是全球性环境问题,它不仅危害居民健康,腐蚀文物古迹和建筑[3],还会使河流和湖泊水体pH值逐渐下降,引起水体中浮游生物种类的减少,严重时会引起鱼虾等水生生物的死亡[4-7]。湖泊pH值也是控制沉积物磷循环[8-10]和湖泊富营养化的重要因素[11]。
北欧和北美地区酸雨对湖泊的影响在20世纪70年代中期就引起了广泛关注[4,12];1980年代已有确凿证据表明该地区有大范围的湖泊酸化现象[13];1990年代后期,随着硫排放的削减,湖泊逐渐从酸化状态中恢复[14]。中国酸雨区是继欧洲和北美之后的世界3大酸雨区之一,重酸雨区(降水年均pH值低于4.5)面积最大,长江中下游以南地区则是全球强酸雨中心[15]。与北美和北欧受酸雨影响的湖泊不同,长江中下游酸雨区内湖泊虽然也受酸雨影响,但至今没有酸化的报道。TAO等[16]研究显示过去60 a来处于酸雨区的太湖虽然酸中和能力(ANC)和pH值都显著提高,但是如果以目前的速度持续酸沉积,则流域中碱性阳离子将在2040年大幅减少,这表明酸雨会对酸雨区流域和湖泊产生潜在影响。而长江中下游地区经济发达,淡水湖泊分布众多[17],其生态安全对于维系长江水系生态平衡和促进区域经济可持续发展意义重大[18],因此预防和应对该地区湖泊面临的生态问题显得十分重要。
长江中下游酸雨区内湖泊处于亚热带地区,营养水平较高[19-20],与国际上相关研究中的湖泊类型差异较大[13,21-22],因此研究酸雨对不同营养水平湖泊的影响显得尤为重要。已有研究证实水体pH值与无机碳之间联系紧密[23-25],而营养水平增加导致的生物因子作用可能增加水体pH值[16],进而减少酸雨区高营养水平湖泊酸化现象。为了研究酸雨对不同营养水平湖泊pH值的影响,选取湖泊pH值作为观察酸雨对湖泊影响的“窗口”,研究酸雨对不同营养水平湖泊pH值的影响。首先于2016年7—8月调查了68个长江中下游湖泊的pH值及其他理化指标,比较其他环境因子和pH值的关系以及酸雨区和非酸雨区pH值的差异;其次,于2017年7—8月开展模拟实验研究酸雨对不同营养水平水体pH值的影响。通过野外调查和模拟实验的结合,探讨不同营养水平湖泊对酸雨的响应,以期为湖泊管理提供科学依据。
1 材料与方法
1.1 野外调查
根据2016年中国环境状况公报公布的数据,长江中下游酸雨区湖泊主要分布在湖南省东部、江西省大部分地区、安徽省东南部和江苏省南部;非酸雨区湖泊主要分布在湖北省、安徽省中北部和江苏省中北部。笔者以长江中下游地区为核心,选取68个湖泊为研究对象(图1),于2016年7—8月对这些湖泊进行调查。
采样点设置在湖心,用YSI 6600V2型多参数水质分析仪原位测定pH值、水温(t)、溶解氧(DO)和浊度(NTU),用透明度盘测定透明度(SD),采集上(水面下0.5 m)、中、下(湖底上0.5 m)3层的混合水样按标准化方法[26]测定总氮(TN)、铵态氮(NH4+-N)、硝态氮(NO3--N)、亚硝态氮(NO2--N)、总磷(TP)、磷酸态磷(PO43--P)、叶绿素a(Chl a)、化学需氧量(CODMn)、溶解性有机碳(DOC)和溶解性无机碳(DIC)含量。
为了分析酸雨对不同营养水平湖泊pH值的影响,选取综合营养状态指数(TLI)法[27]评价湖泊营养状态。用SD、TN、TP、Chl a和CODMn这5个指标计算各湖泊的TLI,其中TLI<30为贫营养,30≤TLI≤50为中营养,50
1.2 模拟实验
为进一步表征不同pH值酸雨对不同营养水平湖泊pH值的影响,设计模拟实验分析单次酸雨添加对不同营养水平水体pH值的影响。于2017年7—8月在位于苏州市东山镇的中国科学院太湖湖泊生态系统研究站东太湖分站(31°02′01″N,120°25′18″ E)开展实验。
1.2.1实验设计
在聚乙烯材质的实验桶(上直径87 cm,下直径77 cm,桶高95 cm)中加入5 cm厚底泥和400 L湖水(湖水经孔径为2 mm的纱网过滤后注入塑料桶)。实验时,为保证桶内水温与自然水体水温的一致性,将实验桶置于0.8 m深的池塘中,桶口离池塘水面15 cm。
实验分为低营养组(L组)和高营养组(H组)2个营养梯度进行,每个营养梯度再分别设置3个酸雨梯度(pH值为5.0、4.0和2.5)和1个空白对照(CK),共计8个处理(L-CK、L-5.0、L-4.0、L-2.5、H-CK、H-5.0、H-4.0和H-2.5),每个处理3个重复。将湖水注入实验桶后,计算其TLI指数,L组桶内湖水为中营养状态;在H组桶内加入KNO3和KH2PO4调节水体营养状态,使其为轻度富营养状态;酸雨母液按n(SO42-)∶n(NO3-)=8∶1配制[28-30],再用纯水稀释母液配制pH值为5.0、4.0和2.5的酸雨溶液,CK处理加入与酸雨等体积的纯水(pH=6.32)。酸雨的降水量以长江中下游南京、武汉、合肥3个城市2016年7月降水日的日均降水量(21.21 mm)来设计,确定降水量为20 mm。模拟降雨用喷洒方式完成,降水持续5 min。实验所用pH计型号为OHAUS®ST-300便携式pH计,配ST-320 电极使用。
1.2.2监测指标
在正式实验开始前,先进行一次预实验,在预实验阶段每隔1 h监测1次水体pH值,获取关于湖水pH值变化的规律,以确定模拟实验的监测时间点和频率。结果显示,06:00—07:00和18:00—19:00 分别是湖水pH值的低值和高值出现的时间段,4 h 1次的监测频率即可描述水体pH值的日变化。
在正式实验中,每天在06:00、10:00、14:00、18:00 和22:00监测实验水体的pH值和温度,06:00 监测完pH值后,即采集500 mL水样用于测定水体Chl a的含量,实验持续5 d。水体pH值和温度用便携式pH计原位测定,Chl a含量用丙酮萃取-分光光度计法测定。
1.3 数据分析
采用SPSS 18.0进行数据分析。首先,将湖泊的理化因子与pH值进行相关性分析,计算Pearson相关系数,筛选出与pH值相关性显著的环境因子。其次,用配对样本t检验来分析酸雨区和非酸雨区湖泊pH值,用独立样本t检验分析L组和H组水体Chl a含量差异是否显著;再次,选取实验中每天6:00的pH值进行单因素方差分析,分析实验期间(第1~5天)酸雨处理对水体pH值的影响是否显著;最后,为了比较各处理之间pH值的差异,对实验期间各处理pH值按时间计算平均值,比较各处理不同时间之间pH值的差异。研究区湖泊分布采用ArcGIS 10.2软件制图,其余图表采用Excel 2016软件制作。
2 结果与分析
2.1 长江中下游地区湖泊pH值
长江中下游68个湖泊夏季pH平均值为9.29(范围为7.79~10.42)。pH值与t和DO在0.01水平上呈显著正相关,与Chl a在0.05水平上呈显著正相关;与NTU和NO3--N含量在0.05水平上呈显著负相关,与TN和DIC含量在0.01水平上呈显著负相关;与SD、NO2--N、NH4+-N、TP、PO43--P、CODMn和DOC含量相关性不显著。
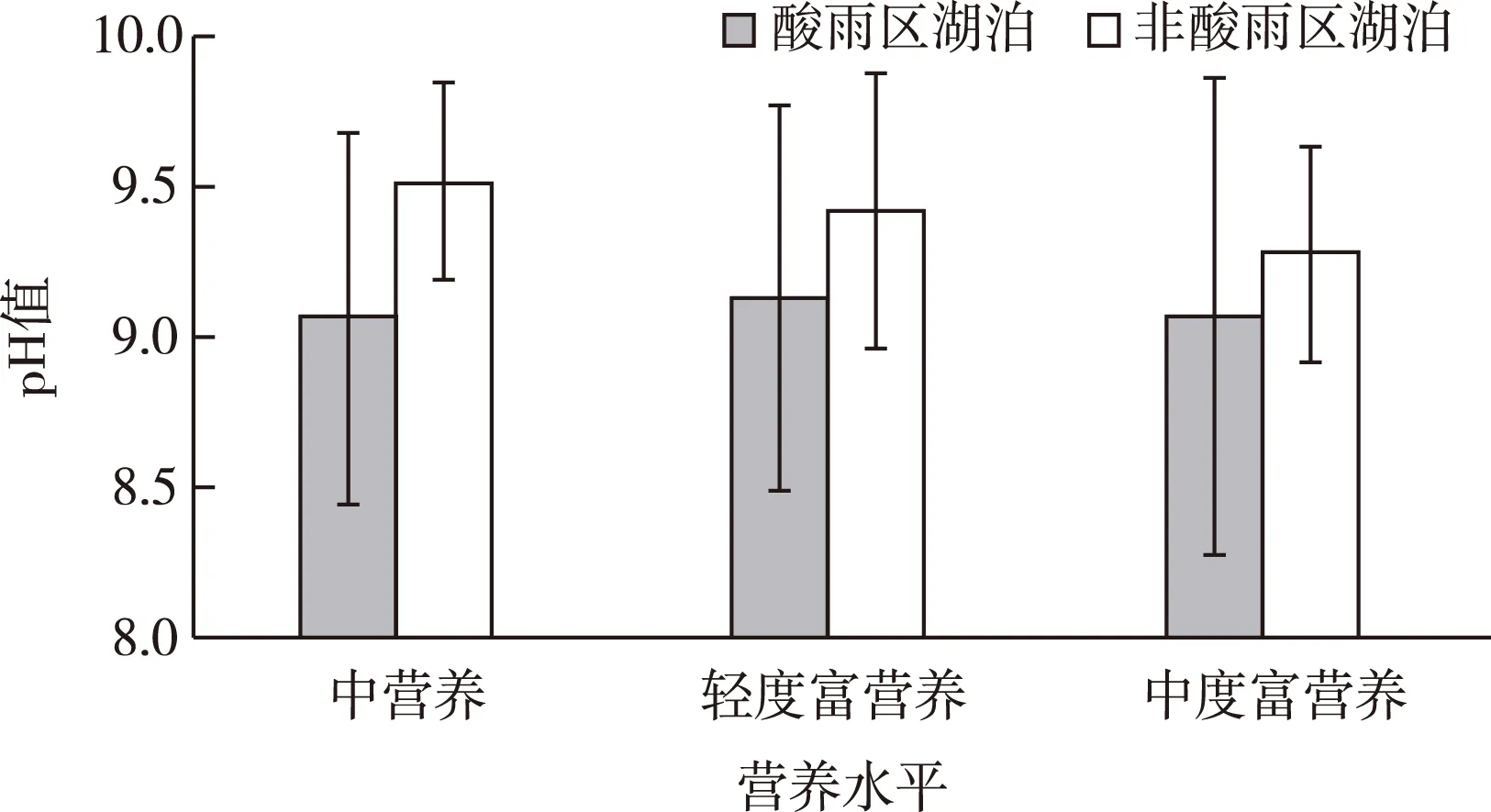
2016年夏季酸雨区湖泊pH均值(9.09)显著低于非酸雨区(9.43)(P<0.05)。根据综合营养指数将68个湖泊分为中营养、轻度富营养和中度富营养3个类型(表1~2)。在这3个类型湖泊中,酸雨区内中营养、轻度富营养和中度富营养湖泊pH值分别比非酸雨区湖泊低0.46、0.30和0.21(图2),但在3个营养水平上差异均不显著(P>0.05)。
表1酸雨区和非酸雨区不同湖泊营养水平(TLI)
Table1Lakeswithdifferenttrophiclevelsinacidrainandnon-acidrainareas1)

营养水平酸雨区湖泊非酸雨区湖泊 中营养珠湖、杨坊湖、固城湖、石臼湖、青岚湖、鄱阳湖、澄湖、天目湖、东洞庭湖、军山湖升金湖、大官湖、东龙感湖、白荡湖、武昌湖、麻塘湖、菜子湖、东巢湖、骆马湖、梁子湖、斧头湖、大冶湖、泊湖、赤湖、赛湖 轻度富营养金溪湖、黄茅潭、南漪湖、昆承湖、西洞庭湖、太泊湖、长荡湖、东太湖、淀山湖、陈家湖、漕湖、莲湖黄盖湖、朱婆湖、保安湖、西凉湖、枫沙湖、大纵湖、女山湖、白马湖、西巢湖、太白湖、赤东湖、花园湖、汤逊湖、网湖、洪泽湖、磁湖、洪湖 中度富营养梅梁湾、滆湖、阳澄湖、青山湖、瑶湖邵伯湖、高邮湖、破罡湖、沱湖、策湖、东湖、严东湖、武山湖、洋湖
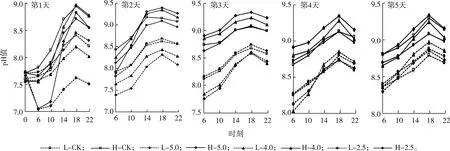
1)TLI计算采用透明度、总氮、总磷、CODMn和叶绿素a这5个指标,其中30≤TLI≤50为中营养,50 表2酸雨区和非酸雨区湖泊理化特性 Table2Physicochemicalpropertiesoflakesinacidandnon-acidrainareas 湖泊类型 SD/mρ(TN)/(mg·L-1)ρ(TP)/(mg·L-1)CODMn/(mg·L-1)ρ(Chl a)/(μg·L-1) 酸雨区-中营养0.70~1.900.29~0.580.012~0.0501.95~3.352.7~33.0 酸雨区-轻度富营养0.10~1.202.34~0.750.022~0.1542.75~5.452.5~44.0 酸雨区-中度富营养0.20~0.351.54~3.560.045~0.2593.75~9.3424.4~113.0非酸雨区-中营养0.55~2.280.49~0.940.014~0.0732.09~3.763.5~38.0非酸雨区-轻度富营养0.14~1.010.64~2.040.024~0.2683.58~9.062.5~70.8非酸雨区-中度富营养0.05~0.521.09~2.330.044~0.4394.42~8.248.4~129.4 图2 2016年夏季长江中下游酸雨区和非酸雨区不同营养水平湖泊pH值 实验期间,水温变化范围为26.77~36.7 ℃,日变化明显,高值出现在14:00。L组ρ(Chl a)平均值(8.58 μg·L-1)显著低于H组(13.87 μg·L-1,P<0.001),且在实验第2~4天与pH值呈显著正相关关系。 在不同pH值酸雨影响下,L组和H组pH值日变化明显,且具有很强的一致性,pH值的低值出现在06:00,而后逐渐上升,高值出现在18:00,而后降低(图3)。L组和H组初始pH值分别为7.66±0.08和7.67±0.07。 L-CK—低营养对照处理;H-CK—高营养对照处理;L-5.0—低营养,降水pH=5.0;H-5.0—高营养,降水pH=5.0;L-4.0—低营养,降水pH=4.0;H-4.0—高营养,降水pH=4.0;L-2.5—低营养,降水pH=2.5;H-2.5—高营养,降水pH=2.5。第1天0时为实验开始前的初始状态。 在模拟降雨后,L-2.5和H-2.5处理pH值在10:00较其他处理显著降低(P< 0.05),分别比06:00 时降低0.71和0.61。H组pH值增加速率快于L组,H-2.5处理pH值在第2天10:00回升至CK处理水平,L-2.5处理pH值至第4天14:00回升至CK处理的水平。 对实验期间各处理pH值计算其日平均值,L组各处理pH值在实验期间一直呈现5.0> CK> 4.0> 2.5的规律;而H组各处理间pH值无明显规律。L组pH值低于H组,但L组和H组不同酸雨处理pH日平均值在实验期间均随时间的推移而增加。L组各处理pH日均值由第1天的7.41~8.04增加到第5天的8.58~8.71,而H组由第1天的7.93~8.35上升到第3天的8.89~9.15后趋于稳定。L组和H组不同酸雨处理pH值差异随时间推移而减小,单因素方差分析结果显示,不同pH值处理酸雨对水体pH值的影响在L组中第1天(P<0.01)、第2天(P<0.001)和第3天(P<0.01)都达显著水平,在H组中仅在第1天(P<0.001)显著;在第5天L组和H组不同酸雨处理间差异均不显著。 模拟实验表明,不同营养水体对不同pH值酸雨均有缓冲能力,高营养水体对酸雨的缓冲能力强于低营养水体。在实验初始阶段,模拟水体pH值受酸雨的影响较大,尤其是pH值为2.5的2个处理,但随着时间的推移这种影响迅速减弱,不同pH值酸雨处理之间差异均不显著,但H组pH值高于L组。富营养湖泊中藻类的光合作用使湖泊pH值升高[31],模拟实验和野外调查均表明Chl a与pH值呈显著正相关,也有其他研究证实了这一点[16,32]。笔者实验中添加pH=2.5的酸雨后L和H组pH均值分别为7.04和7.06,水体不呈酸性,其pH值仍处于藻类生长最适范围内[7],对水体中藻类影响很小,H组Chl a含量高于L组,因此具有更高的缓冲能力。 野外调查显示,DIC与pH值呈显著负相关关系,水温与pH值呈显著正相关关系。这是由于平原地区湖泊矿化度一般很低,水中二氧化碳、碳酸氢根和碳酸根的相对含量是决定氢离子浓度的主要因素[22],而水中CO2溶解度又随着水温的升高而降低[7]。实验中也观察到水体pH值与温度日变化趋势一致:日出后水温上升,水体中CO2溶解度降低,电离的H+含量随之降低,因此水体pH值随之升高;至14:00水温升至高值,而水中H+含量在18:00—19:00降至最低,pH值达到一天中的高值;夜晚藻类呼吸作用产生CO2,且水温降低,CO2溶解度升高,随之电离的H+增多,因此傍晚后pH值开始下降[20,23],日出前水体pH值降到最低。 野外调查表明,溶解氧与pH值呈正相关关系,这与已有的研究结论[32-35]一致。pH值与DO的显著相关性一部分是因为受水体中植物光合作用、水生生物呼吸作用的影响,另一部分可能是水体中氧化还原反应的结果[33]。 模拟实验结束时实验组与对照组(无酸雨添加)之间pH值无显著差异。野外调查结果表明,无论营养水平如何,酸雨区湖泊pH均值都低于非酸雨区湖泊,这是因为模拟实验中仅添加1次酸雨而酸雨区湖泊受酸雨影响是连续多次的。尽管如此,处于全球强酸雨中心之一的长江中下游以南地区的湖泊依然没有发展成为酸性湖泊,说明这一区域湖泊对酸雨依然有较强的缓冲能力,这与欧美北部湖泊是不同的。 湖泊的pH值受到湖泊地质条件、湖泊形态和流域特征以及水生态系统中酸中和物质及过程等多种因素的影响。在酸雨区,流域内土壤和岩石中和外来酸的能力是湖泊是否会被酸化的最重要的单一因素[7]。中国中部和东部的大部分地区属于受酸化影响的地质敏感区,覆盖着具有较小缓冲能力的土壤[36]。同时该地区地处亚热带,水温比欧美北部湖泊高,湖泊营养盐丰富,水体初级生产力比较高,湖泊中的藻类和植物光合作用消耗CO2和HCO3-,能够为湖泊提供一定的缓冲能力[31],防止湖泊被酸化。夏季湖泊野外调查结果和实验结果均证实了这一点。以往长江中下游湖泊调查结果也表明酸雨区湖泊并未出现酸化(pH<5.6)现象[37-38]。但是,不容忽视的是野外采样数据显示酸雨区湖泊pH值低于非酸雨区湖泊,表明酸雨对湖泊pH值产生了一定影响。研究表明过去60 a来,处于酸雨区的太湖酸中和能力和pH值均有显著提高,这与太湖叶绿素a含量增加有关;但如果以目前的速度持续酸沉积,则流域中碱性阳离子将在2040年大幅减少[16],对流域和湖泊都会产生很大影响。 目前,欧洲和北美地区的酸化湖泊正在恢复,而我国正在经历酸沉积过程。研究欧洲和北美从酸化中恢复的湖泊发现,即使湖泊pH值上升,化学条件改善,也不是所有的物种都能够恢复[14],湖泊经历酸化过程对湖泊中一些生物的伤害是不可逆的。长江中下游地区湖泊对区域经济可持续发展具有十分重大的意义,关注酸雨对长江中下游地区湖泊的影响是十分必要的。在后续研究中还需要进一步研究酸雨对该地区湖泊水生生物及生物地球化学循环的影响。 致谢: 孔令阳、葛亚汶、黄靖和张振宇在湖泊调查采样中给予了帮助,杨柳、操庆、殷春雨、王朝霞和高弋明在实验过程中给予了帮助与支持,在此表示衷心感谢。
2.2 模拟酸雨对水体pH值的影响
3 讨论
