经皮冠脉介入术后支架内血栓临床研究进展
2018-10-27郑剑峰综述邱洪审校
郑剑峰 综述 邱洪 审校
(中国医学科学院北京协和医学院国家心血管病中心阜外医院,北京100037)
随着冠状动脉支架的出现,经皮冠脉介入术(PCI)的安全性和有效性有了显著地提升。单纯球囊扩张早期常见的严重并发症如急性血管闭塞,其有显著的发病率和死亡率并有紧急冠状动脉搭桥术的需要。冠状动脉支架显著地减少了球囊血管成形术后急性血管闭塞事件的发生,也从本质上减少了动脉血管的弹性回缩和负性重构引起的再狭窄[1]。在很早期,金属内植体附着血栓或支架内血栓(ST)被认为是严重的并发症,而辅助的药物治疗,支架工艺和操作术也不断在改进以进一步减少其发生。
1 ST的认识
ST定义的敏感性和特异性取决于获得证据的等级以及数据的准确性,由于受许多因素的作用并不能容易地作出诊断。标准化的ST定义[2]是由学术研究联合会(ARC)于2007年根据把握水平(确定的,可能的和不能排除的ST)和标准化的ST产生时间(急性、亚急性、晚期和极晚期ST)而建立的分级(见表1、表2)。

表1 ARC定义的ST(根据把握水平分层)
在介入治疗的早期,低压力球囊扩张、单一抗血小板药物治疗和裸金属支架(BMS)植入的策略有着较高的ST的发生率约为20%。Colombo等[3]首次介绍了应用高压力充分扩张支架联合双联抗血小板药物治疗方法,这种方式使得ST发生率在PCI术后6个月达到可接受的<2%,此后该方案便被广泛地接受和使用。在药物洗脱支架(DES)问世之前,ST一直被视作支架植入早期才会出现的并发症。2004年,McFadden等[4]报道了4例出现在第一代DES(西罗莫司DES/CYPER和紫杉醇DES/TAXUS)的晚期和极晚期ST。
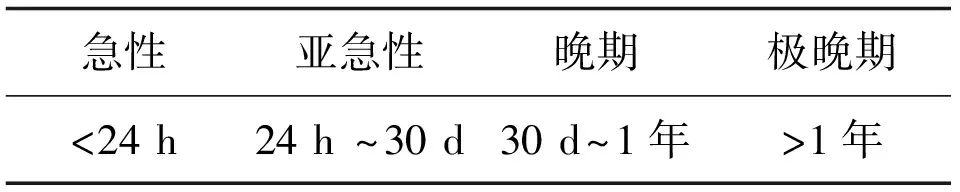
表2 ARC定义的ST(根据时间分层)
随后,一项大型注册研究显示,第一代DES植入术后,极晚期ST以0.4%~0.6%的年增长率稳定地发生[5]。最近几年,反复发生的ST也被人们所意识到,相关文献报道反复ST的发生率在5.9%~18.8%,而其死亡率在11%~42%[6]。ADAPT-DES注册研究[7]为期2年的随访数据显示,在新一代DES和足量足程的抗血小板药物治疗下,ST的发生率大约在1%,这其中确定/可能的ST约50%发生在PCI术后30 d内,而约15%发生在PCI手术1年之后。EXAMINATION研究[8]5年的随访结果显示,在1、2和3年时新一代DES组的ST发生概率要明显低于BMS组且有统计学上的差异。而之后4和5年的结果显示,两组ST事件的发生并无显著的差异。可见对于预防早期和晚期ST新一代DES具有明显的优势,但在极晚期ST的预防上其效果与BMS相当。多中心的CORONOR研究[9],非选择性的纳入了4 184例稳定性冠心病的患者(如心肌梗死或血运重建时间>1年)并取得了4 094例患者5年的随访结果,其研究显示在稳定性冠心病出院患者中,心肌梗死以每年0.8%的速度增长,而和极晚期ST相关的心肌梗死约占20%并且一半以上表现为ST段抬高型心肌梗死,其死亡风险也随之增长,修正的死亡率约是非支架相关心肌梗死死亡率的4倍。
2 ST的临床表现、诊断和病理生理机制
2.1 临床表现
典型的ST的临床表现包括胸痛、靶血管区域心电图缺血的改变。然而,ST也可以表现为猝死,在形成侧支循环的情况下会无典型的症状。以冠状动脉造影为基础的血栓表现为充盈缺损。当造影发现有充盈缺损时,血管内超声(IVUS)/光学相干断层扫描(OCT)等腔内影像学技术可能需要被应用于进一步诊断及探测潜在的ST机制。OCT得益于其高分辨率,能清晰地展现支架及血栓的形态,Adriaenssens等[10]通过OCT随访发生ST的患者,发现支架内皮覆盖不全和支架贴壁不良是最多被观察到的,并且随着时间的延长ST发生率会逐步下降。
2.2 ST的病理生理机制
许多机制会导致ST的发生,包括患者相关因素、病变相关因素、操作因素以及术后管理等因素都与ST发生相关。这些造成ST的因素中至少包含有以下一项的病理生理机制:(1)在血管内皮化前致栓性的内皮下成分、支架杆和多聚物涂层暴露于血液中,激活外源性凝血级联瀑布;(2)持续慢冠状动脉血流和低鞘管压导致的内源性凝血途径激活;(3)药物抑制血小板激活不足;(4)系统性高凝状态表现,例如,由急性冠脉综合征(ACS)和恶性肿瘤引起的高凝状态[11]。对于早期ST,手术操作是重要的因素,次优结果如冠状动脉慢血流、不充足的管腔大小、残余夹层和组织脱垂等和ST发生密切相关。由于血管还没有再内皮化,期间抑制血小板激活是非常必要的,若中断抗血小板药物治疗支架能造成灾难性的后果。而晚/极晚期ST,研究显示血管内皮化延迟、持续纤维蛋白沉积和进行性的血管炎症都与之相关。和BMS相比,DES出现支架植入后显著的再内皮化延迟,这很可能是导致第一代DES有更高的晚期ST发生率的原因。晚期支架贴壁不良多是血管正性重构的结果,而DES更多地出现这种情况并会进一步导致ST的发生[12]。新生动脉粥样硬化斑块能够在植入支架后的血管新生内膜下发展,斑块的破裂和腐蚀会导致ACS的进展并成为导致血栓形成的不稳定因素,其已经被视作潜在的极晚期ST的原因[13]。
3 ST的治疗策略
ST的优先治疗措施是急诊介入手术包括血栓抽吸、经皮球囊血管成形术以及支架植入术等。额外植入新支架并不是必须的,但对于明显存在残余夹层、新生斑块破裂以及支架断裂的患者来说是推荐使用的。如果IVUS/OCT证实支架膨胀不全,可以根据临近正常参考段血管选择合适的非顺应性球囊进行高压力球囊血管成形术。如果导致支架膨胀不良的原因是血管壁僵硬,这时植入新的支架将会是极其有害的,此时支架的复合涂层将会暴露于膨胀不全的病变处进而诱发血栓的形成。如果球囊扩张不充分,那么患者应该先暂时接受并在ST症状消失后寻找明确的治疗方案。随后的措施取决于支架的位置、解剖结构以及术者经验,其包括:(1)冠状动脉旋磨:消磨支架或其下的钙化斑块;(2)准分子激光:能够消融未充分膨胀的支架杆改善局部条件;(3)冠状动脉搭桥手术:尽管不能阻止膨胀不良部分的血栓进展,但能恢复支架远端区域血流。而对于支架贴壁不良的患者,由于血液低流动性的空隙存在,容易发生ST[12]。因此,推荐运用合适大小的球囊充分扩张贴壁。
4 抗血栓药物及策略
ISAR和STARS试验建立了运用阿司匹林和一种噻吩吡啶类药物的双联抗血小板治疗,并成为冠状动脉支架术后的医疗标准。新型抗血小板药物P2Y12受体抑制剂如普拉格雷、替格瑞洛以及坎格瑞洛等的出现,解决了氯吡格雷抵抗相关的ST等问题,并且其比氯吡格雷的作用更强,能更迅速地抑制血小板活性、持续更长时间。新型P2Y12受体抑制剂或者高剂量氯吡格雷的应用虽能降低ST的发生率,但相应的出血风险却增加,而有潜在高凝风险的患者可能会从中获得更多净效益。目前,替格瑞洛已经展现出潜在的多效性作用,除了有更低的ST风险外,还存在有证可循的心血管疾病生存上的显著获益[14]。在当今口服双联抗血小板药物治疗的时代,静脉注射的血小板糖蛋白ⅡbⅢa受体抑制剂药物如阿昔单抗、替罗非班和依替巴肽等的作用仍不明确,但大体来说,在ACS患者中应用血小板糖蛋白ⅡbⅢa类药物相比于单用肝素能减少急性ST的发生。
2017年新的ESC指南建议[15],在稳定性冠心病的患者中不论接受何种支架,推荐持续双联抗血小板药物治疗6个月,优先选择DES并根据PRCISE-DAPT评分决定是短时间3个月(评分≥25)还是标准的6个月,而ACS患者建议双联抗血小板药物至少12个月,有高出血风险(评分≥25)可双联抗血小板药物6个月;但对于植入可降解支架的患者,指南还是建议双联抗血小板药物治疗至少12个月。一项有关双联抗血小板治疗药物试验的meta分析显示[16],延长双联抗血小板药物治疗虽能降低ST发生率,但应该根据患者个体情况而定,其推荐的最佳双联抗血小板药物治疗时间窗应该在6~30个月,一刀切的标准并不是最好的选择。更进一步说,双联抗血小板药物治疗时间在临床实践中是动态变化的,需要根据患者情况在后续的随访中不断调整。尽管一些研究支持在植入新一代DES后双联抗血小板药物治疗时间<6个月是安全的[17],但这些研究受到许多混杂因素的限制及影响,因而在医疗实践中并不推荐<6个月的双联抗血小板药物治疗。
5 ST的预防
合适的支架及手术策略的选择和患者依从性教育是首要的。一项纳入了49项随机试验的大规模网络meta分析显示[18],第二代氟聚合物涂层依维莫司DES,相比于其他永久涂层聚合物DES和BMS,在为期2年的随访中有明显更低的ST发生率。全降解冠状动脉支架可能会降低极晚期ST的发生,但是来自多项真实世界注册研究的数据显示,全降解支架在植入后的前6~12个月比第二代DES有更高的ST发生率,主要不良事件发生在术后的前1个月。Roy等[19]的研究报道,IVUS指导下的支架植入相比于单纯造影指导下的支架植入更能减少ST的发生。ST的风险随着支架长度和数量的增加而增长,因而并不推荐过度使用支架;但是,支架必须要覆盖住全部的病变,因为支架边缘残余的斑块也能够产生夹层、慢血流并导致ST。患者依从性的教育亦是重要措施,ST随着停用双联抗血小板药物治疗时间的变化而变化。支架植入术后1个月停用双联抗血小板药物发生ST风险最高,一直到6个月时仍然是很高危的,随后其风险开始下降[20-21]。对于需要择期进行侵入性检查或者手术的支架植入患者,推荐其在支架植入术后1年以后进行。如果有不可抗拒的原因需要提前中断双联抗血小板药物治疗,则应该尽可能的延迟。
6 总结
ST是介入术后严重的并发症,在BMS和DES中早期和晚期ST事件的发生是相似的,对于极晚期ST,尽管不常见,但其更多地发生在第一代DES中。许多ST的危险因素已经被血管内影像技术和病理学研究所证实。ST是一个复杂的临床问题,合适的患者、病变及支架的选择、良好的手术结果和有效的双联抗血小板药物治疗是将ST风险降到最低的关键。相信,未来随着新技术及新发明的不断涌现,这一棘手的问题也终将得以解决。
