乌苯美司抗肿瘤作用研究进展
2018-10-26倪隽陈淑珍
倪隽,陈淑珍
乌苯美司抗肿瘤作用研究进展
倪隽,陈淑珍
100050 北京,中国医学科学院北京协和医学院医药生物技术研究所肿瘤室
乌苯美司(ubenimex)商品名为百士欣(Bestatin),是细胞表面氨基肽酶N/CD13(aminopeptidase N/CD13,APN/CD13)、氨基肽酶 B 的抑制剂,主要通过调节机体免疫功能及诱导肿瘤细胞凋亡等发挥抗肿瘤作用。本文就乌苯美司来源及特点、药代动力学特性、抗肿瘤作用及联合用药研究进展作一简要综述。
1 来源与作用特点
乌苯美司是 1976 年由日本学者梅泽滨夫从橄榄网状链霉()的培养液中分离而得的一种低分子二肽化合物,化学名为 N-[(2S, 3R)-3-氨基-2-羟基-4-苯丁酰]-L-亮氨酸,呈白色结晶粉末状,易溶于冰醋酸,在水或甲醇中微溶,结构如图 1 所示。1987 年作为具有免疫调节功能的抗癌辅助药在日本正式上市,国内商品名为百士欣,属于国家二类新药并于 1998 年上市应用,由四川抗生素工业研究所研制,浙江普洛康裕制药有限公司生产,且目前市场上的片剂和胶囊剂具有生物等效性。乌苯美司的临床试验中出现的不良反应主要有皮疹、红斑以及胃肠道反应,继续服药或停药后绝大部分症状会自行消失[1]。
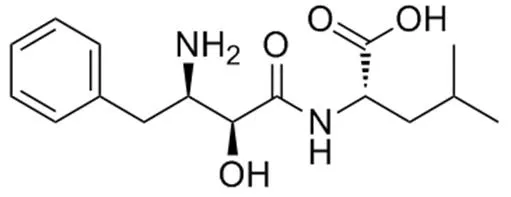
图 1 乌苯美司化学结构
2 药代动力学特性
乌苯美司在体内作用时间较短,成人单次口服 30 mg 后 1 h 血药浓度达到峰值(2.2 μg/ml),随后呈双相性下降,主要分布于肝脏、肾脏和小肠,极少数进入红细胞和骨骼肌[2]。免疫细胞化学方法结果显示,乌苯美司在小肠中主要分布于上皮细胞微绒毛、胞质与胞核中,并在有寡肽转运蛋白(peptide transporter,PEPT)1 和 PEPT2 存在的部位大量聚集[3],且涉及有机阴离子转运蛋白(organic anion transporter,OAT)1 和 OAT3 的参与[4]。Inui 等[5]通过观察兔小肠刷状缘膜囊泡发现乌苯美司的吸收受氢离子梯度及膜电势的影响,加入阳性对照头孢菌素或缩二氨酸处理后,乌苯美司的吸收会被抑制,表明 H+/二肽转运系统是肠道对乌苯美司的主要吸收方式。经体内代谢后,乌苯美司的原型以及两种生物活性代谢产物(-)-N-[(2S,3R)-3-amino- 2-hydroxy-4-(4'-hydroxy)phenylbutyryl]-L-leucine(OH-ubenimex) 和 (2S,3R)-3-amino-2-hydroxy-4-phenylbutyric acid[(2S,3R)-AHPA] 分别以 67% ~ 73%、9% ~ 25% 和 2% ~ 5% 的比例随尿液排出[6],因此,乌苯美司主要以原型形式排泄。
当乌苯美司与其他药物联合用药时,会产生药物-药物相互作用(drug-drug interactions,DDIs)。有文献指出,氨甲蝶呤与乌苯美司的 DDI 药代动力学机制为:两者在肠黏膜中均由 P-糖蛋白转运,在肾脏中均由 OAT 转运[7]。而在肾脏中头孢克肟和乌苯美司 DDI 靶标转运蛋白为 PEPT1 和 OAT1/3[8]。Huo 等[9]经体内体外实验证实,P 糖蛋白抑制剂可显著增加乌苯美司在肠道内的吸收,并增强其药效。白藜芦醇通过下调多药耐药基因(multidrug resistance,Mdr)1 和 Mdr2、上调 PEPT1 蛋白的表达水平来促进乌苯美司在肠道中的吸收[10]。综上,DDI 可能会对药物吸收、代谢等方面产生影响,可为临床上制定联合用药方案提供理论基础与创新思路。
3 作用靶点
现有研究显示乌苯美司最主要的抑制靶点为氨肽酶,此酶通过水解肽段氨基端上氨基酸来降解细胞外基质和基底膜,进而促进肿瘤的转移,在一些高侵袭性、快速增殖的恶性肿瘤中表达上调[11]。乌苯美司可通过结合氨肽酶的 Zn2+和疏水活性中心抑制氨肽酶的活性[12]。目前在乌苯美司抑制的十几种氨肽酶中,研究较多的是氨肽酶 N(aminopeptidase N,又称 CD13)和氨肽酶 B,其中又以 CD13 最为重要。除上述氨肽酶的共同水解作用影响肿瘤侵袭转移之外,CD13 还与血管形成、病毒受体、抗原呈递、调节细胞因子相关[13]。Harbut 等[14]在 2008 年研制的具有乌苯美司活性的高效探针可更广泛地检测金属氨肽酶在不同生物系统中的功能特性。
除了靶向氨肽酶,乌苯美司另一个抑制靶点是白三烯 A4(leukotriene A4,LTA4)水解酶,两者结合过程中 Glu-296 是重要的结构决定因素[12]。此外,有研究者发现乌苯美司还是一种肿瘤二肽酶的竞争性抑制剂,此酶从小鼠腹水肿瘤细胞中分离纯化得到,与氨肽酶结合方式不同的是,乌苯美司与二肽酶结合过程虽缓慢,但并不紧密[15]。综上,乌苯美司的作用靶点主要为氨肽酶和 LTA4 水解酶。
4 抗肿瘤作用机制
早期认为,乌苯美司在体内的抗肿瘤活性是通过影响机体免疫反应来杀伤肿瘤细胞的,如激活免疫细胞巨噬细胞,降解灭活免疫活性因子,活化粒细胞和NK 细胞,促进抗肿瘤非特异性免疫反应等[3],随后大量研究发现即使不通过免疫反应,乌苯美司依然具有抗肿瘤作用,因而乌苯美司的抗肿瘤作用包括直接的以及通过免疫调节产生的间接抗肿瘤作用。
4.1 细胞增殖抑制作用与细胞凋亡诱导作用
2000 年,Imamura 和 Kimura[16]发现人早幼粒急性白血病细胞系 HL60 细胞增殖可被乌苯美司抑制。乌苯美司还可直接诱导慢性粒细胞性白血病细胞 K562 细胞产生凋亡效应,抑制细胞增殖。该过程依赖于 caspase-3 的活化,还与丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)和糖原合成酶激酶-3β(glycogen synthase kinase-3β,GSK-3β)的磷酸化以及细胞周期蛋白 D1 表达受到抑制有关[17]。在正常大肠癌细胞中死亡相关蛋白激酶(death associated protein kinase,DAPK)基因启动子是呈甲基化状态的,而用乌苯美司处理细胞后,该基因启动子逆转为去甲基化状态,DAPK mRNA 和蛋白均恢复表达,细胞增殖被抑制并发生凋亡[18]。另有文献表明乌苯美司及其类似物通过结合 BIR3 结构域,致使凋亡抑制因子 1 自动泛素化从而被降解,最终导致肿瘤细胞发生凋亡[19]。此外,Sekine 等[20]发现在人实体瘤细胞中,乌苯美司在不引起肿瘤细胞凋亡的情况下能促进 Fas 激动性抗体 CH11 诱导肿瘤细胞(人类宫颈癌细胞 HeLa S3 和纤维肉瘤细胞 HT-1080)凋亡,增强 caspase-8 的活化。目前,在已成功合成的乌苯美司类似物中,LYP 更有效地在体内抑制卵巢癌 ES-2 移植瘤的生长,其中 LYP2 可抑制包括 HL60、A549 及 PLC 等 6 种肿瘤细胞生长,IC50值均低于乌苯美司,而且 LYP3 在 ES-2 和 HL60 肿瘤细胞中的生长抑制作用同样优于乌苯美司。且上述类似物具有更好的水溶性及生物稳定性,在未来的研究中可能成为乌苯美司的有效替代物[21-22]。
4.2 侵袭转移抑制作用
大量研究发现,在转移性肿瘤中,乌苯美司可通过抑制 CD13 活性进而遏制肿瘤细胞侵袭转移,并呈乌苯美司药物浓度依赖性,同时伴随小鼠存活时间的延长。早期学者发现乌苯美司可显著下调 68 kD IV型胶原蛋白酶蛋白(活性形式)的表达水平,乌苯美司对肿瘤细胞侵袭的抑制作用可能与其影响IV型胶原蛋白酶由潜在形式向活性形式的转化过程及肿瘤细胞胶原酶的分泌过程有关[23]。近年来,Liang 等[24]发现人骨肉瘤细胞经乌苯美司给药处理后,MAPK 与 PI3K 蛋白表达水平以及 p38、ERK1/2 和 JNK 磷酸化水平降低,NF-κB 蛋白水平降低,同时还检测到肿瘤侵袭转移相关标志性蛋白分子基质金属蛋白酶(metal matrix proteinase,MMP)2 和 MMP9 的酶活性及表达水平被抑制,肿瘤侵袭现象减弱。尽管 CD13 在前列腺癌细胞中表达含量不高,乌苯美司同样可以通过下调 CD13 表达来遏制细胞侵袭与转移,伴随 LC3B 蛋白表达上调以及自噬性细胞死亡[25],在肾癌细胞中给药后出现了上述类似现象,但乌苯美司是通过阻碍 CD13 活性,而非影响其表达含量来体现抑制细胞侵袭作用的[26]。
4.3 血管形成抑制作用
CD13 在肿瘤血管生成过程中发挥重要作用,经肿瘤微环境的影响因素低氧或血管形成生长因子刺激后,人脐静脉血管内皮细胞(human umbilical vein endothelial cells,HUVECs)中 CD13 的表达升高,HUVECs 的血管形成能力增强,乌苯美司能抑制 HUVECs 在基底膜基质中形成毛细管网络的能力,这种血管形成抑制作用可能与乌苯美司抑制 CD13 的表达相关[27]。Pasqualini 等[28]通过绒毛膜尿囊膜血管实验发现,乌苯美司可抑制成纤维细胞生长因子 2(fibroblast growth factor-2,FGF-2)所引发的血管形成过程,另在视网膜新生血管形成模型中,同剂量乌苯美司也可阻断低氧环境下的血管生成。此外,乌苯美司类似物 LYP 能够更加有效抑制 CD13 的活性,通过抑制血管内皮细胞毛细管的形成达到抗肿瘤作用[29]。
4.4 免疫调节作用
长久以来,乌苯美司主要用于肿瘤的辅助治疗,提高机体免疫力,减轻化疗中的不良反应,提高患者生活质量。大量文献显示,乌苯美司用于胃癌、卵巢癌、结肠癌、肺癌、急性髓系白血病、肾癌等恶性肿瘤的临床试验和治疗,乌苯美司会通过增加患者外周血中 CD3+、CD4+淋巴细胞数量,提高 CD4+/CD8+比值,改善 NK 细胞活性,调节免疫因子,增强 NO 分泌能力及巨噬细胞吞噬功能,使外周血髓系衍生抑制细胞(myeloid derived suppressor cells,MDSCs)和肿瘤相关巨噬细胞(tumor-associated macrophages,TAMs)恢复至正常水平等生物效应来改善机体免疫机能。2016 年和 2017 年,研究者分别对纳入标准的 9 项随机对照试验(810 例患者)以及 12 项随机对照试验(762 例患者)进行 Meta 分析,收集评价乌苯美司对恶性肿瘤患者的免疫影响,结果证实了上述观点[30-31]。在临床前基础分子机制研究方面,科学家们的关注点主要集中在乌苯美司对机体中免疫效应细胞因子的影响,除可增加 IL-1 和 IL-2 的分泌外[32],乌苯美司还可抑制促炎性细胞因子及趋化因子,如IL-6、CXCL8/IL-8、CCL3/巨噬细胞炎症蛋白-1α 等的生成及表达[33-34]。
5 联合用药
由于肿瘤的复杂性,对于一些难治愈、易复发的恶性肿瘤,传统治疗手段如放疗、化疗的治愈效果并不明显,旨在提高疗效的联合用药策略将是未来治疗癌症之大方向。乌苯美司现与多种化药联合用于治疗肿瘤,效果明显。近期研究表明,乌苯美司联合化疗药物 5-氟尿嘧啶、阿霉素、亚叶酸钙等治疗肝动脉栓塞中晚期复发性肝癌(尤其是肿瘤直径 < 3 cm 及 3 ~ 5 cm 的小肝癌)时,会增强细胞凋亡以及细胞内活性氧水平,治疗效果优于单纯化疗[35]。对于晚期胃癌,与替吉奥联合奥沙利铂化疗方案联用后,乌苯美司能降低患者血清 MMP 2 及 MMP 9 水平,增强抗肿瘤效果[36]。乌苯美司还可加强全反式维甲酸对急性早幼粒细胞白血病细胞增殖的抑制作用及诱导细胞分化的能力[37]。此外,乌苯美司可显著提高顺铂对 A549 细胞生长抑制作用,其或成为 CD13+非小细胞肺癌顺铂治疗的增敏剂[38]。
6 展望
乌苯美司作为氨肽酶抑制剂,在阻抑肿瘤细胞生长、抑制肿瘤侵袭和转移等方面体现了一定的抗肿瘤效果,与其他药物联合使用时发挥了较显著的协同抗癌功能,并在免疫方面起到了不可忽视的调节作用。尽管乌苯美司已经在临床上使用多年,但其作用机制尚未充分阐明。目前除了作用于肿瘤本身的分子机制外,近年来学者逐渐开始关注其在肿瘤微环境中的功能作用,临床上研究主要集中于在各种癌症中的作用试验以及与其他药物的联合治疗,有关乌苯美司的抗肿瘤作用机制、肿瘤微环境调节作用、联合用药仍然值得进一步研究。由于乌苯美司的抗肿瘤作用和免疫调节作用均不强,因此,以乌苯美司为先导化合物发现更加有效、精准、低毒、少复发的癌症靶向治疗手段将是未来研究中的大方向。同时,乌苯美司来源于微生物,说明微生物也是发现免疫调节药物的重要资源,我们也可以从微生物中筛选更强的乌苯美司抗肿瘤作用类似物。
[1] Ito K, Irie Y, Hagiwara T, et al. Toxicological studies on bestatin. II. Subacute toxicity test and recovery study in beagle dogs. Jpn J Antibiot, 1983, 36(11):2985-3052.
[2] Scornik OA, Botbol V. Cellular uptake of 3H-bestatin in tissues of mice after its intravenous injection. Drug Metab Dispos, 1997, 25(7): 798-804.
[3] Fujiwara K, Shin M, Yoshizaki Y, et al. Immunocytochemistry for bestatin and its application to drug accumulation studies in rat intestine and kidney. J Mol Histol, 2011, 42(6):589-596.
[4] Zhu Y, Meng Q, Wang C, et al. Organic anion transporters involved in the excretion of bestatin in the kidney. Peptides, 2012, 33(2):265-271.
[5] Inui K, Tomita Y, Katsura T, et al. H+ coupled active transport of bestatin via the dipeptide transport system in rabbit intestinal brush-border membranes. J Pharmacol Exp Ther, 1992, 260(2):482- 486.
[6] Abe F, Kuramochi H, Takahashi K, et al. Biological activity of the main metabolites of ubenimex in humans. J Antibiot (Tokyo), 1988, 41(12):1862-1867.
[7] Zhu Y, Meng Q, Wang C, et al. Methotrexate-bestatin interaction: involvement of P-glycoprotein and organic anion transporters in rats. Int J Pharm, 2014, 465(1-2):368-377.
[8] Wang L, Wang C, Liu Q, et al. PEPT1- and OAT1/3-mediated drug-drug interactions between bestatin and cefixime in vivo and in vitro in rats, and in vitro in human. Eur J Pharm Sci, 2014, 63:77-86.
[9] Huo X, Liu Q, Wang C, et al. Enhancement effect of P-gp inhibitors on the intestinal absorption and antiproliferative activity of bestatin. Eur J Pharm Sci, 2013, 50(3-4):420-428.
[10] Jia Y, Liu Z, Huo X, et al. Enhancement effect of resveratrol on the intestinal absorption of bestatin by regulating PEPT1, MDR1 and MRP2 in vivo and in vitro. Int J Pharm, 2015, 495(1):588-598.
[11] Dubowchik GM, Walker MA. Receptor-mediated and enzyme- dependent targeting of cytotoxic anticancer drugs. Pharmacol Ther, 1999, 83(2):67-123.
[12] Andberg M, Wetterholm A, Medina JF, et al. Leukotriene A4 hydrolase: a critical role of glutamic acid-296 for the binding of bestatin. Biochem J, 2000, 345 Pt 3:621-625.
[13] Saida S, Watanabe K, Kato I, et al. Prognostic significance of aminopeptidase-N (CD13) in hepatoblastoma. Pediatr Int, 2015, 57(4): 558-566.
[14] Harbut MB, Velmourougane G, Reiss G, et al. Development of bestatin-based activity-based probes for metallo-aminopeptidases. Bioorg Med Chem Lett, 2008, 18(22):5932-5936.
[15] Patterson EK. Inhibition by bestatin of a mouse ascites tumor dipeptidase. Reversal by certain substrates. J Biol Chem, 1989, 264(14):8004-8011.
[16] Imamura N, Kimura A. Effect of ubenimex (Bestatin) on the cell growth and phenotype of HL-60 and HL-60R cell lines: up-and down-regulation of CD13/aminopeptidase N. Leuk Lymphoma, 2000, 37(5-6):663-667.
[17] Sawafuji K, Miyakawa Y, Weisberg E, et al. Aminopeptidase inhibitors inhibit proliferation and induce apoptosis of K562 and STI571-resistant K562 cell lines through the MAPK and GSK-3beta pathways. Leuk Lymphoma, 2003, 44(11):1987-1996.
[18] Yuan CJ, Huang XD, Yu T, et al. Effect of Ubenimex on the proliferation, apoptosis of colorectal cancer cell and its mechanism. Chin J Cancer Prev Treat, 2014, 21(9):665-668. (in Chinese)
袁昌劲, 黄晓东, 余涛, 等. 乌苯美司对大肠癌细胞增殖与凋亡影响及其机制探讨. 中华肿瘤防治杂志, 2014, 21(9):665-668.
[19] Sato S, Aoyama H, Miyachi H, et al. Demonstration of direct binding of cIAP1 degradation-promoting bestatin analogs to BIR3 domain: Synthesis and application of fluorescent bestatin ester analogs. Bioorg Med Chem Lett, 2008, 18(11):3354-3358.
[20] Sekine K, Fujii H, Abe F, et al. Augmentation of death ligand-induced apoptosis by aminopeptidase inhibitors in human solid tumor cell lines. Int J Cancer, 2001, 94(4):485-491.
[21] Luan Y, Wang Q, Liu N, et al. Synthesis and activity evaluation of a new bestatin derivative LYP2 as an aminopeptidase N inhibitor. Anticancer Drugs, 2011, 22(1):99-103.
[22] Luan Y, Ma C, Sui Z, et al. LYP3, a new bestatin derivative for aminopeptidase N inhibition. Med Chem, 2011, 7(1):32-36.
[23] Yoneda J, Saiki I, Fujii H, et al. Inhibition of tumor invasion and extracellular matrix degradation by ubenimex (bestatin). Clin Exp Metastasis, 1992, 10(1):49-59.
[24] Liang W, Gao B, Xu G, et al. Possible contribution of aminopeptidase N (APN/CD13) to migration and invasion of human osteosarcoma cell lines. Int J Oncol, 2014, 45(6):2475-2485.
[25] Wang X, Niu Z, Jia Y, et al. Ubenimex inhibits cell proliferation, migration and invasion by inhibiting the expression of APN and inducing autophagic cell death in prostate cancer cells. Oncol Rep, 2016, 35(4):2121-2130.
[26] Liu S, Xie F, Wang H, et al. Ubenimex inhibits cell proliferation, migration and invasion in renal cell carcinoma: the effect is autophagy-associated. Oncol Rep, 2015, 33(3):1372-1380.
[27] Bhagwat SV, Lahdenranta J, Giordano R, et al. CD13/APN is
activated by angiogenic signals and is essential for capillary tube formation. Blood, 2001, 97(3):652-659.
[28] Pasqualini R, Koivunen E, Kain R, et al. Aminopeptidase N is a receptor for tumor-homing peptides and a target for inhibiting angiogenesis. Cancer Res, 2000, 60(3):722-727.
[29] Gao JJ, Xue X, Gao ZH, et al. LYP, a bestatin dimethylaminoethyl ester, inhibited cancer angiogenesis both in vitro, and in vivo. Microvasc Res, 2011, 82(2):122-130.
[30] Li S, Wang F, Wang XY, et al. Effect of ubenimex combined with radiotherapy or chemotherapy on immune functions of malignant tumors: a meta-analysis. Pharma J Chin PLA, 2016, 32(5):462-465, 479. (in Chinese)
李莎, 王芳, 王晓燕, 等. 乌苯美司联合放化疗对恶性肿瘤患者免疫功能影响的Meta分析. 解放军药学学报, 2016, 32(5):462-465, 479.
[31] Meng H, Sun X, Nian JY, et al. Ubenimex combined with chemotherapy in the treatment of malignant tumor: a systematic review. China Pharm, 2017, 28(24):3387-3390. (in Chinese)
孟慧, 孙旭, 念家云, 等. 乌苯美司联合化疗用于恶性肿瘤的系统评价. 中国药房, 2017, 28(24):3387-3390.
[32] Shibuya K, Hayashi E, Abe F, et al. Enhancement of interleukin 1 and interleukin 2 releases by ubenimex. J Antibiot (Tokyo), 1987, 40(3): 363-369.
[33] Lkhagvaa B, Tani K, Sato K, et al. Bestatin, an inhibitor for aminopeptidases, modulates the production of cytokines and chemokines
by activated monocytes and macrophages. Cytokine, 2008, 44(3):386- 391.
[34] Lv J, Zou L, Zhao L, et al. Leukotriene B4-leukotriene B4 receptor axis promotes oxazolone-induced contact dermatitis by directing skin homing of neutrophils and CD8+ T cells. Immunology, 2015, 146(1):50-58.
[35] Yamashita M, Wada H, Eguchi H, et al. A CD13 inhibitor, ubenimex, synergistically enhances the effects of anticancer drugs in hepatocellular carcinoma. Int J Oncol, 2016, 49(1):89-98.
[36] Li W, Yao ZQ, Liu ZQ, et al. Clinical effect of ubenimex capsules combined with SOX chemotherapy on treatment of advanced gastric cancer. Prog Mod Biomed, 2017, 17(23):4495-4497, 4470. (in Chinese)
李炜, 姚忠强, 柳仲秋, 等. 乌苯美司胶囊联合SOX化疗对晚期胃癌患者的临床疗效研究. 现代生物医学进展, 2017, 17(23):4495- 4497, 4470.
[37] Hirano T, Kizaki M, Kato K, et al. Enhancement of sensitivity by bestatin of acute promyelocytic leukemia NB4 cells to all- trans, retinoic acid. Leuk Res, 2002, 26(12):1097-1103.
[38] Cao BS, Ji LY, Wang HX, et al. Effect of ubenimex, a CD13 inhibitor, on the chemosensitivity of A549 cells to cisplatin. Chin J Clin Oncol, 2012, 39(22):1778-1782. (in Chinese)
曹宝山, 姬利延, 王荟霞, 等. CD13抑制剂乌苯美司对A549细胞顺铂敏感性的影响及其机制. 中国肿瘤临床, 2012, 39(22):1778- 1782.
国家自然科学基金(81621064);中国医学科学院医学与健康科技创新工程(2016-I2M-2-002)
陈淑珍,Email:bjcsz@imb.pumc.edu.cn
2018-06-12
10.3969/j.issn.1673-713X.2018.05.011
