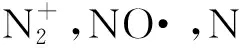电晕放电等离子体与H2O2氧化降解甲基蓝的 光谱行为比较
2018-09-27董发勤霍婷婷
李 苗 董发勤 周 磊,3 霍婷婷,3 马 杰,3
(1. 西南科技大学材料科学与工程学院 四川绵阳 621010; 2. 西南科技大学固体废物处理与资源化教育部重点实验室 四川绵阳 621010; 3. 西南科技大学环境与资源学院 四川绵阳 621010)
印染行业近年来得到了迅猛发展,随之而来的印染废水排放量日益增加。废水具有成分复杂、有机污染物浓度高、毒性大、颜色深的特点,直接排放不仅给人类造成视觉污染,而且严重威胁了人体健康与生态环境安全[1]。根据印染废水的分类,以排放量最大的棉和涤纶印染废水为例,染色废水量约占60%,在印染企业产生的印染废水中所占比重最大[2],这也是近年来用染料配置模拟染色废水作为目标污染物的主要原因之一。
随着染料种类和染色工艺的发展,传统的印染废水处理方法,如生物法、物化法和化学法已不能有效降解以有机污染物为主甚至含有毒有害物质的印染废水,具体表现为耗时长、成本高、二次污染物的引入等缺点[3-4]。H2O2氧化(H2O2oxidation, HO)与电晕放电(Corona discharge, CD)等离子体技术作为两种高级氧化技术,由于其处理效率高、不造成二次污染、后续处理简单的特点,在处理废水中有机污染物方面得到了广泛应用[5-6]。目前关于H2O2对印染废水的降解一般加入Fe2+,UV,O3,Cu2+等催化剂加快其分解,或通过多种催化方法的组合[7-10],仅使用H2O2氧化降解印染废水的报道较少。电晕放电等离子体技术富集了强氧化性的自由基等高能电子、臭氧氧化及紫外光解等物理化学效应,对难降解有机废水的处理效果优于各方法单独使用,因而在印染废水处理领域得到了广泛应用[11]。
近年来,更多的报道为偶氮及蒽醌类染料废水的处理[12-13],而对三苯甲烷类染料废水的研究较少,且研究多针对各种工艺参数的优化及处理效果的比较[14-15],较少文献研究不同方法降解同种染料废水的光谱行为差异。本论文以三苯甲烷类染料甲基蓝为目标污染物,配置染色废水,从电晕放电等离子体与H2O2氧化过程产生的不同活性物质的角度出发,在研究两种处理方式对甲基蓝废水脱色效果的基础上,分析两种处理方法对甲基蓝结构中不同基团的破坏,对甲基蓝的降解机理进行探讨。
1 实验部分
1.1 试剂与装置
1.1.1 实验试剂
实验中涉及到的试剂主要包括甲基蓝、H2O2(质量分数30%),均为分析纯。
甲基蓝(Methyl Blue, MB)分子式为C37H27N3Na2O9S3,相对分子质量为799.8,结构如图1所示,最大吸收波长在314 nm处。实验所用甲基蓝溶液的质量浓度均为1 000 mg/L,所测pH值为8.74。

图1 甲基蓝结构式Fig.1 Chemical structure of methyl blue
1.1.2 实验装置
采用电晕放电等离子体针-板反应器作为主体装置。该反应器由重庆大学电气工程学院研制,实验系统包括高压电源、冷却风机和等离子体反应器,主体反应器由有机玻璃水槽、高压钨针电极、绝缘上盖和低压电极组成。
此外,实验中用到的仪器还包括太仓市华美生化仪器厂DQHZ-2001B型恒温震荡培养箱,美国热电Evolution 300型紫外-可见分光光度计,德国Frontier傅里叶变换红外光谱仪。
1.2 实验方法
采用电晕放电等离子体及H2O2氧化两种处理方法对甲基蓝溶液进行降解。本实验过程所涉及的电晕放电时间均为30 min,间隔5 min取样,H2O2氧化时间均为1 d,取样间隔时间分别为2,4,8,12,24 h,反应器及恒温震荡培养箱(30 ℃)的操作参数在整个实验体系中均保持不变。各实验过程如下:
(1)H2O2氧化甲基蓝:将100 mL含有一定体积分数H2O2的甲基蓝溶液加入锥形瓶,放入恒温震荡培养箱中反应。
(2)电晕放电等离子体对甲基蓝的降解:向反应器中加入180 mL的待处理甲基蓝溶液,接通高压电极(开始计时),高压电极击穿溶液上方的空气形成电晕放电,产生气相等离子体,迁移至液相,进行降解。
各过程所取样品稀释50倍进行测定。
1.3 分析方法
1.3.1 紫外-可见光谱(UV-Vis)分析
采用美国热电Evolution 300型的紫外-可见分光光度计对降解过程的甲基蓝溶液进行吸光度测定。所取样品在容量瓶中稀释50倍,后移入石英比色皿中在200~700 nm波段内进行扫描。
1.3.2 红外光谱(FT-IR)分析
甲基蓝溶液经过两种不同的降解方式处理后,取样,经旋转蒸发仪旋转蒸干,浓缩液40 ℃烘干备用。红外光谱测定时采用KBr一起研磨、压片。然后用Frontier型傅里叶变换红外光谱仪于4 000~400 cm-1范围内扫描。
2 结果与讨论
2.1 两降解过程甲基蓝脱色率变化
电晕放电等离子体与H2O2氧化处理甲基蓝过程溶液的脱色率变化如图2所示,其中吸光度低于初始值的脱色率为正,吸光度高于初始值的脱色率为负。由图2(a)发现,在电晕放电等离子体降解甲基蓝过程中,溶液的脱色率先降低后升高,导致该现象的原因是钨钢针电极溶出的碳元素与电晕放电产生的含氮高活性粒子键合生成发色的C=N加深了甲基蓝颜色[16]。随着放电时间的延长,溶液的脱色率逐渐升高,是因为活性粒子(羟自由基、含氮的高活性粒子、高压电子、紫外光、双氧水、臭氧等)有效降解了溶液中的有机物[17]。观察降解过程溶液的表观颜色发现,放电5 min的甲基蓝样品在所有样品中颜色最深,后又逐渐变浅,进一步印证了C=N键的生成。如图2(b)所示,H2O2氧化甲基蓝过程中,溶液的脱色率随着作用时间的增长逐渐升高。反应2 h甲基蓝的脱色率达到80%,这是因为反应开始H2O2浓度较高,分解产生的OH·浓度较大,甲基蓝的脱色率也随之增加。随着反应时间的增加,未分解的H2O2浓度较小,甲基蓝的浓度逐渐变小,溶液的脱色率增加较缓慢,反应12 h后脱色率达到97%。但在作用12 h后溶液的脱色率几乎未发生明显改变,这可能是因为降解过程生成的中间产物与溶液中未反应的甲基蓝的降解产生竞争。
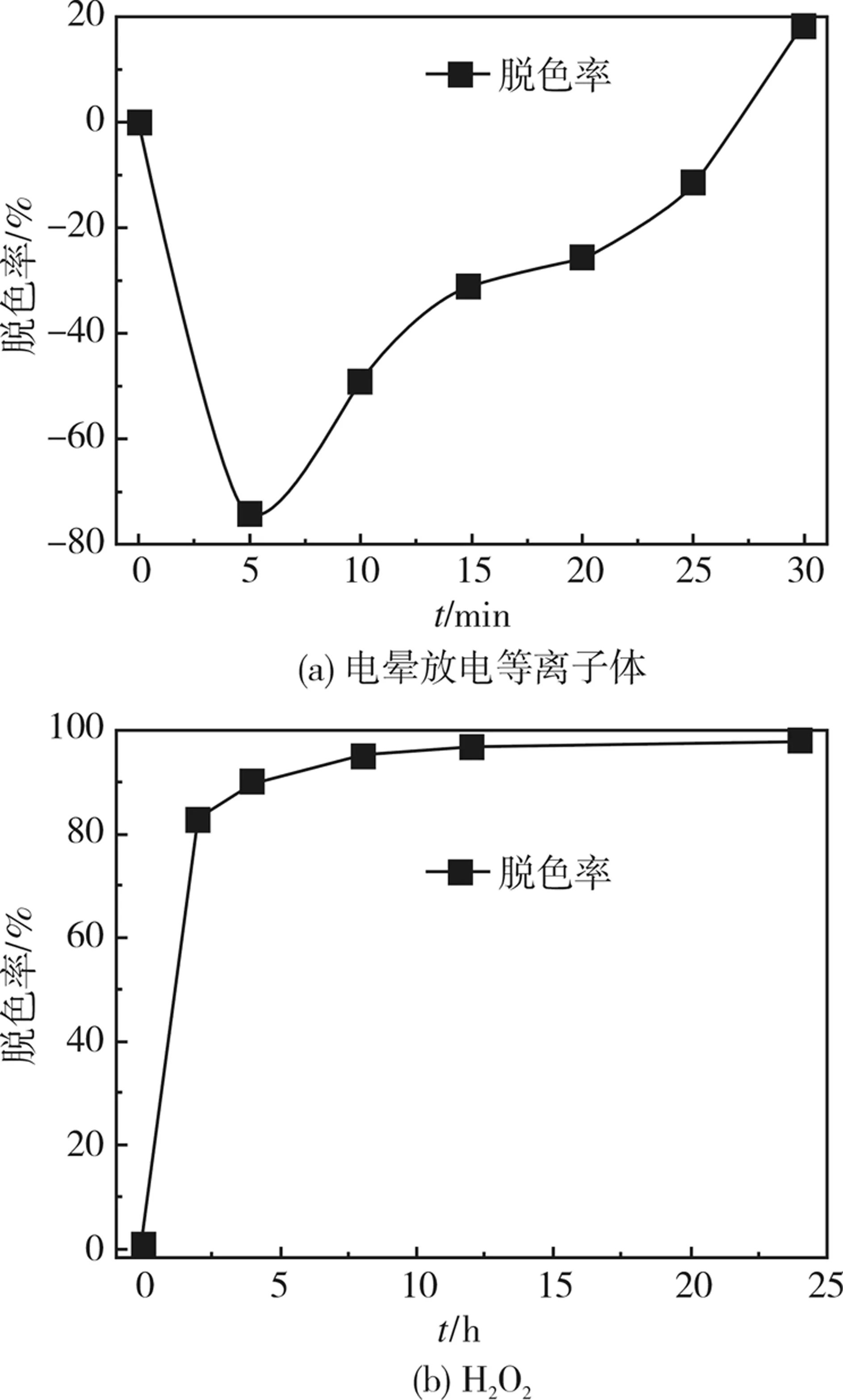
图2 电晕放电等离子体和H2O2 氧化降解甲基蓝溶液过程脱色率变化Fig.2 Changes of color removal in the process of Corona discharge and H2O2 oxidation
2.2 两降解过程甲基蓝溶液的UV-Vis分析
图3所示为甲基蓝溶液在电晕放电与H2O2氧化过程的UV-Vis谱图。观察甲基蓝原溶液的紫外-可见光谱图,在314 nm与603 nm处分别存在一个吸收峰,前者是甲基蓝结构中的芳香环产生,而603 nm处的吸收峰是甲基蓝结构中的C=C,C=N等发色团的共轭产生[18-19]。如图3(a)所示,电晕放电等离子体降解甲基蓝过程,随着放电时间增加,甲基蓝紫外-可见光谱图中的吸收峰强度均发生了一定变化,说明电晕放电产生的活性物种(羟自由基、含氮的高活性粒子、高压电子、紫外光、双氧水、臭氧等)能够有效降解甲基蓝溶液[20]。其中甲基蓝结构中的芳香环浓度越来越低,而发色基团吸光度先增大后又减小,说明电晕放电等离子体可有效降解甲基蓝溶液。图3(b)为甲基蓝与H2O2作用过程的UV-Vis谱图。由图发现,H2O2与甲基蓝作用后,甲基蓝溶液紫外-可见谱图中原有的两吸收峰均消失,在279 nm与372 nm处产生新的吸收峰,说明H2O2有效破坏了甲基蓝结构,生成的中间物质在279 nm与372 nm有吸收[21]。进一步的定性分析将在后期进行。
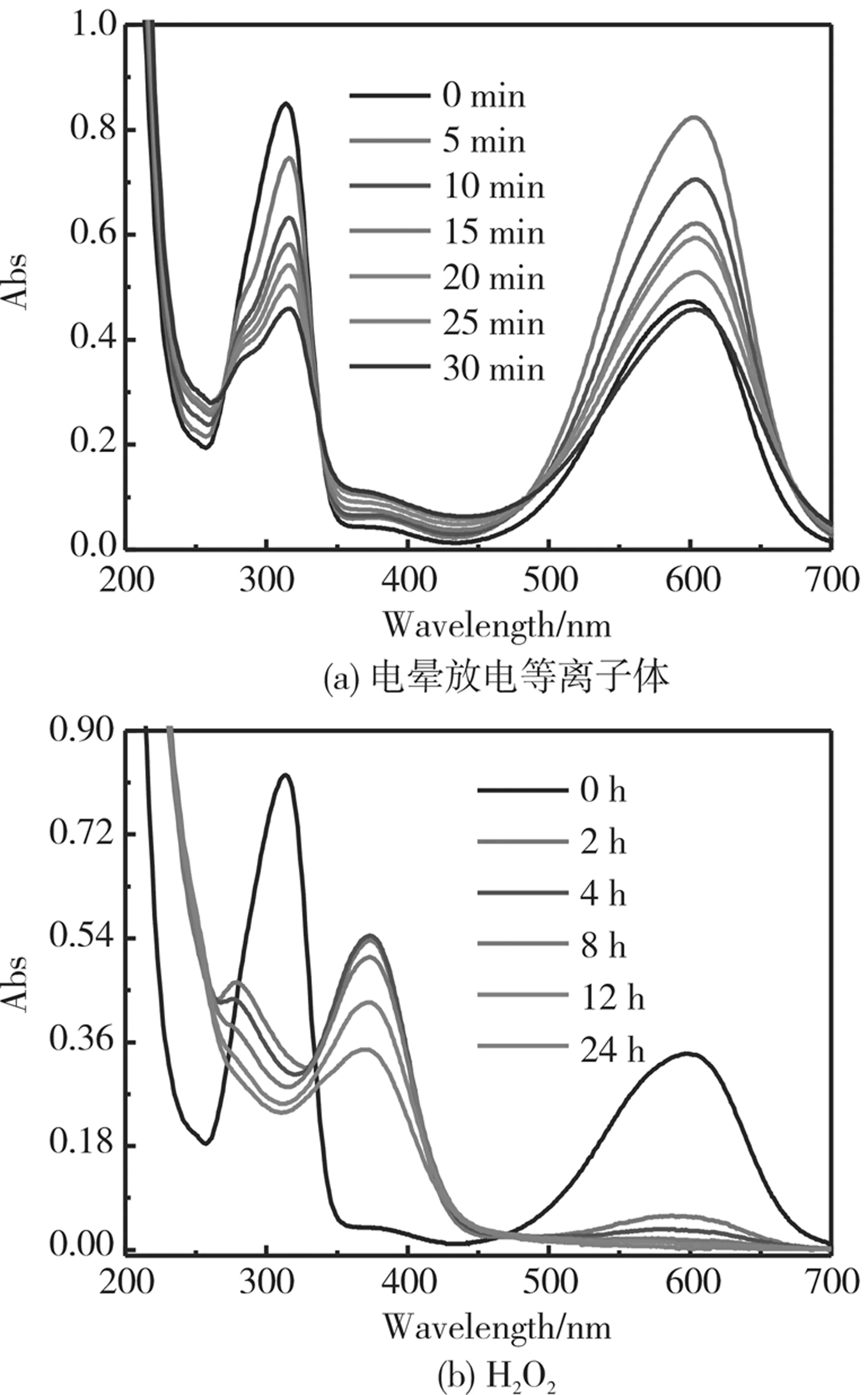
图3 电晕放电等离子体和H2O2 氧化降解甲基蓝溶液过程UV-Vis谱图Fig.3 Changes in the UV-Vis spectra with time during the process of Corona discharge and H2O2 oxidation
图4为H2O2氧化甲基蓝紫外-可见光谱图中新吸收峰的吸光度随H2O2体积分数变化图。由图观察到,H2O2的体积分数由1%增至2%时,两新吸收峰强度均增加,说明H2O2体积分数的增加破坏了更多的甲基蓝分子,进而生成更多的中间新物质;H2O2体积分数由2%增至3%时,新吸收峰强度没有明显变化,说明此时甲基蓝分子基本被完全破坏;H2O2体积分数由3%增至5%时,新吸收峰的吸光度逐渐降低,说明H2O2分解的OH·可有效降解中间新物质;但当H2O2的体积分数增至6%时,新峰吸光度又升高,此时H2O2分解产生的OH·达到饱和,过多的H2O2与OH·作用,从而消耗掉部分羟自由基,导致中间产物的浓度又逐渐升高,许志至[22]采用Fe2+/H2O2氧化体系降解实际印染废水研究中,H2O2用量增加时,溶液的COD去除率反而降低,所以过量的H2O2并不能对印染废水的降解达到更好的效果。因此选择H2O2的体积分数为5%对其中间物质的降解效果最好。
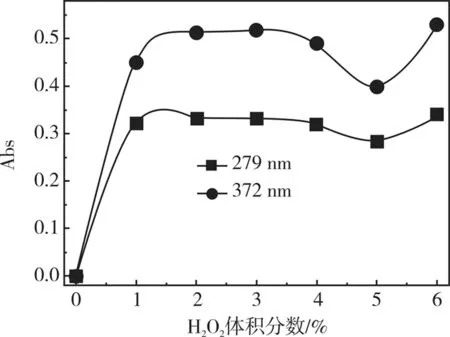
图4 不同体积分数H2O2对 UV-Vis谱图中新吸收峰吸光度的影响Fig.4 Effects of different volume fractions of H2O2 on the new adsorption in the UV-Vis spectra
2.3 甲基蓝溶液降解前后的FT-IR分析
甲基蓝降解前后的整体红外光谱如图5所示。为了更好地分析电晕放电及H2O2氧化对甲基蓝结构的影响,利用peakfit软件对红外谱图分峰处理,结果如图6所示。参照文献及红外光谱手册[23-24]对其进行解析,将各官能团和键的特征振动频率列于表1。
结合图5、图6及表1可以看出,相比甲基蓝原样谱图,降解后的样品谱图发生了明显变化。电晕放电降解30 min后,甲基蓝结构中N-H键3 432.8 cm-1处不对称伸缩振动峰红移了0.3 cm-1,烯烃和苯环上C-H键2 975.9 cm-1处的伸缩振动峰向高波数偏移了0.5 cm-1,1 638.7 cm-1处RCH=CHR的双键伸缩振动位置蓝移了3.2 cm-1,1 121.1 cm-1和1 034.3 cm-1处磺酸基S=O的伸缩振动峰分别红移了3.1 cm-1和15 cm-1;C=N,R2C=CR2与1 619.9 cm-1处脂和芳胺的吸收峰在降解后的样品中未出现,说明电晕放电有效打断了这3个键。此外,在1 692.4 cm-1和1 400.4 cm-1处各出现了一个新峰,分别是C=O和N=O的吸收峰,说明电晕放电等离子体技术有效破坏了甲基蓝结构。
H2O2氧化甲基蓝1 d,甲基蓝结构中N-H键3 432.8 cm-1处不对称伸缩振动峰红移了2.4 cm-1,烯烃和苯环上C-H键2 975.9 cm-1处的伸缩振动峰向低波数偏移了1.2 cm-1,1 676.7 cm-1处的R2C=CR2与1 638.7 cm-1处的RCH=CHR分别蓝移了2.2,0.3 cm-1,1 121.1 cm-1和1 034.3 cm-1处磺酸基S=O的伸缩振动峰分别红移了5 cm-1和4.3 cm-1;1 657.9 cm-1处C=N与1 619.9 cm-1处脂和芳胺的吸收峰在降解后的样品中未出现,说明H2O2氧化破坏了甲基蓝结构中C=N,另外在 1 386.4 cm-1处产生了N=O双键的吸收峰。
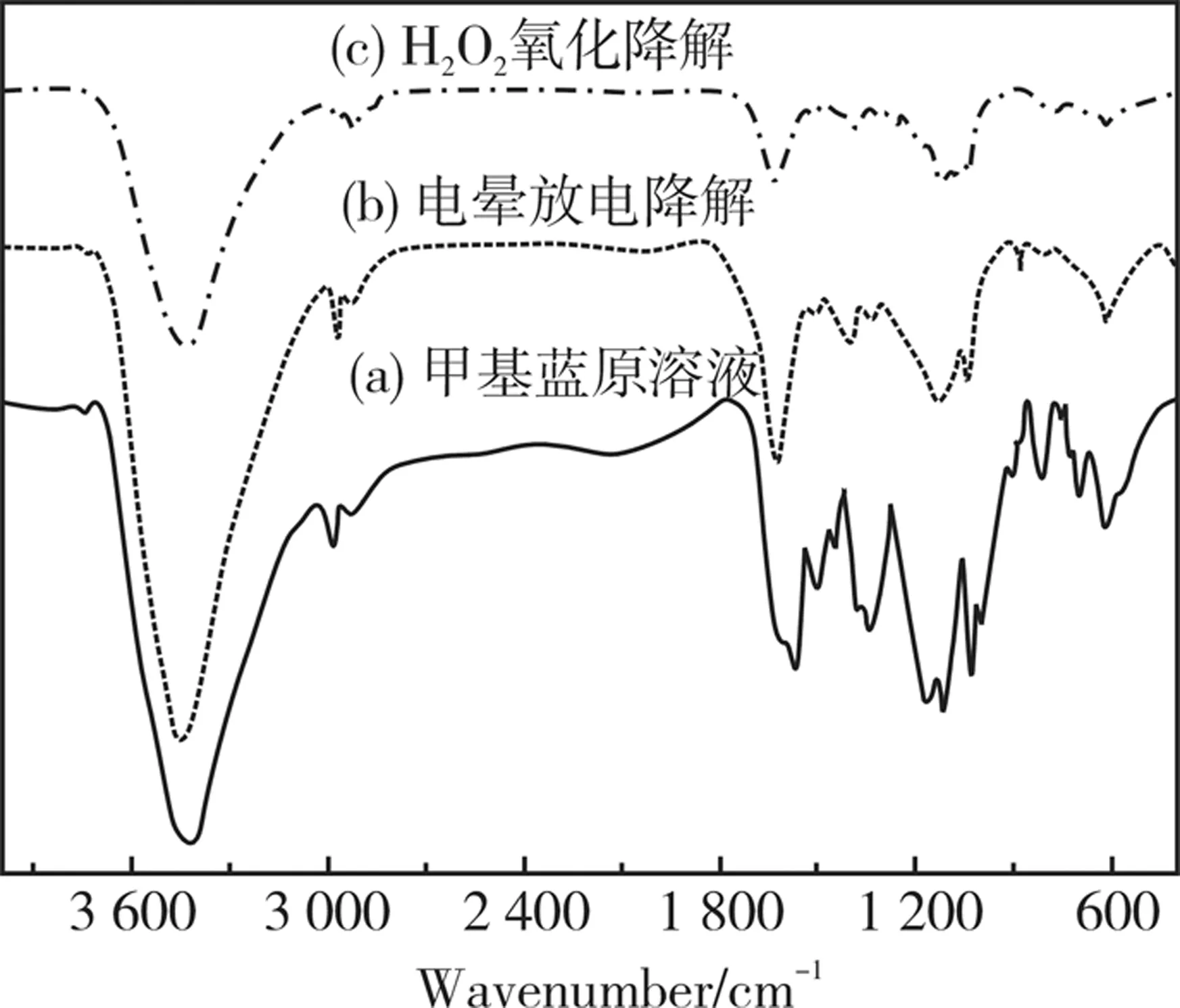
图5 甲基蓝溶液降解前后红外光谱图Fig.5 FT-IR spectra of methyl blue before and after degradation
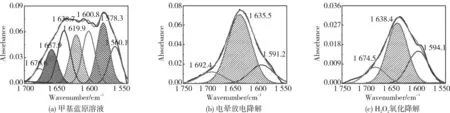
图6 甲基蓝降解前后的红外分峰图Fig.6 Fitting curves of FTIR spectra of methyl blue before and after degradation

基团特征振动频率类型甲基蓝原样峰位/cm-1电晕放电降解后峰位/cm-1H2O2氧化后峰位/cm-1NHυNH3 432.83 433.13 435.2δNH758.3,616.4616.3617.9=CHυ=CH2 975.92 976.42 974.7C=NυC=N1 657.91 692.4(C=O)-C=CR2C=CR21 676.7-1 674.5RCH=CHR1 638.71 635.51 638.4芳环骨架振动1 600.8,1 578.3,1 560.1,1 493.5,1 451.31 591.21 594.1,1 523.1CNυCN1 371.1,1 341.61 342.91 268.9,1 315.41 619.9(脂和芳胺)--
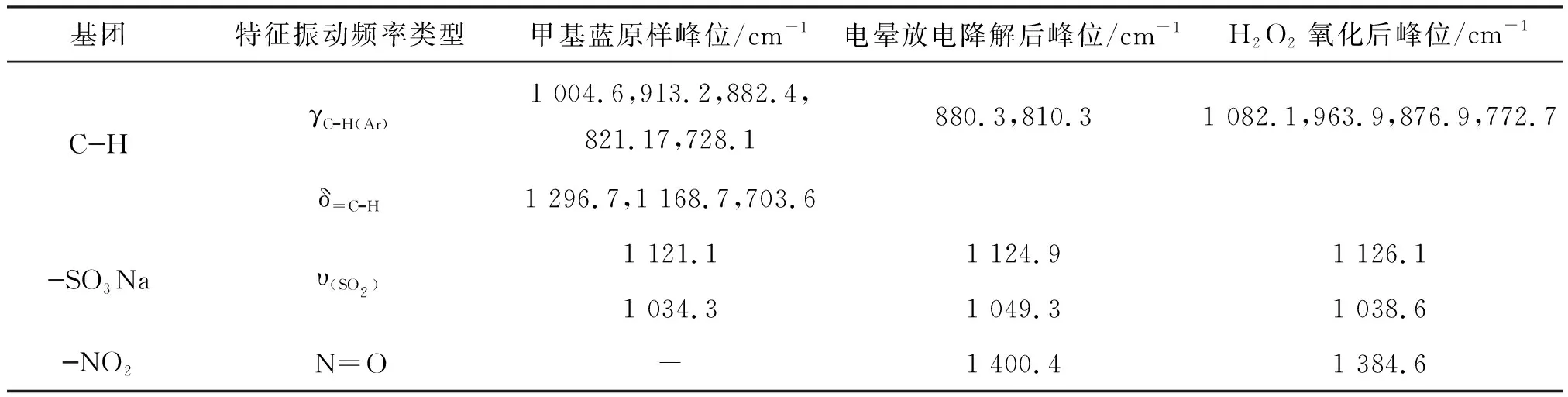
续表1 甲基蓝溶液降解前后红外官能团对照表Table 1 Comparison of FT-IR functional groups before and after degradation of methyl blue(continued)
注:“-”表示未检出该基团。
3 结论