高温煤气脱硫剂发展现状研究
2018-09-18卢建军
冯 宇 ,李 阳 ,卢建军 ,米 杰
(1.太原理工大学煤科学与技术教育部和山西省重点实验室,山西 太原 030024;2.太原理工大学轻纺工程学院,山西 晋中 030600)
目前,我国雾霾频发,大气污染状况严重,而燃煤排放被当作造成雾霾的罪魁祸首,大量的低阶煤由于热值太低得不到充分利用[1]。基于这一国情,有限煤炭等化石能源的高效转化与清洁利用成为我国亟待解决的重要问题[2]。
整体煤气化联合循环发电(IGCC)由于其所拥有的环境友好性、经济型和高效性,在许多国家和地区内被广泛研究和工业化应用[3,4]。然而,煤气化的产品气中含有的H2S,若不加脱除,直接用于发电会变成SO2污染大气,化工生产中用作合成氨、制氢、甲醇、合成油、合成天然气等的原料也会造成催化剂中毒失活。
目前国内外对脱硫剂性能的选择标准主要集中在以下几点[5,6]:(1)热力学性质:脱硫剂制备材料必须是热力学性能较优的,这样有利于在需要的温度下脱除99%以上的H2S;(2)硫容:高温煤气脱硫剂应具有优良的硫吸附能力,这将有助于减少脱硫剂的用量和体积上的要求;(3)脱硫剂硫化与再生动力学:硫化与再生动力学应维持较高速率以减少硫化-再生循环所需时间;(4)稳定性:脱硫剂应具有较高的机械与热稳定性,以抵御多次硫化-再生循环中的反复与长时间高温加热;(5)可再生性:金属硫化物完全转化回到金属氧化物而不产生副产物(例如硫酸盐)的能力,一般来说,再生反应是放热的,温度控制是防止烧结的必要条件之一;(6)低成本:脱硫剂材料应以低成本获得。
从20世纪中期至今,关于脱硫剂的制备工作已经有世界范围内的众多科研机构和学者进行了不计其数的试验和研究。如今被用在中高温煤气脱硫剂中的活性组分主要可以为两类:单一金属氧化物和复合金属氧化物。虽然煤气高温脱硫剂的研制已经取得了一定的成果,但是与工业要求还有一定的差距。本文针对目前高温脱硫剂存在的优缺点进行了系统的总结,并对今后脱硫剂的研究进行了分析。
1 单一金属氧化物脱硫剂
1.1 铁基脱硫剂
作为目前世界范围内研究和工业化最广泛的中高温煤气脱硫剂,氧化铁脱硫剂具有活性组分Fe2O3储量丰富、价格合理以及热力学性能优良、硫容大和反应活性高等优点[4]。
Lin等[7]在脱硫剂制备过程中,以铁元素含量为考察因素,发现通过增加脱硫剂中的铁含量可以显著提高脱硫剂的性能,且氧化铁脱硫剂的高反应活性归因于纳米铁颗粒在脱硫剂孔隙结构中的高度分散。Mi等[8]通过使用紫砂土作为载体制备氧化铁脱硫剂并进行了多次硫化-再生循环测试,结果表明在第一次硫化-再生循环之后,脱硫剂的硫容下降了约10%,但是在循环2次之后,硫容维持在一个固定数值不再降低,Mi等也因此认为该脱硫剂具有可被用于高温煤气脱硫的能力。Fan等[9]采用胶晶模板法制得三维有序大孔氧化铁脱硫剂(图1),并且在固定床反应器上对其进行了穿透动态评价实验。表征及实验结果证实,该脱硫剂大孔结构整齐有序,三维空间相互贯通,活性组分高度分散在载体上。对比传统方法制备的脱硫剂具有比表面积大和穿透硫容高的优点。

图1 三维有序大孔氧化铁脱硫剂Fig.1 Three-dimensionally ordered macroporous iron oxide for H2S removal
有学者在以赤泥为活性组分的脱硫剂制备过程加入黏土作为粘结剂,以期脱硫剂的循环使用反应活性和机械性能可以得到改善[10,11]。在固定床反应器测试中发现,该脱硫剂的脱硫性能在第5次循环中明显降低,这被归因于脱硫剂在连续循环中累积热烧结而引起的脱硫剂孔隙结构退化所导致。
综上可知,目前所研究的氧化铁脱硫剂已经具备较好的脱硫性能,但如何保证在多次的硫化-再生循环使用过程中确保铁基高温煤气脱硫剂的反应活性、硫容和机械性能保持稳定,仍然是困扰铁基脱硫剂成功工业化的关键问题之一,还需要更加深入的研究。
1.2 锌基脱硫剂
相比于其他氧化物,以ZnO为活性组分的脱硫剂拥有较高的脱硫精度和脱硫效率,这是因为ZnO和H2S的反应在热力学上具有更多的优势,能够把反应气中H2S的体积分数降低到低于10-6,这也是为什么众多学者将ZnO作为精脱硫剂的活性组分的最主要原因[3,4]。
为了消除硫化-再生循环过程中脱硫剂内部微观结构的反复收缩和膨胀产生的不良影响,Mi等[12]利用均匀沉淀法制备出ZnS脱硫剂前体,然后在空气气氛下通过原位合成法制备得到了新鲜ZnO脱硫剂。该方法基于金属硫化物的占位机制,可以在制备过程中预留较金属氧化物晶体所需的更大的内部空间,从而在脱硫剂硫化过程中避免了由分子体积扩大造成的脱硫剂内部体积膨胀而导致的脱硫剂结构性能降低,提高了单位脱硫剂的脱硫效率。Ma等[13]利用高压浸渍法将硝酸锌溶液负载到半焦上制备得到了Z20SC氧化锌脱硫剂。在固定床脱硫实验中,该脱硫剂前20h的H2S出口含量都为零,展现出了优良的反应活性和较高的穿透硫容。此外,硫化动力学结果表明,等效粒子模型可以很好的描述硫化反应:初始阶段硫化反应主要由化学反应控制,随后则由扩散控制。然而,有些观点则与传统ZnO硫化动力学所得出的ZnS向内生长不同,Neveux等[14]认为,硫化过程中ZnS成核之后经历了由内向外生长的过程,并且通过动力学研究证实了这一发现。

图2 35%ZnO/MCM-41脱硫剂的透射电镜图Fig.2 TEM micrographs of sorbent 35%ZnO/MCM-41
如图2中所示,Jia等[15]以硅酸钠作为硅源、单金属ZnO作为活性组分,通过一步水热合成法制备得到了MCM-41分子筛负载的纳米ZnO脱硫剂。研究发现,当脱硫剂负载质量分数35%的ZnO时,该脱硫剂具有最好的硫化性能并且硫容达到11.01g硫/100g脱硫剂。之后对该脱硫剂进行连续六次硫化-再生循环后发现,该脱硫剂在循环中的有效利用率均不低于70%,表明该ZnO/MCM-41脱硫剂拥有优良的化学和机械稳定性。
Kim等[16]利用由聚丙烯腈(PAN)衍生而来的碳纳米纤维(CNF)负载ZnO在600℃通过静电纺丝来制备中温脱硫剂,如图3所示。相比纯的ZnO脱硫剂,该脱硫剂由于载体CNF自身对H2S的物理吸附及ZnO在CNF上的均匀分布而拥有更大的硫容和更优良的脱硫性能。

图3 柔性氧化锌/碳纳米纤维的中温脱硫剂制备Fig.3 Preparation of flexible zinc oxide/carbon nanofiber webs for mid-temperature desulfurization
ZnO脱硫剂的硫容和穿透时间对温度比较敏感,随着温度的升高其硫容逐渐增大,且穿透时间也逐渐延长,尤其是在600~700℃范围内的脱硫反应快速且彻底。但是,ZnO在还原性气氛中被还原成单质锌之后,低熔点的单质锌会在高于600℃的温度下升华造成脱硫剂活性组分的流失,进而导致脱硫剂硫化性能的降低。
1.3 铜基脱硫剂
金属铜氧化物与H2S的反应之间具有良好热力学性质,然而,非结合形式下的CuO在H2和CO的存在的环境中很容易被还原成金属铜,这在很大程度上降低了脱硫剂脱硫效率[4,17]。因此,针对氧化铜脱硫剂的研究焦点主要是氧化铜的稳定性。为了解决氧化铜基脱硫剂的这一问题并提高氧化铜基脱硫剂的硫化性能,不少学者对将氧化铜负载到载体上或者与其他金属和金属氧化物掺杂混合的脱硫剂进行了广泛的研究。
为了能使氧化铜保持稳定,以至于不用完全还原成为单质铜,Abbasian和Slimane[18]设计了一种以Cr2O3为载体、以Cu2O为活性组分的CuCr-29铜基高温煤气脱硫剂,目标温度范围为550~650℃。实验证明,相对于γ-Al2O3,Cr2O3和Cu2O的结合更能使Cu2O在反应中保持稳定。随后,通过该脱硫剂的再生研究发现:在15个硫化-再生循环周期内,脱硫剂硫化性能维持稳定且脱硫剂中没有无硫酸盐的形成。
Kyotani等[19]研究发现氧化铜脱硫剂脱硫性能下降可以归结于两方面原因,首先,硫化产物是孔隙率很低的硫化铜,硫化铜覆盖在脱硫剂表面形成致密的外壳,限制了CuO与H2S脱硫反应的快速高效反应;其次,纯氧化铜孔隙率较低,可提供与H2S反应的面积很小。因此,在制备铜基高温煤气脱硫剂时必须加入孔隙结构丰富的载体来负载氧化铜,纯氧化铜很少被单独采用作为脱硫剂的活性组分。在发现问题的症结之后,Karayilan等[20]通过络合反应制备了Mn-Cu和Mn-Cu-V混合金属氧化物脱硫剂。研究结果表明当再生温度低于700℃时,再生后脱硫剂的脱硫活性显著降低,这可能是由于硫酸盐的形成而导致的结果。
总的来说,添加剂的加入能够在一定程度上抑制氧化铜被还原为单质铜,但对于铜基脱硫剂的改性并不是很成功。
1.4 锰基脱硫剂
氧化锰可以说是单一金属脱硫剂中最稳定的一个,在硫化反应过程中很难被还原为单质锰,且其硫容大,反应温度也很高,但是氧化锰的脱硫精度较低且再生时容易生成MnSO4[3,4]。Wang等[21]利用锰的不同前驱体通过超临界水浸渍法制备活性炭负载锰氧化物脱硫剂,并对这些脱硫剂的脱硫性能和物性进行了测试。研究发现,以Mn(NO3)2为前驱体的脱硫剂要比以Mn(AC)2为前驱体的脱硫剂具有更好的脱硫性能,这是因为Mn3O4可以很好的分散在活性炭上,而由Mn(AC)2得到的副产物MnSiO4则团聚在载体和活性组分表面,降低了该脱硫剂的硫化性能。
如图4所示,为了提高活性组分的分散程度,Liu等[22]以氧化锰为活性组分通过浸渍法制备了SBA-15负载型脱硫剂。在固定床石英反应器中700~850℃下进行的循环性能测试的结果表明:高度分散在SBA-15上的氧化锰和氧化铜具有可观的硫化性能和硫容。1Cu9Mn/SBA-15脱硫剂在800℃下的硫容达到了13.8g硫/100g脱硫剂,这也说明SBA-15在高温下良好的热稳定性增加了该型脱硫剂在高温下的硫容。BET、XRD等表征也表明该脱硫剂的结构在脱硫前后保持完整。

图4 SBA-15负载型锰基脱硫剂反应示意图Fig.4 Diagram of desulfurization using Mn/SBA-15 sorbent
Zhang等[23]利用工业水玻璃为硅源制备MCM-41分子筛并通过溶胶凝胶法制备得到了铁掺杂的氧化锰基脱硫剂。通过考察金属氧化物的负载量、铁锰比以及反应温度对该脱硫剂硫化性能的影响发现,铁掺杂之后,Fe3+可以取代Mn2O3立方晶体中的Mn3+形成 (FexMn2-x)O3作为脱硫剂的活性组分进行反应。同时,9次连续进行的硫化-再生循环也表明该FeMn4Ox/MCM-41脱硫剂具有较高的硫容和良好的循环稳定性。
1.5 钙基脱硫剂
钙基脱硫剂被广泛应用主要有两个原因:一是其所采用活性组分来源广泛、原料储量大、具有很大的价格优势;另外,得益于优良的动力学和热力学性能,氧化钙脱硫反应具有快速高效、硫容大的特点,且Ca价态单一,无论在还原性和氧化性气氛下其硫化性能都不会受太大影响[3,4]。然而,氧化钙脱硫剂同样有一些缺点,即在氧化钙与H2S反应之后,产生的硫化钙孔隙率低、较为致密,笼罩在脱硫剂外部,在很大程度上遏制了H2S与活性组分氧化钙的全面接触,进而使得脱硫剂的硫化性能退化[24];此外,钙基脱硫剂的再生副产物硫酸盐(CaSO4)同样会很轻松地“封闭”活性组分且导致脱硫剂无法完全再生,循环稳定性较差,使得脱硫剂使用寿命严重降低,很难达到工业化所需要的长期循环使用的要求。
由于钙基脱硫剂的再生反应是放热反应,不适当的硫化或者再生工艺条件会导致脱硫剂床层飞温、内部结构烧结,孔结构性能退化的同时其脱硫剂的机械强度变差。Wheelock等[25]提出对钙基脱硫剂的再生过程进行改良进而提高并改善钙基脱硫剂的机械稳定性:在空气中高于1000℃的高温下首先将硫化钙氧化生成硫酸钙,之后再将硫酸钙在一氧化碳下逐步还原为氧化钙。这样既能使钙基脱硫剂反应性得到全面再生还可以提高其机械强度。
然而,在实际操作中,钙基脱硫剂的再生过程远比上述文献中所描述的过程更为繁琐,极差的再生性能也是钙基脱硫剂应用范围狭窄并慢慢淡出研究视线的最主要原因。
1.6 稀土金属基脱硫剂
稀土金属氧化物在作为脱硫剂活性组分时,在强还原性气氛中700℃高温下依然可以保持较高脱硫精度和硫容,此外,硫单质可以通过简单的稀土金属氧化物的再生过程而被直接回收[3,4]。稀土金属氧化物在脱硫领域的应用有着很好的前景,并且在最近几年开始慢慢显现。
Stephanopoulos等[26]研究了以氧化铈和氧化镧为活性组分的脱硫剂,并在800℃下测试了其硫化-再生循环性能。研究表明,该型脱硫剂在很高的空速(80000h-1和400000h-1)下,吸附和脱附过程非常迅速,在很短的接触时间内(毫秒级别)可将H2S体积分数降低到百万分之几的水平。任何类型的无硫气体,包括水蒸气,都可以用来再生该脱硫剂。结果表明,稀土氧化物(氧化铈和氧化镧)在350~800℃的温度范围内,对各种燃料电池都是一种很好的可再生型燃料脱硫剂。
在稀土元素中,除了铈,镧和钐的氧化物同样被较多的应用在H2S的反应脱除中。Liu等[27]通过溶胶凝胶法制备了以M41为载体、具备高比表面积的氧化镧基高温煤气脱硫剂,由硫化-再生循环测试得到的结果可知,该型脱硫剂的穿透硫容和饱和硫容分别可达到3.24和3.70g硫/100g脱硫剂。在固定床反应器上进行的十余次硫化-再生循环测试也说明该氧化镧基高温煤气脱硫剂可以被应用在需要高稳定性脱硫剂的化工行业中。
类似的,Liu等[28]利用同样的制备方法和载体制备了以氧化钐为主要活性组分的高温煤气脱硫剂,并对硫化反应温度、空速以及脱硫剂组成对该脱硫剂性能的影响在固定床反应器上进行了考察。此外,他们还采用18O2同位素对硫化和再生过程进行了示踪法研究,Sm2O2S的存在极大地促进了硫化和再生反应的进行。硫化-再生循环测试表明该脱硫剂具备了在化工行业中应用的可行性。
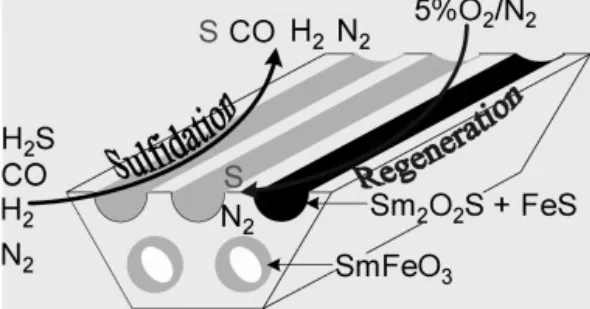
图5 介孔材料负载的氧化钐高温煤气脱硫剂Fig.5 Diagram of Sm-based/meso material supported sorbent
1.7 复合金属基脱硫剂
由于单一金属氧化物脱硫剂所存在的一些缺点,在一定程度上限制了高温煤气脱硫剂在工业领域的应用和推广。为了改善单一金属氧化物脱硫剂的硫化性能及优化其结构,有不少研究都把考察重心转移到了以复合金属氧化物为活性组分的脱硫剂制备当中。复合金属氧化物一般有两种形式:一是以两种金属氧化物的形式相互结合,这两种金属氧化物的选择大多数是存在一种优缺点互补的关系,以铁酸锌脱硫剂(ZnFe2O4)为例,即氧化铁的硫容很大,而氧化锌则热力学性能优良,对H2S存在很强的亲和力,可以做到精脱硫,因此,氧化铁与氧化锌的结合就能够在很大程度上改善脱硫剂的脱硫性能;二是一种活性金属氧化物混合另一种惰性氧化物,如Zn2TiO4。在脱硫剂的制备过程中加入惰性氧化物在充当脱硫剂活性组分载体的同时,不仅可以提高活性组分的分散度还可以增强脱硫剂的机械强度和稳定性。复合金属氧化物脱硫剂中,被关注较多、研究较为广泛的是钛酸锌(Zn2TiO4)、铁酸锌(ZnFe2O4)以及一些其他具有特殊结构或者电子特性的复合金属氧化物脱硫剂[3,4]。
铁酸锌脱硫剂既保持了氧化铁脱硫剂成本低、易于再生和硫容高的特点,又结合了氧化锌脱硫剂脱硫精度高、脱硫反应快的优点,与单一氧化锌或氧化铁脱硫剂的脱硫性能和脱硫精度相比均得到了很大幅度的提升[29],然而硫化-再生过程中金属锌的损失现象却依然存在,并不能完全抑制锌的流失。在高温还原气氛下,铁酸锌会分解生成氧化锌和氧化铁,所以,铁酸锌脱硫剂的使用温度一般局限在 600℃以内[4]。
随着对工业化和商用脱硫剂脱硫反应性、机械强度高、再生能力和稳定性等要求的提高,Li等[30]利用固定床反应器中在300℃下对采用溶胶-凝胶自燃烧法制备的Ni掺杂铁酸锌脱硫剂进行了硫化和再生性能测试。多次硫化-再生循环结果表明,铁酸锌脱硫剂的硫化活性在第二个周期中略有下降并在剩余的循环中保持稳定,这也表明镍改性后的脱硫剂保持了较高的反应性,而且硫化-再生循环中维持了较好的结构和机械稳定性。Ahmed等[31]的动力学研究结果则表明,添加少量的TiO2或者CuO可以通过优化脱硫剂孔隙结构而大幅度提高脱硫剂整体的硫化性能。
为了避免锌基脱硫剂活性组分的挥发损失,大量科研工作者重新引入了TiO2新物质,形成Zn-Ti面新型脱硫剂。中国科学院山西煤炭化学研究所的卫小芳和黄戒介等[32]对在在固定床反应器和热重分析仪上研究了Zn2TiO4脱硫剂的硫化和再生性能。结果表明:此脱硫剂在400~600℃范围内的反应活性很高。此外,还有学者[33,34]对添加Co3O4后钛酸锌脱硫剂的脱硫性能进行了考察,发现与纯钛酸锌脱硫剂相比,加入Co3O4后脱硫剂的反应活性和稳定性均得到了一定程度的改善。
除了上述的铁酸锌和钛酸锌脱硫剂,还有一些其他复合金属氧化物脱硫剂同样具备较好的硫化性能。如图6,Xia等[35]制备了Mn-Fe-Mo/FSM-16复合型高温煤气脱硫剂,并在固定床上550~750℃范围内考察了脱硫剂的脱硫性能。结果发现,600℃下,50%4Mn1Fe-3%Mo/FSM-16脱硫剂的硫化性能最好,且硫容高达18.15g硫/100g脱硫剂。

图6 Mn-Fe-Mo/FSM-16脱硫剂硫化及再生过程示意图Fig.6 Diagram ofthe desulfurization-regeneration process using Mn-Fe-Mo/FSM-16 sorbent
此外,通过飞行质谱(TOF-MS)测定发现在再生过程中的硫单质可以被高效回收。
综上所述,为了弥补单金属氧化物脱硫剂的不足,除了铁酸锌和钛酸锌外,国内外研究者们还在其他方面进行了大量探索,主要集中在两种或者两种以上金属之间的组合,或者通过助剂或者载体的选择来改善其脱硫性能。
2 结语
单一金属高温煤气脱硫剂各有优缺点和适用范围,而复合金属高温煤气脱硫剂则结合了单一金属脱硫剂的优点摒弃了缺点,在脱硫效率、使用温度以及再生性能方面都有很大的提高。总的来说,各种脱硫剂都具有其优点及特点,脱硫剂要根据实际工业情况去因地制宜地进行选择和使用。
