特立氟胺治疗多发性硬化的临床研究进展
2018-09-10檀国军郭力
檀国军 郭力
近20年来,疾病修正疗法(disease-modifying therapy,DMT)逐渐成为多发性硬化(multiple sclerosis,MS)治疗的长期综合管理策略,旨在减少MS复发频率、减轻恶化的程度、延缓疾病自然进程并缓解患者临床症状、改善患者预后[1]。早期MS常用的DMT手段以注射给药为主,如干扰素 β(interferon-β,IFN-β)、醋酸格拉默等,但注射给药途径的不便性在很大程度上限制了MS患者的应用人群,大大降低了长期用药的依从性,约20%~46%的患者可能因此中断治疗[2]。口服免疫调节剂如特立氟胺(teriflunomide)的研发大大提高了患者的治疗自我满意度与依从性。2012年,特立氟胺成为首个在复发-缓解型MS患者中获批上市的口服DMT类免疫调节剂,并逐渐成为MS的一线治疗选择。本文回顾了特立氟胺在MS人群中的作用机制、研究历程与最新临床数据,旨在为临床医生提供循证依据。
特立氟胺是一种可逆性的二氢乳清酸脱氢酶抑制剂和免疫调节剂,能可逆性抑制二氢乳清酸脱氢酶(一种嘧啶从头合成的关键线粒体酶)的活性,阻止新生嘧啶合成,进而抑制活化T、B细胞的增殖,使CD4+/CD8+T细胞比值增高、调节性T细胞数量增加。静息淋巴细胞的稳态增殖可通过嘧啶补救合成途径来实现,因此,特立氟胺不干扰静息态淋巴细胞的稳态增殖[3-4]。
特立氟胺的口服生物利用度近100%,口服摄入后的1~4 h内到达血浆峰值。半衰期约为18~19 d,约3个月时可达到稳态水平。主要经胆汁排泄,血液透析或腹膜透析无法清除。
1 有效性
1.1 随机对照研究
2001年4月开展的一项Ⅱ期概念验证研究(NCT 01487096)首次证实了特立氟胺的有效性和安全性,特立氟胺7 mg与14 mg治疗患者36周发现孤立活动病灶数量分别下降了61.1%和61.3%,临床转归及磁共振成像预后也有所改善[5]。另几项Ⅱ期研究则证实,与单用IFN-β[6]或醋酸格拉默[7]相比,特立氟胺联合治疗可带来更多获益。此外,NCT01487096的扩展研究验证了特立氟胺的长期安全性,并推动了多项Ⅲ期研究的开展[8]。
多项Ⅲ期临床研究均显示[9-13],特立氟胺较安慰剂可显著降低MS患者的年复发率 (annualized relapse rate,ARR,风险降低 22.3%~36.3%,P≤0.01)、增加无复发患者的比例(P≤0.01)、延缓新发或复发性钆增强T1病灶出现的时间(P≤0.002)、延缓总病灶体积的增大(增长速度降低67.4%,P=0.0003)、减少联合孤立病灶出现的风险(降低69%,与其他所有组别比较P<0.001)、降低患者出现持续残疾恶化的风险(降低 29.8%~31.5%,P≤0.03)、降低患者复发事件的风险(P<0.01)、改善患者残疾状况评分(P<0.05)。TESMO亚组分析还显示,所有组别的MS患者(不同年龄、性别、疾病状态、MS亚型、MRI特征、总病灶体积、既往DMT治疗史)均可从特立氟胺治疗中获益(组间P>0.05)[14]。TENERE研究则显示特立氟胺 14 mg治疗与IFN-β治疗的有效性类似,两组的校正ARR无差异(0.26 vs.0.22)。此外,特立氟胺治疗组的治疗满意度评分较IFN-β治疗有明显改善[15]。
荟萃分析显示[16],无论是特立氟胺7 mg[危险度(risk ratio,RR)=0.72]或 14 mg 治疗(RR=0.67),均较安慰剂显著降低MS的ARR。14 mg特立氟胺还可显著延缓患者的残疾进展(与安慰剂相比RR=0.69;进展定义为EDSS评分较基线时增加≥1分,或基线时评分≥5.5分的患者增加≥0.5分,且持续≥12周)。
RADUE等分析了TEMSO研究中的969次MRI随访图像(基线患者N=801),在评估特立氟胺对复发型MS患者脑体积萎缩程度的影响后发现[17],自基线开始的1年和2年时,特立氟胺使患者的脑体积萎缩风险分别降低了36.9%(P=0.0001)和 30.6%(P=0.0001)。 这一结果与特立氟胺延缓残疾恶化的临床效应一致,亦提示特立氟胺具有潜在的神经保护作用。
目前还有两项研究正在评估特立氟胺在不同亚组MS患者中的最佳获益。TERIKIDS(NCT02201108)是一项评估特立氟胺在儿童RRMS患者中有效性和安全性的III期试验;一项Ⅳ期研究(NCT01970410)则旨在评估特立氟胺治疗那他珠单抗治疗中止后、伴有进行性多灶性白质脑病发生风险患者的有效性和安全性。
1.2 长期扩展研究 Ⅲ期研究TEMSO随访9年的扩展研究(n=742)显示[18],中位治疗时长超过 190(最长 325)周/患者时,63%的患者仍在接受治疗。特立氟胺组患者的ARR较安慰剂组显著降低,所有治疗组绝大多数评估时间点的ARR均<0.3,且随着治疗时间的推移,ARR仍在持续下降。≥55%的患者研究期间疾病无复发。特立氟胺14mg治疗组患者发生残疾进展的风险显著低于安慰剂组[P=0.03;特立氟胺组扩展残疾状态量表 (expanded disability status scales,EDSS)评分≤2.5分]。从安慰剂转换为特立氟胺治疗后,患者T1-Gd病灶平均数量减少,且此后一直维持较低水平(≥80%的患者研究期间无T1-Gd病灶出现),提示特立氟胺长期治疗的良好有效性[18]。TOWER最长随访6年的扩展研究 (n=751)结论与之类似,患者的ARR和EDSS评分在特立氟胺长期治疗期间均可维持较低水平[19]。
总之,特立氟胺长期治疗期间,患者疾病活动度下降,且在治疗期间维持在较低水平,患者发生残疾进展的风险也显著降低。在影像学方面,长期治疗可使MRI显示的病灶总体积缩小,T1-Gd病灶和孤立活动性病灶数量减少[20]。
1.3 早期治疗研究 10%~85%的临床孤立综合征(clinically isolated syndrome,CIS)患者会最终发展为临床确诊的MS(clinically definite MS,CDMS)[21]。 MRI正常和异常的 CIS患者转化为CDMS的风险分别为20%和80%[22]。多项对照临床研究显示,DMTs药物可降低高风险CIS患者的CDMS转换率并减少新发MRI病灶[13,23],且早期应用DMTs药物在CDMS转换率和减少发作次数方面可长期获益,最长随访11年时,患者的残疾进展和疾病进展率仍处于较低水平[24-26]。
TOPIC研究证实了特立氟胺在CIS人群中的显著临床获益[13]。与安慰剂相比,特立氟胺7 mg与14 mg治疗均显著降低CIS患者因复发而进展为CDMS的风险(分别降低37.3%和 42.6%,P≤0.027),降低MRI表现的复发风险(即MRI可见新发病灶风险,分别降低31.4%和 34.9%,P≤0.002),降低患者 ARR(分别降低 33.1%和 31.9%),并减少T1-Gd增强病灶数量 (分别减少 21.4%和 58.5%,P=0.0008)[18]。 TOPIC 扩展研究(最长随访 7 年,n=423)则显示,≥78%的CIS患者至随访结束时都未发生12周残疾进展事件,≥63%的患者未经历因复发而进展为CDMS的临床事件。与最初接受安慰剂治疗、进展时再开始特立氟胺14 mg治疗的患者相比,最初即接受特立氟胺14 mg治疗的患者转化为 CDMS的风险显著较低 (HR:0.529,P=0.0149)[27]。
1.4 真实世界研究 一项真实世界、观察性队列研究回顾性分析了102例复发-缓解型MS患者 (随访最长28个月)及其1521份血液样本的数据[28],结果显示,11%的特立氟胺治疗患者随访期间EDSS评分有所改善,67.5%的患者EDSS评分维持稳定。共10例患者(9.8%)发生复发,其中3例在治疗开始后6个月内复发。约16.5%(n=17)的患者中止特立氟胺治疗,其中53%因不良事件、29%因复发中止。真实世界的有效性和安全性数据支持了特立氟胺随机对照研究的结果。
另一项主要探讨患者报告转归包括治疗满意度的真实世界Ⅳ期研究(Teri-PRO,n=1000)则显示[29],采用药物治疗满意度调查问卷(treatment satisfaction questionnaire for medication,TSQM V1.4,包括有效性、副反应、便利性和全球满意度)进行评估时,复发型MS患者接受特立氟胺治疗48周后的平均TSQM全球满意度评分处于较高水平(68.2分),其他治疗满意度如有效性等评分亦较高(66.3~90.4分)。从其他药物转换至特立氟胺治疗的患者,治疗48周后的所有四方面TSQM评分项目均有显著改善 (P<0.0001)。其次,患者治疗依从性高,98.2%的患者报告治疗依从度≥80%。不良事件特征谱也与既往随机对照研究一致。因此,真实临床应用中的患者对特立氟胺治疗保持较高的满意度,而从其他药物转换至特立氟胺治疗的患者中治疗满意度也显著提高;而高满意度可能会进一步提高患者依从性,并进一步改善长期转归。
1.5 中国人群研究 32个中心共148例 (12.7%)中国RRMS患者参与了TOWER研究[30],患者随机接受特立氟胺7 mg、14 mg或安慰剂治疗≥48周,主要和次要研究终点分别为ARR和12周残疾进展风险。除了中国患者首次MS症状发作至入组的时间较短 (平均5.02年vs.全球平均8.0年)、以及2年内曾接受其他DMT治疗的患者比例较小(2.0%vs.32.8%)之外,纳入中国患者的其他人口学特征和基线特征与全球总体TOWER人群一致。结果显示,在中国人群中,特立氟胺14 mg较安慰剂大幅降低患者的 ARR(下降71.2%,P=0.0012)和 12周残疾进展风险(68.1%,P=0.1194)。不良事件的发生率与全球总体人群类似,其中2例死亡事件(安慰剂组呼吸道感染致死1例;特立氟胺14 mg组自杀1例)均考虑与治疗无关。因此,特立氟胺在中国人群中的有效性和安全性转归均与全球总体人群一致[30]。
2 安全性
特立氟胺主要II期、III期临床研究如NCT01487096[8]、TESMO[18]、TOWER[19]和 TOPIC[20]研究的长期安全性数据(累积特立氟胺暴露时长超过6800患者/年)显示,在最长达13年的长期治疗过程中,特立氟胺治疗无新型或预期外的不良事件发生,提示其安全特性在长期内无改变。所有研究中因不良事件导致治疗中止的发生率均<15%。多数研究均可观察到中性粒细胞和淋巴细胞数量减少,但平均数量仍在正常范围且治疗期间维持稳定 (平均减少≤15%)。随访长达9年时,仅<6%的患者上报中性粒细胞和白细胞减少症,且并未导致严重或机会致病性感染风险增加。无血液细胞恶性肿瘤事件。因此,特立氟胺长期治疗并不影响机体的免疫保护功能,这可能与其免疫调节剂而非免疫抑制剂的作用机制有关[20]。
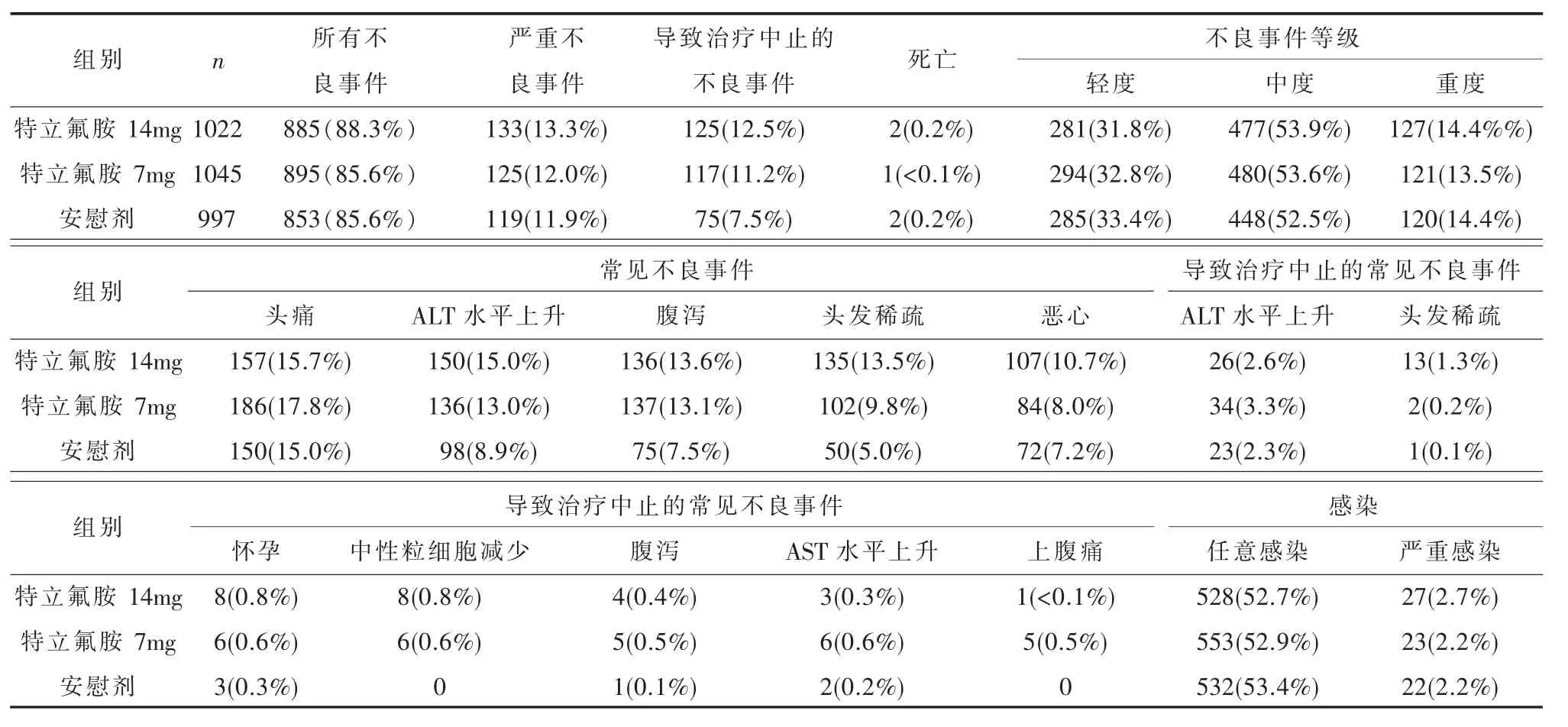
表1 特立氟胺安全性meta分析结果
荟萃分析(n=3044)显示,特立氟胺14 mg或7 mg组患者与安慰剂组患者常见不良反应事件的发生率分别为≥10%和≥5%,包括丙氨酸氨基转移酶(alanine aminotransferase,ALT)水平上升、头痛、腹泻、头发稀疏和恶心等。绝大多数不良事件都是轻至中度的,具有自限性且较少导致治疗中止。ALT水平上升是最常导致治疗中止的不良事件,治疗方案规定一旦确认ALT水平上升至3倍正常上限就应立即停止治疗;其次最常导致治疗中止的事件分别为头发稀疏和怀孕[31]。特立氟胺与安慰剂治疗的严重不良事件发生率无明显差异,总体而言,特立氟胺的安全性与耐受性特征与安慰剂类似[16](表1)。此外,还有两项研究显示特立氟胺不损害疫苗(如流感疫苗[32]和狂犬病疫苗[33])的有效免疫反应和血清保护率。
因此,两种剂量的特立氟胺长期安全性特征均稳定、一致且可管理[31]。中国患者人群应用特立氟胺的不良事件特征谱及发生率与全球总体人群一致[30]。美国食品和药品监督管理局关于特立氟胺安全性监测的指南建议,服用特立氟胺前应检测血常规、肝功能、血压,并进行结核筛查;治疗开始后的前6个月每个月监测肝功能,之后每6个月监测一次;出现肝毒性症状时及时监测血常规,并周期性监测血压[34]。
3 总结
多项特立氟胺单药或联合治疗复发型、复发缓解型MS的II/III期临床试验,均证实特立氟胺在MS人群中具有良好的有效性和安全性。真实世界的长期治疗过程中,特立氟胺也可持续、稳定有效,安全性易于管理,长期治疗期间无新型的、预期外的安全性事件发生。患者报告的转归调查还显示,特立氟胺长期治疗的患者依从性好、治疗满意度高。此外,早期控制疾病活动性对减少临床和亚临床发作、延缓疾病进展、预防患者残疾加重和维持生活质量具有关键作用。基于CIS患者的临床数据,早期识别和DMT治疗可能使MS患者获得改善短期或长期临床结局的最佳机会。
特立氟胺具有便捷的服用方式、一致且显著的有效性和良好的耐受性。中国人群的疗效及安全性与全球总体人群表现一致,也为特立氟胺在中国患者中的应用提供了循证依据。
