多孔Ti/SnO2-Sb2O5/CNT-PbO2电极的制备及其电催化氧化有机染料废水的研究
2018-09-01邢俊涛周秉武
邢俊涛 周秉武
上海闵欣环保设备工程有限公司 (上海 201109)
随着有机合成染料工业的发展,染料在纺织、皮革、造纸、汽油和食品等行业被广泛用作着色剂[1-3]。因此,大量有毒和生物不可降解的有机染料污染物排放到环境中,这对人类健康和生态系统具有很大的危害[4]。研究发现,这些污染物采用常规的处理方法(物理吸附[5]、化学氧化[6]、生物降解[7])都不能得到有效治理。因此,一种有效的有机染料污染物的降解技术为当前形势所需[8]。
在去除有机污染物方面,高级氧化工艺(AOPS)被认为是更绿色和更有效的方法之一,如光催化氧化[9]、芬顿氧化[10]、电催化氧化[11]等。电化学氧化技术是在电流作用下利用反应体系中产生的高活性氧化剂氧化分解有机物。该技术具有氧化效率高、反应速率快、操作简便、易自动化管理[12-13]的特点,电极材料通常在电化学氧化中起重要作用。许多专家已经对铂(Pt)[14]、石墨[15]、生化需氧量(BDD)[16]、氧化钌(RuO2)[17]、氧化铱(IrO2)[18]和氧化锡(SnO2)[19]等电极材料用于电催化氧化有机污染物进行了研究。近年来,多孔钛(Ti)作为一种新型材料,具有耐蚀性好、比表面积大、孔隙率高、生物相容性好等优点,被广泛应用于电化学氧化[11,20-21]。赵伟等[21]研究了多孔Ti作为基体材料对二氧化铅(PbO2)电极的理化性质和电化学性能的影响[11]。何亚鹏等在多孔Ti基底上掺杂含硼金刚石制备出一种新型的膜电极,用来促进有机污染物的电化学氧化。与此同时,碳纳米管(CNT)因其优良的化学稳定性、大的比表面积和优良的导电性成为最有应用前景的电极载体材料。李海珍等[22]利用CNT制备出的CNT@MCo2O4(M=Ni,Mn,Cu,Zn)4 种杂化材料能有效吸附可引起肺水肿的甲基橙染料污染物。吴根英等[23]利用CNTs的优异性能和氟树脂(FR)的憎水性能,采用电化学共沉积法制备出掺杂型FR-CNTs-PbO2/SnO2-Sb/Ti(Sb为元素锑)复合电极,发现该电极对罗丹明B染料废水的去除率高达90%。
在本研究中,为提高PbO2电极的性能提出了一种改进多孔Ti/SnO2-Sb2O3/PbO2电极的方法,以多孔Ti作基体,采用涂覆法和电沉积法制备了三维多孔Ti/SnO2-Sb2O3/CNT-PbO2电极,分别对多孔Ti/SnO2-Sb2O3/PbO2和多孔Ti/SnO2-Sb2O3/CNT-PbO2电极的结构参数和电极稳定性进行了表征。同时对两种电极进行了电化学性能测试,最后利用两种电极对有机染料污染物(罗丹明B、亚甲基蓝、酰胺黑10B)的模拟废水进行电催化氧化研究。
1 实验部分
1.1 试剂
外径为50 μm,长度为10~20 m 的 CNT,中国科学院成都有机化学有限公司;多孔Ti(w=99.9%,20 mm×20 mm×1 mm),宝鸡金凯科工贸有限公司;五水合氯化锡(SnCl4·5H2O)、三氯化锑(SbCl3)、硝酸铅[Pb(NO3)2]、氟化钠(NaF)、盐酸(HCl)、氢氧化钠(NaOH)、异丙醇、硝酸(HNO3)、硫酸钠(Na2SO4)、亚甲基蓝、酰胺黑10B、罗丹明B,分析纯,国药集团化学试剂有限公司。
1.2 电极的制备
1.2.1 多孔Ti基体预处理
多孔 Ti基板尺寸为 20 mm×20 mm×1 mm,用600目(0.325 mm)砂纸打磨,在15%NaOH中于60℃下脱脂30 min;将基材在30%HCl中于100℃下蚀刻1 h,得到均匀粗糙的灰色基体;在超纯水中,控制功率为 150~180 W,超声(30~50 kHz)清洗 20~60 min,得到经预处理的多孔Ti板基体,置于去离子水或异丙醇中保存。
1.2.2 中间层SnO2-Sb2O3的制备
先将预处理后的Ti基体浸入涂层溶液(0.475 g SbCl3,6.65 g SnCl4·5H2O 和 1 mL 浓 HCl溶解在 25 mL异丙醇中)5 min,置于130℃的烘箱中干燥10 min,然后把带有涂层溶液的基体放入马弗炉中,在500℃下热氧化15 min。上述过程重复12次,最后将电极在500℃下烧结60 min,这样Ti基体表面即可制备出SnO2-Sb2O3涂层。中间层制备的主要目的是增加电极的电导率,同时阻止TiO2在Ti基体表面的形成[24]。
1.2.3 活化层PbO2和CNT-PbO2的制备
以多孔Ti/SnO2-Sb2O3(4.0 cm2)为阳极,铜箔电极(30 mm×30 mm)为阴极,在电解液 [0.1 mol/L HNO3,2 g/L CNT,0.5 mol/L Pb(NO3)2和 0.04 mol/L NaF]中,电极间距为1.5 cm、电流密度为20 mA/cm2、65℃的条件下电沉积1 h,即得多孔Ti/SnO2-Sb2O3/CNT-PbO2电极。利用相同的方法制备得到多孔Ti/SnO2-Sb2O3/PbO2电极,只是电沉积溶液中不加入CNT。
1.3 电极的表征
1.3.1 物理表征
电极的表面形貌采用 S-570型扫描电子显微镜(SEM,日立高新技术公司)观察,并利用该仪器配备的X射线能谱仪(EDS)测定电极的元素含量。
采用D-max/3C型 X射线衍射仪(XRD,日本理学株式会社)测定电极的晶体结构,测试条件为:Cu靶K系射线为射线源,电压为 45 kV,电流为30 mA,扫描速度为 0.02(°)/min。
1.3.2 电化学测试体系
采用循环伏安和线性极化曲线对电极的电化学性能进行测试。电化学测试仪器为CHI 760 D电化学工作站,所有测试均采用标准的三电极体系:工作电极为待研究电极,参比电极为饱和甘汞电极(SCE),辅助电极为铂片电极。
线性极化曲线的测量:在三电极体系中,将工作电极置于电极液为0.5 mol/L H2SO4的体系中进行测定,扫描电位范围为0.5~2.5 V(相对于SCE,下同)。
加速寿命的测量:采用加速寿命测试实验来考察所制备电极的稳定性。相关测试方法为:以所测试电极为阳极,铜箔作为阴极,电极间距为1.5 cm,在常温(25℃)下,3 mol/L H2SO4溶液中,500 mA/cm2的电流密度下进行恒电流电解,测定电极电位随时间的变化,当电位达10 V时即可认定为电极失效。
计时电流曲线的测量:在三电极体系中,将工作电极置于电极液为0.5 mol/L H2SO4的体系中(含有各种有机污染物和不含有机污染物)进行测定。
交流阻抗曲线的测量:在三电极体系中,将工作电极置于电极液为0.5 mol/L H2SO4的体系中进行测定,电化学阻抗谱(EIS)实验电位选择在析氧区(E=1.85 V,相对于SCE),振幅为10 mV,扫描频率范围为 100 kHz~100 MHz。
1.4 羟基自由基(·OH)强度的测定
对苯二甲酸作为捕获剂极易与·OH反应生成具有高荧光性的产物对2-羟基对苯二甲酸,该物质的生成量和电化学反应过程中产生的·OH的量相等,因此可以通过荧光光谱仪测定对2-羟基对苯二甲酸的荧光强度来表征·OH的产生量。具体测定方法如下:
利用自制的多孔Ti基体电极作为阳极,以等面积大小的不锈钢作为阴极,含有0.5 mol/L对苯二甲酸、0.5 g/L NaOH以及0.25 mol/L NaSO4的溶液作为电解液,电流密度为30 mA/cm2,在常温下进行电化学反应,每5 min取样2 mL,用去离子水稀释10倍,采用LS-50荧光光谱仪(美国Perkin Elmer公司)测量对2-羟基对苯二甲酸的荧光光谱,激发波长为315 nm,发射波长为425 nm,荧光光谱的测定范围为380~520 nm。
1.5 电催化氧化有机染料污染物
选取一些典型染料有机物(罗丹明B、酰胺黑10B和亚甲基蓝)模拟废水进行电催化氧化实验。分别用多孔Ti/SnO2-Sb2O3/CNT-PbO2和Ti/SnO2-Sb2O3/PbO2电极作阳极、铜箔作阴极,电极间距为15 mm,电解液为0.05 mol/L Na2SO4,在实验之前将pH调节至7,模拟废水溶液体积为80 mL;使用直流电源(RXN-605D)将电流密度控制在30 mA/cm2,搅拌速率约为800 r/min;实验在25℃下进行120 min。在电解过程中,定期取样,用TU-1810紫外/可见分光光度计(北京普西仪器有限公司)分析有机染料污染物的颜色,并测定过程中化学需氧量(COD)的值。
电极电催化氧化过程中的电流效率(GCE)和能耗(SCE)通过公式(1)和(2)计算可得。
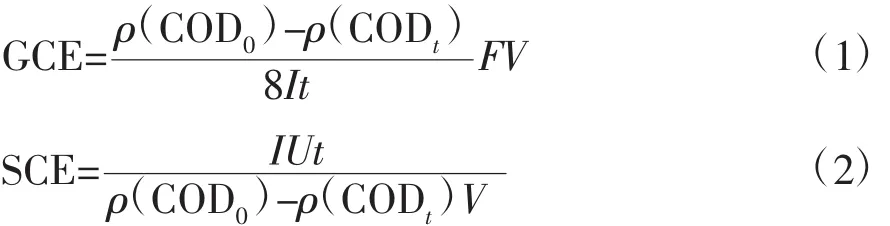
式中:ρ(COD0)和ρ(CODt)分别为模拟废水COD初始质量浓度和降解t时间后的质量浓度,mg/L;U为电位,V;I为电流,A;F 为法拉第常数,96485 C/mol;V为电解液体积,L。
2 结果与讨论
2.1 电极形貌与晶体结构
2.1.1 SEM与EDS表征
图1中 (a)~(d)为不同多孔Ti基体表面的SEM图。从图1(b)可以看到,多孔Ti板具孔洞结构,与图1(c)相比,CNT掺杂[图1(d)]的电极表面致密均匀,有利于提高其比表面积和PbO2电极的稳定性。图1中 (e)、(f)是活性层PbO2和CNT-PbO2的能谱图,从(f)图中可以看到活性层中含有Pb,C,O元素,说明CNT分散到多孔Ti基体PbO2活性层中。另外,CNT-PbO2表面晶粒较小,主要是由于CNT为PbO2在Ti/SnO2-Sb2O3上的生长提供了更多的接合点,使得PbO2结晶的机会提高。

图1 不同多孔Ti基体表面的表征结果
2.1.2 XRD表征
为了进一步验证图1观察的结果,同时也检查电极涂层的晶体结构和晶格参数,不同Ti基体上所制备的电极涂层的XRD图谱如图2所示。
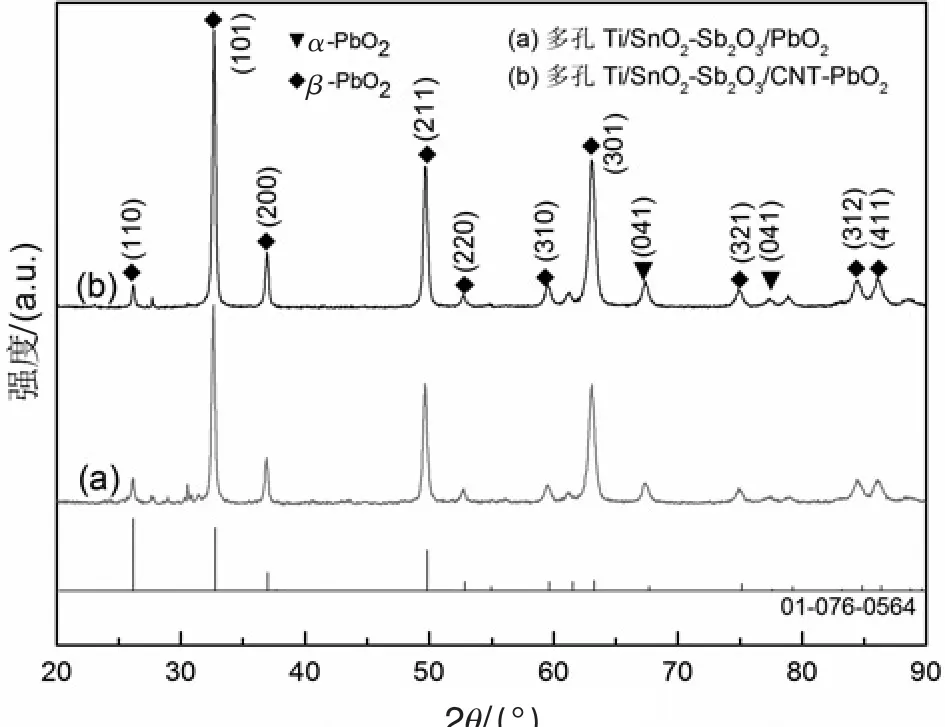
图2 电极的XRD图
2θ分 别 为 25.3°(110),32.7°(101),36.4°(200),48.9°(211),53.2°(220),59.3°(310),63.2°(301),75.3°(321),85.8°(312)及 85.9°(411)时出现了 β-PbO2晶体的衍射峰;标准图谱中,32°(101),49.2°(211)和 59.2°(301) 三处衍射峰最强。在 2θ为 67.8°(041),76.9°(400)处出现了微弱的α-PbO2晶体衍射峰。这表明电极的电导率因β-PbO2晶体的形成而增强。从图中对比得出,CNT掺杂改性后的电极出峰强度相对更高,衍射峰半宽度相对减小,即CNT的掺杂使得结晶角度增加,结晶尺寸偏小,这与图1的分析相吻合。电极表面晶体越小,比表面积越大,电极活性部位的表面积也越大,电催化活性也相对较高。
2.2 电极电化学性能分析
2.2.1 线性极化曲线的比较研究
图3表示了在0.5 mol/L H2SO4溶液中20 mV/s的扫描速率下不同电极的线性极化曲线。结果表明,多孔Ti/SnO2-Sb2O3/CNT-PbO2的析氧电位(1.83 V)高于多孔 Ti/SnO2-Sb2O3/PbO2(1.79 V)。塔菲尔(Tafer)曲线是评估析氧电位的另一种方法[27-28]。从图3中的插图可以看出,多孔Ti/SnO2-Sb2O3/CNTPbO2电极的塔菲尔斜率高于多孔Ti/SnO2-Sb2O3/PbO2电极的塔菲尔斜率,间接表明多孔Ti/SnO2-Sb2O3/CNT-PbO2电极的析氧电位较高,这与极化曲线说明的结果相一致。

图3 不同电极在0.5 mol/LH2SO4中扫描速率为20mV/s下的线性极化曲线(内插图为氧化反应的塔菲尔拟合曲线)
2.2.2 电化学阻抗的表征
图4给出了0.5 mol/LH2SO4溶液中多孔 Ti/SnO2-Sb2O3/PbO2(a)和多孔Ti/SnO2-Sb2O3/CNT-PbO2电极(b)在析氧区域的EIS。根据图4中的EIS数据拟合出等效电路图5。图5中每个元件参数的模拟数据列于表1中。在图5所示电路中,Rs表示欧姆电阻,包括电解液和活性物质的电阻;引入Qdl取代与电极活性表面积成正比的双电层电容器[29-30];Rct表示电荷转移电阻。从图4可知,两种电极的EIS中都出现了一个明显的半圆,其半径大小通常反映析氧反应传荷电阻Rct的大小,表1显示PbO2与CNT-PbO2电极对应的Rct值分别为1.225和1.147 Ω·cm2,表明多孔 Ti/SnO2-Sb2O3/CNT-PbO2电极的析氧活性更高。析氧活性的高低取决于电极表面活性点的多少,活性点越多,其析氧反应活性越高。多孔Ti/SnO2-Sb2O3/CNT-PbO2电极具备较大的比表面积、更多的活性点,从而具备较高的析氧活性。数据表明,CNT掺杂改性PbO2电极能够减少体系中的欧姆电阻和电荷传递电阻,有益于电极活性的提高。
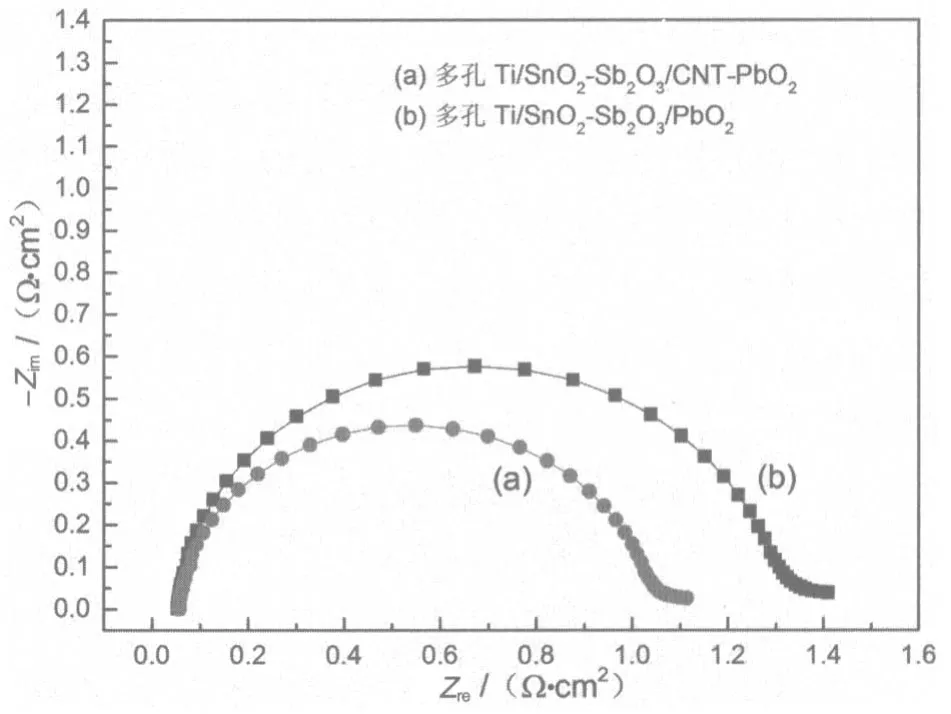
图4 电极在0.5 mol/LH2SO4溶液中的EIS(U=1.85 V)
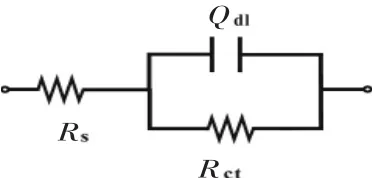
图5 基于阻抗实验数据的等价电路图
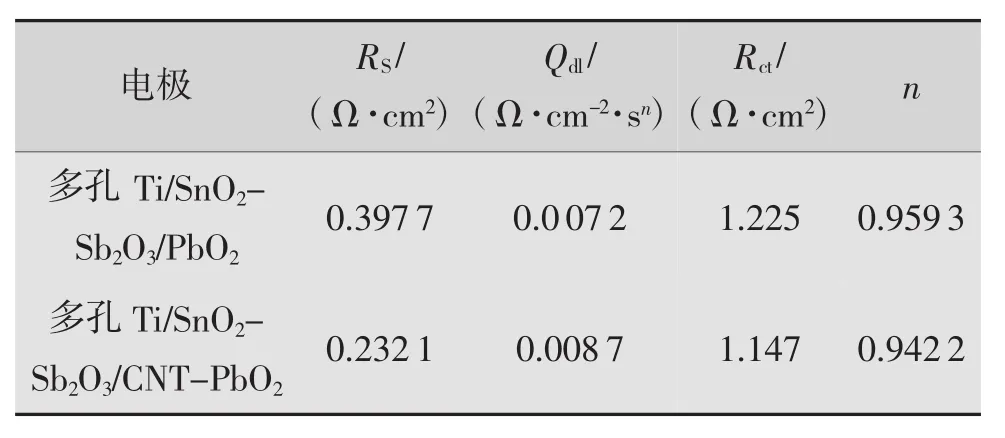
表1 各电器元件的电阻值
2.2.3 电极加速寿命的表征
对不同Ti基体 PbO2电极在3 mol/L H2SO4溶液中电流密度为0.5 A/cm2时的加速寿命进行测试,记录槽电压随时间的变化,当槽电压跃升到10 V时即认为电极失活。结果见图6。
从图6可知,多孔Ti/SnO2-Sb2O3/CNT-PbO2电极使用寿命为279 h,远高于多孔Ti/SnO2-Sb2O3/PbO2电极的加速寿命(214 h)。
多项实验结果一致表明多孔Ti基体活性层掺杂CNT有利于提高电极的稳定性。其主要有以下原因:首先,SEM图表明多孔Ti/SnO2-Sb2O3/CNT-PbO2电极表面晶粒尺寸小,表面致密的结构会防止电解液的渗透,防止基体表面形成TiO2膜(该膜不利于基体与活性层的结合)。此外,多孔Ti基体本身的表面特性可以使SnO2-Sb2O3夹层或CNT-PbO2膜与基体结合更紧密,降低了膜的脱落概率[30]。其次,电极表面所发生的析氧反应对电极的稳定性也有重要影响,阳极表面的析氧反应会导致CNT-PbO2氧化层的剥离和溶解。因此,当析氧过电位越高时,产氧的副反应就越少,从而延长电极的使用寿命。最后,CNT-PbO2活性层的存在可以进一步减少内部应力,提高Ti基体电极的稳定性[31]。
2.2.4 计时电流曲线的表征
为了分析CNT在多孔Ti/SnO2-Sb2O3/PbO2活性层掺杂对有机染料的降解效果,通过计时电流时间曲线来研究电极对不同有机染料的反应情况[21],如图7所示。对比分析可以看出,在未加入有机染料时,CNT-PbO2电极的电流密度比活性层PbO2电极高。加入有机染料后,体系中电流密度有所提高,CNT-PbO2电极的电流密度同样高于PbO2电极,表明这些有机染料容易被CNT-PbO2电极氧化。由于反应电流密度越高,电极材料性能越好,因此,可以推测CNT掺杂改性有利于提高电极对有机染料的降解效果。

图7 不同电极的计时电流密度-时间曲线(U=2.5 V)
2.3 电极·OH产生能力的比较研究
对于电极催化降解有机物的能力来说,·OH在PbO2电极表面的生成量起重要作用,所以有必要对·OH的生成量进行检测。从图8可知,2-羟基对苯二甲酸的荧光强度随着反应时间的增加而增强,表明在电化学反应过程中明显地产生了·OH。同时比较不同电极的荧光强度可以发现CNT-PbO2电极的荧光强度高于PbO2电极,表明多孔电极有更高的电催化氧化能力。
2.4 电极对有机染料模拟废水处理能力比较研究
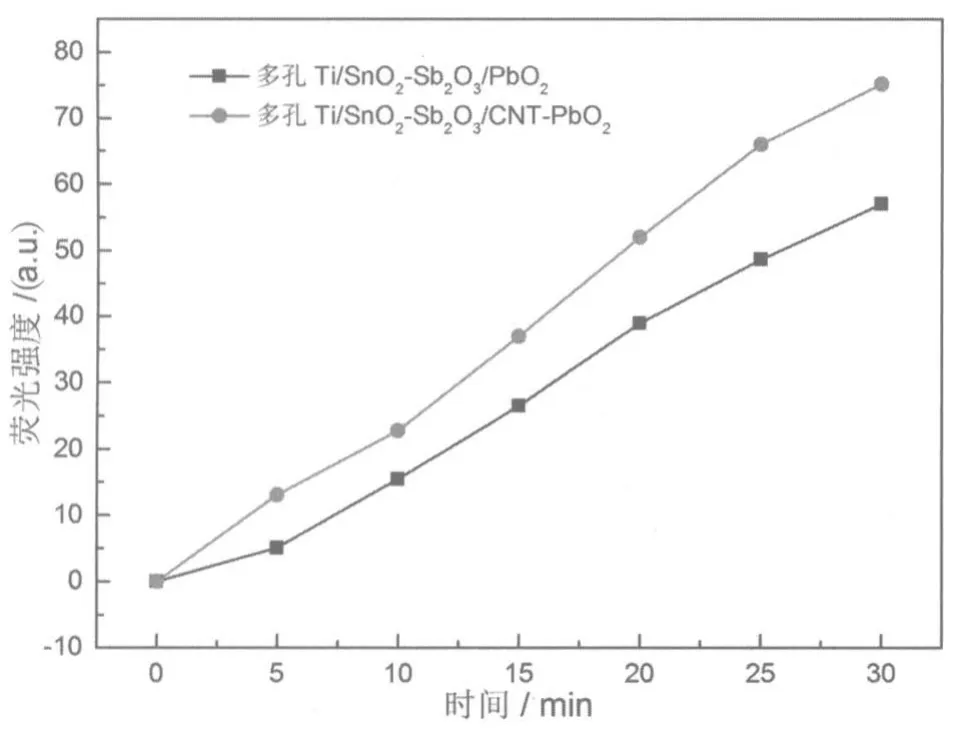
图8 电极在0.5 mol/L对苯二甲酸水溶液中电催化氧化进程的荧光光谱
从图9中可以看出在不同电极下电催化反应的COD去除率的变化,A,B,C分别为罗丹明B、亚甲基蓝、酰胺黑10B的COD降解图。罗丹明B在CNT-PbO2电极和PbO2电极上COD的去除率分别为78%和46%,亚甲基蓝在CNT-PbO2电极和PbO2电极上COD的去除率分别为77%和54%,酰胺黑10B在CNT-PbO2电极和PbO2电极上COD的去除率分别为63%和54%,表明这些有机染料废水都可以通过电催化被降解,而且CNT-PbO2电极对有机废水的COD去除率较高,具有较好的电催化活性。表2为不同PbO2电极电催化降解3种有机废水的GCE和SCE数据。对比分析可知,在降解同一染料时,多孔Ti/SnO2-Sb2O3/CNT-PbO2电极的GCE高,SCE较低。从经济方面进行分析,多孔Ti/SnO2-Sb2O3/CNT-PbO2可减少能量消耗,节约成本,更适于在工业生产中应用。
3 结论
对多孔Ti基体PbO2电极进行了改性研究,主要在制备PbO2电极的电沉积溶液中掺杂CNT,制备了Ti/SnO2-Sb2O3/CNT-PbO2复合电极,从电极的形貌特征、结构、电化学性能指标和电催化性能等方面对改性电极进行考察,得出如下结论。
(1)不同电极的SEM表明:CNT掺杂改性多孔Ti/SnO2-Sb2O3/PbO2电极后,改变了PbO2晶体的表面结构特征,能够减小晶体尺寸,使得晶体表面更加粗糙。EDS结果表明CNT被成功地掺杂到多孔Ti/SnO2-Sb2O3/PbO2电极中。
(2)电极的 XRD谱图表明:多孔 Ti/SnO2-Sb2O3/CNT-PbO2电极具有更小的晶粒尺寸,进一步验证了SEM观察的结果。
(3)电化学测试表明:多孔Ti/SnO2-Sb2O3/CNTPbO2的析氧电位明显高于多孔Ti/SnO2-Sb2O3/PbO2电极的析氧电位,分别为1.83和1.79 V。掺杂CNT减少了体系中的欧姆电阻和电荷传递电阻,使多孔Ti/SnO2-Sb2O3/CNT-PbO2具备更高的电化学活性和更大的比表面积。

图9 不同电极作用下,罗丹明B(A),亚甲基蓝(B),酰胺黑10B(C)染料废水COD去除率随时间变化的趋势
(4)电极加速寿命表明:CNT掺杂可以明显延长电极的使用寿命,Ti/SnO2-Sb2O3/CNT-PbO2电极的寿命为279 h,远高于多孔Ti/SnO2-Sb2O3/PbO2电极的加速寿命(214 h)。
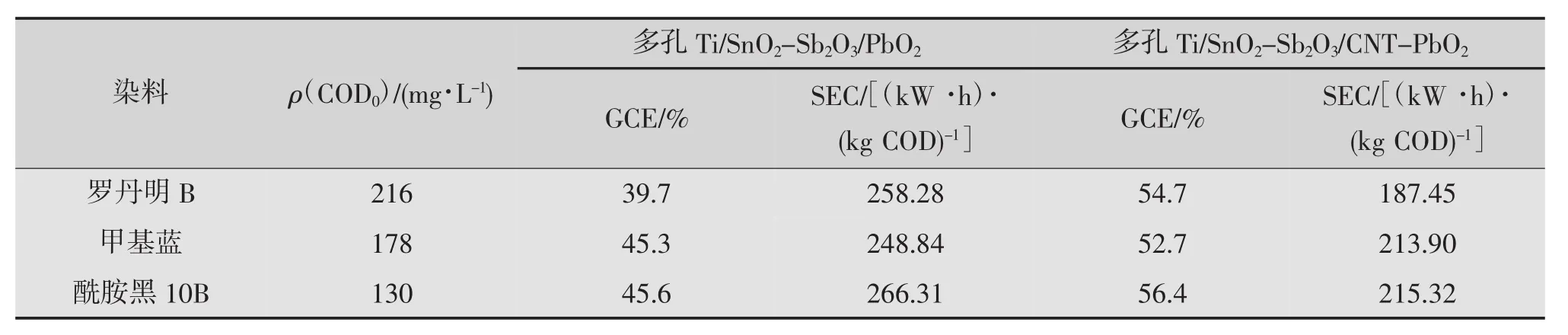
表2 不同电极对3种染料废水降解的一般电流效率(GCE)和能量消耗(SCE)
(5)CNT掺杂改性多孔 Ti/SnO2-Sb2O3/CNTPbO2电极具有良好的电催化降解有机染料(罗丹明B、亚甲基蓝、酰胺黑10B)的能力。
由此可见,多孔Ti/SnO2-Sb2O3/CNT-PbO2电极作为新型电极处理染料废水切实可行,具有很大的应用价值。
