爱格丽干白葡萄酒发酵过程中典型乙酸酯的生成动力学
2018-08-31李运奎汪兴杰靳国杰宋鸿聪陶永胜
李运奎 汪兴杰 靳国杰 宋鸿聪 刘 浩 陶永胜
(1.西北农林科技大学葡萄酒学院, 陕西杨凌 712100; 2.陕西省葡萄与葡萄酒工程技术研究中心, 陕西杨凌 712100)
0 引言
香气物质是葡萄酒重要的风味物质,按照来源不同,主要分为品种香气物质、发酵香气物质和陈酿香气物质,其中发酵香气物质主要来源于酵母主导的葡萄糖代谢路径[1]。发酵香气物质中,酯类物质是主要的呈香物质,对果香有重要贡献[2]。乙酸酯类物质是由乙酸和醇类物质在低pH值条件下反应生成的一类重要酯类香气物质[3],其中,乙酸乙酯、乙酸异戊酯和乙酸苯乙酯是葡萄酒中较为重要的乙酸酯类物质[4]。乙酸乙酯和乙酸异戊酯在模拟葡萄酒中的嗅觉阈值分别为7.5 mg/L和30 μg/L[5],在葡萄酒中的检出量通常高于嗅觉阈值[5-6],是果香的有力贡献者[2-3]。乙酸苯乙酯同时也是重要的苯乙基类化合物,但在葡萄酒中的检出量通常低于嗅觉阈值(250 μg/L),因此在多数情况下与其他物质联合呈香[5]。总体上,由于嗅觉阈值相对较低,乙酸酯类物质含量的微小变化可能会对葡萄酒香气及感官质量产生显著影响[3,7]。此外,乙酸酯类物质的浓度与其相关高级醇浓度呈线性相关,即高级醇是乙酸酯类物质生成的限制性前体物质[8]。
通常情况下,监测发酵过程中香气物质的含量变化可为香气物质调控提供指导,建立相应的香气物质生成动力学模型则可以更好地表征香气物质含量的动态变化,揭示香气物质的生成规律。已有研究中,分别基于Luedeking-Piret方程[9]、偶联温度、二氧化碳溶解量和初始酵母浓度等变量[10]和偶联香气物质在气液两相中分配平衡常数的克劳修斯-克拉伯龙方程[11-14]建立了部分重要发酵香气物质(包括了部分乙酸酯及其高级醇)的生成动力学模型。然而,现有模型中的特征参数很难被赋予明确的物理化学意义,极大地限制了其在生产中的应用。此外,乙酸酯类及其相关的乙醇、乙酸和高级醇类物质主要来源于葡萄糖代谢[1],但现阶段以葡萄糖为反应底物,基于经典化学反应动力学理论直接构建香气物质生成动力学模型的报道很少。且研究表明,乙酸乙酯、乙酸异戊酯和乙酸苯乙酯是爱格丽干白葡萄酒中含量最高的3种乙酸酯类[15]。因此,本文以爱格丽葡萄汁为原料,接种商业酿酒酵母启动发酵,酿造干白葡萄酒。定时取样监测发酵葡萄汁的乙醇和乙酸含量变化,同时进行重要乙酸酯类(乙酸乙酯、乙酸异戊酯和乙酸苯乙酯)及其相关高级醇类(异戊醇和苯乙醇)香气物质的SPME-GC-MS分析,从经典化学反应动力学角度建立香气物质的生成动力学模型,并结合目标香气物质的实验数据得到具体的动力学参数,以期为葡萄酒酿造过程中乙酸酯类香气物质生成的调控提供理论和数据支撑。
1 材料与方法
1.1 酵母菌株与葡萄原料
酿酒酵母活性干粉ACTIFLORE F33(法国Laffort公司)。爱格丽葡萄原料于2015年9月12日采自陕西杨凌官村葡萄基地(108° 4′27.95″E,34°16′ 56.24″N),葡萄浆果糖度(以葡萄糖计)为(177.0±1.2)g/L,酸度(以酒石酸计)为(6.84±0.22)g/L。
1.2 仪器与试剂
TRACE 1310-ISQLT型GC-MS联用仪(美国Thermo Fisher Scientific公司);DB-WAXETR型气相色谱柱(60 m×0.25 mm×0.25 μm,美国Agilent J&W公司);50 μm/30 μm CAR/DVB/PDMS型萃取头(美国Supelco公司);FA2014N型电子天平(上海菁海仪器有限公司);HH-S6型电热恒温水浴锅(北京科伟永兴仪器有限公司);KH-500DE型数控超声波清洗器(昆山禾创超声仪器有限公司);DGX-9243BC型鼓风干燥箱(上海南荣实验室设备有限公司),Millipore型纯水制备仪(美国Bedlford公司)。
分析纯试剂:氢氧化钠(广州金华大化学试剂有限公司),葡萄糖(天津科密欧化学试剂有限公司),亚硫酸(SO2质量分数6%以上,天津天力化学试剂有限公司)。色谱纯试剂:异戊醇(纯度99%以上)、苯乙醇(纯度99%以上)、乙酸乙酯(纯度99.9%以上)、乙酸异戊酯(纯度99%以上)、乙酸苯乙酯(纯度98%以上)和2-辛醇(纯度99%以上)(Sigma-Aldrich上海公司)。
1.3 爱格丽干白葡萄酒酿造
爱格丽葡萄除梗破碎后,葡萄汁装于20 L玻璃发酵罐中,按 60 mg/L添加SO2。葡萄汁4℃静置12 h后,分离上层澄清葡萄汁,当自然升温至15℃,按200 mg/L添加活性干酵母,启动酒精发酵。添加白砂糖调整最终酒精度,控制发酵温度在15~18℃。当发酵葡萄汁的比重处于0.992~0.996且残糖低于2 g/L时,终止发酵,葡萄酒转入干净玻璃罐中,按50 mg/L补加SO2,4℃下密封贮藏。期间进行2~3次自然澄清转罐处理,最后,葡萄酒满罐密封于4℃存放直至分析。葡萄酒酿造实验重复3次。发酵过程中测定还原糖、乙醇和挥发酸含量的变化,测定方法参照GB/T 15038—2006,每次测定重复3次。
1.4 香气成分分析
香气物质标准品于模拟葡萄酒溶液(体积分数12%的乙醇,6 g/L酒石酸,pH值3.2)中配置成5个不同的浓度,配置完成后,所有溶液4℃条件下避光保存[16]。香气物质标准品与样品中的目标香气物质均采用SPME-GC-MS分析[17],重复测定3次。
SPME方法:在15 mL装有磁力搅拌子的顶空瓶中加入8 mL酒样(含内标物2-辛醇,0.4 mg/L)或标准品溶液,加入2.0 g NaCl,然后将顶空瓶放入电磁搅拌器上水浴,40℃条件下平衡15 min;插入萃取纤维,40℃吸附30 min,立即将萃取头在GC进样口解吸8 min,用于GC-MS分析。
GC-MS条件:无分流进样;色谱柱DB-WAXETR升温程序为以3.0℃/min的速度从40℃升至130℃,再以4℃/min的速度从130℃升至250℃,保持8 min。离子源温度250℃,连接杆温度250℃,进样口温度250℃,电压70 eV,质谱扫描范围25~350,扫描速率0.2次/s。
香气物质的定性分析采用与香气物质标准品的质谱图特征离子比对、Wiley 275.L谱库(Agilent Technologies公司)查询等方法进行。定量分析采用内标标准曲线法进行,香气物质的标准曲线通过五点标度法获得[15]。
1.5 香气物质生成动力学模型构建
葡萄酒酿造中,发酵香气成分的生成主要来源于葡萄糖的代谢[1],因此,本研究以葡萄糖为反应底物(初始浓度CG0),t时刻生成的某香气物质(计量系数为f)浓度为CP。根据化学反应动力学理论[18],该香气物质生成反应的表观速率方程微分形式可写为
(1)
式中r——速率
k——速率常数,mmol1-n/(L1-n·d)
CG——t时刻的葡萄糖浓度,mmol/L
n——反应表观级数,表征反应物对反应速率的影响程度
对式(1)两边做定积分,则
(2)
当n≠1时(非一级反应),由式(2)可得
(3)
由式(3)得速率常数k(n≠1时)计算公式为
(4)
式(3)即为由葡萄糖生成香气物质的非一级反应表观速率方程积分形式的通式。
当n=1时(一级反应),由式(2)可得
(5)
式(5)即为由葡萄糖生成香气物质的一级反应表观速率方程积分形式的通式。由式(5)得速率常数k(n=1时)的表达式为
(6)
相比于香气物质浓度随时间变化的C-t图及对其变化趋势的拟合图,香气物质生成动力学模型的建立能揭示香气物质生成的更多信息,如:速率方程可以给出香气物质浓度随时间的变化情况(这类似于拟合函数的作用);反应级数可以表征葡萄糖初始浓度对香气物质生成速率的影响,级数越大,影响越大;速率常数则可以表征香气物质生成的速率及各种因素对反应速率的影响。反应温度、发酵液组成、催化剂等因素对香气生成的影响,由速率常数k体现,如温度的影响可通过阿伦尼乌斯公式进行描述。
采用SPSS进行统计分析和检验,采用Origin Pro绘制相关曲线。
2 结果与讨论
爱格丽酒样的残糖质量浓度(以葡萄糖计)为(2.21±0.15)g/L,酸度(以酒石酸计)为(6.45±0.36)g/L。发酵进行顺利,乙醇体积分数和挥发酸质量浓度(以乙酸计)均呈现先增加后趋于稳定的变化趋势,最终生成量分别为(11.83±0.19)%和(398±14)mg/L。
2.1 发酵过程中目标香气物质检出量
乙酸乙酯、乙酸异戊酯和乙酸苯乙酯分别由乙醇、异戊醇和苯乙醇与乙酸反应生成。通常情况下,乙醇和乙酸并不被认为是香气物质,因此本文仅对异戊醇、苯乙醇、乙酸乙酯、乙酸异戊酯和乙酸苯乙酯5种目标香气物质进行分析研究。
发酵过程中目标香气物质的检出量如表1所示。醇类物质的检出量普遍高于乙酸酯类物质,但除乙酸异戊酯外,其他香气物质的检出量在发酵后期均有一定幅度下降。MOURET等[8]在研究中认为香气物质的开始生成期和终止生成期分别为检出量超过最大检出量10%和90%的时期。结合香气物质的测定时间间隔,定义香气物质的开始生成期为香气物质检出量达到最大检出量0~10%的测定时期,另外,由于香气物质在最大检出量时的生成量与损失量基本相互抵消,因此定义香气物质的终止生成期为香气物质的最大检出量时期。分析可知,在本文条件下,异戊醇、苯乙醇和乙酸乙酯的检出量在发酵的第2天未达到最大检出量的10%,因此这一时期即为这3种物质的开始生成期,乙酸异戊酯和乙酸苯乙酯在发酵第2天的检出量分别达到了最大检出量的12.1%和10.4%,因此这两种物质的生成时期与发酵时期一致。另外,5种目标香气物质分别在发酵的第16、12、16、20、12天达到最大检出量,即这一发酵时刻为香气物质的终止生成期。
香气物质在发酵过程中的香气活性值变化如图1所示。乙酸苯乙酯和苯乙醇以及乙酸异戊酯和异戊醇的香气活性值变化趋势相同,这也表明了酯类物质与其前体物质的含量生成变化基本具有一致性。乙酸异戊酯、苯乙醇、异戊醇和乙酸异戊酯的香气活性值分别在发酵的第2、4、6、12天达到或超过1,但乙酸苯乙酯在香气活性值大于1后,含量即降低至嗅觉阈值以下。另有研究表明,控制发酵温度在18~20℃时,爱格丽葡萄酒中乙酸苯乙酯的最终质量浓度会超过400 μg/L,而苯乙醇的检出量较之本研究(发酵温度15~18℃)中略有降低[15]。这表明,发酵温度对乙酸苯乙酯的生成可能有一定影响。而通常情况下,苯乙醇、乙酸苯乙酯和乙酸乙酯对花香或果香有重要贡献,因此,在发酵过程中,对苯乙醇、乙酸苯乙酯和乙酸乙酯的生成进行调控,对果香和花香香气的强化有一定积极作用。乙酸乙酯在本研究中检出量一直低于其嗅觉阈值,这与WANG等[15]、李娜娜等[19-20]、南立军[21]对爱格丽干白葡萄酒香气的研究结果一致,说明这可能是爱格丽葡萄的品种特性,且以上研究表明爱格丽干白葡萄酒中乙酸乙酯的含量还受采收时间、发酵前葡萄预处理温度甚至葡萄整形方式的影响。究其原因,可能是爱格丽葡萄浆果中酵母营养成分尤其是可同化氮的差异,造成酿酒酵母乙酸乙酯的合成代谢减少。该品种葡萄酒中乙酸乙酯的酵母代谢生成的调控值得深入研究。
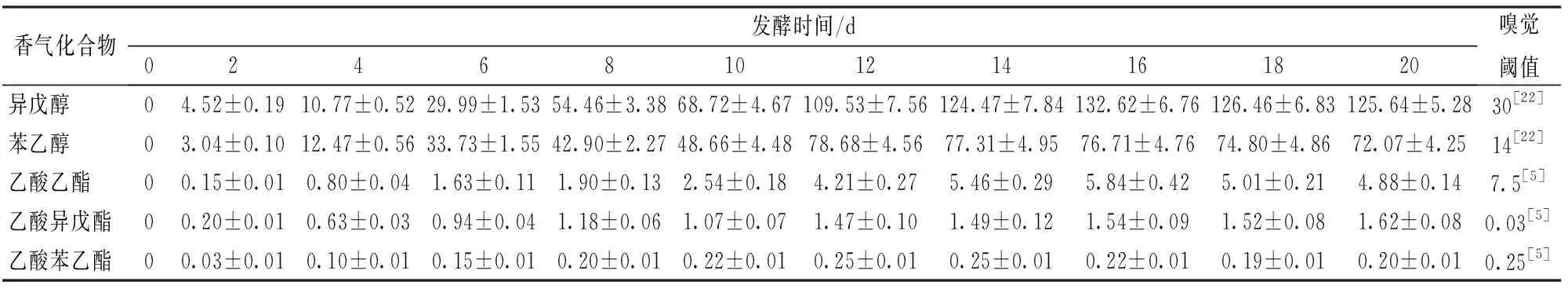
表1 目标香气物质在发酵过程中的检出量(质量浓度) Tab.1 Detected concentration of objective aroma compounds during fermentation mg/L
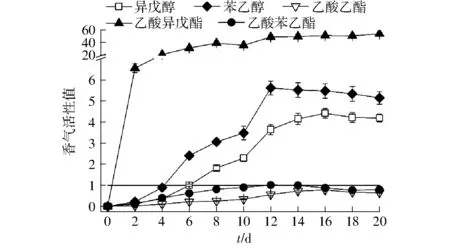
图1 目标香气物质在发酵过程中的香气活性值变化 Fig.1 Changes of odor activity value for considered aroma during fermentation
2.2 目标香气物质生成动力学模型建立
为进一步研究香气物质的生成动力学特征,对香气物质的开始生成期Tint、半生成期t1/2及其在整个发酵周期中所处时期Thalf、终止生成期Ttmt和生成周期Tdrt等特征参数进行了定义和推导。
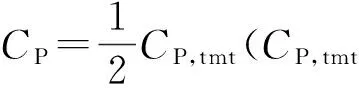
(7)

(8)
香气物质的半生成期直观给出了生成一半香气物质需要的时间,与速率常数类似可表征反应速率。香气物质半生成期在整个发酵周期中所处时期Thalf为
Thalf=t1/2+Tint
(9)
式中Tint——在整个发酵周期中香气物质开始生成的时期
香气生成周期Tdrt为
Tdrt=Ttmt-Tint
(10)
本文中生成动力学模型的拟合结果表明,香气物质从开始生成到最大生成量这一时期的浓度变化符合零级动力学模型,即香气物质浓度变化与发酵时间呈良好的线性相关。即当n=0时(零级反应),式(4)可简化为
CP=kt
(11)
则速率常数k为
(12)
依据式(11)和式(12)建立的目标香气物质生成动力学模型表达式和速率常数k如表2所示。模型决定系数R2>0.95,显著性水平P<0.001,目标香气成分的实验观测值和模型预测值符合良好(图2),表明动力学模型结果良好。
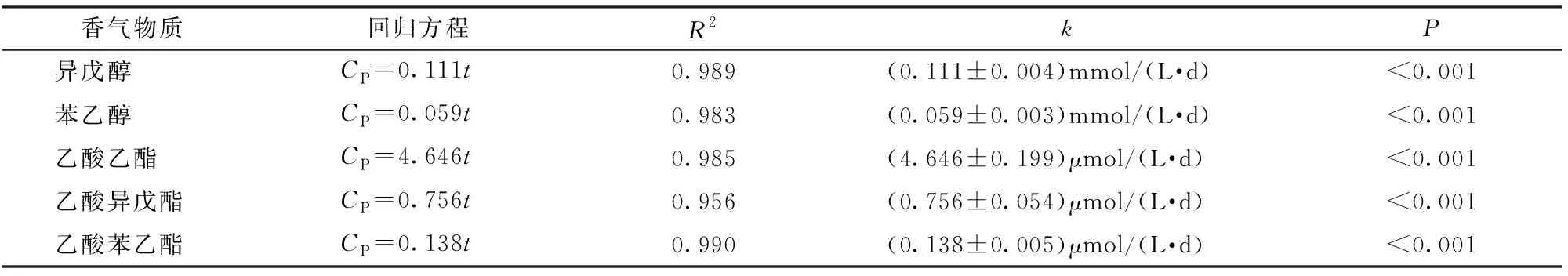
表2 香气物质生成动力学模型的表达式与速率常数 Tab.2 Expressions and rate constants of production kinetic models for objective aroma compounds
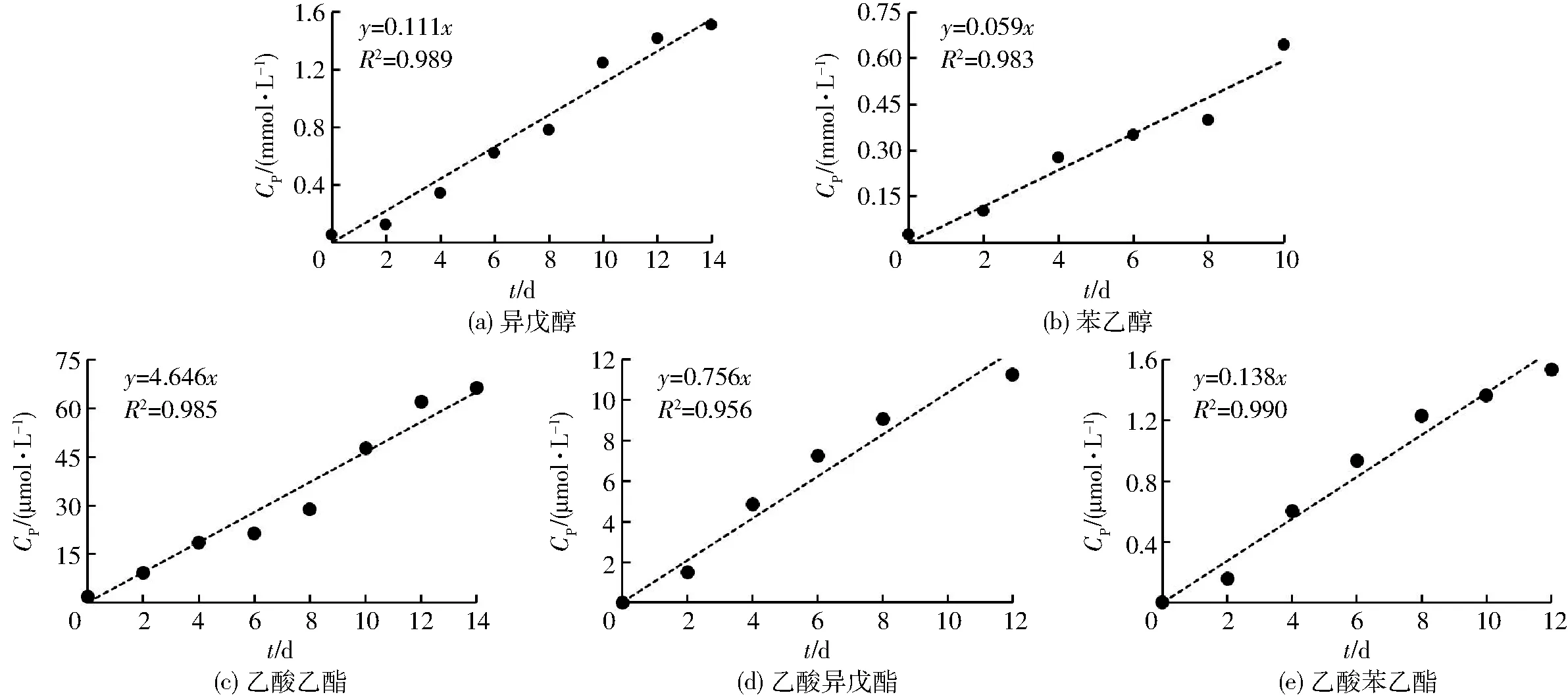
图2 目标香气成分的实验观测值和线性回归预测值 Fig.2 Observed values and linear regression predicted values of objective aroma compounds
本文仅对目标香气物质从开始生成到最大生成量阶段的生成动力学进行了动力学建模,模型的表达式为零级动力学模型,但通常情况下,香气物质含量在发酵后期均有一定幅度下降或保持稳定[8],因此对整个发酵过程中香气物质含量变化建立的动力学模型研究中,均未出现零级动力学模型,而这还可能与不同研究中发酵体系和发酵周期等的差异有关[8,13-14]。另外,相比于基于克拉伯龙-克劳修斯方程[12]、Luedeking-Piret方程[9]以及偶联温度、二氧化碳溶解量和初始酵母浓度等变量建立的模型[10],本文建立的生成动力学模型仅与香气物质生成量和葡萄糖含量有关,模型变量减少。
目标香气物质生成动力学模型的动力学特征参数分析结果如表3所示。总体上,目标香气物质之间的特征参数值差异较大,这可能与香气物质的化学性质不同有关[23]。异戊醇和乙酸异戊酯是香气活性值较高的香气物质。其中,异戊醇的生成速率最快,通常在高级醇中含量也最多[5,24]。异戊醇的Thalf为8.8 d,Tdrt为14 d,而乙酸异戊酯的Thalf为10.2 d,Tdrt为20 d,因此,乙酸异戊酯生成相比于其限制性反应底物异戊醇,有延滞效应。
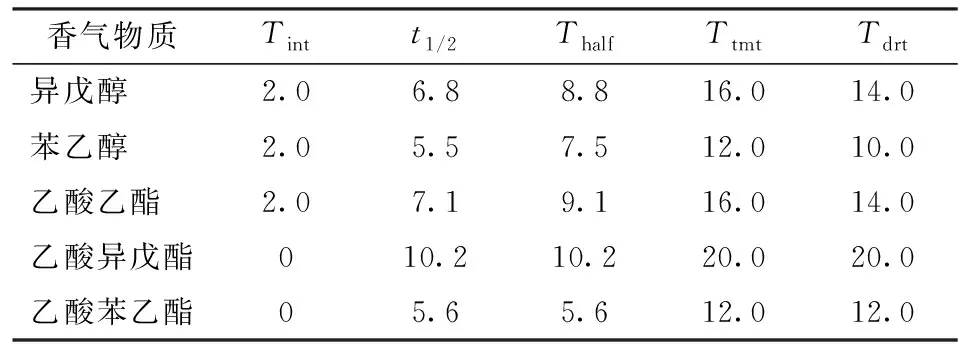
表3 香气物质生成动力学模型中的特征参数 Tab.3 Kinetics characteristic parameters of objective aroma compounds d
动力学模型揭示出,乙酸乙酯的生成速率是3种酯类物质中最高的,这可能与其反应底物乙醇和acetyl-CoA均大量来源于葡萄糖代谢有关[1,3],而乙酸苯乙酯生成速率最慢则可能与苯乙醇的含量较低有关。乙酸乙酯的Thalf为9.1 d,Ttmt为16 d,而其反应底物乙醇和乙酸含量在16 d也分别达到了最大值,但乙酸乙酯的检出量仍然低于嗅觉阈值。文献[25]指出14℃酿造环境下,乙酸乙酯的生成量要高于22℃时,因此本研究的发酵温度可能是限制乙酸乙酯生成的一个重要因素。动力学模型揭示出,苯乙醇的生成周期比乙酸苯乙酯短。作为乙酸苯乙酯生成的限制性底物,苯乙醇主要来源于酵母代谢的莽草酸途径[26-27]。因此,在本文条件下,可尝试在乙酸乙酯和乙酸苯乙酯生成的发酵Thalf时期,补加达到目标酒度所需的糖分,或适当添加酵母生长剂,促进乙酸、乙醇和苯乙醇的生成量,并延长苯乙醇的生成周期,从而达到提高乙酸乙酯和乙酸苯乙酯生成的作用。
2.3 目标香气物质生成动力学模型统计检验

图3 标准化残差检验与诊断的散点图 Fig.3 Scatter diagrams of rigorous statistical diagnosis for standardized residual
为进一步验证模型的准确性,本实验对目标香气物质的生成动力学模型进行了严格的统计检验。其中,模型的残差分析结果如表4所示。显著性水平Sig.值的结果表明,目标香气物质的Levene方差同质性检验结果的显著性均大于0.05,因此可认为该残差序列方差齐。Durbin-Watson统计量的分析结果均在0~4范围内,且绝大部分在2附近,表明残差独立性强。残差正态性检验K-S统计量分析结果表明,目标香气物质的显著性均大于0.05,则可认为该残差序列服从正态或近似正态分布。因此,残差分析结果表明,目标香气物质的回归模型成立。
此外,标准化残差的散点图如图3所示,残差值经拟合所得直线平行(重合)于横坐标,说明残差的方差齐。而标准化残差随机分布在(-2, 2)范围内,说明残差序列与预测值序列无关,变量间无非线性关系、没有重要自变量未进入模型,无实验异常点,残差独立。标准化残差的P-P图如图4所示。实验点的标准化残差在(-2, 2)区间以外无分布(概率小于等于0.05),说明无实验异常点。标准化残差点近似在一条直线上,直线的斜率为标准差(1),截距为均值(0),说明鉴别样本数据近似于正态分布,且数据点的随机分布表明残差独立。综上,统计诊断结果表明,目标香气物质生成动力学模型成立。
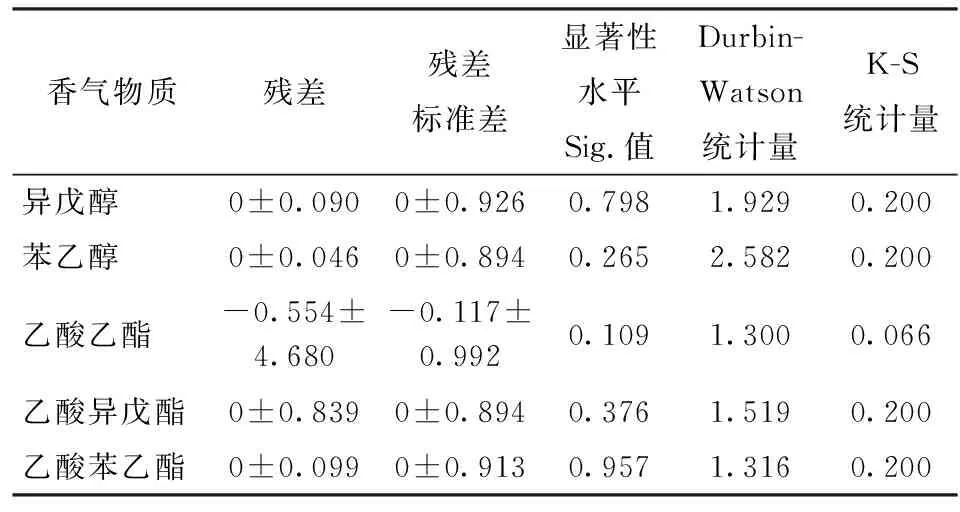
表4 香气物质生成动力学模型的残差分析 Tab.4 Residual analysis of kinetic models for objective aroma compounds
注:显著性水平Sig.值为残差方差齐性检验Levene统计量,将待检验的残差序列按大小顺序分为两组,再进行Levene方差同质性检验,显著性Sig.值大于0.05则认为该残差序列方差齐;Durbin-Watson统计量取值为0~4,其值越接近2,则残差独立性越强;K-S 统计量大于0.05则认为该残差序列服从正态或近似正态分布
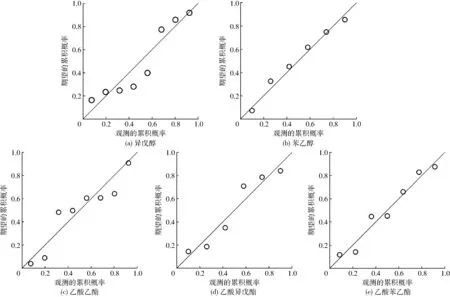
图4 标准化残差检验与诊断的P-P图 Fig.4 P-P diagrams of rigorous statistical diagnosis for standardized residual
总体上,现阶段乙酸酯类及其高级醇类香气物质的生成动力学模型研究中,异戊醇、苯乙醇、乙酸乙酯、乙酸异丁酯和乙酸异戊酯是主要研究对象[8,10,13],这可能与它们的检出量通常高于嗅觉阈值,从而表现为香气活性物质有关[5-6]。而乙酸苯乙酯在葡萄酒中检出量通常低于嗅觉阈值[5],这可能是乙酸苯乙酯的相关生成动力学模型研究欠缺的主要原因。因此,本研究结果可作为前人研究的补充,同时为重要乙酸酯类物质的生成、预测和调控提供数据支撑。
3 结束语
基于经典化学反应动力学原理构建了发酵香气物质的生成动力学模型,并得到了爱格丽葡萄汁发酵过程中的重要乙酸酯类(乙酸乙酯、乙酸异戊酯和乙酸苯乙酯)及其相关高级醇类(异戊醇和苯乙醇)的生成动力学具体形式及性质。研究结果表明,乙酸酯类香气物质的生成具有零级动力学特征(R2>0.95,P<0.001)。动力学模型揭示出,乙酸乙酯的生成与乙醇和乙酸具有同时性,而乙酸异戊酯和乙酸苯乙酯的生成分别相对于异戊醇和苯乙醇有延滞效应。为调控增加香气活性较弱的乙酸苯乙酯和乙酸乙酯的生成,可适当在发酵较为旺盛的半生成期,调节发酵基质成分,促进酵母代谢产物生成,提高乙酸酯类香气物质的前体物质的生成量,并延长其生成周期。
