珍珠莲中主要成分高圣草酚的药代动力学研究
2018-08-29谢瑶周妮孙志伟黄静秦文
谢瑶,周妮,孙志伟,黄静,秦文
(湖北三峡职业技术学院医学院,湖北 宜昌 443000)
珍 珠 莲 Ficus sarmentosa var.henryi(King)Corner为桑科榕属攀援藤状灌木,广泛分布于华东、华南和华西各省[1],具有祛风除湿、消肿止痛、解毒杀虫的功效,可用于治疗风湿性关节痛、肠炎、痢疾等疾患[2]。王学贵等[3]通过对珍珠莲中的黄酮类化学成分的分离鉴定,发现高圣草酚为其主要成分。现代药理学研究表明高圣草酚有抑制异常的毛细血管通透性增加及阻力下降,扩张冠状动脉,影响血压,增加冠脉血流量,改善微循环等重要生物活性[4]。本研究检测不同给药途径下大鼠血浆中高圣草酚的浓度,研究高圣草酚的药代动力学过程,计算腹腔注射和静脉注射高圣草酚的药代动力学参数,为高圣草酚不同剂型的制备以及临床应用提供理论依据。
1 材料与仪器
1.1 药品 珍珠莲药材购于宜昌市宜草堂大药房,由湖北三峡职业技术学院医学院药学教研室胡兴娥教授鉴定为珍珠莲Ficus sarmentosa var.henryi(King)Corner。高圣草酚对照品由本实验室分离提纯,经紫外分光光度法(UV)、质谱(MS)、核磁共振(NMR)分析数据确证其结构为高圣草酚,对照品纯度高于98%。内标物黄芩苷购自中国药品生物制品检定所。
1.2 试剂与动物 乙腈和甲醇为色谱纯(美国Fisher Scientific公司),甲酸为色谱纯(天津康克德公司),实验用水为娃哈哈纯净水。12只雄性SD大鼠,体重(230±20)g,由三峡大学动物实验中心提供(许可证号为:SCXK(鄂)20170012)。
1.3 仪器 WATERS ACQUITYTM UPLC超高效液相色谱仪、质谱仪(美国Waters公司),Thermo Syncronis C18色谱柱(50 mm×2.1 mm,1.7 μm)(美国Thermo公司),涡旋混合器(XK96-B,姜堰市新康医疗器械有限公司),氮吹仪(D10型,杭州蓝焰科技有限公司)。
2 实验方法
2.1 色谱/质谱条件 色谱柱为Thermo Syncronis C18色谱柱(50 mm×2.1 mm,1.7 μm);流动相A为0.2%甲酸溶液,流动相B为乙腈溶液,梯度洗脱,洗脱程序为:(1)0~4 min,流动相B比例由20%上升至25%;(2)4~6.5 min,流动相B比例由25%上升至75%。流速0.25 ml/min,柱温30℃。
离子源为ESI源,正离子模式,质谱多反应监测(multiple-reaction-monitoring,MRM)检测,高圣草酚及内标黄芩苷质谱条件见表1,MS/MS质谱图见图1,源喷雾电压为3.2 kV,离子源温度为120℃,去溶剂气体为N2,温度为400℃,流速为600 L/h。碰撞气Ar压力为2.95×10-3mbar。
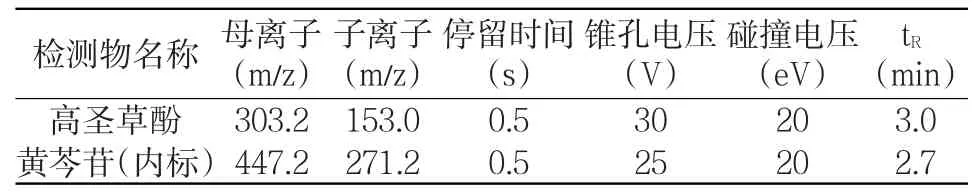
表1 高圣草酚及内标黄芩苷最优化MRM条件

图1 高圣草酚(A)与内标黄芩苷(B)的化学结构及质谱图
2.2 溶液的配制 对照品储备液的配制:取高圣草酚对照品适量,置于100 ml容量瓶中,用甲醇溶液溶解并稀释至刻度,配制成100 mg/L的高圣草酚储备液,临用前用甲醇稀释。
内标溶液的配制:取黄芩苷对照品5 mg,精密称定,置于100 ml容量瓶中,加甲醇溶液溶解并稀释至刻度;精密量取上述溶液1 ml,置于100 ml容量瓶中,加甲醇溶液溶解并稀释至刻度,即得。
2.3 血浆样品预处理 取待测血浆样品100 μl于1.5 ml具塞离心管中,加入甲醇与内标溶液各10 μl,混匀后加入 500 μl 0.2%甲酸-乙腈溶液,涡旋混匀5 min后15 000 r/min离心10 min。转移上清液于另一离心管中,35℃氮气吹干,取100 μl溶剂(乙腈-水,25∶75,v/v)复溶,溶液在4℃离心机中离心10 min后进样,进样量为10 μl。
3 生物样品方法学考察
3.1 方法专属性 大鼠空白血浆、空白血浆加对照品高圣草酚及内标、静脉注射1 h后血浆样品加内标的色谱图见图2,结果表明血浆中杂质不干扰样品及内标物的测定。高圣草酚的保留时间为3.0 min,内标的保留时间为2.7 min。
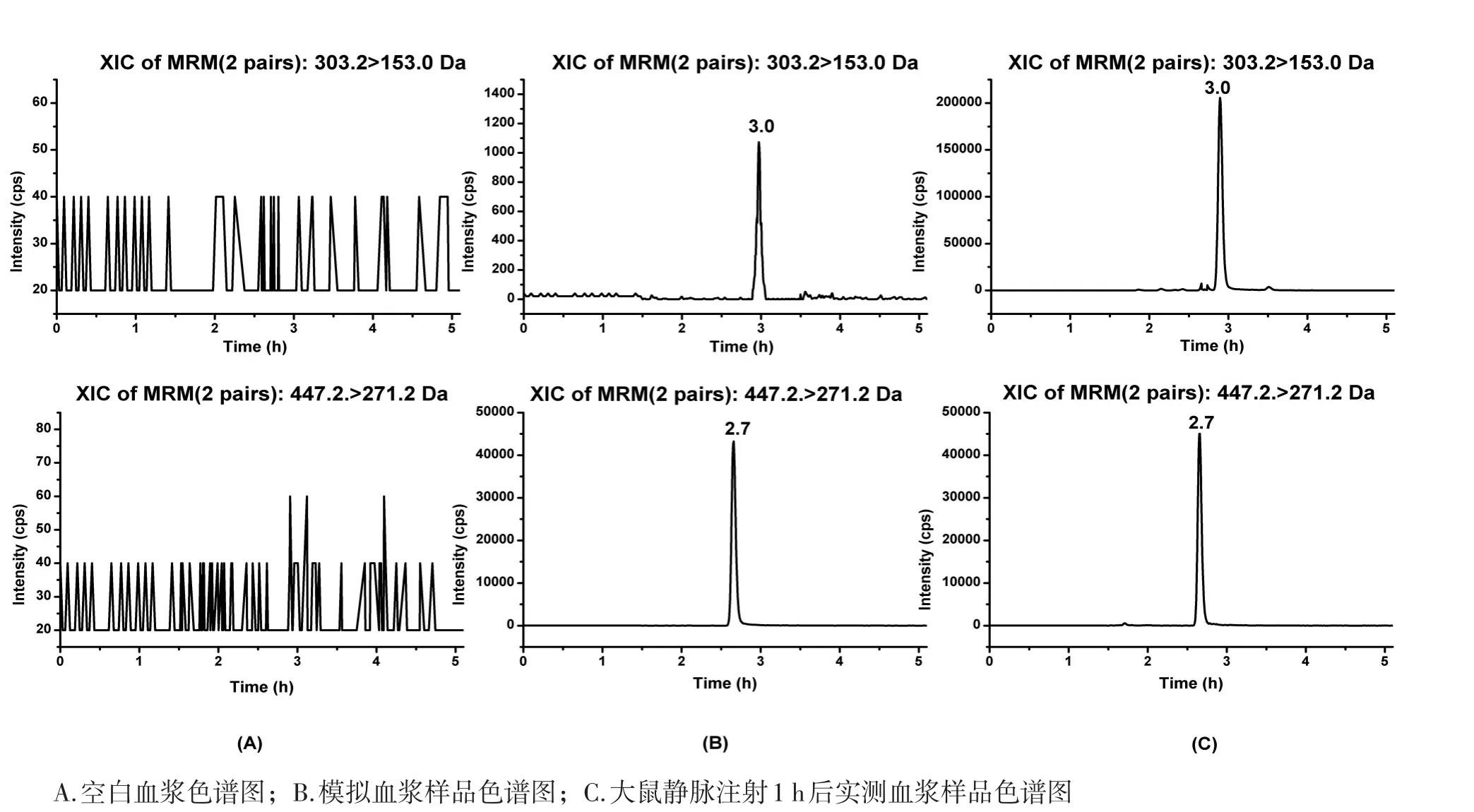
图2 血浆中高圣草酚和内标黄芩苷色谱图
3.2 线性关系及定量下限 配成浓度相当于4.0、10、50、100、200、400、800 ng/ml的高圣草酚血浆标准溶液,再按“2.3项”处理后检测,测定高圣草酚峰面积AS、内标峰面积AI,以AS/AI为纵坐标(Y),以所对应各点浓度C为横坐标(X)绘制标准曲线。得高圣草酚的标准曲线回归方程Y=0.225X+0.398(r=0.9938)。定量下限为 4.0 ng/ml(n=7,RSD=2.35%)。
3.3 精密度与准确度 取空白大鼠血浆100 μl,按“2.3项”下方法配制低、中、高3个质量浓度(分别为10、100、640 ng/ml)的高圣草酚血浆样品,每个质量浓度进行6个样品分析,连续测定3 d,用当日标准曲线计算高圣草酚样品的质量浓度,从而考察方法的精密度与准确度,结果见表2。
3.4 提取回收率 取空白大鼠血浆100 μl,按“2.3项”下方法配制低、中、高3个质量浓度(分别为10、100、640 ng/ml)的高圣草酚血浆样品,每个质量浓度进行6个样品分析,另取空白血浆100 μl,按“2.3项”下操作,获得的上清液中加入相应质量浓度的标准溶液 10 μl和内标溶液 10 μl,氮气流下吹干,将残留物加入100 μl甲醇溶解,取10 μl进样,获得相应峰面积比(3次测定的平均值)。以每一种浓度2种处理方法的峰面积比值计算提取回收率。结果见表2,内标黄芩苷的提取回收率为85.8%。
3.5 基质效应 取空白血浆100 μl,除不加混合系列标准溶液和内标溶液外,按“2.3项”下操作,向获得的上清液中加入低、中、高3个质量浓度的高圣草酚标准溶液 10 μl和内标溶液 10 μl,涡旋混合,于35℃干浴,氮气流下吹干,以100 μl流动相溶解后进样分析,获得相应峰面积,每一浓度进行6个样品分析;同时另取相应浓度的标准溶液 10 μl和内标溶液 10 μl,35 ℃干浴,氮气流下吹干,以100 μl流动相溶解后进样分析,获得相应峰面积(6次测定的平均值)。以每一浓度两种处理方法的峰面积比值计算基质效应。结果见表2,表明本方法测定大鼠血浆中高圣草酚及内标时无明显基质效应。

表2 高圣草酚的精密度与准确度(n=6)
3.6 样品稳定性 取空白大鼠血浆100 μl,按“2.3项”下配制为低、中、高3个质量浓度(10、100、640 ng/ml)的高圣草酚血浆标准品溶液,每种浓度3份,经历3次冰冻-解冻循环后,考察其稳定性。低、中、高3个浓度的RSD分别为5.5%、4.8%、3.5%,结果显示冻融条件对血浆样品的检测结果没有明显的影响。
4 高圣草酚在大鼠体内的药代动力学研究
4.1 珍珠莲注射剂的制备 取珍珠莲药材适量,各分别加入10倍、8倍量的95%乙醇液回流提取3次,每次2 h,合并3次醇提液,过滤,减压回收乙醇,残渣加适量水溶解,备用。
4.2 给药方案 将12只SD大鼠随机分成2组,给药前每组均禁食12 h(不禁水),分别腹腔注射和静脉注射(20 g/kg)给药。分别于给药后2、5、10、20、40、60、90、120、180、240、360、480 min眼眶取血0.25 ml,注入肝素化的试管,离心5 min(10 000 r/min)取血浆,-20℃冷冻保存备测。
4.3 血药浓度-时间曲线及药物动力学参数 采用DAS2.1药动学软件处理血药浓度-时间数据,得到高圣草酚的药代动力学参数,并比较其腹腔注射和静脉注射的药动学过程,结果发现,静脉注射组的 AUC0-t、AUC0-∞、CLZ/F明显大于腹腔注射组,同时MRT明显低于腹腔注射组;静脉注射组对珍珠莲中高圣草酚的血浆清除率约为腹腔注射组的2~3倍,腹腔注射组高圣草酚的半衰期远大于静脉注射组,差异均有统计学意义(P<0.05),见表3。大鼠单剂量腹腔注射及静脉注射给予20 g/kg高圣草酚后,血药浓度-时间曲线见图3。
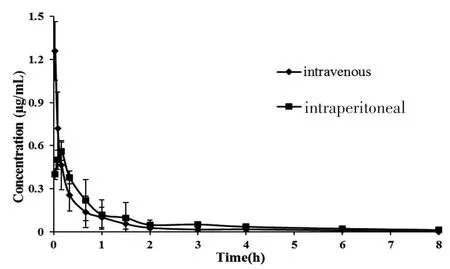
图3 大鼠单剂量腹腔注射及静脉注射给予20 g/kg高圣草酚后的血药浓度-时间曲线图

表3 腹腔注射和静脉注射给予珍珠莲注射液后高圣草酚的主要药动学参数
5 讨论
5.1 色谱条件的选择 本实验选择0.2%甲酸溶液(流动相A)与乙腈(流动相B)为洗脱溶剂,研究最初,曾尝试采用等度洗脱,曾考察色谱条件A∶B=55∶45(v/v),在该色谱条件下,高圣草酚峰形良好,但内标黄芩苷与血浆内源性物质分离度R<1.5;在A∶B=38∶62(v/v)的色谱条件下,内标物黄芩苷与血浆内源性物质分离良好,但高圣草酚色谱峰拖尾严重,拖尾因子T>1.2,因此本研究采用梯度洗脱,洗脱程序为:(1)0~4 min,流动相B比例由20%上升至25%;(2)4~6.5 min,流动相B比例由25%上升至75%。在该色谱条件下血浆内源性物质、黄芩苷、高圣草酚分离良好,黄芩苷、高圣草酚色谱峰拖尾因子T均<1.1。
5.2 质谱条件的选择 高圣草酚[M+H+]峰响应值优于[M+Na+]峰,因此本研究选择[M+H+]峰的正离子选择模式监测,因其响应远高于负离子选择模式检测。
5.3 药代动力学特点 从腹腔注射和静脉注射2种给药途径药动学结果来看,高圣草酚静脉给药后,大鼠体内代谢迅速。本结果显示高圣草酚腹腔给药的消除半衰期为(1.37±0.33)h,静脉注射的消除半衰期为(0.67±0.30)h,差异有统计学意义(P<0.05)。血浆药物浓度经DAS2.1程序处理,高圣草酚在大鼠体内经腹腔与静脉注射给药后的药代动力学参数中 AUC0-t、AUC0-∞、MRT、CLZ/F差异亦有统计学意义。这可能与高圣草酚在大鼠体内的吸收与代谢机制有关[5]。从药时曲线分布可知,静脉注射后血药浓度几分钟就迅速下降了几倍,这可能是高圣草酚经静脉注射后迅速向各脏器分布[6]。
综上所述,由于高圣草酚吸收和代谢的速度较快,静脉注射可用于急性发病期。但是由于吸收时间较长,选择腹腔给药方式可以降低高圣草酚的不良反应和毒性,因此可用于慢性发病期治疗。
