花生种子休眠特异突变材料的创制及理化因素研究
2018-08-29胡晓辉崔凤高张胜忠苗华荣张智猛
胡晓辉,崔凤高,张胜忠,苗华荣,张智猛,陈 静
(山东省花生研究所,山东 青岛 266100)
种子休眠性是植物长期进化过程中形成的自我保护机制,是植物界中普遍存在的特性。作物种子休眠性是一个极其重要和复杂的农艺性状,对农业安全生产有着重要意义。但是很多作物在长期驯化、培育过程中,注重追求高产高效,忽视保留适度种子休眠性,导致种子休眠性减弱甚至丧失,进而引发产量和食用品质下降、种用安全隐患等一系列问题。针对种子休眠性的影响因素、遗传机制和分子机理等研究,在水稻、小麦、玉米等均有报道[1-7]。花生(ArachishypogaeaL.)是我国重要的油料作物和经济作物,年种植面积约4700 khm2,单产、面积、出口均居世界前列。近年来关于花生种子休眠性对我国花生生产的影响多有报道[8-9],如花生收获时期恰逢阴雨天气导致花生在植株上发芽,严重影响产量、品质和种用质量,甚至是引发食用安全隐患,其主要根源是目前选育推广的花生新品种休眠性较弱,所以选育具有适度休眠性的花生品种非常重要。而探索花生种子休眠机理对于培育具有适度休眠性的花生品种具有重要理论意义和指导作用。利用突变体研究种子休眠是一种非常有效的手段,并鉴定出许多控制种子休眠的基因[10],包括种子成熟过程调控因子(ABI3、FUS3、LEC1、LEC2等)、激素相关调控因子(ABA代谢基因CYP707A1和CYP707A2、ABA受体ABI1、ABI2、ABI4等)、种子休眠特异基因(DEP、AtHB20、CBF、MFT、SPT等)等。应用诱变技术育成了一些花生新品种(品系),如早熟花生新品种鲁花6号、鲁花12号[11-13]。本研究以强休眠花生品种花育52号为试材,通过化学诱变方法,结合种子休眠性鉴定,获得弱休眠突变材料,对比野生型和突变材料品质、休眠及吸胀过程中理化性质差异,以期为利用突变材料挖掘花生种子休眠的分子机制奠定基础。
1 材料与方法
1.1 供试材料
试验材料系花育52号[14]及通过化学诱变创制的突变体材料,其中花育52号为山东省花生研究所育成的花生品种。种植方式为起垄双行单粒播种,行距40.0 cm,株距16.7 cm,每个家系种植4行,覆膜。5月上旬播种,成熟后收获晾晒10 d直接进行种子休眠性检测。田间水肥管理等同于常规大田,及时进行病虫害防治。
花育52号通过EMS诱变获得诱变各世代,M2和M3世代进行单株品质测定[15]和休眠性检测,选择出休眠性弱的单株;M4世代检测株行内所有单株品质和3个单株的休眠性,休眠性表现一致的株行用于种子萌发过程中理化特性分析。
1.2 方 法
1.2.1 种子休眠性检测
每品种设3次重复,每次重复为:12 cm培养皿内铺2张滤纸,放置20粒成熟饱满的花生种子,加蒸馏水于30℃条件下暗培养,检测第7 d的发芽率。
以胚根和胚轴长度≥种子长度作为发芽标准,用种子发芽率评价种子休眠性的强弱,发芽率高的种子休眠性弱,发芽率低的种子休眠性强。
1.2.2 化学诱变方法及诱变后代选择
种子准备:选用种子休眠性强的花育52号种子1kg,用1.5% EMS 处理后立即种植于大田获得M0世代;后期对M2、M3、M4世代进行品质检测和休眠性检测,选择弱休眠诱变材料。
1.2.3 抗氧化酶含量和激素含量的测定
分别取无休眠突变材料HY52-100-23、HY52-100-67和休眠品种花育52号(HY52-D)的种子各150粒置于15 cm培养皿内,3次重复;设吸胀时间0、6、12、18、24、48 h,分别取不同吸胀时间的种子进行主要抗氧化酶(POD和CAT)和激素含量的测定。激素包括GA和ABA。采用酶联免疫分析(ELISA)方法,试剂盒来自台湾生工,根据说明书操作,利用芬兰352型酶标仪测定。
1.3 数据分析
利用Excel和SPSS 19.0进行数据处理。
2 结果与分析
2.1 野生型与诱变后代种子休眠性和品质
突变材料HY52-100-23和HY52-100-67的种子发芽率分别为78.33%和83.33%,野生型种子发芽率为35%;野生型材料二者间存在极显著差异(表1)。示踪突变材料HY52-100-23和HY52-100-67的各世代品质的数据表明(表2),野生型花育52号三个年份的油酸含量分别是81.59%、81.75%、81.45%,亚油酸含量分别为4.43%、3.43%、4.5%;M2、M3、M4世代,突变材料HY52-100-23和HY52-100-67的油酸含量分别为85.64%和85.64%、83.63%和80.08%、83.82%和78.94%,亚油酸含量分别为3.99%、3.02%、2.58%和3.99%、3.54%、6.91%。说明突变材料HY52-100-23和HY52-100-67在品质方面与野生型相比没有明显差异,而种子发芽率存在显著差异。

表 1 突变材料和野生型的发芽率

表 2 突变材料和野生型的品质
2.2 不同休眠材料吸胀萌发过程中POD和CAT变化
种子吸胀萌发过程中,突变材料的POD含量呈现先上升后下降的趋势(图1)。突变材料与HY52同阶段相比较,种子吸胀0 h、6 h时POD含量差异不显著,12 h、18 h时POD含量差异极显著,24 h、48 h时POD含量表现不同。种子吸胀萌发过程中,突变材料CAT含量呈上升趋势(图2)。突变材料与HY52同阶段比较,种子吸胀0 h、6 h时CAT含量差异不显著,12 h、18 h、24 h、48 h时CAT含量差异显著。

图1 花生种子吸胀萌发过程中POD变化
注:HY52:花育52号; HY52-ND:HY52-100-23和HY52-100-67。下同。
图2花生种子吸胀萌发过程中CAT变化
Fig.2 Changs in CAT during peanut seed imbibition and germination
Note: HY52: Huayu52; HY52-ND: HY52-100-23和HY52-100-67. Same as below.
2.3 不同休眠材料种子吸胀萌发过程中GA和ABA变化
从图3~5可见,随着种子吸胀萌发,各材料内源激素变化差异较大。HY52内源GA含量变化幅度较小,HY52-100-23和HY52-100-67GA含量变化呈上升趋势(图3)各吸胀时段HY52内源GA含量均低于HY52-100-23和HY52-100-67(0 h除外),0 h和6 h时原种HY52与HY52-100-23、HY52-100-67内源GA含量间差异不显著,12 h、18 h、24 h、48 h时原种HY52与HY52-100-23和HY52-100-67GA含量间差异显著。
种子吸胀萌发过程中,HY52内源ABA含量变幅较小; HY52-100-23和HY52-100-67的ABA含量变化呈下降趋势(图4)。各时段HY52内源ABA含量高于HY52-100-23和HY52-100-67,0 h时原种HY52与HY52-100-23、HY52-100-67内源ABA含量差异不显著,6 h、12 h、18 h、24 h、48 h时原种HY52与HY52-100-23、HY52-100-67内源ABA含量差异显著。
种子吸胀萌发各时段HY52的ABA/GA高于HY52-100-23和HY52-100-67。0 h时原种HY52与HY52-100-23、HY52-100-67的ABA/GA差异不显著,6 h、12 h、18 h、24 h、48 h时原种HY52与HY52-100-23、HY52-100-67的ABA/GA差异显著(图5)。说明种子休眠与内源GA含量呈负相关,与内源ABA含量、ABA/GA呈正相关。

图3 花生种子吸胀萌发过程中GA变化 Fig.3 Changs in GA during peanut seed imbibition and germination
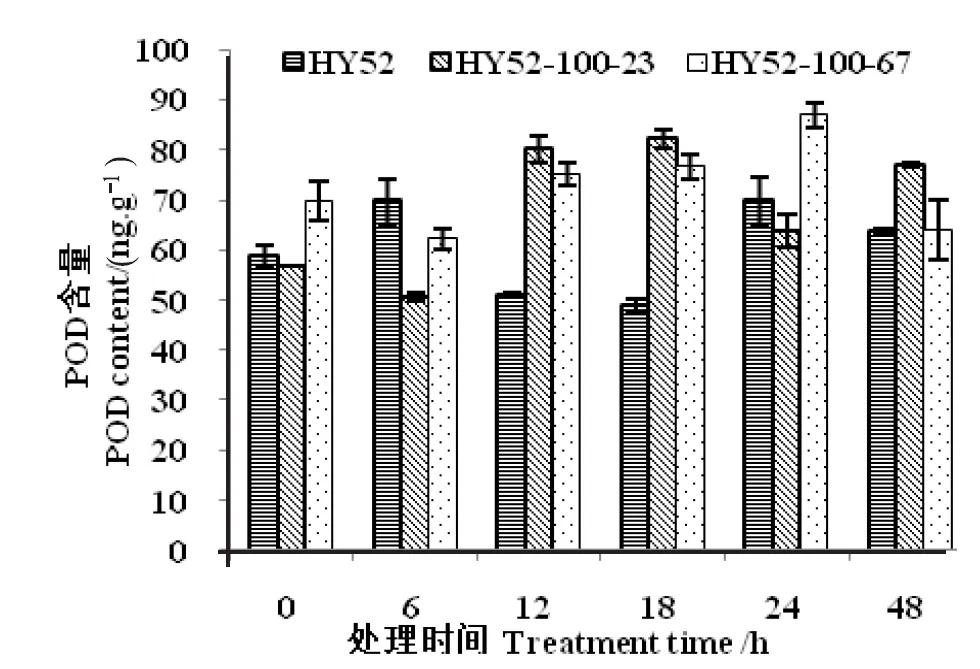
图4花生种子吸胀萌发过程中ABA变化
Fig.4 Changsin ABA during peanut seed imbibition and germination

图5花生种子吸胀萌发过程中ABA/GA变化
Fig.5 Changes in ABA/GA during peanut seed imbibition and germination
3 讨 论
利用突变体研究种子休眠是一种非常有效的手段,通过这种方式鉴定出许多控制种子休眠的基因[10]。本研究以强休眠花生品种花育52号为试材,通过化学诱变方法,结合品质示踪和种子休眠性鉴定,获得弱休眠突变材料,两者之间品质没有差异,而种子发芽率存在显著性差异,突变材料的创制为挖掘花生种子休眠分子机制奠定基础。
玉米种子萌发,胚中POD、CAT含量随萌发时间的延长逐渐升高[16]。强休眠玉米品种4628种子的过氧化物酶(POD)、过氧化氢酶(CAT)显著低于休眠性差品种996;内源激素赤霉素(GA)显著低于休眠性差品种996,脱落酸(ABA)含量显著高于休眠性差品种996[17]。本研究中发现,休眠性弱的突变材料POD、CAT与野生型野生型花育52号相比,种子吸胀萌发初期(0 h、6 h时)差异不显著,中期(12 h、18 h时)显著高于野生型花育52号。
种子休眠和萌发过程中,激素作为信号物质扮演非常重要的角色,是调节生理活动的重要物质。ABA对诱导种子休眠和维持吸胀种子的休眠状态有积极的调控作用,GA对终止种子休眠与促进发芽有着重要的作用[18-21]。已有研究表明吸胀萌发过程,花生种子休眠与内源GA含量、GA/ABA呈负相关,与内源ABA含量呈正相关[22]。本研究得出相似结果,即种子吸胀萌发过程中,休眠品种HY52内源ABA含量显著高于弱休眠突变材料(0h除外);但休眠品种HY52内源ABA含量变化趋势存在一定差异,这可能是其种子休眠不同造成的[22]。种子吸胀萌发过程,弱休眠突变材料内源GA含量从12 h时开始显著高于休眠品种HY52,而ABA和ABA/GA从6 h时开始显著低于休眠品种HY52,表明ABA和ABA/GA对于种子休眠的响应可能更早一些。
4 结 论
本研究利用化学诱变方法创制出弱休眠突变材料,与野生型相比,品质变化不显著,种子萌发率存在显著性差异;种子吸胀萌发过程中,突变材料与野生型在POD、CAT、GA、ABA和ABA/GA方面表现有一定差异。种子吸胀萌发初期,弱休眠突变材料与强休眠野生型的POD、CAT、GA、ABA、ABA/GA差异不显著,中期弱休眠突变材料的POD、CAT、GA显著高于强休眠野生型花育52号,而ABA、ABA/GA显著低于强休眠野生型花育52号;后期弱休眠突变材料的CAT和GA显著高于强休眠野生型花育52号,而ABA、ABA/GA显著低于强休眠野生型花育52号。
