合金Al-Fe/C纳米复合粒子形成机制及其储锂电化学行为
2018-08-24刘道林霍凤莉董星龙
程 厅,高 嵩,丁 昂,刘道林,霍凤莉,高 铭,董星龙
合金Al-Fe/C纳米复合粒子形成机制及其储锂电化学行为
程 厅,高 嵩,丁 昂,刘道林,霍凤莉,高 铭,董星龙
(大连理工大学 材料科学与工程学院,三束材料改性教育部重点实验室,大连 116024)
以微米Al粉和Fe粉为原料,采用直流电弧等离子体气相蒸发法,在氢氩和不同CH4含量气氛下制备了Al-Fe和Al-Fe-C纳米复合粒子。研究纳米粉体的形成机制、结构、形貌及其电化学性能,着重研究C原子的加入对纳米粒子产物的成分组成、相结构及电化学性能的影响,对各种纳米粒子形成规律及嵌/脱锂电化学机制进行了探讨。结果表明:无碳气氛下制备的Al-Fe粒子呈球状;在含碳气氛下,随着C含量的提高,粒子形貌向柱状和线状发展,粉体相组成由Al向Al4C3转变,合金种类由FeAl2向Fe2Al5转变。当电流密度为100 mA/g时,4种复合材料电极的首次放电容量分别为348.8、193.3、275.5和628.8 mA∙h/g,金属间化合物Fe2Al5相的形成有利于提高充/放电容量和抑制体积变化,有效提高了电极的循环稳定性能。
Al-Fe/C;纳米复合材料;锂离子电池;负极材料;直流电弧法
锂离子电池作为一种绿色能量存储装置,由于具有高能量密度、相对低自放电率、无记忆效应、以及长循环寿命等优点,被广泛应用于便携式电子产品中,在电动汽车等动力能源领域具有广泛的应用前景[1−3]。目前,商业化锂离子电池的碳负极材料能量密度较低(375 mA∙h/g),存在锂沉积相关的安全问题[4−6]。发展具有高嵌/脱锂容量、高充/放电功率、优异的循环稳定性能、低成本、安全性好的锂离子电池电极材料,成为当前的研究热点[7−9]。许多金属都可以和Li反应,如Si、Sn、Sb、Al、Mg、Bi、In、Zn、Pb、Ag、Pt、Au、Cd、As、Ga和Ge等[10−14],可以成为锂离子电池负极的候选材料,其中金属Al在自然界中储量丰富,成本低廉,具有较高的理论比容量(形成AlLi、Al2Li3和Al4Li9时对应的理论比容量分别为993、1489和2234 mA∙h/g),以及较宽的充放电平台等优点[15],意味着Al负极材料具有较低的生产成本、稳定的高功率输出,有望成为锂离子电池理想的新型负极材料[16]。
金属Al在嵌/脱锂过程中易于产生较大的体积变化,伴随着内部微观结构的改变,导致活性粒子的破裂粉化,导电能力降低,电极寿命受到极大的影响[17]。锂离子活性材料的纳米化、与缓冲元素的合金化方法,是目前改善电极材料性能的两种有效途径。纳米粒子活性单元的体积小,在嵌/脱锂过程中产生的绝对体积变化量较小,粒子间存在的空间可以缓解膨胀/收缩过程中带来的应力变化,从而可以抑制粉化;纳米结构单元可显著缩短Li+扩散距离,快速吸收和储存大量的Li+;纳米结构具有大比表面积,也有助于提高沿晶界界面的Li+扩散速率。纳米尺寸效应有助于提高容量、倍率、循环性能、以及确立新的储锂体系[18−20]。但是纳米材料的大比表面积、高表面能、易团聚、高表面反应活性等特点,也能带来负面效应,使其容量快速衰减。AU等[21]和SHARMA等[22]分别制备了独立的Al纳米棒和Al纳米薄膜,首次放电容量分别达到1243 mA∙h/g和1293 mA∙h/g,但经过10次循环之后容量快速衰减。储锂金属元素与缓冲元素之间的合金化方法分为两大类:一类是与Li+活性元素之间的合金化,如C、Sb、Si、Sn、Mg等;另一类是与Li+惰性的元素之间合金化,如Fe、Co、Ni、Mn、Cu等。活性合金化元素与Al金属的嵌/脱锂电位不同,依然可以起到稳定电极结构的作用;与惰性元素形成合金后,Al原子作为活性中心与Li+结合生成LiAl嵌锂相,惰性元素作为缓冲基体可缓解体积膨胀所产生的应变,同时阻止纳米粒子之间的团聚,提高电极的循环性能。LARCHER等[23]表明Al2Cu、Al4Mn、Al6Mn等铝合金相没有表现出Li+电化学活性,表明铝基金属键具有一定的特殊性。LINDSAY等[24]采用球磨法制备的Fe2Al5合金相则达到485 mA∙h/g的首次放电容量,但首次库伦效率仅有20%~40%。CHEN等[25]采用高能球磨法制备了Al-C、Al-Fe和Al-Fe-C复合材料,其中成分为Al71Fe9C20(摩尔比)体系的首次可逆容量达436 mA∙h/g,15次循环后容量为255 mA∙h/g。缓冲元素Fe、C有助于提高铝基复合材料的可逆容量,有效减少纳米材料团聚,充分发挥材料的活性[26]。
本文作者在以往合金纳米粒子及碳包覆纳米胶囊的合成基础上[27],使用直流电弧等离子体法,在氢氩、气态碳源(甲烷)气氛中,分别制备了Al-Fe、Al-Fe-C纳米复合粉体,对不同组元蒸发行为、相组成、形貌、电化学特性以及碳元素的影响进行了讨论。
1 实验
1.1 合金Al-Fe/C纳米复合粒子制备
以纯微米Al粉和Fe粉作为原材料,取质量比为7:3,将其混合均匀并压制成块。采用直流电弧等离子体气相蒸发法[28],以该压制原料为阳极、钨棒为阴极,工作室抽真空后充入氩气、氢气和甲烷气体,电弧电流设定在90 A、电压控制在20~30 V范围。不同条件下制备的4种样品及其名称如表1所列,由X射线衍射确定的纳米粉体产物的相组成也一并列出。

表1 合金Al-Fe、Al-Fe-C纳米复合粉体制备条件及相组成
1.2 表征和电化学测试
使用荷兰帕纳科公司的Empyrean型X射线衍射仪(Cu K辐射,=0.15406 nm),进行物相分析,扫描范围20°~80°;使用Tecnai G20 S−TWIM型透射电子显微镜观察纳米粒子形貌和微观结构;使用金义博公司的CS−8800型红外碳−硫分析仪进行碳元素分析;使用日本岛津公司的X射线荧光光谱仪(XRF−1800型)进行Fe、Al元素分析。
为了测试纳米粉体的电化学性能,将活性物质(Al-Fe、Al-Fe-C 纳米复合粉体)、导电剂(Super P)和粘接剂(聚偏氟乙烯,PVDF),按质量比6:2.5:1.5均匀混合并压制成片,置于真空干燥箱中120 ℃干燥12 h,取出后在充满氩气的手套箱中组装成CR2025型纽扣模拟电池,对电极为金属锂片,电解液采用1 mol/L的LiPF6溶液(EC与DEC体积比为1:1),隔膜为微孔聚丙烯膜。在电压范围为0.01~2.00 V、电流密度100 mA/g下进行恒流充放电测试。使用上海辰华CHI660D−1型电化学工作站,以0.10 mV/s扫描速率,在0.01~2.00 V电压范围下测试循环伏安曲线;在频率范围0.1 Hz~100 kHz、振幅5 mV下,进行交流阻抗谱测试。电池性能测试使用LAND CT2001A型系统。
2 结果与讨论
2.1 合金Al-Fe/C纳米复合粒子相组成及形貌
图1所示为4种纳米粉体样品的XRD谱,其中样品A、B1和B2的主相是Al,衍射峰对应的2值分别为38.6°、44.9°、65.2°和78.4°,与单质金属Al(PDF:00−001−1180)的(111)、(200)、(220)和(311)晶面的衍射峰相一致。在高浓度甲烷气氛(4 mol/m3)中制备的纳米粉体(即样品B3),其中不存在单质金属Al相,表明金属Al全部用于形成碳化物(Al4C3,PDF:00−035−0799)和金属间化合物(Fe2Al5,PDF:00−001−1228),以及石墨相(PDF:00−008−0415)。有别于高浓度甲烷气氛条件,当其浓度降为2 mol/m3时(即样品B2),其中部分铝与碳反应生成Al4C3相之外,没有检测到金属间化合物形成,有少量的石墨相。当甲烷浓度更低(0.4 mol/m3,样品B1)或不存在甲烷气氛(样品A)时,制备出的纳米粉体相组成基本一致,即主相为单质Al和次相为FeAl2。表1列出了以上4种纳米粉体的相组成。以上结果表明,气态碳源浓度对纳米粉体产物中相形成及其含量具有较大的影响,同时对金属组元的蒸发行为也产生一定的作用。
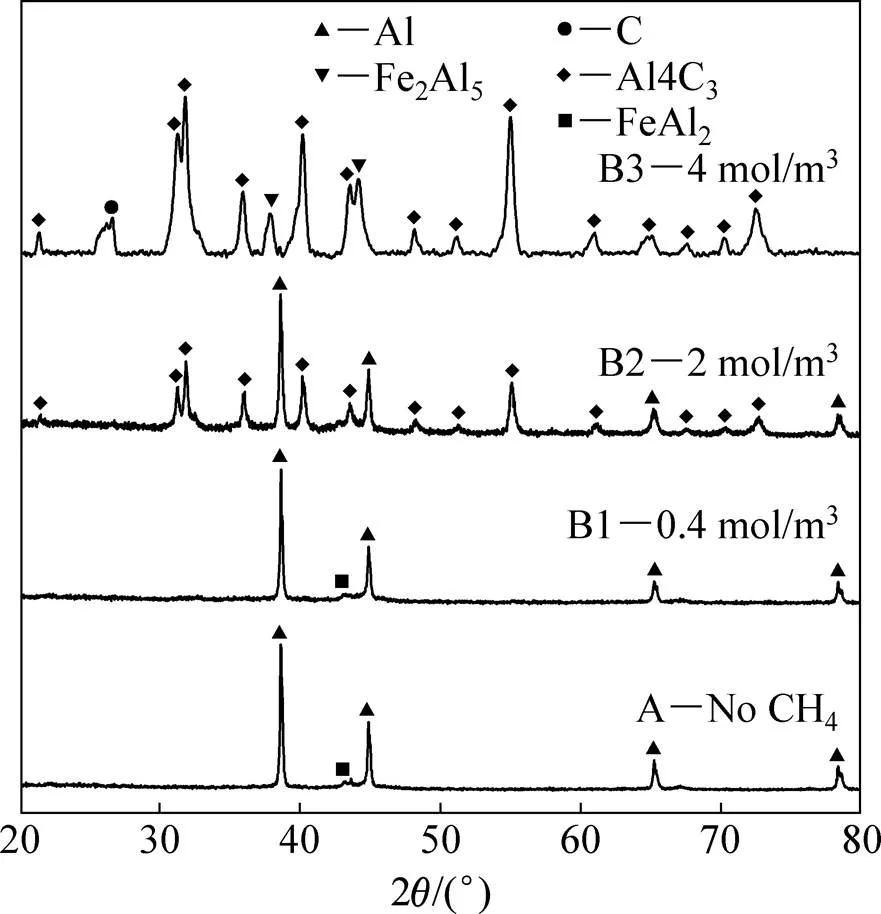
图1 纳米粉体样品的XRD谱
金属组元Al和Fe在共蒸发过程中,存在蒸发速率的差异,导致纳米粉体产物与块体原料之间存在成分差异。表2列出了粉体样品A和B3的成分分析结果,其中样品B3的C含量(质量分数)为18.57%,表明C原子使Al/Fe成分差异进一步增大。直流电弧氢等离子源与普通热源不同,能够产生过饱和的活性原子态氢,对金属的蒸发行为起着决定性作用。纯金属的蒸发速率可用经典的真空蒸发速率公式描述[29]:
=1.574×(/)0.5(1)
式中:是冷凝常数(取=1,主要考虑Al、Fe具有相同的蒸发环境和冷凝条件,便于比较两者蒸发速率的相对大小);是蒸发源温度,K;是摩尔质量,g;是纯组元在温度下的饱和蒸汽压,Pa,可由如下公式计算出Al和Fe的饱和蒸汽压[30]:
lg=−1+lg++(2)
式中:均为常数。由式(2)计算出Al和Fe在1873 K下的饱和蒸汽压分别为100.46 Pa和1.963 Pa。将之代入式(1),求得Al、Fe的蒸发速率分别为18.975 g/(cm2×h)和0.533 g/(cm2×h)。这一结果表明,在相同蒸发条件下,Al的蒸发速率约是Fe的36倍,这是导致粉体产物成分与块体原料成分不同的主要 原因。
在Fe-Al二元平衡相图(见图2)中直观地表现了原料及粉体样品中Al/Fe相对成分之间的差异。如果经历平衡冷却过程,标定成分(70% Al)块体原料的最终产物应该为FeAl3相和过剩的单质Al相,但经过共蒸发及非平衡冷却过程中后,纳米粉体产物(样品A)由FeAl2相和Al相组成,且存在更多的过剩单质Al主相,Al含量为83.0%。此外,C组元介入到共蒸发过程后(样品B3),导致Al/Fe成分差异进一步扩大(89.2% Al),即C的存在使Al组元的蒸发速率进一步变大,Al的碳化物Al4C3成为主相。由此可以发现,C原子会影响金属的蒸发速率,这是由于C原子的存在形成了Al、Fe、C这3种元素共蒸发的热力学条件,Al4C3产物的形成促进了对Al元素的进一步消耗,三元共存的浓度条件被破坏,进而加快了Al元素的蒸发速率,形成了最终纳米粉体产物中相的种类及含量。在非平衡状态下合金纳米粒子的形成过程非常复杂,出现与平衡合金成分不相符合的相种类和组成,金属间化合物的有效形成热将决定其形成的难易程度,通常有效形成热值越小则越容易生成该化合物[31]。

表2 纳米粉体样品A、B3的元素含量

图2 Fe-Al二元相图示意图
图3所示为Al-Fe/C纳米粒子的TEM像,其中图3(a1)和(a2)所示为在氢氩气氛下制备的Al-Fe纳米粒子,图3(b)~(d)所示分别为在氢氩气氛中加入不同浓度甲烷后得到的Al-Fe-C纳米粒子。Al-Fe纳米粒子(见图3(a1))呈规则球状,粒径为20~100 nm范围,由HRTEM图(见图3(a2))可观察到Al-Fe纳米粒子内部的晶格条纹,其间距为0.232 nm,与单质Al的(111)晶面一致。Al-Fe纳米粒子(样品A)中单质Al相为主相,HRTEM分析结果与XRD测试结果一致。由图3(b1)、(c1)和(d1)可知,甲烷浓度较小时,粒子形貌呈短棒状,长度在20~100 nm范围(见图3(b1))。甲烷浓度增加时,粒子粒径变大且形貌呈柱状,长度在80~120 nm范围(见图3(c1))。当甲烷浓度继续增加时,粒子粒径明显变小呈现出不规则的长条线状,长度在80~120 nm范围(见图3(d1))。样品B3粒子形貌有别于其他样品,甲烷浓度过量时,C原子与Al反应生成碳化物,随着反应的持续进行生成了线状产物。在图3(b2)和(d2)中分别观察到单质Al和Fe2Al5相,与XRD测试结果一致。图3(c2)中出现了FeAl2,由于含量较少XRD并未检测出来。FeAl2相表现出一定的几何棒状特征,这是其晶体惯态的一种体现;由于碳物质可以通过包覆形式保护其不发生氧化(钝化)反应,使其形貌特征可以保持。碳物质(石墨)以部分包覆和游离形式存在于纳米粉体中。当甲烷浓度达到4 mol/m3时,图3(d2)中样品B3出现Fe2Al5合金相嵌入于碳物质中,这种结构有利于维持嵌/脱锂过程中电极材料结构的稳定性。

图3 合金Al-Fe/C纳米复合粒子的TEM和HRTEM像
2.2 合金Al-Fe/C纳米复合材料储锂电化学行为
2.2.1 合金Al-Fe/C纳米复合电极循环伏安特性
分别以纳米粉体A、B1、B2和B3作为活性物质制备电极,金属锂片作为对电极,组装成半电池进行电化学性能测试。图4所示为利用4种纳米粉体制备的电极在0.1 mV/s扫描速率下测试的电压−电流密度曲线。从图4中可以看出,在首次循环中4种电极都出现了不可逆的还原峰,其峰电势在0.51~0.69 V范围,这是首次循环过程中在电极表面上形成SEI膜所导致。纳米粉体A即在无碳气氛制备的Al-Fe纳米粒子,其主相和活性组元为单质Al,其嵌/脱锂电位分别出现在0.14 V和0.53 V处(见图4(a)),但在首次循环中没有出现相应的还原峰,这是由于Al相表面氧化膜需要经过首次循环破裂后才可以进行Li+嵌入[32],其他粉体样品中也同样出现类似现象。活性Al相嵌锂后形成Li-Al合金,除Al-Fe纳米粉体A外,在含碳Al-Fe-C纳米粉体B2中也出现嵌锂过程,含碳Al-Fe-C纳米粉体B1中没有出现相应峰是由于嵌锂过程相对较弱所导致。Al相嵌/脱锂电化学过程可由反应式(3)和(4)表示[33]:
Al+Li++e→LiAl (3)
LiAl→Al+Li++e (4)
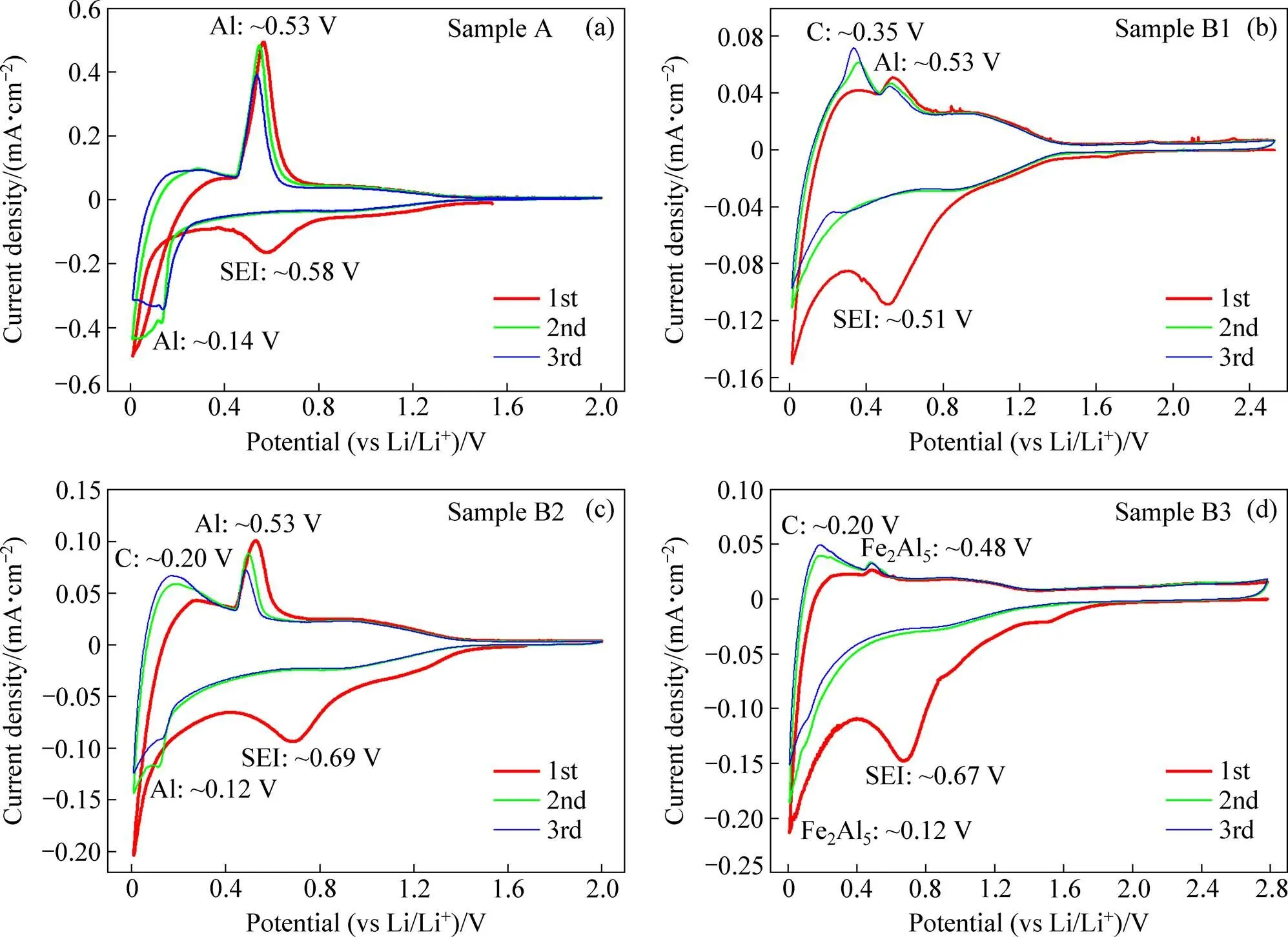
图4 合金Al-Fe/C纳米复合粒子电压−电流密度曲线
含碳Al-Fe-C纳米粉体(B1、B2和B3)的CV曲线上均出现了C的氧化峰(0.20~0.35 V范围),C的作用显著出现[34],表明这些纳米粉体中均存在碳物质,其氧化峰强弱差异是由于其中C含量及其存在形式不同所导致。C含量最高的纳米粉体B3中活性主相为Fe2Al5,CV曲线上出现的还原(0.12 V)和氧化(0.48 V)峰分别对应着Fe2Al5相的嵌/脱锂电化学过程,其反应式可由式(5)和(6)表示[35]:
Fe2Al5+5Li++5e→5LiAl+2Fe (5)
(1−)Li+Al1−xM→(1−)AlLi+M (6)
Fe2Al5(见图4(d))的氧化峰强度在循环过程中不断增强,体现出较好的活性,同时非活性组元Fe的存在一定程度上缓解了电极的体积膨胀,有助于提升电极的循环稳定性。在图5所示的循环性能测试中进一步证实了这种稳定性,与其他样品作比较,样品B3表现出最好的循环稳定性能。
2.2.2 合金Al-Fe/C纳米复合电极充/放电性能
图5所示为样品A、B1、B2和B3纳米复合电极在电流密度为100 mA/g下的首次充放电曲线及其循环性能曲线。从图5(a)中可以看出,样品B3具有最高的首次放电容量628.8 mA∙h/g,循环50次后容量保持在146.2 mA∙h/g;样品A、B1和B2首次放电容量分别为348.8、193.3和275.5 mA∙h/g,循环50次后容量保持在75.8、74.7和88.3 mA∙h/g。由此可见,4种纳米粉体复合电极的循环性能由大到小依次为B3>B2>A>B1,表明复合粉体中碳物质的存在有利于提高循环稳定性能,同时,活性金属化合物Fe2Al5相的形成有利于提高充放电容量和抑制体积变化,也将有利于提高大电流密度下的功率性能[24]。由图5(b)可知,样品A初始容量大于样品B1,而50次循环后两者容量差异较小。由图3(b2)可知,样品B1粒子形貌呈棒状,增加了Li离子的扩散距离,嵌锂反应未能完全进行,使得其初始的容量较小。同时,样品B1中C含量非常低,对改善电极循环稳定性的作用较小。
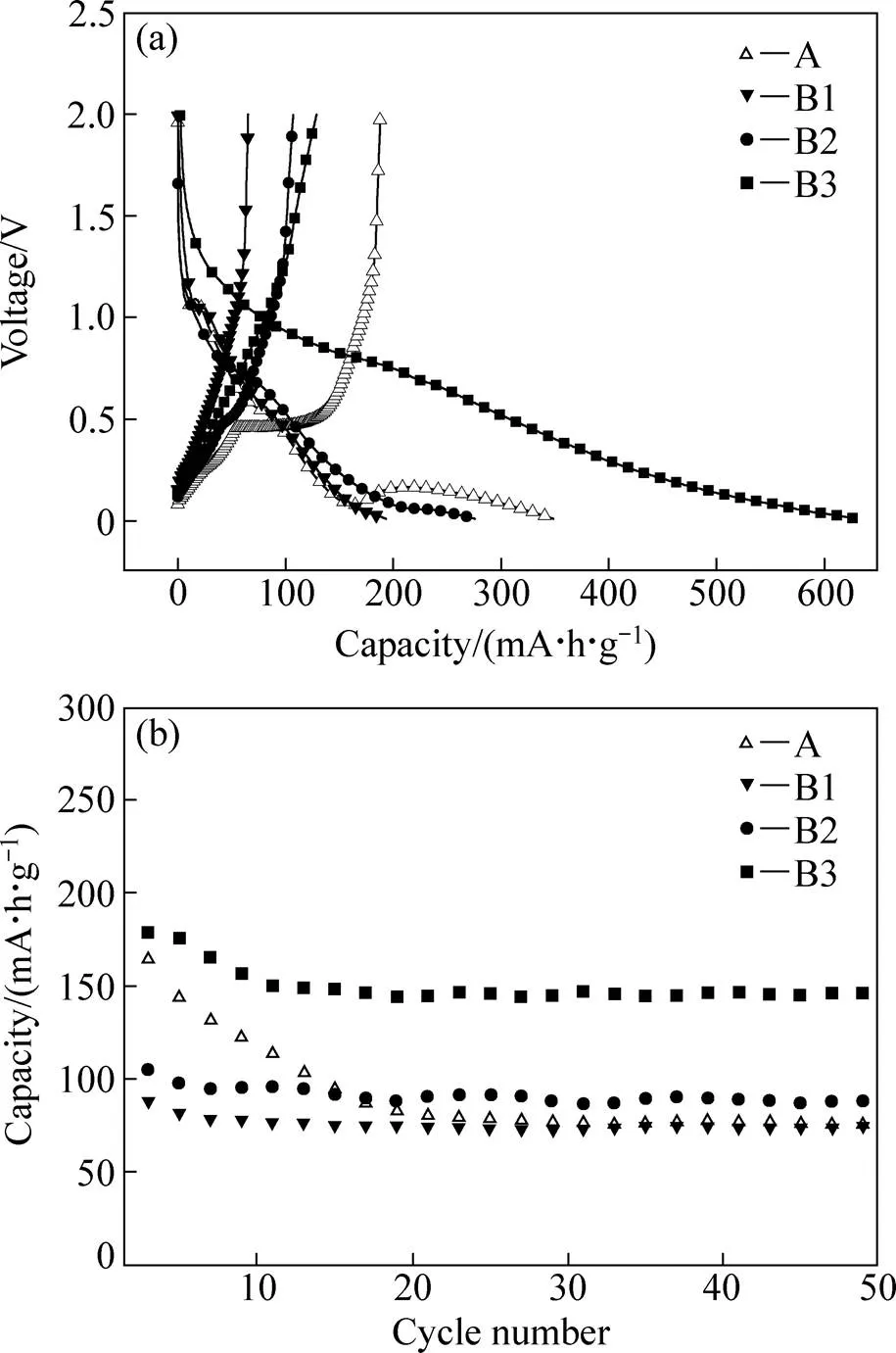
图5 样品A、B1、B2和B3电极在电流密度为100 mA/g下的首次充放电曲线和循环性能曲线
Al-Fe/C纳米复合电极存在首次充放电过程容量衰减问题,其原因归结于以下方面:Al-Fe/C纳米粒子表面的金属氧化物与Li+发生不可逆反应,生成Li的氧化物(Li2O)[36],造成Li+的损失;电解液和活性物质之间形成SEI膜,也造成Li+的损失;活性物质在充放电过程中产生的体积膨胀可使其失去部分电接触,导致循环性能较差[37]。
2.2.3 合金Al-Fe/C纳米复合电极的阻抗谱
为了进一步了解Al-Fe、Al-Fe-C纳米复合材料的电化学特性,分别测试了4种复合材料电极在循环前(见图6(a))及其循环3次后(见图6(b))的电化学阻抗谱,其中嵌入图为对应的等效电路图。从图6中可以看出,4种材料电极初始态(充/放电循环之前)的交流阻抗谱图,均由高频区的一个半圆以及低频区的斜线(Warburg阻抗)所组成。高频区的半圆大小与电荷转移过程有关,而低频区的直线部分与Li+在电极中的Warburg扩散系数相关[38]。在初始状态,样品A、B1,即无碳、含微量碳的粉体材料,两者具有相似的阻抗谱特征;而样品B2、B3,即C含量较高的粉体材料的阻抗谱较为接近。表明初始态电极材料,其电化学阻抗特征主要取决于其中的C含量。在循环3次后,4种样品的交流阻抗谱图均由高频区、中频区的两个扁半圆和低频区的斜线(Warburg阻抗)所组成。高频区的半圆与电极表面SEI膜的形成有关,中频区的半圆与电荷转移过程有关,而低频区的直线部分同样与Li+在电极中的Warburg扩散系数相关。
在初始态、循环后状态相对应的两种等效电路图中,1为电解液电阻,2为Li+在电极材料中的扩散电阻,3为SEI膜电阻,1为Li+在Al-Fe、Al-Fe-C纳米材料电极中的Warburg阻抗;CPEdl为电极与电解液之间的双电层电容,与电极和电解液之间的界面有关;CPEs为SEI膜电容,与SEI膜和电解液之间的界面有关。电化学阻抗re、Li+扩散系数0、法拉第电流密度F,分别表示为

图6 样品A、B1、B2和B3复合电极的循环前(a)、3次循环后(b)的能奎斯特图和等效电路图及拟合曲线
re=1+ct+ω−0.5(7)
0=0.5/(2δc)2(8)
F=/(2) (9)
式中:1为电解液的电阻;ct为2与3之和;为低频区的角频率;ω为re−−0.5关系曲线的斜率(Warburg系数),可由实验数据曲线拟合结果计算得到。将ω代入式(8)中,计算得到Li+的扩散系数0[39]。由式(9)可计算得到法拉第电流密度F。为气体常数,8.314 J/(mol∙K);为法拉第常数,96500 C/mol;为室温298 K;为电极的表面积;为Li+体积摩尔浓度。各种参数拟合及计算结果列于表3中。
从表3中可以看出,初始态时,样品中的C含量可降低电化学阻抗,主要源于导电碳材料减小了溶液与粒子间的接触电阻[40];但经历3次循环之后,由于电极界面形成了SEI膜,电化学阻抗发生了根本变化,即无碳样品A的阻抗最小,而C含量最大的样品B3的阻抗为最大,表明SEI膜的种类及阻抗大小受到界面的极大影响。Li+的扩散速率表明,碳物质的存在促进了Li+的迁移和扩散,经过几次循环之后离子扩散速率进一步提高。样品B3,即在所有样品中C含量最高且唯一含有活性Fe2Al5相,始终保持最大的Li+扩散速率,分别为2.1×10−14 m2/s(初始态)和1.2×10−14 m2/s(循环后),体现出最好的循环稳定性能。总之,阻抗分析表明C含量较多将有利于构造稳定的导电网络,促进Li+的扩散并可充分释放材料的嵌/脱锂活性。
3 结论
1) 直流电弧等离子体蒸发法是制备Al-Fe/C纳米复合粉体材料的有效方法。当气态碳源—甲烷浓度较小时,粉体中以Al为主相;随着甲烷浓度的增加,单质Al含量逐渐减少,而Al4C3相在增加。
2) C的存在可促进Al组元的快速蒸发,使合金相由FeAl2向富Al的Fe2Al5相转变。同时,随着甲烷浓度的增加,粉体颗粒的外在形貌由球状向柱状和线状演化,这是由于形成了较多游离碳物质和碳化物所导致,将对电化学性能产生极大影响。
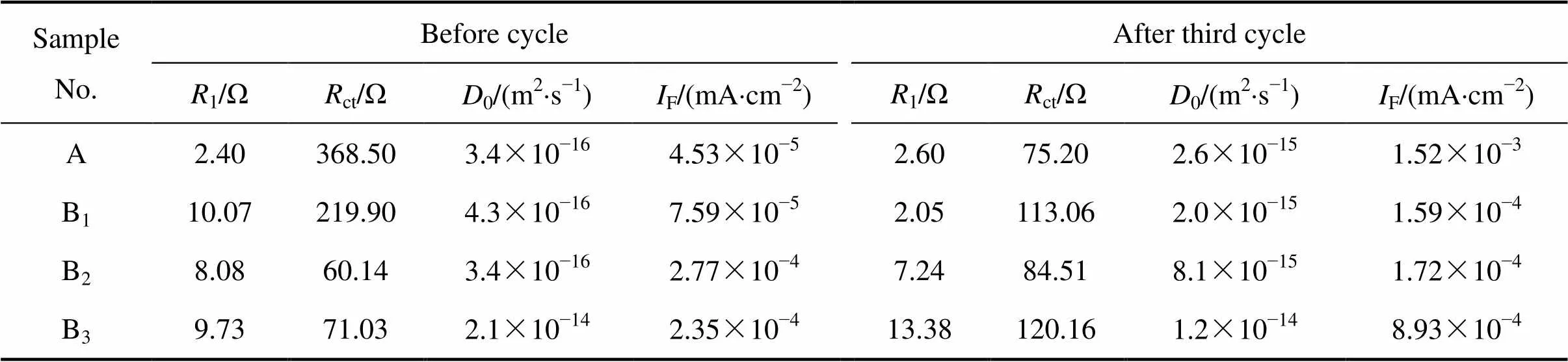
表3 样品A、B1、B2和B3电极的等效电路参数
3) 在4 mol/m3甲烷浓度条件下制备的Al-Fe-C纳米粒子,形成了由Al4C3、Fe2Al5和石墨相构成的复合粉体,表现出优异的电化学性能和循环稳定性能,首次放电容量628.8 mA∙h/g,50次循环后容量为146.2 mA∙h/g。
4) 复合粉体中碳物质的存在有利于构造稳定的导电网络,提高Li+的扩散速率和释放电极材料的储锂活性,活性金属化合物Fe2Al5相有利于提高充/放电容量和抑制体积变化,有效提高了电极的循环稳定性能。
[1] RWDDY T B, LINDEN D. Linden’s handbook of batteries[M]. McGraw-Hill, 2011: 2−8.
[2] LOEFFLER N, BRESSER D, PASSERINI S. Secondary lithium-ion battery anodes: from first commercial batteries to recent research activities[J]. Platinum Metals Review, 2015, 59(1): 34−44.
[3] 李姣姣, 王先友, 杨顺毅, 龙晚妹, 王 宏, 白 俐, 吴 强. 碳化钙骨架碳负极材料的制备及电化学性能[J]. 中国有色金属学报, 2011, 21(12): 3087−3093. LI Jiao-jiao, WANG Xian-you, SHUN Yi-yang, WAN Mei-long, WANG Hong, BAI Li, WU Qiang. Preparation and electrochemical properties of calcium carbide skeleton carbon anode materials[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(12): 3087−3093.
[4] LIANG Bo, LIU Yan-ping, XU Yun-hua. Silicon-based materials as high capacity anodes for next generation lithium ion batteries[J]. Journal of Power Sources, 2014, 267: 469−490.
[5] SHUKLA A K, KUMAR T P. Materials for next-generation lithium batteries[J]. Current Science, 2008, 94(3): 314−331.
[6] LI Z, HUANG J, LIAW B Y, METZLER V, ZHANG J B. A review of lithium deposition in lithium-ion and lithium metal secondary batteries[J]. Journal of Power Sources, 2014, 254: 168−182.
[7] RAHMAN M A, WONG Y C, SONG G. A review on porous negative electrodes for high performance lithium-ion batteries[J]. Journal of Porous Materials, 2015, 22(5): 1313−1343.
[8] ROBERTS A D, LI X, ZHANG H F. Porous carbon spheres and monoliths: morphology control, pore size tuning and their applications as Li-ion battery anode materials[J]. Chem Inform, 2014, 43(13): 4341−4356.
[9] SU X, WU Q, LI J. Silicon-based nanomaterials for lithium-ion batteries: A review[J]. Advanced Energy Materials, 2014, 4(1): 375−379.
[10] WUHui, CUI Yi. Designing nanostructured Si anodes for high energy lithium ion batteries[J]. Nano Today, 2012, 7(5): 414−429.
[11] WINTER M, BESENHARD J O. Electrochemical lithiation of tin and tin-based intermetallics and composites[J]. Electrochimica Acta, 1999, 45(1): 31−50.
[12] NITTA N, YUSHIN G. High-capacity anode materials for lithium-ion batteries: Choice of elements and structures for active particles[J]. Particle & Particle Systems Characterization, 2014, 31(3): 317−336.
[13] GORIPARTI S, MIELE E, ANGELIS F D. Review on recent progress of nanostructured anode materials for Li-ion batteries[J]. Journal of Power Sources, 2014, 257(3): 421−443.
[14] WANG Jian-tao, YANG Juan-yu, LU Shi-gang. A mini review: Nanostructured silicon-based materials for lithium ion battery[J]. Nanoscience & Nanotechnology-Asia, 2016, 6(1): 3−27.
[15] HAMON Y, BROUSSE T, JOUSSE F, TOPART P, BUVAT P, SCHLEICH D. Aluminum negative electrode in lithium ion batteries[J]. Journal of Power Sources, 2001, 97: 185−187.
[16] LI Qing-feng, NIELS J B. Aluminum as anode for energy storage and conversion: A review[J]. Journal of Power Sources, 2002, 110(1): 1−10.
[17] THACKERAY M M, VAUGHEY J T, JOHNSON C S, KROPF A J, BENEDEK R, FRANSSON L M L, EDSTROM K. Structural considerations of intermetallic electrodes for lithium batteries[J]. Journal of Power Sources, 2002, 113(1): 124−130.
[18] LI Shu-wei, ZHAO Chun-song, LI Bo, WU Hui. Performance enhancement of nanostructure silicon anode for lithium ion battery[J]. Current Nanoscience, 2015, 12(2): 169−174.
[19] GUO Yu-guo, HU Jin-song, WAN Li-jun. Nanostructured materials for electrochemical energy conversion and storage devices[J]. Advanced Materials, 2008, 20(23): 2878−2887.
[20] ROY P, SRIVASTAVA S. Nanostructured anode materials for lithium ion batteries[J]. Journal of Materials Chemistry A, 2014, 3(6): 2454−2484.
[21] AU M, MCWHORTER S, AJO H, ADAMS T, ZHAO Y P, GIBBS J. Free standing aluminum nanostructures as anodes for Li-ion rechargeable batteries[J]. Journal of Power Sources, 2010, 195(10): 3333−3337.
[22] SHARMA S K, KIM M S, KIM D Y, YU J S. Al nanorod thin films as anode electrode for Li ion rechargeable batteries[J]. Electrochimica Acta, 2013, 87(1): 872−879.
[23] LARCHER D, BEAULIEU L Y, MAO O, GEORGE A E, DAHN J R. Study of the reaction of lithium with isostructural A2B and various AlB alloys[J]. 2000, 147(5): 1703−1708.
[24] LINDSAY M J, WANG G X, LIU H K. Al-based anode materials for Li-ion batteries[J]. Journal of Power Sources, 2003, 119(3): 84−87.
[25] CHEN Zhong-xue, QIAN Jiang-feng, AI Xin-ping, CAO Yu-liang, YANG Han-xi. Electrochemical performances of Al-based composites as anode materials for Li-ion batteries[J]. Electrochimica Acta, 2009, 54(16): 4118−4122.
[26] WANG C Y, MENG Y S, CEDER G, LI Y Z. Electrochemical properties of nanostructured Al1−xCualloys as anode materials for rechargeable lithium-ion batteries[J]. Journal of the Electrochemical Society, 2008, 155(9): S10−S10.
[27] DONG Xin-long, ZHANG Zhi-dong, JIN S R, SUN Wei-ming, ZHAO Xin-guo, LI Zhi-jie, CHUANG Y C. Characterization of Fe-Ni(C) nanocapsules synthesized by arc discharge in methane[J]. Journal of Materials Research, 1999, 14(5): 1782−1790.
[28] 董星龙, 孙维民, 王 维, 李志杰. 一种自动控制直流电弧金属纳米粉生产设备及方法: 中国, CN200410021190.1[P]. 2004−02−23. DONG Xing-long, SUN Wei-ming, WANG Wei, LI Zhi-jie. A method and equipment of automatic DC are discharge for metal nanoparticles production: China, CN200410021190.1[P]. 2004−02−23.
[29] LANGMUIR I, IKLE M. The vapor pressure of metallic tungsten[J]. Physical Review, 1913, 2(5): 329−342.
[30] 戴永年, 杨 斌. 有色金属真空冶金[M]. 北京: 冶金工业出版社, 2009: 38−42. DAI Yong-nian, YANG Bin. Vacuum metallurgy of nonferrous metals[M]. Beijing: Metallurgical Industry Press, 2009: 38−42.
[31] 雷军鹏, 董星龙, 赵福国, 吕 波, 黄 昊, 雷明凯. Fe(Ni)-Sn体系金属间化合物纳米粒子中初生相的预测[J]. 金属学报, 2008, 44(8): 922−926.LEI Jun-peng, DONG Xing-long, ZHAO Fu-guo, LV Bo, HUANG Hao, LEI Min-kai. Prediction of the primary intermetallic compound nanoparticles formed in Fe(Ni)-Sn system[J]. Acta Metallurgica Sinica, 2008, 44(8): 922−926.
[32] 赵亚楠, 薛方红, 黄 昊, 刘春静, 甘小荣, 董星龙. 纳米铝粒子电极的脱/嵌锂离子特性[J]. 材料研究学报, 2011, 25(4): 386−390. ZHAO Ya-nan, XUE Fan-hong, HUANG Hao, LIU Chun-jin, GAN Xiao-rong, DONG Xing-long. Lithium Ion intercalation/deintercalation properties of aluminum nanoparticles as anode materials for Li-ion batteries[J]. Chinese Journal of Materials Research, 2011, 25(4): 386−390.
[33] LIANG Pu, ZHANG Lin-ping, WANG Fei, SUN Zhao-bo, HU Qing, YANG Sen, WANG Li-qun, SONG Xiao-ping. Effects of Cr content on electrochemical properties of melt-spun Al75−xSi25Cralloy anodes for lithium-ion batteries[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(6): 1393−1400.
[34] LI Wei, YANG Rong, ZHENG Jie, LI Xing-guo. Tandem plasma reactions for Sn/C composites with tunable structure and high reversible lithium storage capacity[J]. Nano Energy, 2013, 2(6): 1314−1321.
[35] FLEISCHAUER M D, OBROVAC M N, MCGRAW J D. AlM (M=Cr, Fe, Mn, Ni) thin-film negative electrode materials[J]. Journal of the Electrochemical Society, 2006, 153(3): A484−A491.
[36] LIU C J, XUE F H, HUANG H, YU X H, XIE C J, SHI M S, CAO G Z, JUNG Y G, DONG X L. Preparation and electrochemical properties of Fe-Sn(C) nanocomposites as anode for lithium-ion batteries[J]. Electrochimica Acta, 2014, 129(10): 93−99.
[37] JEONG G J, KIM Y U, SOHN H J, KANG T. Particulate-reinforced Al-based composite material for anode in lithium secondary batteries[J]. Journal of Power Sources, 2001, 101(2): 201−205.
[38] XIE J X, IMANNISHI N, ZHANG T, HIRANO A, TAKEDA Y, YAMAMOTO O. Li-ion diffusion in amorphous Si films prepared by RF magnetron sputtering: A comparison of using liquid and polymer electrolytes[J]. Materials Chemistry & Physics, 2010, 120(2): 421−425.
[39] CUI Yan, ZHAO Xiao-li, GUO Rui-song. Improved electrochemical performance of La0.7Sr0.3MnO3and carbon co-coated LiFePO4synthesized by freeze-drying process[J]. Electrochimica Acta, 2010, 55(3): 922−926.
[40] KONG Jun-hua, LIU Zhao-lin, YANG Zheng-chun, TAN Hui-ru, XIONG Shan-xin, WONG S Y, LI Xu, LU Xue-hong. Carbon/SnO2/carbon core/shell/shell hybrid nanofibers: Tailored nanostructure for the anode of lithium ion batteries with high reversibility and rate capacity[J]. Nanoscale, 2012, 4(2): 525−530.
Formation mechanism and electrochemical behaviors of Al-Fe/C nanocomposite particles for lithium ion battery
CHENG Ting, GAO Song,DING Ang, LIU Dao-lin, HUO Feng-li, GAO Ming, DONG Xing-long
(School of Materials Science and Engineering, Key Laboratory of Materials Modification by Laser, Ion, and Electron Beams, Dalian University of Technology, Dalian 116024, China)
Al-Fe and Al-Fe-C nanocomposite particles were prepared through DC arc-discharge method under a methane atmosphere with micro-sized aluminium and iron powders as the raw materials. The formation mechanism, structures, morphologies and electrochemical performances of the nanoparticles’ samples were studied. The effects of carbon atoms on the composition, phase structure and electrochemical properties were studied, and the formation mechanism of nanoparticles as well as electrochemical intercalation/deintercalation of lithium ions were also discussed. The results indicate that the Al-Fe particles prepared in a carbon-free atmosphere are spherical in shapes, meanwhile, the carbon-containing atmosphere causes the morphology of particles columnar or linear, the composition changes from Al to Al4C3and from FeAl2to Fe2Al5in Al-Fe-C nanocomposite particles. The first discharge capacities of four kinds of nanoparticles’ electrodes are 348.8, 193.3, 275.5 and 628.8 mA∙h/g, under the current density of 100 mA/g, respectively. The presence of intermetallic Fe2Al5in the powders favors to improve the capacities and restrain the volume changes during the intercalation/deintercalation of lithium ions, thus the cycle stability of electrode was greatly enhanced.
Al-Fe/C; nanocomposite; lithium ion battery; anode; DC arc-discharge method
Projects(51271044, 51331006) supported by the National Natural Science Foundation of China
2016-07-15;
2018-05-12
DONG Xing-long; Tel: 0411-84706130; E-mail: dongxl@dlut.edu.cn
国家自然科学基金资助项目(51271044,51331006)
2016-07-15;
2018-05-12
董星龙,教授,博士;电话:0411-84706130;E-mail:dongxl@dlut.edu.cn
10.19476/j.ysxb.1004.0609.2018.07.11
1004-0609(2018)-07-1361-10
TB34
A
(编辑 何学锋)
