重金属在油菜秆热解过程中的迁移规律
2018-08-08蔡攀蒋绍坚付国富彭好义刘僖朱明伟
蔡攀,蒋绍坚,付国富,彭好义,刘僖,朱明伟
重金属在油菜秆热解过程中的迁移规律
蔡攀,蒋绍坚,付国富,彭好义,刘僖,朱明伟
(中南大学 能源科学与工程学院,湖南 长沙,410083)
以含重金属油菜秆为研究对象,采用热重分析仪研究其热解特性,采用管式炉热解装置研究热解温度和热解时间对Cd,Zn,Mn,Cu,Cr和Ni等重金属迁移的影响。研究结果表明:随升温速率增加,油菜秆质量损失率增大,TG和DTG曲线向高温区移动,残余固体质量增大;油菜秆热解产炭中重金属明显富集(Cd除外),且重金属总保留率随热解温度升高呈先升高后降低趋势,而随热解时间延长则逐步降低;在热解温度为500 ℃、热解时间为10 min时,重金属总保留率最高;各重金属的挥发性存在较大差异,其中Cd为易挥发性元素,Zn和Cu为中等挥发性元素,Mn,Cr和Ni为难挥发性元素。
土壤修复;油菜秆;重金属;热解特性;迁移
土壤重金属污染是我国面临的严重问题之一。据2014年环保部和国土资源部公布的全国土壤污染状况调查公报,全国土壤总的点位超标率达16.1%[1],且以Cd,Ni,As和Pb等重金属污染物为主。由于重金属污染物不容易降解,在生态环境中容易通过水体、食物链等载体转移至动物和人体中,因此,土壤重金属污染对人体健康构成严重威胁。目前,土壤重金属污染的修复方法主要有物理修复法、化学修复法和植物修复法[2]。其中,植物修复方法是利用修复植物吸收土壤中的重金属并将其富集到可收割部位,达到治理土壤污染的目的[3]。与物理和化学修复法相比,植物修复法具有成本低廉、环境友好、能大规模原位治理等优点而成为土壤重金属修复的理想方法。然而,利用植物修复法修复重金属污染的土壤时会产生大量富集重金属的生物质。CHEN等[4]发现蜈蚣草可富集As高达36 t/m2。YANG等[5]的研究表明,采用东南天景修复重金属污染土壤时其上部含Zn高达20 g/kg,含Cd达500 mg/kg。若不采取适当的方法对这些修复植物加以处置,则其中的重金属会重新释放至环境中造成二次污染。目前,国内外修复植物的处置方法主要有焚烧法[6]、灰化法[7]、热解法[8−9]。焚烧法和灰化法存在较严重的重金属二次污染风险,热解法与焚烧法和灰化法相比热解温度更低,重金属大部分富集在固态产物中,从而降低了重金属直接以气态形式释放至环境中而产生二次污染的风险。此外,修复植物经热解后,其中所含重金属的生物毒性和生物有效性明显降低[10−11]。热解得到的生物炭可以作为重金属企业的燃料或其他用途,从而实现修复植物的减量化、无害化、资源化利用,因此,热解法是具有发展前景的修复植物处置方法[12]。LIU等[13]对含重金属芦竹进行了热解实验研究,发现热解时间为2 h,当热解温度由250 ℃升至500 ℃时,生物炭产率由55.5%降至12.3%;当热解温度为300 ℃,热解时间由0.5 h延长至3.0 h时,生物炭产率由35.2%降至23.3%。STALS等[14]对含重金属的硬木修复植物进行热解实验,发现随着热解温度升高,重金属元素逐渐向生物油中迁移,但大部分仍保留在生物炭中。夏娟娟等[15]对修复植物长香稻谷热解半焦中重金属的形态分布进行了研究,发现随着热解温度升高,重金属不稳定态占比下降,稳定态占比增加,故控制热解条件不仅可以改变生物质热解产物的分布,而且能改变生物质中重金属的去向和分布。为此,本文作者以含Cd,Zn,Mn,Cu,Cr和Ni等重金属的油菜秆为研究对象,研究其热解过程中重金属的迁移规律,以期将重金属最大程度地富集于热解炭中,降低重金属二次污染的风险,为含重金属生物质的热解炭化工艺条件的选择和优化提供理论指导。
1 材料与方法
1.1 实验材料
实验材料来源于湘潭某重金属污染土壤植物修复示范区收获物油菜秆。首先,将收集的油菜秆用自来水清洗后自然晒干,然后将其切段并过筛处理,使其颗粒直径为0.9 mm,最后将油菜秆颗粒装入封口袋备用。
1.2 TG实验
利用SDT−Q600型热综合分析仪进行TG实验。每次实验称取油菜秆质量20 mg,控制N2流量为 100 mL/min,分别以5,20和35 ℃/min的升温速率从室温升至700 ℃。实验数据由计算机采集,并绘制成TG曲线。对TG曲线微分得到DTG曲线。
1.3 热解实验
利用TC GC−1200型真空管式炉进行油菜秆的热解实验。每次实验时,将装有10 g油菜秆的瓷坩埚置于石英管中,以500 mL/min的流速通入N2吹扫30 min后,用升温速率为15 ℃/min的加热反应器加热至设定的热解温度,待物料达到热解终温后继续保温至设定的热解时间,随后停止加热;待反应器自然冷却至室温后取出热解残渣。考察热解温度对实验结果的影响时,设定热解时间为30 min,热解温度分别选取350,400,500,600和650 ℃;考察热解时间对实验的结果影响时,设定热解温度为650 ℃,热解时间分别选取10,30,50,70和90 min。
1.4 分析与测试
在重金属质量分数检测之前,先对实验样品进行微波消解[16]。每次消解实验称取0.25 g实验样品于消化罐中,加入7 mL HNO3和2 mL H2O2,开启微波消解系统,以1 kW的功率将溶液加热至180 ℃并保温15 min,停止微波加热,待溶液冷却至室温后,转移溶液至50 mL容量瓶中,加去离子水定容摇匀,用全谱直读等离子体发射光谱仪(ICP−OES)测定溶液中的重金属浓度,从而得出样品中重金属质量分数。采用5E−MAG6600型工业分析仪对原料进行工业分析。油菜秆的重金属质量分数和工业分析结果如表1所示。

表1 油菜秆的重金属质量分数和工业分析
2 结果与分析
2.1 含重金属的油菜秆热解特性
图1所示为油菜秆在不同升温速率(5,20和35 ℃/min)下热解的TG曲线DTG曲线。从图1可以看出油菜秆的热解过程可分为3个阶段。以油菜秆在20℃/min下的热重曲线为分析对象,第1阶段为水分析出阶段(室温~157.8 ℃),该阶该TG曲线出现小幅度下滑,DTG曲线出现1个较小的质量损失峰,此阶段的质量损失率为7.7%,与油菜秆中水分质量分数9.04%较吻合。第2阶段为快速质量损失阶段(157.8~ 355.8 ℃),油菜秆中的纤维素和半纤维素在该阶段快速分解殆尽,产生大量挥发性物质被析出,导致图中的TG曲线急剧下降,DTG出现明显的质量损失 峰。该阶段的质量损失率为58.5%,质量损失峰所对应的温度为328.7 ℃,最大质量损失率为20%/min。第3阶段为缓慢炭化阶段(355.8~700 ℃),木质素在该阶段缓慢分解产生少量挥发性物质,并最终生成生物炭(主要为灰分和固定碳)。该阶段的TG和DTG都相对平缓,质量损失率仅为17%;当温度升至终温时,仍有20%左右的质量残余,这与油菜秆中灰分质量分数(4.71%)和固定碳质量分数(17.30%)之和相吻合。
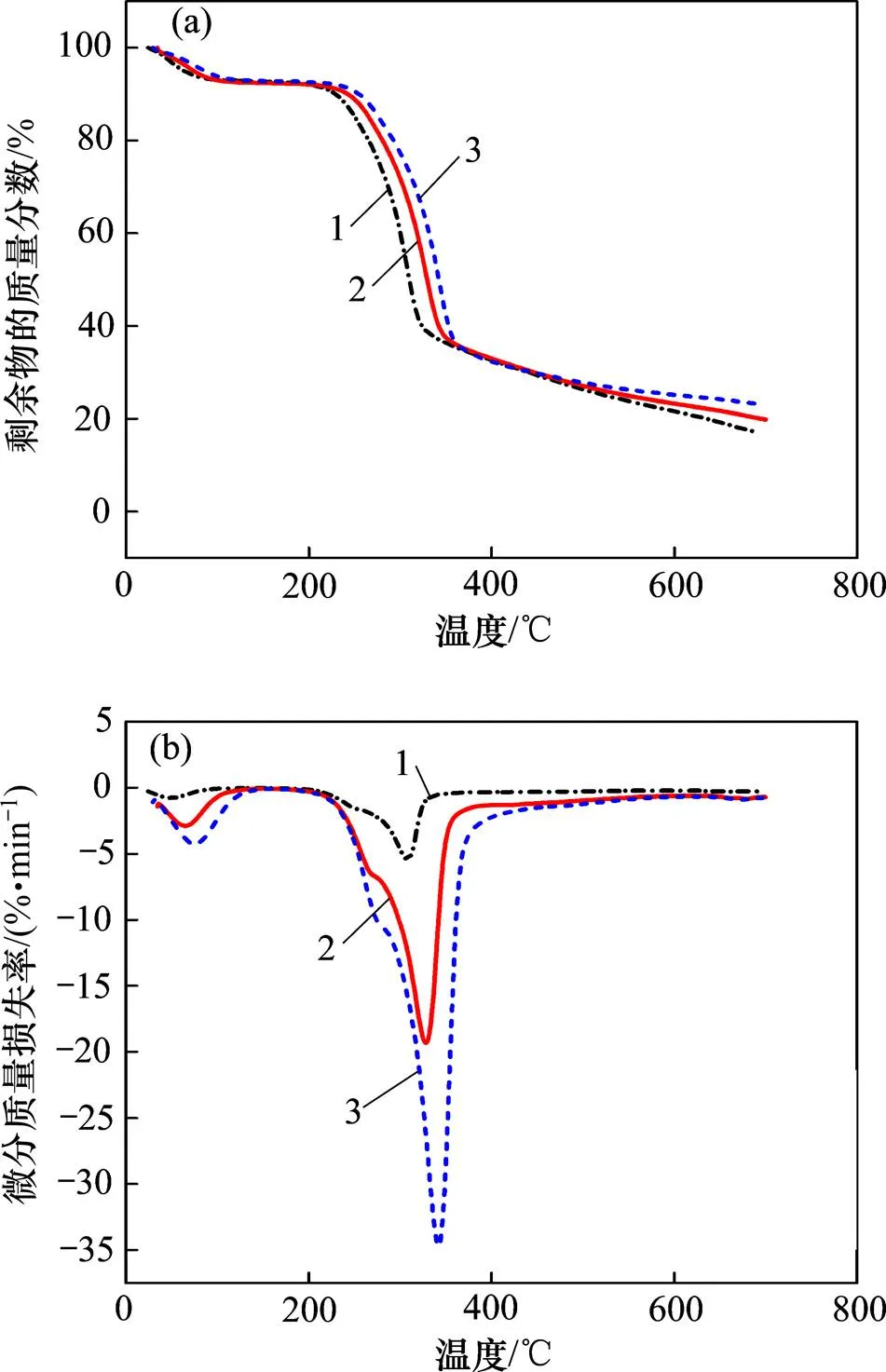
(a) TG曲线;(b) DTG曲线
从图1(a)可知:升温速率越大,油菜秆热解过程质量损失越少。这是因为升温速率增大致使热解过程所停留的时间越短,不利于油菜秆的热解,导致固体残余量增加。因此,在油菜秆热解过程中,选取较大的升温速率有利于提高生物炭产率。从图1(b)可知:随着升温速率增大,油菜秆的质量损失率增大,DTG曲线整体向高温区移动。这是因为升温速率增大导致油菜秆颗粒表面和中心的温差增大,从而引起如下2个方面的变化[17]:一方面,油菜秆表面和中心的温差增大促进二者之间传热,使油菜秆试样温度快速升高,从而质量损失率增大;另一方面,在温差增大的同时,油菜秆颗粒热解过程加快,迅速产生大量挥发分,而这些挥发分未能及时析出导致传质阻力增大,阻碍热解过程中传质,颗粒热解产物需要在更高的温度下才被析出,出现热滞后现象,导致DTG曲线向高温区移动。
2.2 热解温度和热解时间对生物炭产率的影响
结合油菜秆的热解特性可知,在大的升温速率下有利于生物炭的生成。升温速率对生物炭的特性(如pH、元素组分、工业组分、比表面积等)也存在一定影响。在通常情况下,随着升温速率增大,生物炭的pH增大[18];C质量分数增加,H和O质量分数降低,比表面积降低[19];挥发分质量分数降低,固定碳质量分数增加,灰分质量分数增加[20]。由于本次研究目的主要侧重于重金属保留率及生物炭产率,故不考虑升温速率对生物炭品质的影响。因此,为提高生物炭产率,选择管式炉允许的最大升温速率(15 ℃/min)作为热解炭化实验的升温速率。
图2所示为热解温度和热解时间对生物碳产率的影响。从图2(a)可知:当热解温度由350℃升至400 ℃时,生物炭产率下降较快(下降3%左右),而在400~ 650 ℃时,生物炭产率下降速率变小。这是因为350~400 ℃温度段主要处于油菜秆质量损失的第2阶段,该阶段质量损失率较大,因此,生物炭产率在该温度区间下降较快,而400~650℃温度段处在油菜秆质量损失的第3阶段,该阶段质量损失速率较小,所以,生物炭产率在该温度区间下降缓慢。从图2(b) 可以看出:生物炭产率随热解时间的延长缓慢下降(下降量小于2%)。出现该现象的原因是650 ℃处在油菜秆质量损失的第3阶段,因此,在该热解温度下,热解时间对生物炭产率影响不大。

(a) 生物炭产率与热解温度的关系(30 min);(b) 生物炭产率与热解时间的关系(650 ℃)
2.3 重金属迁移规律
为分析重金属在生物炭中的残留情况,引入重金属总保留率和各重金属保留率这2个参数。
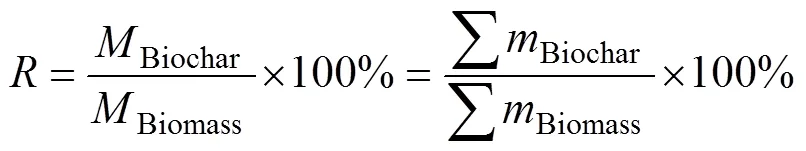
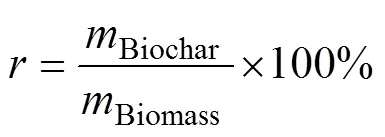
式中:为重金属总保留率,%;Biochar为生物炭中所有重金属总质量,mg;Biomass为油菜秆油料中所有重金属的总质量,mg;为各重金属保留率,%;Biochar为生物炭中各重金属质量,mg;Biomass为油菜秆原料中各重金属质量,mg。
将热解温度为350,400,500,600和650 ℃制备的生物炭分别记为T350,T400,T500,T600和T650,热解时间为10,30,50,70和90 min制备的生物炭分别记为t10,t30,t50,t70和t90,生物炭中的各重金属质量分数及重金属总保留率如表2所示。从表2可以看出:油菜秆中主要含Cd,Zn, Mn,Cu,Cr和Ni等重金属,其中Zn和Mn质量分数最大,分别达到24.4 mg/kg和24.3 mg/kg,远大于其他4种重金属的质量分数;Cd质量分数随热解温度升高而降低,Mn,Cu和Cr质量分数的变化趋势则与之相反,而Zn和Ni质量分数随热解温度升高呈先升高后降低趋势;Cd,Zn,Mn和Ni质量分数随热解时间延长而降低,而Cu和Cr质量分数随热解时间延长反而呈升高趋势。出现上述变化规律的原因是:生物炭中各重金属质量分数不仅与油菜秆热解过程中重金属的挥发有关,而且与油菜秆的质量损失有关[21]。除Cd外,其他5种重金属在生物炭中均出现明显的富集现象,夏娟娟等[22]也得到相似的结论,这表明经热解后的油菜秆有利于重金属的回收。

表2 生物炭中的重金属质量分数及重金属总保留率
从表2还可看出:重金属总保留率随着热解温度升高先缓慢升高,并在500 ℃达到最大值86.34%,超过500℃之后快速降低,在650 ℃时降至70.79%;重金属总保留率随着热解时间延长不断降低,在30~ 50 min骤降14.02%,在其他时间段的变化量均较小。重金属总保留率呈上述变化趋势的原因是物料中的Zn和Mn质量分数远大于另外4种重金属的质量分数,所以,Zn和Mn的保留率变化趋势在很大程度上决定了重金属总保留率变化趋势,且Zn和Mn的保留率均随热解温度升高表现为先升高后降低,随热解时间延长而降低。因此,选择合适的热解条件可以将原料中大部分重金属固定在生物炭中。当热解温度为500 ℃、热解时间为10 min时,可将至少86.34%的重金属保留在生物炭中。
不同热解条件下各重金属的保留率如图3所示。从图3(a)可知:各重金属在不同热解温度下的迁移特性差异明显,其中Cd和Ni的保留率随热解温度升高而降低,Cu和Cr的变化趋势则与之相反,而Zn和Mn的保留率随热解温度升高先升高后降低。出现此现象的原因是重金属的保留率与热解温度密切相 关[23]。热解温度升高,一方面可以促重金属化合物分解为小分子而挥发,也可以增大颗粒间的孔隙从而降低重金属扩散的阻力,促进重金属的挥发[24];另一方面,可能促进重金属与矿物质之间的相互作用,形成更稳定的金属化合物,抑制重金属的挥发[25]。从图3(b)可以看出:各种金属保留率随热解时间变化趋势明显;当热解温度为650 ℃时,Cd几乎完全挥发,Zn,Mn和Ni的保留率随热解时间延长呈降低趋势,而Cu和Cr的变化趋势则与之相反。这可能是因为随着热解时间的延长,Cd,Zn,Mn和Ni的重金属化合物不断分解而挥发,导致其保留率降低,而Cu和Cr则生成更稳定的金属化合物,抑制其挥发。重金属及其化合物的熔沸点也在很大程度上影响重金属的保留率[26],由于Cd及其化合物的熔点和沸点较低,Cd在热解温度为650 ℃时几乎完全挥发;而Mn,Cr,Ni及其化合物的熔点和沸点较高,Mn的保留率在各热解温度下均维持在80%左右,Cr和Ni的保留率在热解温度高于600 ℃时仍超过80%;Zn和Cu及其化合物的熔点和沸点适中,Zn的保留率在600 ℃之前均保持在80%以上,而在650 ℃时骤降至60.41%,Cu的保留率在650 ℃之前均在56%左右,在650 ℃时小幅上升至68.18%。
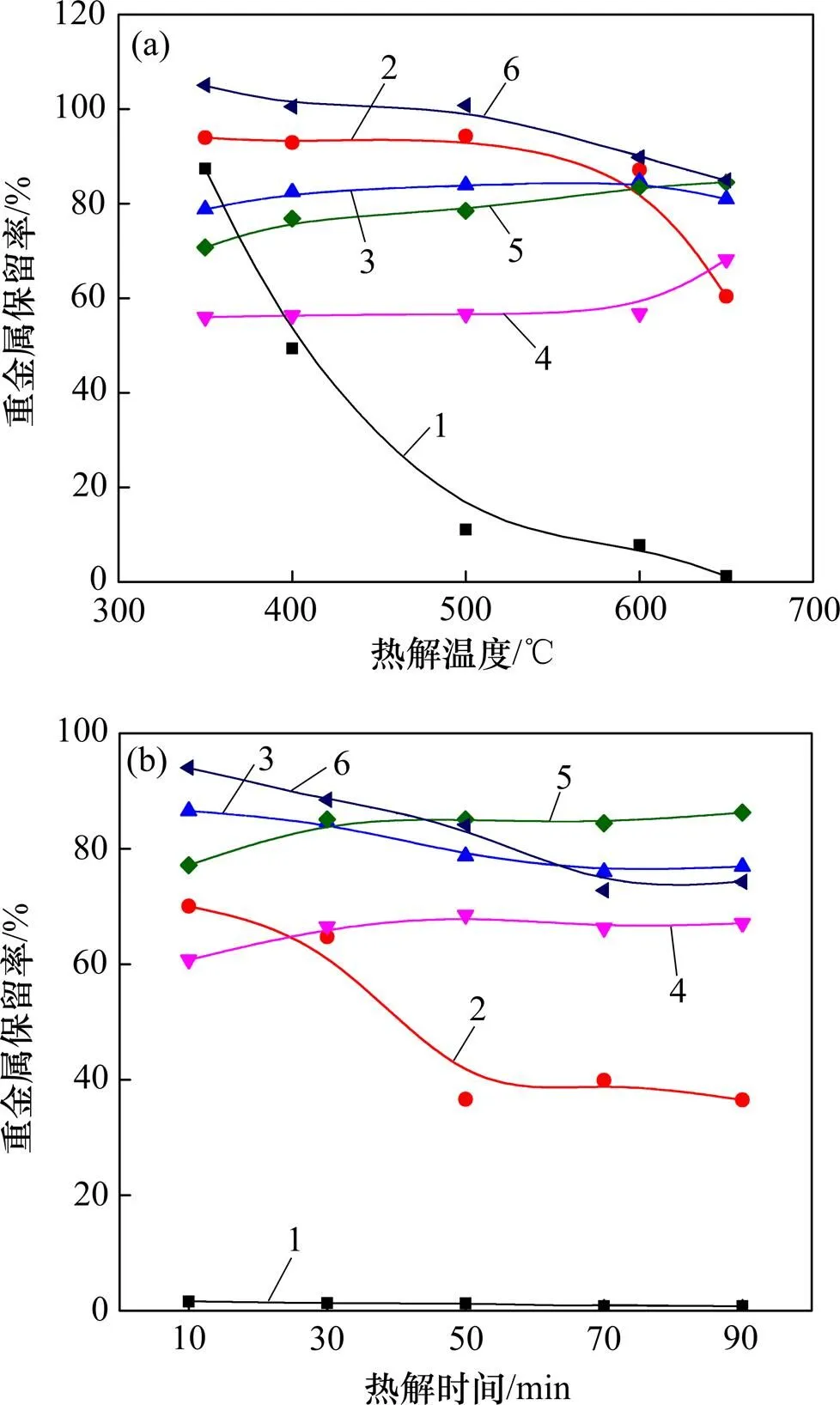
(a)不同热解温度下重金属的保留率;(b) 不同热解时间下重金属的保留率
综合上述分析结果可知油菜秆中存在的6种重金属的挥发性存在较大差异。根据不同热解条件下各重金属的挥发情况,可认为Cd为易挥发元素,Zn和Cu为中等挥发性元素,Mn,Cr和Ni为难挥发性元素。
3 结论
1) 油菜秆的质量损失过程可分为水分析出、快速质量损失和缓慢炭化3个阶段,这3个阶段的质量损失率分别为7.7%,58.5%和17.0%。升温速率增大导致热解过程向高温区移动,质量损失速率增大,固体残余量增加。
2) 生物炭产率随热解温度升高和热解时间延长呈下降趋势,油菜秆中各重金属在热解后明显富集于生物炭中(Cd除外)。重金属总保留率随热解温度升高呈先升高后下降趋势,随热解时间延长呈下降趋势,当热解温度为500 ℃、热解时间为10 min时,重金属的保留率最大,超过86.34%。
3) Cd和Ni的保留率随热解温度升高而下降,Cu和Cr的变化趋势则与之相反,而Zn和Mn的保留率随热解温度升高表现为先升高后降低规律;Zn,Mn和Ni的保留率随热解时间延长而降低,Cu和Cr则相反。根据各重金属在不同热解条件下的挥发特性,可认为Cd为易挥发元素,Zn和Cu为中等挥发性元素,Mn,Cr和Ni为难挥发性元素。
[1] 环境保护部. 环境保护部和国土资源部发布全国土壤污染状况调查公报[EB/OL]. [2014−04−17]. http://www.zhb.gov.cn/ gkml/hbb/qt/201404/t20140417_270670.htm.Ministry of Environmental Protection. The national survey on soil pollution issued by Ministry of Environmental Protection and Ministry of Land and Resources issued[EB/OL]. [2014−04−17]. http://www.zhb.gov.cn/gkml/hbb/qt/201404/t20140417_270670.htm.
[2] 樊霆, 叶文玲, 陈海燕, 等. 农田土壤重金属污染状况及修复技术研究[J]. 生态环境学报, 2013, 22(10): 1727−1736. FAN Ting, YE Wenling, CHEN Haiyan, et al. Study on the pollution status and remediation technology of heavy metals in farmland soils[J]. Journal of Ecology and Environment, 2013, 22(10): 1727−1736.
[3] LIU Weitao, ZHOU Qixing, ZHANG Zhineng, et al. Evaluation of cadmium phytoremediation potential in Chinese cabbage cultivars[J]. Journal of Agricultural and Food Chemistry, 2011, 59(15): 8324−8330.
[4] CHEN Tongbin, WEI Chaoyang, HUANG Zechun, et al. Arsenic hyperaccumulator Pteris Vittata L. and its arsenic accumulation[J]. Chinese Science Bulletin, 2002, 47(11): 902−905.
[5] YANG Xiaoe, LONG Xinxian, NI Wuzhong, et al. Sedum alfredii H: a new Zn hyperaccumulating plant first found in China[J]. Chinese Science Bulletin, 2002, 47(19): 1634−1637.
[6] YAN Xiulan, CHEN Tongbin, LIAO Xiaoyong, et al. Arsenic transformation and volatilization during incineration of thehyperaccumulator Pteris vittata L[J]. Environmental Science & Technology, 2008, 42(5): 1479.
[7] BARBAROUX R, PLASARI E, MERCIER G, et al. A new process for nickel ammonium disulfate production from ash of the hyperaccumulating plant Alyssum murale[J]. Science of the Total Environment, 2012, 423(8): 111−119.
[8] KOPPOLU L, AGBLEVOR F A, CLEMENTS L D. Pyrolysis as a technique for separating heavy metals from hyperaccumulators. Part Ⅱ: Lab-scale pyrolysis of synthetic hyperaccumulator biomass[J]. Biomass and Bioenergy, 2003, 25(6): 651−663.
[9] KOPPOLU L, PRASAD R, CLEMENTS L D. Pyrolysis as a technique for separating heavy metals from hyperaccumulators. Part III: pilot-scalepyrolysisof synthetic hyperaccumulator biomass[J]. Biomass and Bioenergy, 2004, 26(5): 463−472.
[10] YUAN Xingzhong, HUANG Huajun, ZENG Guangming, et al. Total concentrations and chemical speciation of heavy metals in liquefaction residues of sewage sludge[J]. Bioresource Technology, 2011, 102(5): 4104−4110.
[11] 孙阳, 刘亚男, 郭朝晖, 等. 植物修复收获物热解制备生物炭过程中重金属的稳定性研究[J]. 中南大学学报(自然科学版), 2016, 47(7): 2189−2195. SUN Yang, LIU Yanan, GUO Zhaohui, et al. Study on the stability of heavy metals during phytoremediation of biochar pyrolysis[J]. Journal of Central South University(Science and Technology), 2016, 47(7): 2189−2195.
[12] SAS-NOWOSIELSKA A, KUCHARSKI R, MALKOWSKI E, et al. Phytoextraction crop disposal: an unsolved problem[J]. Environmental Pollution, 2004, 128(3): 373−379.
[13] LIU Yanan, GUO Zhaohui, SUN Yang, et al. Stabilization of heavy metals in biochar pyrolyzed from phytoremediated giant reed (Arundo donax) biomass[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(3): 656−665.
[14] STALS M, CARLEER R, REGGERS G, et al. Flash pyrolysis of heavy metal contaminated hardwoods from phytoremediation: characterisation of biomass, pyrolysis oil and char/ash fraction[J]. Journal of Analytical & Applied Pyrolysis, 2010, 89(1): 22−29.
[15] 夏娟娟, 赵增立, 李海滨, 等. 修复植物热解半焦中重金属形态分布研究[J]. 环境污染与防治, 2011, 33(1): 57−60. XIA Juanjuan, ZHAO Zengli, LI Haibin, et al. Study on speciation and distribution of heavy metals in the pyrolytic char of phytoremediation[J]. Environmental Pollution and Control, 2011, 33(1): 57−60.
[16] 杨刚, 袁大刚, 钟贵江, 等. 微波消解-ICP-AES法测定钒钛矿区优势植物中重金属质量分数[J]. 光谱学与光谱分析, 2012, 32(5): 1391−1393. YANG Gang, YUAN Dagang, ZHONG Guijiang, et al. Determination of heavy metals in the dominant plants of vanadium and titanium mines by microwave digestion[J]. Spectroscopy and Spectral Analysis, 2012, 32(5): 1391−1393.
[17] MAITI S, PURAKAYASTHA S, GHOSH B. Thermal characterization of mustard straw and stalk in nitrogen at different heatingrates[J]. Fuel, 2007, 86(10/11): 1513−1518.
[18] 王章鸿, 郭海艳, 沈飞, 等. 热解条件对生物炭性质和氮、磷吸附性能的影响[J]. 环境科学学报, 2015, 35(9): 2805−2812. WANG Zhanghong, GUO Haiyan, SHEN Fei, et al. The effect of pyrolysis conditions on biological properties of carbon and nitrogen and phosphorus adsorption[J]. Journal of Environmental Sciences, 2015, 35(9): 2805−2812.
[19] AHMAD M, MOON D H, VITHANAGE M, et al. Production and use of biochar from buffalo-weed(Ambrosia trifida, L. ) for trichloroethylene removal from water[J]. Journal of Chemical Technology & Biotechnology, 2013, 89(1): 150−157.
[20] CAO Xinde, HARRIS W. Properties of dairy-manure-derived biochar pertinent to its potential use in remediation[J]. Bioresource Technology, 2010, 101(14): 5222−5228.
[21] 吴贤豪, 李建新, 王永川, 等. 超积累植物热解中重金属迁移及渗滤特性研究[J]. 环境科学学报, 2017, 37(7): 2707−2712. WU Xianhao, LI Jianxin, WANG Yongchuan, et al. Study on migration and percolation characteristics of heavy metals in hyperaccumulator[J]. Chinese Journal of Environmental Science, 2017, 37(7): 2707−2712.
[22] 夏娟娟, 钟慧琼, 赵增立, 等. 修复植物热解过程中重金属元素迁移行为研究[J]. 生态环境学报, 2010, 19(7): 1696−1699. XIA Juanjuan, ZHONG Huiqiong, ZHAO Zengli, et al. Study on migration behavior of heavy metals during phytoremediation pyrolysis[J]. Journal of Ecological Environment, 2010, 19(7): 1696−1699.
[23] KELLER C, LUDWIG C, DAVOLI F, et al. Thermal treatment of metal-enriched biomass produced from heavy metal phytoextraction[J]. Environmental Science & Technology, 2005, 39(9): 3359−67.
[24] 薛辉, 仲兆平, 钟道旭, 等. 超积累植物与煤在混烧过程中重金属的迁移特性[J]. 环境工程学报, 2016, 10(5): 2581−2586. XUE Hui, ZHONG Zhaoping, ZHONG Daoxu, et al. Migration characteristics of heavy metals during the co-combustion of hyperaccumulator and coal[J]. Journal of Environmental Engineering, 2016, 10(5): 2581−2586.
[25] YU Jie, SUN Lushi, XIANG Jun, et al. Vaporization of heavy metals during thermal treatment of model solid waste in a fluidized bed incinerator[J]. Chemosphere, 2012, 86(11): 1122.
[26] YANG Jiangguang, TANG Chaobo, HE Jing, et al. Heavy metal removal and crude bio-oil upgrade from Sedum alfredii Hance harvest using hydrothermal upgrading[J]. Journal of Hazardous Materials, 2010, 179(1/2/3): 1037.
Migration behaviors of heavy metals during pyrolysis of rape stalk
CAI Pan, JIANG Shaojian, FU Guofu, PENG Haoyi, LIU Xi, ZHU Mingwei
(School of Energy and Engineering, Central South University, Changsha 410083, China)
Heavy metals contaminated rape stalks were taken as the research object, pyrolysis characteristics were studied by thermogravimetric analyzer and the effects of pyrolysis temperature and pyrolysis time on the migration of heavy metals such as Cd, Zn, Mn, Cu, Cr and Ni were investigated by tube furnace pyrolysis reactor. The results show that with the increase of the heating rate, TG and DTG curves of rape stalk shift to higher temperature section, the mass loss rate of rape stalk increases and the mass of residual solid increases. All heavy metals in rape stalks are obviously enriched in biochar after pyrolysis except Cd, the total retention rate of heavy metals increases first and then decreases with the increase of pyrolysis temperature, and decreases with the increase of pyrolysis time. The total retention rate of heavy metals is the highest when the pyrolysis temperature is 500 ℃ and pyrolysis time is 10 min. There is a great difference in the volatility of various heavy metals, and it can be considered that Cd is volatile element, Zn and Cu are medium volatile elements, Mn, Cr and Ni are less volatile elements.
soil remediation; rape stalk; heavy metal; pyrolysis characteristics; migration
10.11817/j.issn.1672-7207.2018.07.030
TK6
A
1672−7207(2018)07−1808−07
2017−10−12;
2017−12−22
国家自然科学基金资助项目(21577176) (Project(21577176) supported by the National Natural Science Foundation of China)
蒋绍坚,教授,硕士生导师,从事低碳能源技术(高效清洁燃烧、生物质能利用等)研究;E-mail: sjjiang@csu.edu.cn
(编辑 陈灿华)
