HS/GC-MS/MS法检测海产品中二甲苯
2018-08-02周秀锦杨会成邵宏宏相兴伟
周秀锦,杨会成,邵宏宏,张 静,相兴伟,韩 超,郑 斌
(1.舟山出入境检验检疫局,浙江 舟山 316000;2.浙江海洋开发研究院,浙江 舟山 316000;3.温州出入境检验检疫局,浙江 温州 325000)
二甲苯是有机化工的重要原料,广泛应用于涂料、橡胶、医药和农药等多个行业,美国政府工业卫生学家会议(ACGIH)[1]将其归类为A4级,属于低毒类化学物质。国内外因二甲苯引发的急、慢性中毒案件时有发生,主要与摄入含有二甲苯的物质以及生活、工作环境中接触二甲苯有关[2-4]。二甲苯的检测方法主要有气相色谱法(GC)[5-7]、气相色谱-质谱法(GC-MS)[8-10]、气相色谱-串联质谱法(GC-MS/MS)[11-12]等,但研究对象大多为大气、海水[13]、底泥沉积物[14]、尿液和血液[15-18]等基质。前处理方法有固液萃取、顶空进样、固相微萃取和吹扫捕集等,其中固液萃取操作繁琐、样品前处理时间较长、易造成二甲苯损失且重现性差;固相微萃取因样品用量小、方便灵活而成为目前的研究热点,但设备和耗材相对昂贵限制了其普及性;吹扫捕集虽可解决二甲苯损失的问题,但与之相比,动态顶空进样更为简单、快速,且在分析过程中不易引入溶剂、基质干扰小,常作为挥发物的前处理方式。目前尚未见GC-MS/MS法测定海产品中二甲苯的研究报道,本文采用直接动态顶空技术与GC-MS/MS相结合的方法,建立了一种海产品中二甲苯3种同分异构体的HS/GC-MS/MS检测方法,并应用于东海区域海产品中二甲苯的分析检测。
1 实验部分
1.1 仪器与试剂
GCMS-TQ8040气相色谱-质谱联用仪、AOC-5000 plus顶空进样器(日本岛津公司);20 mL顶空进样瓶;Milli-Q超纯水仪(美国Millipore公司);XS105电子天平(瑞士Metler-Toledo公司);GM300研磨仪(德国Retsch公司);OGS100烘箱(美国热电公司)。
邻二甲苯(o-Xylene,OX;批号261947;纯度99.5%)、对二甲苯(p-Xylene,PX,批号253439;纯度99.9%)、间二甲苯(m-Xylene,MX;批号261948;纯度99.8%)标准溶液均购自美国o2si公司。NaCl为优级纯,500 ℃灼烧2 h,置于干燥器内备用;实验用水为超纯水。
1.2 标准溶液与试样制备
用水配制3种二甲苯的混合标准储备液,质量浓度均为10.0 mg/L,置于4 ℃冰箱避光保存。
取代表性海产品样品约500 g,用GM300研磨仪充分捣碎均匀,装入洁净容器中,密封,于-18 ℃以下冷冻存放。
1.3 样品前处理
取洁净的20 mL顶空进样瓶于烘箱内,130 ℃烘烤30 min,冷却后加入2.0 g NaCl备用。准确称取样品2.0 g于装有NaCl的顶空进样瓶中,加入8.0 mL水,迅速密封,旋涡30 s充分混匀,超声5 min后,待测。
1.4 气相色谱-三重四极杆串联质谱条件
1.4.1顶空条件顶空进样系统采用高速振荡模式,顶空瓶平衡温度:90 ℃;平衡时间:40 min;进样方式:顶空进样;进样量:1 mL。
1.4.2气相色谱条件色谱柱:HP-INNOWax(60 m×0.25 mm×0.25 μm);柱温程序:初始温度40 ℃,保持2 min;以5 ℃/min升至100 ℃,保持2 min;再以40 ℃/min升至200 ℃,保持2 min;进样口温度:220 ℃,进样方式:分流进样(分流比10∶1);载气:氦气;载气控制方式:线速度36.1 cm/s。
1.4.3质谱条件离子化方式:EI;离子源温度:230 ℃;色谱-质谱接口温度:280 ℃;检测器电压:调谐电压+0.1 kV;电子能量70 eV;扫描开始时间5.01 min,结束时间19.80 min;扫描模式:多反应监测(MRM);扫描间隔0.3 s;溶剂延迟时间为7 min。优化后的保留时间和质谱参数见表1。

表1 3种二甲苯同分异构体的保留时间和质谱参数Table 1 Retention time and MS parameters of three xylene isomers
*quantitative ion pair
1.5 基质加标标准工作曲线
取与待测样品基质相同的空白样品2.0 g,加入适量的二甲苯混合标准工作液,得到质量浓度分别为5.0、10.0、20.0、50.0、100.0 μg/kg基质标准溶液,按“1.3”和“1.4”方法检测后,绘制标准工作曲线。
2 结果与讨论
2.1 样品前处理的优化
NaCl会降低苯系物在水中的溶解度,提高样品中苯系物的离子强度,增强其检测信号[19-20]。本实验针对基质相对复杂的黄鱼样品,分别加入0、1.0、1.5、2.0、2.5、3.0 g的NaCl,其他步骤按照“1.3”和“1.4”进行分析,结果发现分析灵敏度随着NaCl添加量的增加而提高。当NaCl添加量为2.0 g时,PX、MX和OX的灵敏度最大,响应值分别比未加NaCl时提高了17.9%、16.8%和18.5%;当NaCl添加量高于2.0 g时,二甲苯响应值变化不明显。同时对超声时间进行了优化,将2.0 g黄鱼样品分别超声0、3、5、7、10 min,其他步骤按照“1.3”和“1.4”进行分析,结果发现分析灵敏度随着超声时间的延长而提高。当超声时间为5 min时,PX、MX和OX的灵敏度最大,响应值分别比未超声时提高了5.0%、6.3%和5.7%;当超声时间大于5 min时,响应值变化不明显。故本实验选择NaCl的添加量为2.0 g,超声时间5.0 min。
2.2 顶空进样平衡温度与平衡时间的选择
采用空白黄鱼样品,添加3种二甲苯混合标液,使其最终含量均为20.0 μg/kg,对顶空进样平衡温度进行优化。平衡时间设为40 min,考察了平衡温度(60、70、80、90、95 ℃)的影响,按实验条件进样测定,记录峰面积。结果显示,在60~90 ℃范围内,随着平衡温度的升高,3种二甲苯同分异构体的峰面积明显增加,而平衡温度为95 ℃时,峰面积则无明显增加。另外,由于提取溶剂水的沸点为100 ℃,若平衡温度过高,顶空瓶承受的压力更大,存在安全隐患。因此,实验选择顶空进样平衡温度为90 ℃。
以水为提取溶剂,对顶空进样平衡时间进行优化。将平衡温度设为90 ℃,考察了平衡时间分别为35、40、45 min的效果,按实验条件进样测定,记录峰面积。结果显示,在35~40 min范围内,随着平衡时间的延长,3种二甲苯同分异构体的峰面积显著增加,而平衡时间增至40~45 min时,峰面积无明显增加。推测平衡时间为40 min时,顶空进样瓶中待测物气-液两相已达平衡。若平衡时间过长,可能会引起顶空进样瓶的气密性变差,导致检测结果的误差增大。因此,选择顶空进样平衡时间为40 min。
2.3 升温方式的选择
由于待测物邻二甲苯、间二甲苯和对二甲苯为同分异构体,沸点均在138.4~144.4 ℃之间,且极性较接近,主要碎片离子相同,因此气相色谱选择程序升温以更好地对其进行分离。初始温度设为60 ℃,保持6 min,然后以10 ℃/min升温至150 ℃,使沸点低、极性较小的成分先流出,最后以30 ℃/min升温至260 ℃,实现了3种二甲苯同分异构体的充分分离,同时避免了鱼类和贝类样品复杂基质的干扰。
2.4 色谱柱的选择
参考SN/T 2251-2009标准[21]中推荐的两种色谱柱HP-50+和DB-5MS,本实验比较了HP-50+、DB-5MS、Rxi-5Sil MS和HP-INNOWax 4种色谱柱的分离效果。结果表明,间二甲苯和对二甲苯在HP-50+和DB-5MS色谱柱上不能分离;Rxi-5Sil MS柱虽耐水性较好,但对间二甲苯和对二甲苯的分离效果也不理想,且当两者浓度较高时,色谱峰部分重叠;而HP-INNOWax色谱柱的极性较强,在低温状态下,可完全实现间二甲苯和对二甲苯的分离,且分离度大于1.5,无基质干扰。因此,实验选用HP-INNOWax为本方法的色谱柱。

图1 3种二甲苯同分异构体在多反应监测模式下的总离子流图Fig.1 Total ion chromatogram of 3 xylene isomers under multiple reaction monitoring mode
2.5 质谱条件的优化
在选定的色谱条件下,首先用Q3 SCAN全扫描方式得到邻二甲苯、间二甲苯和对二甲苯的总离子流色谱图,选择m/z和相对丰度较高的一级碎片为目标化合物的母离子,同时确定其保留时间。再根据已确定的母离子,进行不同碰撞能量(CE)的Product ion模式测定,进一步优化碰撞能量和离子对,以保证检测的灵敏度和准确性。在表1的质谱优化条件下,3种二甲苯同分异构体的MRM总离子流色谱图见图1,三者得到了较好分离。
2.6 线性范围、精密度与检出限
在优化条件下,采用黄鱼样品基质加标绘制标准工作曲线,以峰面积对相应质量浓度做回归分析,3种二甲苯同分异构体(MX,PX,OX)均在5.0~100.0 μg/kg范围内呈良好的线性关系,其相关系数(r2)分别为0.991、0.994、0.995;以3倍信噪比为基准,得到3种化合物的方法检出限(LOD)均为2.5 μg/kg,以10倍信噪比为基准,得到方法定量下限(LOQ)均为5.0 μg/kg。
为验证方法的准确度,对典型海产品如黄鱼、南美白对虾、贻贝和蟹样品进行了6.0、15.0、50.0 μg/kg 3个不同水平的二甲苯同分异构体加标回收实验,按“1.3”和“1.4”条件处理,每一水平平行测定7次,计算得平均回收率为89.6%~112.4%,相对标准偏差(RSD)不大于11.5%(见表2)。

表2 二甲苯同分异构体的平均回收率及相对标准偏差Table 2 Average recoveries and relative standard deviations of xylene isomers
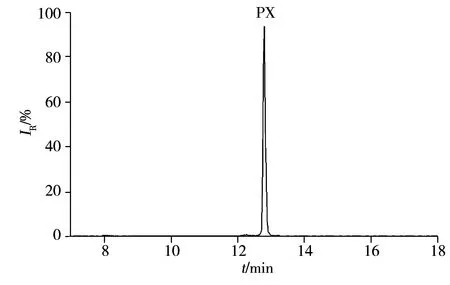
图2 花蛤阳性样品的总离子流谱图Fig.2 Total ion chromatogram of a positive clam sample
2.7 实际样品的测定
在优化条件下,采用本方法检测了舟山地区南美白对虾、黄鱼、贝壳类、蟹等各类海产品共32个样品。结果显示,4批海产品中检出对二甲苯,检出量分别为7.85、12.40、8.21、7.89 μg/kg;邻二甲苯和间二甲苯均未检出。由此可见,对二甲苯对部分海产品造成了一定污染,其主要污染源可能来自附近炼油厂的重整工艺。图2为花蛤阳性样品的总离子流色谱图。
3 结 论
本文建立了海产品中3种二甲苯同分异构体的顶空/气相色谱-串联质谱测定方法,方法的线性范围、灵敏度、检出限和回收率等技术指标均满足要求。3种二甲苯同分异构体的加标回收率为89.6%~112.4%,RSD不大于11.5%。应用本方法对浙江舟山地区的海产品进行了分析,发现4批海产品中检出对二甲苯,表明部分海产品已受到一定程度的污染,应引起广泛的关注。本方法的检测结果表明有必要定期对海产品中二甲苯引起的潜在风险进行评估。相关研究初步为海产品中二甲苯的监测和预警提供了依据。
