依达拉奉治疗2型糖尿病合并脑梗死临床研究*
2018-07-23吕巧云赵慧芳温子海李晓华
张 莹,吕巧云,赵慧芳,温子海,李晓华
(河北省唐山市丰南区医院内科,河北 唐山 063300)
2 型糖尿病(type 2 diabetes mellitus,T2DM)患者诱发心脑血管疾病的可能性为非糖尿病患者的2~4倍,而脑血管病是T2DM患者致残或致死的根本原因[1]。糖尿病患者通常合并胰岛素分泌受阻,血液黏稠度较高,再加上中老年患者的占比偏高,极易诱发脑梗死。目前,T2DM慢性并发症发病机制较复杂,尚未明确。有研究证实,其发病机制和可溶性细胞间黏附分子-1(soluble intercellular adhesion molecule-1,sICAM -1)、S100B 蛋白及白细胞介素6(IL-6)等指标相关[2]。本研究中观察了T2DM合并脑梗死患者给予依达拉奉治疗前后患者血清、血液流变学指标的变化。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:经颅脑 CT确诊;符合世界卫生组织(WHO)糖尿病诊断(1999年)[3]和第4届全国脑血管病学术会议公布的诊断标准;本研究经医院医学伦理委员会批准,患者知情同意并签署知情同意书。
排除标准:感染、缔结组织疾病或肿瘤;心脏、肝脏及肾功能不全;T2DM疾病发作。
病例选择与分组:选择我院内分泌科2016年1月至2017年9月收治的T2DM合并脑梗死患者70例,其中男 33例,女 37例;年龄(61±8)岁;病程 2~20年,中位病程7.5年。将70例患者随机分为对照组与观察组,各35例。两组患者一般资料比较,差异无统计学意义(P > 0.05),具有可比性。详见表 1。
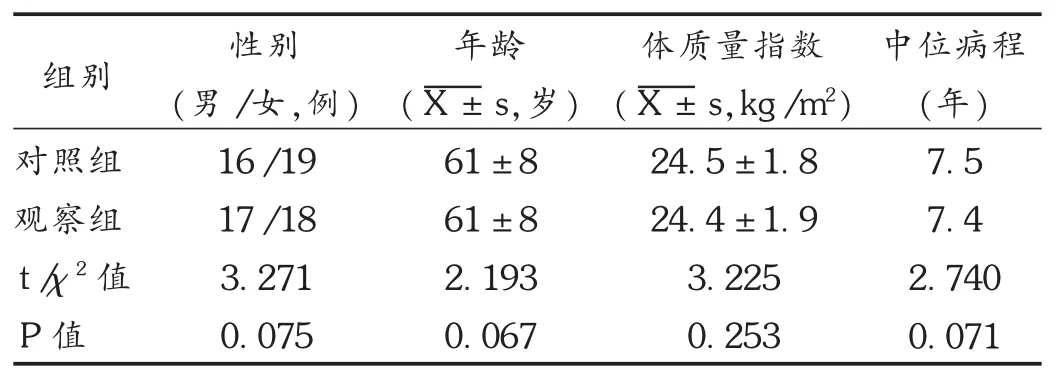
表1 两组患者一般资料比较(n=35)
1.2 方法
对照组患者予降血糖、恢复循环等常规治疗,如口服降糖药、饮食干预等。治疗组患者在对照组治疗基础上,加用依达拉奉注射液(国药集团国瑞药业有限公司,国药准字H20080056,规格为每支20 mL∶30 mg)30 mg加入0.9%氯化钠注射液250 mL中,静脉滴注,每日1次。两组疗程均为2周。
1.3 观察指标与疗效判定标准
日常生活活动能力与神经功能:根据Bathel指数[4]、美国国立卫生研究院卒中量表(NIHSS)[5]分别对治疗后进行评价。Bathel指数共10项,总分100分,分值越高,说明患者的日常活动能力相对越好。NIHSS用于评估患者的神经功能缺损状况,共纳入12项,分值越小,提示病情越轻。
血清学、血液流变学指标:采集患者空腹静脉血并加入采血管,室温下凝固后,以3 000 r/min转速离心处理10 min,抽取上清液放入-80℃冰箱储存,使用双抗体夹心法测定sICAM-1和IL-6水平及 S100B蛋白浓度。
按照《中药新药临床研究指导原则》相关标准[6]进行疗效判定。显效:临床症状、体征大体消失,NIHSS评分下降程度≥75%;有效:临床症状或体征有所改善,NIHSS评分下降程度为30%~74%;无效:临床症状相较于治疗前未变化或加重,NIHSS评分下降程度≤30%。总有效=显效+有效。
1.4 统计学处理
2 结果
结果见表2至表5。观察组有2例患者出现低血糖,3例伴有轻微恶心,1例天门冬酸氨基转移酶轻度上升,治疗后均已消失。其他患者未见不良反应。两组患者不良反应发生率比较,差异有统计学意义(P<0.05)。

表2 两组患者临床疗效比较[例(%),n=35]
表3 两组患者血清学指标比较(s,n=35)

表3 两组患者血清学指标比较(s,n=35)
注:与本组治疗前比较,*P<0.05;与对照组治疗后比较,△P < 0.05。下表同。
指标sICAM-1(ng/mL)IL -6(ng/L)S100B 蛋白(μ g/L)时间治疗前治疗后治疗前治疗后治疗前治疗后对照组334±31 307±32*15.3 ± 1.7 12.8 ± 1.9*2.17 ± 0.42 1.81 ± 0.37*观察组331±28 300±27*△15.1 ± 1.5 11.7 ± 1.4*△2.15 ± 0.43 0.97 ± 0.18*△
表4 两组患者血液流变学指标比较(s,n=35)

表4 两组患者血液流变学指标比较(s,n=35)
组别 时间对照组观察组治疗前治疗后治疗前治疗后全血高切黏度(mPa·s)5.58 ± 1.03 4.40 ± 1.02*5.74 ± 1.12 3.28 ± 0.93*△全血低切黏度(mPa·s)13.35 ± 2.26 9.76 ± 1.72*13.76 ± 2.42 7.27 ±1.84*△血小板黏附率(%)68.46 ±7.82 58.92 ± 6.31*69.72 ±7.48 50.16 ± 5.68*△红细胞比容(%)49.10 ±2.52 43.13 ± 2.00*49.77 ±2.78 37.48 ± 2.13*△
表5 两组患者血糖、NIHSS评分及Bathel指数比较(s,n=35)

表5 两组患者血糖、NIHSS评分及Bathel指数比较(s,n=35)
组别对照组观察组时间治疗前治疗后治疗前治疗后血糖(mmol/L)15.40 ± 2.34 9.57 ± 1.55*15.68 ± 2.48 7.27 ± 1.31*△NIHSS评分(分)35.15 ± 5.34 28.27 ± 4.16*34.77 ± 4.28 20.28 ± 3.16*△Bathel指数38.43 ± 6.30 57.61 ± 5.06*39.02 ± 7.24 62.50 ± 5.30*△
3 讨论
3.1 T2DM与血清指标
sICAM-1在机体中有较多的分布,在血管内皮细胞中的表达偏高。作为T2DM典型的大血管并发症,脑梗死同样与sICAM-1紧密相关。sICAM-1可以介入脑梗死后机体的炎性反应,糖尿病状态下有突出的炎性反应[7]。T2DM同时伴有脑梗死患者的血清sICAM-1水平相较于T2DM患者明显更高[8]。有研究证明,脑梗死缺血情况下的脑组织,损伤前血清S100B浓度显著上升,对神经系统造成损伤;CT证实有病变者该指标均会上调,提示有脑外伤或脑损伤[9-11]。同时,炎性因子可以促进脑内毛细血管内皮细胞sICAM-1的过表达,通过释放缩血管类物质,加速血管收缩,减小血流量,使脑梗死恶化。本研究结果显示,依达拉奉注射液可以降低sICAM-1和IL-6水平。可能的作用机制为对损伤部位自由基进行清除,减少血管内皮受损和抑制炎性反应。可见,该药对T2DM改善作用,能使患者成功获益。
3.2 T2DM 与血糖
T2DM患者极易合并脑血管意外,推测与高胰岛素血症、高血糖症等有很大关联[12]。高血糖症作为关键的影响因子,减少一氧化氮(NO)的释放,加速形成超氧离子,抑制机体的血管舒张功能。同时,高血糖时还将加剧患者的脑血管病变,尤其脑缺氧或是缺血情况下糖元无氧酵解快速,酸性代谢产物在细胞中堆积,出现外酸中毒,脑细胞代谢也将明显受损。本研究结果显示,依达拉奉给药后患者的血糖水平显著低于常规用药。另外,高血糖还将升高患者的糖化血红蛋白水平,增加血黏度。本研究证实,观察组患者全血高切黏度及全血低切黏度等各项指标,均低于治疗前和对照组,说明该药可改善患者的血液流变学指标,调节血糖,减少脑血管病事件。
3.3 依达拉奉在T2DM治疗中的应用
依达拉奉是自由基清除剂、抗氧化剂,核心成分为3-甲基-1-苯基-2-吡唑啉-5-酮,相对分子质量为174.20,具有亲脂性基团,通透率高达60%。作为典型的自由基捕获剂,可对黄嘌呤氧化酶及次黄嘌呤氧化酶自身的活性进行抑制,诱导分泌前列环素,抑制炎性介质白三烯,下调羟自由基的浓度,减小梗死体积,延缓迟发性神经元死亡,防止出现脂质过氧化反应,预防脑水肿和抑制内皮细胞损伤[13]。其还可调节血糖浓度及血液动力学参数,维持心肌直径及正常线粒体结构,对心肌提供较好的保护[14-15]。本研究结果提示,患者各项指标均有所下降,无明显不良反应,安全性高。
综上所述,依达拉奉治疗T2DM,可改善其血糖水平,降低NIHSS评分,提高日常生活能力,改善血液流变学指标,降低sICAM-1,IL-6水平和S100B蛋白浓度,疗效较好,值得推广。
