水解法制备β-FeOOH纳米粒子及其在废水处理方面的应用
2018-07-14陈丽洁
陈丽洁
(巴音郭楞职业技术学院,新疆 库尔勒 841000)
在我国制定可持续发展战略后,环境保护更加引起人们广泛的关注,工业生产过程产生的废弃物的无害化处理及回收利用显得更加重要。石油化工在国民经济中占有相当重要地位,在石油的炼制精制过程中,会产生大量的碱渣废水。进行专门针对这种废水处理的研究就显得日益重要。
炼油厂碱渣废水主要来自石油化工行业炼油厂催化裂化的汽油碱洗废碱液,液总烃碱洗废碱液和常减压装置的碱渣废水。其中含有大量的硫化物、硫醇、酚、噻酚、硫醚、醌、环烷酸等有毒有害污染物,pH值在10~14之间,碱渣废液通常呈黑褐色,并伴有恶臭气味。碱渣废液中的酚具有含挥发酚量高、有较强刺激性气味等特点。碱渣废液的强碱性使其储存和处理成为难题[1-2]。
炼油厂目前一般采用回萃取、中低温湿式氧化或用大量水稀释后再用常规技术处理等方法处理。但是由于该废水污染物浓度较高 、毒性大、可生化性差等特点,处理结果往往达不到相关的技术和经济要求。因此研究开发这类工业废水净化处理技术,是目前废水处理技术研究领域内的一个难点。
目前常用的方法主要有:中和法、膜分离法(超滤和反渗透)生化法、(厌氧、好氧)湿式氧化法。中和法包括硫酸中和法、CO2中和法、和硫化钠法。但是中和法采用的气体难以收集不易控制,操作困难,反应条件要求苛刻[3]。生化法主要受限于可降解的炼油碱渣废水的处理,一般需要大量的稀释因素(水)。并且该方法极其容易受到pH值,天气,温度等影响[3-4]。湿式氧化工艺在处理高浓度、难降解有机废水方面有其独特的优势。湿式氧化分为湿式空气氧化(WAO)[5]、湿式催化氧化(CWO)[6-7]。它具备WAO的优点,同时反应时间更短、转化效率更高,但H2O2、催化剂活性对反应影响较大[8]。
本文主要针对新疆独山子石化炼油厂在炼油过程中产生的碱渣废液进行了深入的研究。目前碱渣主要集中储放在独山子附近山上的废液池内。由于碱渣废水的高碱性和时间的积累,池底的防护层出现了泄露和渗透的危险。因此,对废碱液的集中处理就显得非常紧迫和重要。其主要成分有汽油碱渣、钝化液等多种废液,同时含有大量固体油泥。由于其成分复杂,因此主要采用预处理和湿式氧化法两步结合组成[9-10]。本工艺采用预处理结合湿法催化的方法,使用浓硫酸调节pH值至2~4将碱渣废水的COD初始值大约为50000~60000 mg/L降低到30000 mg/L左右, 后经湿式催化氧化后,废水水质COD值降低到1000mg/L左右,本方法有效处理了工业碱渣废液,对于国内外广泛存在的其他行业产生的高浓度有机废水的处理也具有普遍意义。
2 实验部分
2.1 实验设备
实验仪器设备见表1。
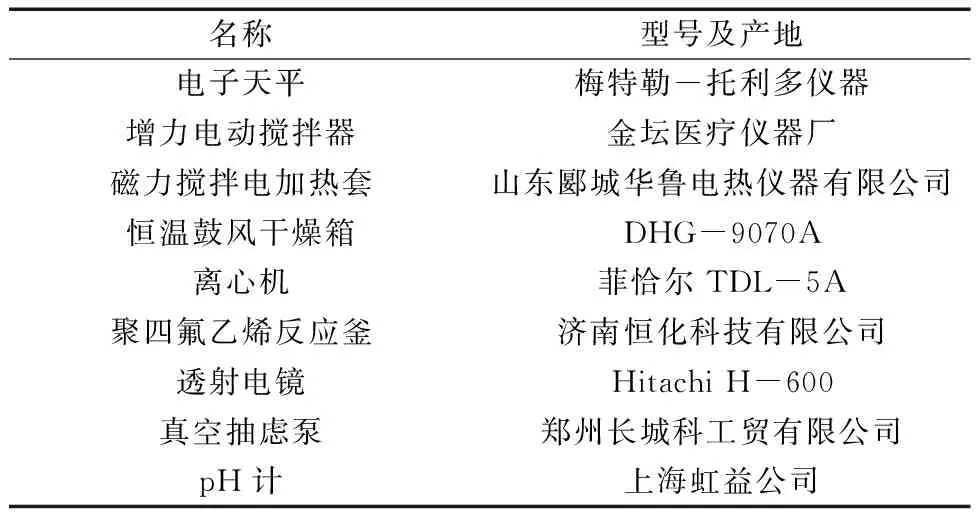
表1 实验仪器设备Table.1 Experiment equipment.
2.2 实验药品
实验药品见表2。
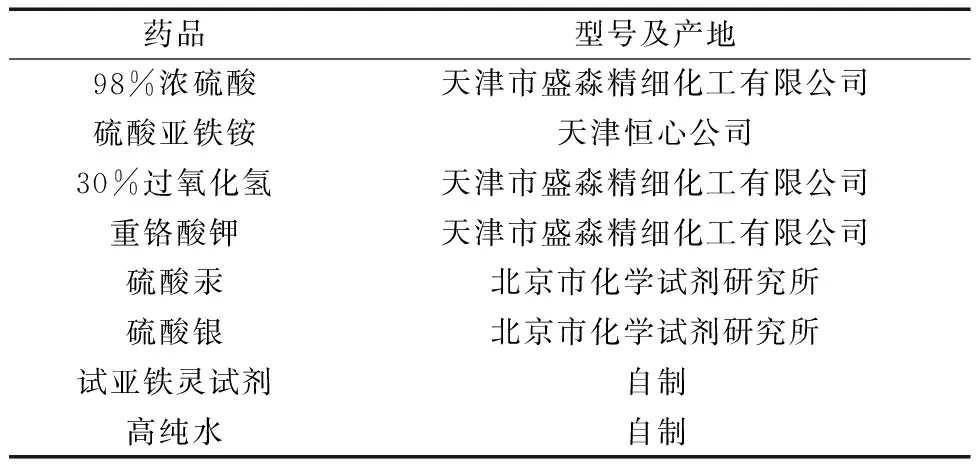
表2 实验药品Table.2 Experimental medicine.
2.3 实验步骤
2.3.1催化剂制备方法
催化剂的制备本实验所用的催化剂是自制的β-FeOOH,是通过氯化铁水解的方法得到[9]。取原碱渣废水1500 mL,先用工业滤网将废水过滤一次,然后在电动搅拌器的作用下利用滴管不断的向废水中滴加浓硫酸使废水的pH值调至2左右。碱渣废水静置2 h左后真空抽滤2~3次。向反应釜中分别加入50 mL废水、催化剂、双氧水。加好试剂后放入烘箱内反应,温度上升至150℃时开始计时,反应时间为2 h。待反应结束测定溶液的COD。
2.3.2COD值测定方法
向三颈瓶中加入0.4 g硫酸汞,再加20.00mL废水,加入10.00mL重铬酸钾标准溶液及数粒沸石,加入30 mL硫酸-硫酸银溶液,轻轻摇动锥形瓶使溶液混匀,加热回流2 h(自开始沸腾时计时)。关掉电源等废水冷却后,用90 mL水冲洗冷凝管壁,取下锥形瓶。等再度冷却后,加3滴试亚铁灵指示液,用硫酸亚铁铵标准溶液滴定。测定水样的同时,取20.00 mL二次蒸馏水,按同样步骤做空白试验。利用以下公式算出COD值。
c=0.2500×10.00/V
(1)
式中:c——硫酸亚铁铵标准溶液的浓度,mol/L;
V——硫酸亚铁铵标准溶液的用量,mL;
0.2500——重铬酸钾标准溶液的浓度,mol/L;
10.00——重铬酸钾标准溶液的体积,mL。
CODcr=(V0-V1)c*8*1000/V
(2)
式中:c——硫酸亚铁铵标准溶液的浓度,mol/L;
V0——滴定空白时硫酸亚铁铵标准溶液的用量,mL;
V1——滴定水样时硫酸亚铁铵标准溶液用量,mL;
V——水样体积,mL;
8——氧(1/2氧)的摩尔质量,g/mol;
1000——体积单位换算系数。
COD去除率=(原样的COD-处理后的COD)/原样的COD×100%
( 3 )
2.3 结果及表征
样品的物相是由粉末X-射线电子衍射(Bruker D8,德国)进行表征,射线源:Cu Kα辐射(λ=1.54178 Å),扫描范围:10~80°。样品的形貌测定是在场发射扫描电子显微镜(FESEM,Hitachi S-8010,日本)和透射电子显微镜(TEM)上进行。
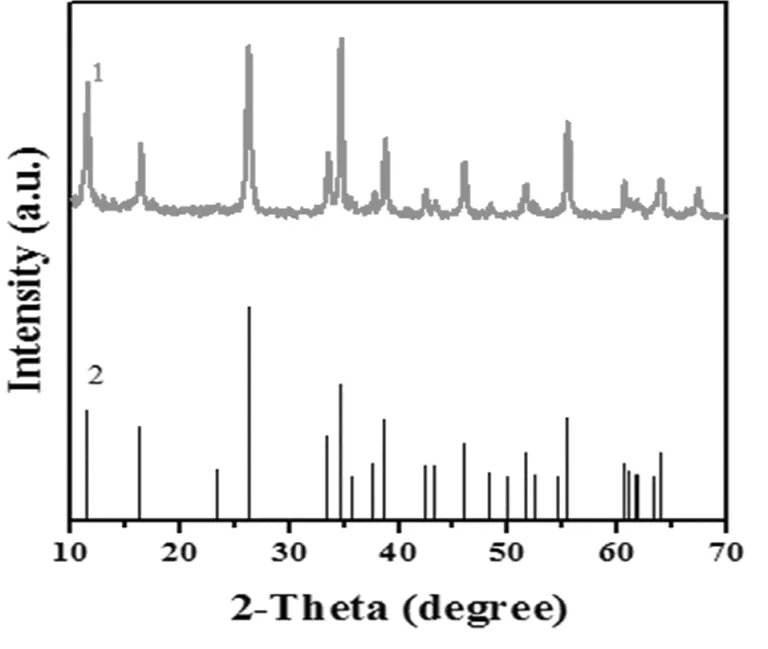
图1 水解样品XRDFig.1 The XRD pattern of hydrolytic prepared sample
图1为样品的XRD图,从图中可以看出,该样品峰型尖锐且与标准β-FeOOH(PDF#34-1266)在XRD谱图中基本保持一致不含有其它杂峰。证明成功合成β-FeOOH且尺寸较小,结晶度较高。

图2水解法制备样品的TEM (a) 为低倍电镜图;(b) 为高倍电镜图
Fig.2The TEM pattern of the hydrolysis-prepared sample;(a) Morphology at low magnification;(b) Morphology at high magnification
从TEM图2中可以看出合成的催化剂尺寸极小,约为100 nm,与XRD图中的峰型对应一致。这样的纳米催化剂有着较大的比表面积和更多的活性位点,因此有比块状材料更优异的性能,且水解法制备的样品形貌均一,有益于性能表达。将该催化剂应用于碱渣废水的处理中,并分别探究了双氧水和催化剂量及pH对于废水处理的影响(初始废液COD=12303 mg/L)。

图3(a) 不同量的双氧水的影响;(b) pH的影响
Fig.3(a) The effect of different amount of H2O2;(b) The effect of pH
图3(b)可知当pH值在3.98时,COD的去除率最高,pH值的减小或增大,都会引起处理效果的下降,根据WPO反应原理,当pH值较高时,OH-浓度高会抑制·OH的反应。另外过氧化氢是一种弱的二元酸,在碱性条件会使双氧水产生无效分解,降低其利用率。废水中的丙酮和苯酚被羟基自由基氧化成甲酸和乙酸等低分子酸类,废水中本身含有大量的钠离子,所以两者形成了缓冲溶液。从图上可以看出在不同pH值进水条件下,COD去除率相差无几,推测pH不是主要影响因素。因此选择pH值=3,探究过氧化氢用量的影响。从图3(a)可以看出,过氧化氢的量在3~4 mL,差别不大,考虑节约成本,因此筛选最佳条件为pH值=3,过氧化氢量为3mL。
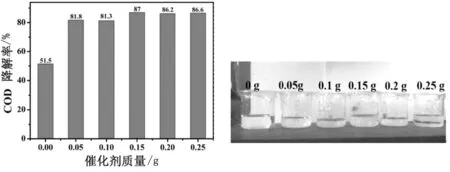
图4催化剂量的影响
Fig.4The effect of catalyst dosage.
图4为双氧水预处理后的废液加入不同催化剂的量对废水处理后的照片,(双氧水为 3 mL,pH值为2.7)从左至右催化剂用量分别为0 g,0.05 g,0.1 g,0.15 g,0.2 g,0.25 g)。从图4上看出废水溶液处理后都变为澄清液。可以看出当加入0.15 g催化剂FeOOH时COD的去除率最高,FeOOH作为催化剂引发羟基自由基的产生,催化剂浓度过低不利于羟基自由基的产生,当溶液中的催化剂浓度过高时与双氧水迅速反应产生大量自由基,其中一部分自由基会发生副反应从而降低了双氧水的作用。从图四右图看出不同量的催化剂的条件下,COD的去除率相差不是很大,从经济节省方面考虑,FeOOH用量为0.05 g即可。
3 结果与讨论
本工作使用湿式催化氧化能够很好的处理炼油碱渣废水,使用廉价的铁盐水解制备了纳米催化剂,当H2O2用量为3 mL,β-FeOOH用量0.05 g,pH值为2.7时,COD的去除率为81.9%。从炼油碱渣废水的性质来说,废水浓度高成分复杂,含有多种常规工艺难以处理的污染物,因此,很适合用湿式催化氧化法来处理。在优选H2O2/COD的最佳比的实验中,我们发现OH·的产生速率与H2O2的浓度有关。我们发现了COD值随着H2O2浓度的增加而升高。H2O2浓度越高,OH·的产生速率也越大,在OH·作用下,COD明显降低。当H2O2的的量大于3 mL时,COD值降低不是很明显,所以H2O2,的用量为3 mL时比较经济。因此,本文针对难以处理的碱油废液发明了湿法催化还原的方法,将原始废液COD由12303 mg/L 降至1000 mg/L,为工业废液处理提供了借鉴,证明 -FeOOH 是处理废水中污染物的替代品,值得更多的工作者对其研究。
