超声引导下经连续椎旁神经阻滞复合全麻对开胸手术患者炎性反应和血流动力学的影响
2018-07-12梁友君褚立君龙先铭
梁友君 褚立君 龙先铭
开胸手术作为引起机体较大创伤手术形式之一,其在术中的创伤和术后的剧烈疼痛可以导致患者围手术期机体的全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)[1-2]。然而,全身炎症反应又是诱发患者多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS)的基础,而围手术期有效的镇痛不仅是减轻患者术后疼痛及降低术后心血管及肺部并发症的关键,也是使炎性反应减轻,促进患者康复的手段[4-5]。因此,对于开胸手术不同的麻醉方式和术后镇痛的选择将直接影响患者术后并发症、炎性反应及血流动力学的改变[6]。本研究旨在对超声引导下连续性胸椎旁神经阻滞(continuous thoracic paravertebral block,CTPVB)复合全麻方案对开胸手术炎性反应及血流动力学的影响进行评价,进而客观的论证胸椎旁神经阻滞的麻醉有效性。
1 资料与方法
1.1 一般资料
选择2016年3月至2017年12月钦州市第一人民医院收治的138例拟行开胸手术患者,年龄45~69岁,身体质量指数(body mass index,BMI)<25 kg/m2,体重55~82 kg。依据随机数表法将其分为观察组和对照组,每组69例。观察组采用超声引导下CTPVB复合全麻方案,对照组采用全身麻醉方案。观察组中男性44例,女性25例;年龄45~69岁,平均年龄(58.2±4.3)岁。对照组中男性45例,女性24例;年龄46~65岁,平均年龄(57.8±4.8)岁。两组患者的一般资料比较,差异无统计学意义,具有可比性。所有患者均已签署知情同意书,本研究获得医院医学伦理委员会的批准。
1.2 纳入与排除标准
(1)纳入标准:①无长期服用安定类药物、抗交感神经药及抗精神病药物史;②无严重中枢神经系统和循环系统疾病和代谢及内分泌疾病;③无穿刺部位感染及脊柱畸形的需开胸手术;④对开胸手术知情同意。
(2)排除标准:①双测开胸手术者;②有严重心、肝、肺、肾功能不全疾患;③肿瘤患者、穿刺部位有瘢痕感染和凝血酶异常者;④有手术史以及脊椎畸形者。
1.3 仪器材料与药物
(1)仪器材料。采用M2430型便携式超声诊断仪(美国安捷伦科技有限公司);WY-3型电子镇痛泵[扬州市五洋医疗器械有限公司,国食药监械(准)字2008第3540060]。Mallinckrodt,39F型双腔支气管导管(美国泰科公司;国食药监械(进)字2012第3461311)。
(2)药物。罗库溴胺(国药准字号2009318,浙江仙琚制药股份有限公司),咪哒唑仑(批号SH008,上海罗氏制药公司),依托咪酯(国药准字号H32022992,江苏恩华药业股份有限公司),芬太尼(国药准字号H20030199,宜昌人福药业有限公司);苯磺顺阿曲库胺(国药准字号H20060869,江苏恒瑞医药股份有限公司),瑞芬太尼(国药准字号H20143314,江苏恩华药业股份有限公司)、丙泊酚(国药准字号J20080023,Fresenius Kabi AB,瑞典)、托烷司琼(国药准字号H20041547,北京双鹭药业股份有限公司)、罗哌卡因(国药准字号H20050325,广东华润顺峰药业有限公司)。
1.4 麻醉方法
(1)两组患者入院后均行常规检测,检测内容包括心电图、血氧饱和度、右侧静脉穿刺置管检查中心静脉压,术后对桡动脉进行穿刺并行有创血压监测。
(2)对照组麻醉方案。进行全身麻醉,给予罗库溴胺0.6 mg/kg,咪哒唑仑0.03 mg/kg,依托咪酯0.3 mg/kg,芬太尼2~4 μg/kg,继而将Mallinckrodt,39F型双腔支气管导管顺利插入,术中靶控输注苯磺顺阿曲库胺,瑞芬太尼和丙泊酚,通过脑电双频指数(bispectral index,BIS)对麻醉深度进行检测,使麻醉深度值维持在40~60,利用镇痛泵采用间断患者自控镇痛(patient controlled analgesia,PCA):输注芬太尼10 μg/ml+托烷司琼0.1 mg/ml,100 ml,最大剂量为2 ml/h。PCA剂量0.5 ml/次,时间15 min。
(3)观察组麻醉方案。患者侧卧位,手术测朝上,弓背屈曲,在M2430型便携式超声诊断仪引导下行CTPVB复合全麻方案,在超声探头7 Mz频率引导下,将穿刺点设为手术测T4棘突下缘旁开2.5~3 cm处,穿刺置管下椎旁间隙,对探头位置调整,将穿刺针位置通过超声下进行实时观察调整,顺序穿过皮肤、肋间外肌、肋间内膜抵达椎旁间隙,注入15 ml 0.375%罗哌卡因,随着药液在胸膜外进行扩散,胸膜被推移向下、向腹侧,硬膜外导管通过穿刺针向椎旁间隙设置,置管的深度为2~3 cm。固定导管后对麻醉平面进行检测,麻醉椎管内神经阻滞的范围为T4~T8节段,全麻诱导,方法同对照组,术后进行CTPVB镇痛,镇痛泵成分为0.25%罗哌卡因200 ml,4 ml/h持续硬膜外输注,单次剂量为1 ml,时间锁定30 min。
(4)术后处理[16]。术后给予静脉镇痛处理,打开WY-3型电子镇痛泵的左右耳夹,接上药盒与延长管,排气后开始运行。镇痛药物选择芬太尼8~10 μg/kg用生理盐水稀释至100 ml,设定负荷量为2 ml,背景剂量2 ml/h,单次剂量0.5 ml,锁定时间15 min。
1.5 观察指标
ELISA方法检测并比较两组患者术后48 h血浆炎性因子白介素6和白介素10(interleukin,IL-6、IL-10)及肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平变化;以及术后进行视觉模拟评分,观察术后12 h、24 h和48 h视觉模拟评分(VAS);比较两组患者手术室静息时(T0)、CTPVB复合全麻给药15 min后(T1)、诱导插管后(T2)、切皮后5 min(T3)及拔管前(T4)各时间点平均动脉压(mean artery pressure,MAP)和心率(heart rate,HR),研究其对血流动力学MAP和HR的影响。VAS评分标准:0分为无痛,10分为剧痛[7-8]。
表1 两组患者开胸手术前后炎性因子水平比较
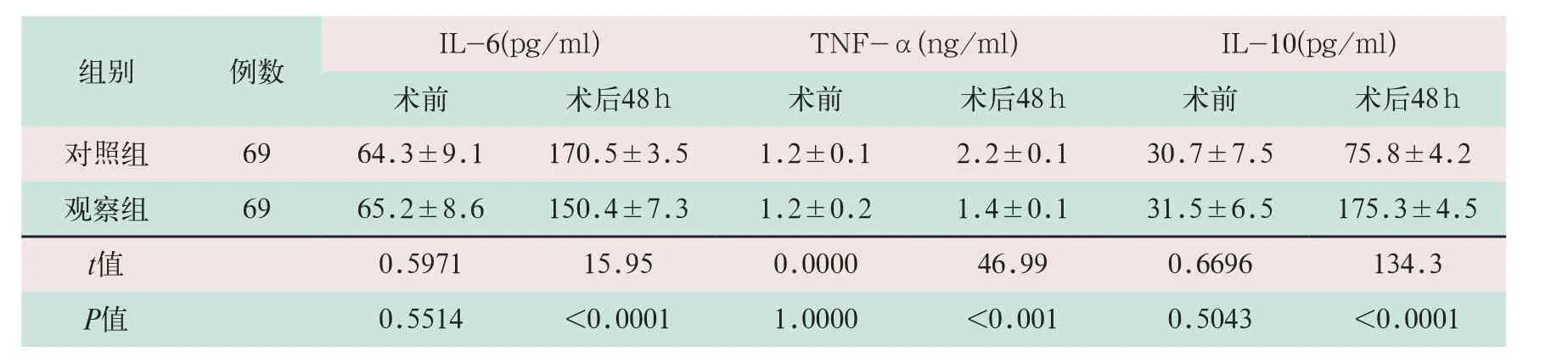
表1 两组患者开胸手术前后炎性因子水平比较
注:表中IL-6为白细胞介素-6,TNF-α为肿瘤坏死因子-α,IL-10为白细胞介素-10。
组别 例数 IL-6(pg/ml) TNF-α(ng/ml) IL-10(pg/ml)术前 术后48 h 术前 术后48 h 术前 术后48 h对照组 69 64.3±9.1 170.5±3.5 1.2±0.1 2.2±0.1 30.7±7.5 75.8±4.2观察组 69 65.2±8.6 150.4±7.3 1.2±0.2 1.4±0.1 31.5±6.5 175.3±4.5 t值 0.5971 15.95 0.0000 46.99 0.6696 134.3 P值 0.5514 <0.0001 1.0000 <0.001 0.5043 <0.0001
表3 两组患者不同时间血流动力学比较
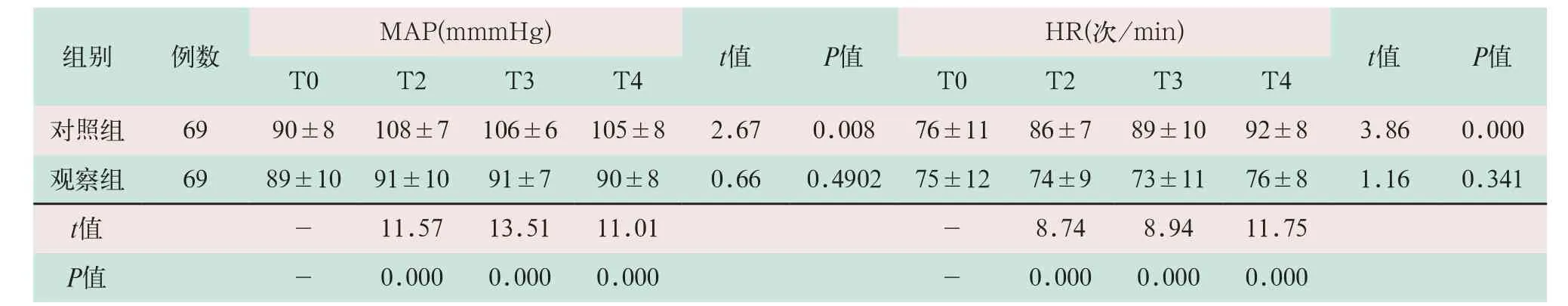
表3 两组患者不同时间血流动力学比较
注:表中MAP为平均动脉压;HR为心率;T0为手术室静息时,T1为全麻给药15 min后,T2为诱导插管后,T3为切皮后5 min,T4为拔管前。
组别 例数 MAP(mmmHg)t值 P值T0 T2 T3 T4 T0 T2 T3 T4 t值 P值 HR(次/min)对照组 69 90±8 108±7 106±6 105±8 2.67 0.008 76±11 86±7 89±10 92±8 3.86 0.000观察组 69 89±10 91±10 91±7 90±8 0.66 0.4902 75±12 74±9 73±11 76±8 1.16 0.341 t值 - 11.57 13.51 11.01 - 8.74 8.94 11.75 P值 - 0.000 0.000 0.000 - 0.000 0.000 0.000
1.6 统计学方法
采用SPSS 19.0软件进行数据统计与处理,计量资料比较用t检验,重复测量数据采用重复测量方差分析,以P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者术后炎性因子水平比较
两组患者开胸手术前血清中IL-6、TNF-α和IL-10水平比较,差异均无统计学意义,术后48 h两组患者的炎性因子水平均明显上升,且观察组血清中炎性因子IL-6和TNF-α水平明显低于对照组,两组比较差异有统计学意义(t=15.95,t=46.99;P<0.05);IL-10则在术后观察组明显高于对照组,两组比较差异有统计学意义(t=134.3,P<0.05),见表1。
2.2 两组患者术后VAS评分比较
观察组开胸手术后2 h、12 h、24 h和48 h各时段咳嗽时镇痛效果VAS评分显著低于对照组,两组比较差异有统计学意义(t=13.91,t=17.1,t=2.321,t=9.231;P<0.05),见表2。
表2 两组患者开胸手术后不同时间咳嗽时镇痛效果比较
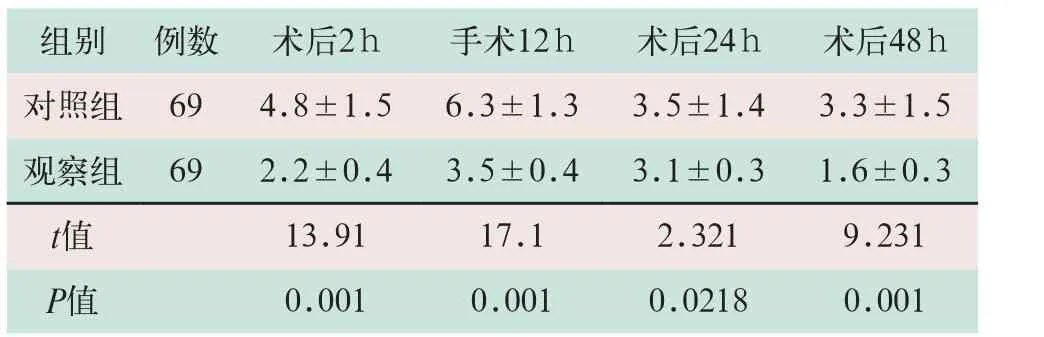
表2 两组患者开胸手术后不同时间咳嗽时镇痛效果比较
组别 例数 术后2 h 手术12 h 术后24 h 术后48 h对照组 69 4.8±1.5 6.3±1.3 3.5±1.4 3.3±1.5观察组 69 2.2±0.4 3.5±0.4 3.1±0.3 1.6±0.3 t值 13.91 17.1 2.321 9.231 P值 0.001 0.001 0.0218 0.001
2.3 两组患者血流动力学比较
对照组和观察组患者开胸手术时间和出血量差异均无统计学意义。观察组MAP和HR在T0、T2、T3、T4时段数值无明显变化;对照组MAP和HR数值在T2~T4时与T0比较明显增高,两组MAP在T0时与T2、T3和T4时段数值比较差异有统计学意义(t=11.57,t=13.51,t=11.01;P<0.05);两组HR在T0时与T2、T3和T4时段数值比较差异有统计学意义(t=8.74,t=8.94,t=11.75,P<0.05),见表3。
3 讨论
有研究显示,在既往有心律失常、高血压和冠心病等病症的患者中,经过开胸手术后明显增加了心血管并发症的发生率[9-10]。此外由于患者经过开胸手术后,其气道的分泌物明显增加,术后患者咳嗽和呼吸因疼痛而不敢用力进行,从而引起呼吸活动不畅,咳嗽无力和通气障碍而导致肺部不张、肺部感染以及低氧血症等,低氧血症可以导致心血管并发症的发生[11]。而术后炎症因子的增加将导致过度应激,过度应激削弱肌体正常生理贮备,加重炎症反应,激发SIRS,因此术后镇痛将有助于患者康复[12]。
全身麻醉复合硬膜外麻醉是开胸手术较佳麻醉方法,其完善的镇痛,可以有效改善细胞免疫抑制以及心肌供血,降低应激反应,使得术后肺部感染可以有效的预防,通过硬膜导管进行镇痛,且麻药用药量少,镇痛有效,术后苏醒快,但由于胸段胸椎体呈叠瓦状排列,硬膜外穿刺存在容易穿破硬脊膜,导致围手术期低血压,硬膜外感染,硬膜外血肿,神经损伤以及全脊髓麻醉等严重的并发症[13-14]。椎旁神经阻滞即从椎旁间隙注入局麻药,使注射部位的单侧多个节段肋间神经被阻滞,与硬膜外麻醉相比,椎间神经阻滞由于只对一侧胸壁产生麻醉效果,因此对血流动力学和呼吸影响较小,在胸外手术中受到越来越多的重视[15]。但也有研究认为,作为手术后镇痛的需求,单次椎旁间隙麻醉注射并不能很好的满足[16]。本研究主要关注在超声引导下对穿刺针实时的调整,可以使穿刺针精确抵达胸内筋膜腹侧,药液扩散可以被实时观察,达到成功率较高的超声引导下胸椎旁神经阻滞[17]。
超声引导下CTPVB复合全麻术在开胸手术中优点众多,本研究表明:①相比普通的全身麻醉,超声引导下CTPVB复合全麻术可以使术后应激反应减轻,适当的应激反应有利于机体应对防御,过度会使身体受到损害,超声引导下胸椎旁神经阻滞复合全麻能更有效的抑制开胸手术患者的应激反应;②血流动力学稳定,与全身麻醉方法相比,椎旁神经阻滞可提供与硬膜外相同的镇痛效果下,围手术期血流动力学更为稳定,血压心率更平稳;③总结术后镇痛药物使用情况发现,超声引导下CTPVB复合全麻术显著减少全麻药物和镇痛药物的用量,减少了患者阿片类药物的使用,术后活动早,良好的镇痛使患者敢于咳嗽咳痰,可以防止术后肺部感染的发生,有利于患者康复;④超声引导下CTPVB复合全麻术相对于盲探技术有众多潜在优点,可视化解剖学结构,穿刺针尖,穿刺针轴,导管位置及局部麻醉剂的扩展,能够更好地缩短操作时间,使阻滞时间延长,麻醉剂量减少,并发症发生率及手术失败率降低,从而弱化患者的不适感,加快患者痊愈。这些与过去研究报道的超声引导下胸椎旁神经复合全麻术的优点基本一致[18-19]。
有研究报道,如果于胸内筋膜背侧注入药物,呈云雾状的药液单纯扩散至肋间隙或局限于注射节段,此时可以有3个节段感觉阻滞,然而药物注射到胸内筋膜腹侧,药物则成间隙内线性扩散合并肋间隙扩散,将产生至少5个节段感觉阻滞[20]。这与本研究术中结果基本一致。以往认为,常规全身麻醉与硬膜外麻醉是开胸手术患者最佳麻醉方案,发现上述麻醉方式镇痛完善,明显改善心肌供血降低机体应激反应[21-23]。本研究显示,CTPVB复合全麻术后患者VAS评分明显低于对照组,并且炎性因子水平明显低与对照组,同时对血流动力学也无明显影响,这也最大限度避免了术后对心血管病的影响,降低心血管并发症以及肺部感染并发症的发生。
本研究的不足之处为样本量相对较少,研究内容尚不够全面深入,日后需要进一步深入探究超声引导下CTPVB复合全麻术的优点及缺点,为其广泛应用提供实验临床依据。在开胸手术麻醉方案的选择中,采用超声引导下CTPVB复合全麻术方案,可优化术后镇痛效果,明显改善VAS评分,减轻炎症反应,促进术后康复,具有较高的临床应用价值。
