不同氮磷钾肥对海泡石钝化修复镉污染土壤的稳定性研究
2018-06-25徐应明黄青青谢忠雷尹秀玲
黄 荣, 徐应明①, 黄青青, 谢忠雷, 尹秀玲,, 秦 旭
(1.农业部环境保护科研监测所/ 农业部产地环境污染防控重点实验室, 天津 300191; 2.吉林大学环境与资源学院, 吉林 长春 130012)
据2014年环境保护部和国土资源部联合发布的《全国土壤污染状况公报》显示,我国土壤污染形势严峻,其中中南地区土壤中镉污染问题尤其突出[1]。水稻作为我国主要粮食作物,其重金属含量与食品安全已经成为全社会广泛关注的热点[2]。现有的农田土壤重金属污染修复方法中,钝化修复技术具有修复效果好、操作简便且不影响农业生产等优点,适宜于大面积中轻度重金属污染农田修复治理[3]。但钝化修复主要使土壤中重金属活性降低,并没有将其从土壤中去除,农艺措施、耕作制度及自然环境的变化都可能影响其在土壤中有效态含量的变化,导致钝化后的重金属重新活化释放。
氮、磷、钾肥作为肥料3要素,是农作物增产的主要保障,对植物生长具有不可替代的作用,但也有许多研究表明不同种类化肥对土壤重金属的有效性以及植物对重金属的吸收存在一定影响,如施用尿素后可引起土壤pH值和重金属形态变化[4];铵态氮肥能降低土壤pH值,提高土壤根系重金属活性,从而促进玉米对重金属的吸收[5];磷肥通过3种磷酸根(H2PO4-、HPO42-和PO43-)增加土壤表面电荷,进而影响土壤对重金属的吸附,且在一定pH值范围内磷酸根还能与金属阳离子结合产生沉淀[6-7];钾肥主要通过其伴随阴离子对土壤重金属活性产生影响[7]。
不同种类化肥对钝化修复效应具有协同促进作用还是拮抗抑制作用?目前鲜有研究涉及。明确不同肥料对钝化修复效应及其稳定性的影响,制定科学合理的施肥方案对于原位钝化修复技术的推广具有重要意义。笔者在前期研究的基础上,采用天然黏土矿物海泡石作为钝化材料,以水稻为供试植物,研究不同氮、磷和钾肥对海泡石钝化修复镉污染土壤的影响,旨在为南方镉污染水稻田钝化修复条件下的合理施肥提供科学依据。
1 材料与方法
1.1 试验方法
连续2 a水稻盆栽试验在智能温室开展,每盆种植3株水稻,共设置8种处理:(1)对照(CK);(2)单施海泡石(S);(3)海泡石+尿素(S+N1);(4)海泡石+碳铵(S+N2);(5)海泡石+钙镁磷肥(S+P1);(6)海泡石+普钙(S+P2);(7)海泡石+KCl(S+K1);(8)海泡石+K2SO4(S+K2);其中氮、磷和钾肥分别以含N、P2O5和K2O计算,其质量分数均为0.2 g·kg-1,海泡石添加剂量为10 g·kg-1。第1年水稻收获后,保存盆中土壤用于第2年继续种植,第2年不再添加钝化剂海泡石,但肥料与第1年处理一致。每个处理均设置3个重复。
供试水稻品种为欣荣优华占,全生育期为120 d左右。供试土壤采集于湖南省郴州市某镉超标水稻田,其pH值为6.56,阳离子交换容量为16.6 cmol·kg-1,w(总氮)为1.29 g·kg-1,w(总磷)为0.68 g·kg-1,w(总镉)为1.58 mg·kg-1。海泡石为天然黏土矿物材料,采用X射线荧光分析方法确定其主要成分CaO、MgO、Al2O3和SiO2的质量分数分别为41.7%、16.8%、7.4%和32.5%。
1.2 样品分析
水稻成熟后收获,将水稻分为根、秸秆和籽粒3部分,洗净、风干称重,然后粉碎保存用于后续测定。收获水稻的同时采集土壤,土壤样品风干后过1 mm孔径筛,混匀保存用于后续测定。水稻样品中Cd含量测定:准确称取0.250 0 g样品,加入8 mLw为65%~68%的浓HNO3,静置过夜,通过电热消解仪(ED54,中国莱博泰科)消解,消解液中Cd含量采用电感耦合等离子体质谱仪(iCAP,美国赛默飞世;Cd的检测限为0.1×10-12)测定。在整个测定过程中植物样品采用湖南大米〔GBW10045(GSB-23)〕和空白样品进行全程质量控制。Cd元素回收率均在95%~105%范围内。
土壤pH值用去离子水〔V(水)∶m(土)=2.5∶1〕浸提后,采用pH计(PB-10,德国Sartorius)测定[8]。土壤中可提取态Cd以0.025 mol·L-1HCl为浸提液〔V(水)∶m(土)=5∶1〕浸提后[8],对浸提液采用原子吸收分光光度计(ZEEnit 700P,德国耶拿)测定。
1.3 数据分析
稳定效率(K)表示不同化肥对土壤中Cd的稳定性;钝化能力(Cap)表示不同化肥作用下钝化剂对重金属的钝化容量,值越大意味着钝化能力越强[9]。计算公式如下:

(1)

(2)
式(1)~(2)中,K为稳定效率,%;Ce为添加海泡石、肥料处理土壤中Cd浸出浓度,mg·L-1;Ci为对照处理土壤中Cd浸出浓度,mg·L-1;Cap为钝化能力,mg·g-1;V为浸提液体积,mL;m为浸提时所取土壤质量,g;ω为土壤中钝化剂质量分数。试验中V∶m为5∶1,ω为1%。
所有数据均采用3次重复的平均值±标准偏差来表示,数据统计分析采用SPSS 20.0软件,采用Origin Pro 8.5软件制图。
2 结果与分析
2.1 不同处理对水稻生物量的影响
如图1所示,添加海泡石在2 a内均增加了水稻籽粒和秸秆的生物量,但是均未达到显著水平(P>0.05),这可能是因为海泡石为天然黏土矿物,其含有的氮磷钾等养分极少,但海泡石能够钝化土壤中的Cd,减小Cd离子对水稻的胁迫,有利于水稻生长。

CK—对照; S—单施海泡石; S+N1—施海泡石+尿素; S+N2—施海泡石+碳铵; S+P1—施海泡石+钙镁磷肥; S+P2—施海泡石+普钙;S+K1—施海泡石+KCl; S+K2—施海泡石+K2SO4。直方柱上方英文小写字母不同表示同一部位不同处理组间水稻生物量差异显著(P<0.05)。
第1年,与单施海泡石相比,添加肥料均增加籽粒生物量,其中碳铵、尿素和钙镁磷肥达到了显著水平(P<0.05),普钙、K2SO4和KCl均未达到显著水平(P>0.05)。不同肥料的增产效果排序为碳铵>尿素>钙镁磷肥>K2SO4>普钙>KCl。第2年,除了2种氮肥增加水稻生物量外,其他肥料均使水稻生物量有所降低。
2.2 不同处理对水稻地上不同部位Cd含量的影响
不同处理水稻中糙米、秸秆和根系中镉含量见图2。可以看出,单施海泡石显著降低水稻各部位中Cd含量(P<0.05),与对照相比,第1年水稻糙米、秸秆和根系中w(Cd)降幅分别为41.4%、74.0%和36.8%;第2年水稻糙米、秸秆和根系中w(Cd)降幅分别为32.7%、38.9%和30.9%,说明海泡石有持续钝化效果。与单施海泡石相比,第1年的试验结果表明在海泡石钝化的基础上加施尿素、碳铵和钙镁磷肥均降低糙米中Cd含量,施普钙、K2SO4和KCl均增加糙米中Cd含量;第2年的试验结果中,施碳铵、钙镁磷肥和K2SO4均降低糙米中Cd含量,施尿素、普钙和KCl均增加糙米中Cd含量。碳铵和钙镁磷肥在连续2 a的试验中均降低糙米中w(Cd),第1年的降幅分别为28.4%和26.9%;第2年的降幅分别为2.10%和11.4%。KCl和普钙在2 a内均增加糙米中w(Cd),第1年增幅分别为31.6%和39.3%;第2年增幅分别为9.24%和53.8%。
与单施海泡石相比,第1年的试验结果表明分别加施6种肥料均增加秸秆中Cd含量,增幅的顺序为碳铵>尿素>KCl>K2SO4>普钙>钙镁磷肥;第2年的试验结果中,碳铵、尿素和KCl使秸秆中Cd含量增加,K2SO4、普钙和钙镁磷肥使秸秆中Cd含量有所降低。第1年的试验结果显示,与单施海泡石相比,除了钙镁磷肥外其他5种肥料均增加根系中Cd含量,其增幅顺序为KCl>K2SO4>普钙>尿素>碳铵;第2年除了2种磷肥以外,其他4种肥料均增加了水稻根系中Cd含量。
表1为不同处理对水稻不同部位Cd富集的影响。结果表明,水稻不同部位对Cd的富集能力的大小顺序为根系>秸秆>糙米,且根系中Cd含量远远大于秸秆和糙米中Cd含量。海泡石在连续2 a内均显著降低了水稻不同部位对Cd的富集(P<0.05)。与单施海泡石相比,加施钙镁磷肥2 a内均降低水稻不同部位对Cd的富集,而施KCl均增加水稻对Cd的富集。

CK—对照; S—单施海泡石; S+N1—施海泡石+尿素; S+N2—施海泡石+碳铵; S+P1—施海泡石+钙镁磷肥; S+P2—施海泡石+普钙; S+K1—施海泡石+KCl; S+K2—施海泡石+K2SO4。直方柱上方英文小写字母不同表示同一年份不同处理组间Cd含量差异显著(P<0.05)。
2.3 不同处理对土壤pH值和土壤有效态Cd含量的影响
如表2所示,与对照相比,海泡石钝化以及海泡石钝化的基础上施6种肥料均显著增加土壤pH值。第1年的试验结果中,与单施海泡石相比,加施尿素和钙镁磷肥增加土壤pH值,施普钙、KCl和K2SO4使土壤pH值有所降低,而施碳铵对土壤pH值没有影响。第2年施尿素、碳铵、KCl和K2SO4均使土壤pH值有所降低,施钙镁磷肥显著增加了土壤pH值(P<0.05),施普钙对土壤pH值没有影响。
从图3可以看出,单施海泡石显著降低土壤w(有效态Cd),与对照相比,第1年和第2年分别降低68.6%和32.2%。另外,与单施海泡石相比,第1年加施6种肥均增加土壤有效态Cd含量,增加幅度的顺序为KCl>普钙>K2SO4>尿素>碳铵>钙镁磷肥;第2年除了2种氮肥使土壤有效态Cd含量有所增加外,其余4种肥料均降低土壤有效态Cd含量,其降幅顺序为钙镁磷肥>普钙>K2SO4>KCl。
2.4 不同处理对土壤中Cd的稳定性及钝化能力的影响
海泡石以及各种肥料对Cd稳定性的影响用K表示,其值越大表示越有利于Cd的稳定。钝化剂对重金属的钝化容量用Cap表示,该值越大意味着钝化能力越强[9]。如图4所示,第1年海泡石对Cd的K值远远大于第2年,且第1年添加不同肥料均降低Cd的稳定性,其中钙镁磷肥的降低幅度最小,KCl的降低幅度最大;第2年尿素和碳铵使Cd的稳定率分别降低4.54%和10.2%;钙镁磷肥、普钙、KCl和K2SO4使Cd的K值分别增加42.4%、39.2%、15.9%和30.0%。
如表3所示,第1年海泡石对Cd的钝化容量为98.2 mg·kg-1,施尿素和碳铵分别使Cd的钝化容量降低21.1和4.47 mg·kg-1;钙镁磷肥和普钙分别使Cd的钝化容量降低4.27和29.50 mg·kg-1;KCl和K2SO4分别使Cd的钝化容量降低58.00和23.50 mg·kg-1。
表1不同处理对水稻各部位中Cd的富集系数
Table1Cdbioaccumulationcoefficientofbrownrice,shootandrootrelativetotreatment

处理第1年富集系数第2年富集系数糙米秸秆根系糙米秸秆根系 CK0.15±0.03a0.51±0.03a2.44±0.89ab0.10±0.01a0.33±0.06a1.23±0.24ab S0.09±0.02bc0.13±0.03e1.54±0.18bc0.07±0.01b0.20±0.01bcd0.85±0.04cde S+N10.04±0.01d0.31±0.04bc2.43±0.59ab0.09±0.02ab0.38±0.03a0.91±0.09cde S+N20.06±0.01cd0.39±0.04b2.41±0.64ab0.07±0.01b0.25±0.02b1.33±0.02a S+P10.06±0.02cd0.15±0.05de1.20±0.01c0.06±0.02b0.14±0.01e0.69±0.07e S+P20.11±0.02ab0.23±0.05cd2.50±0.31ab0.08±0.01b0.18±0.02cde0.79±0.08de S+K10.12±0.02ab0.27±0.07c2.71±0.37a0.11±0.02a0.23±0.02bc1.07±0.19bc S+K20.12±0.03ab0.23±0.06cd2.54±0.68ab0.07±0.016b0.15±0.04de0.10±0.21bce
CK为对照,S为单施海泡石,S+N1为施海泡石+尿素,S+N2为施海泡石+碳铵,S+P1为施海泡石+钙镁磷肥,S+P2为施海泡石+普钙,S+K1为施海泡石+KCl,S+K2为施海泡石+K2SO4。同一列数据后英文小写字母不同表示不同处理组间Cd富集系数差异显著(P<0.05)。
第2年尿素和碳铵分别使Cd的钝化容量降低5.90和13.23 mg·kg-1;钙镁磷肥、普钙、KCl和K2SO4均增加Cd的钝化容量,其对海泡石钝化能力的促进作用从大到小依次为钙镁磷肥>普钙>K2SO4>KCl。
表2不同处理对土壤pH值的影响
Table2SoilpHrelativetotreatment

处理第1年第2年 CK6.86±0.09c6.98±0.07d S7.65±0.02ab7.26±0.06b S+N17.74±0.02a7.11±0.09c S+N27.65±0.12ab7.12±0.08c S+P17.72±0.04a7.42±0.06a S+P27.62±0.08ab7.26±0.04b S+K17.55±0.06b7.12±0.03c S+K27.52±0.11b7.22±0.06bc
CK为对照,S为单施海泡石,S+N1为施海泡石+尿素,S+N2为施海泡石+碳铵,S+P1为施海泡石+钙镁磷肥,S+P2为施海泡石+普钙,S+K1为施海泡石+KCl,S+K2为施海泡石+K2SO4。同一列数据后英文小写字母不同表示不同处理组间土壤pH值差异显著(P<0.05)。

CK—对照; S—单施海泡石; S+N1—施海泡石+尿素; S+N2—施海泡石+碳铵; S+P1—施海泡石+钙镁磷肥; S+P2—施海泡石+普钙; S+K1—施海泡石+KCl; S+K2—施海泡石+K2SO4。直方柱上方英文小写字母不同表示同一年份不同处理组间可交换态Cd含量差异显著(P<0.05)。
3 讨论
植物体内Cd的富集主要受土壤中有效态Cd含量影响,降低土壤中Cd的生物有效性是减少植物吸收Cd的根本途径[10]。土壤有效态Cd含量受许多因素的影响,其中土壤pH值是较为关键的影响因子之一[11-12]。连续2 a的试验结果显示海泡石显著增加土壤pH值(表2),降低土壤中可交换态Cd含量(图3),从而显著降低水稻糙米、秸秆和根系中Cd的富集。这主要是因为一方面海泡石自身呈碱性(pH值为10.1),酸性土壤溶液中的H+能够与海泡石发生反应从而中和消耗部分H+以缓和土壤酸度[3],提高土壤pH值,促进土壤中Cd离子的沉淀作用,降低Cd的活性,笔者试验结果与已有研究[3,11,13]基本一致;另一方面,海泡石对土壤中Cd离子具有吸附等作用,可以进一步降低Cd离子活性。
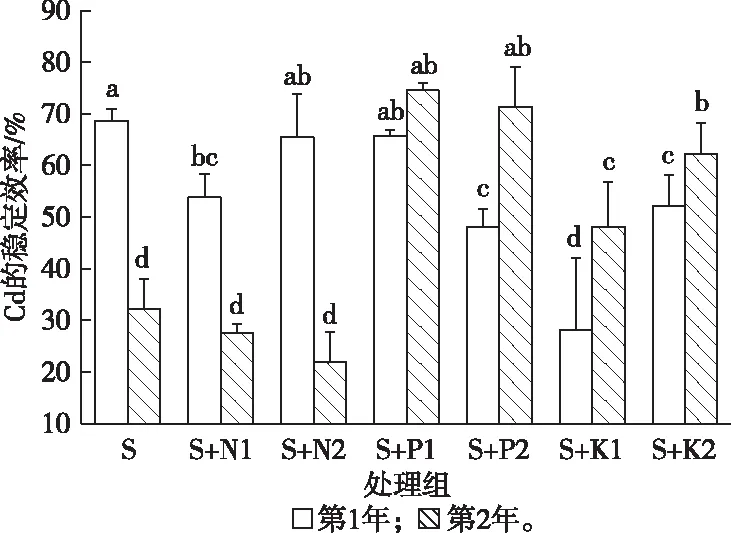
CK—对照; S—单施海泡石; S+N1—施海泡石+尿素; S+N2—施海泡石+碳铵; S+P1—施海泡石+钙镁磷肥; S+P2—施海泡石+普钙; S+K1—施海泡石+KCl; S+K2—施海泡石+K2SO4。直方柱上方英文小写字母不同表示同一年份不同处理组间Cd的稳定效率差异显著(P<0.05)。
表3不同处理对土壤Cd钝化能力的影响

Table 3 Soil Cd inactivation capacity relative to treatment mg·kg-1
S为单施海泡石,S+N1为施海泡石+尿素,S+N2为施海泡石+碳铵,S+P1为施海泡石+钙镁磷肥,S+P2为施海泡石+普钙,S+K1为施海泡石+KCl,S+K2为施海泡石+K2SO4。同一列数据后英文小写字母不同表示不同处理组间Cd的钝化能力差异显著(P<0.05)。
第1年试验中2种氮肥对土壤pH值均有一定影响,但都未达到显著水平(P>0.05);第2年试验中继续施2种氮肥均显著降低土壤pH值。这可能是因为尿素施入土壤中最初以CO(NH2)2分子形式存在,在脲酶作用下水解成碳酸铵、碳酸氢铵和氢氧化铵等碱性化合物,随着种植时间的推移,尿素水解的碳酸氢铵被植物以NH4+吸收时会分泌H+,从而导致根系周围发生酸化[14]。另外,尿素和碳铵在2 a内均增加土壤有效态Cd含量(图3),但是碳铵在2 a内均显著降低糙米中Cd含量(图2),加施尿素第1年糙米中Cd含量略有降低,第2年糙米中Cd含量略有增加,但均未达到显著水平(图2),这可能是因为尿素和碳铵显著增加了水稻秸秆和籽粒生物量(图1),从而对糙米中Cd起稀释作用。此外,尿素和碳铵在2 a试验中均对土壤钝化条件下Cd的K值产生不利影响,其中第1年尿素产生的不利影响大于碳铵,第2年碳铵产生的不利影响大于尿素(图4)。
磷肥对土壤中重金属生物有效性的影响是个复杂的过程,是多种因素综合作用的结果[6,15-18]。一方面磷肥施入土壤后会改变土壤pH值,普钙属于生理酸性肥料,施入土壤后随着根系对P的吸收会引起土壤局部酸化;钙镁磷肥属于碱性肥料,施入土壤后会增加土壤pH值[15]。2 a试验中钙镁磷肥均使土壤pH值升高(表2),而普钙则未对土壤pH值产生明显影响。这与王朋超等[15]的研究结果有些许偏差,造成这种偏差的原因有可能是该试验所选取的供试植物为水稻,水稻在种植期间大部分时间处于淹水状态,淹水会对土壤pH值产生一定影响[19]。另一方面磷肥中的3种磷酸根(H2PO4-、HPO42-和PO43-)能够诱导与土壤中的Cd2+结合形成磷酸金属盐等难溶化合物,研究表明这一过程在碱性条件下更容易生成溶解度较小的正磷酸金属盐[20],降低Cd的移动性,从而降低Cd的生物有效性[6];此外,普钙和钙镁磷肥都属于含钙磷肥,施入土壤后可显著提高土壤交换态Ca2+含量,而Ca2+与Cd2+之间存在较强的竞争效应,这都会影响土壤Cd的生物有效性[16]。钙镁磷肥更有利于降低土壤中Cd的生物有效性(图3)和水稻各部位Cd的富集(图1),主要是因为钙镁磷肥显著增加了土壤pH值,更有利于正磷酸金属盐的生成,从而降低了水稻对Cd的吸收。钙镁磷肥和普钙在第1年均对土壤钝化条件下Cd的稳定性产生不利影响,但钙镁磷肥的影响要小于普钙;第2年钙镁磷肥和普钙均对土壤钝化条件下Cd的稳定性产生促进作用,钙镁磷肥的促进作用大于普钙。
KCl在2 a内显著增加糙米中Cd含量,K2SO4在第1年促使糙米中Cd含量略有增加,第2年使糙米中Cd含量略有降低。钾肥施入后均降低土壤pH值(表2),增加土壤可交换态Cd含量(图3),且KCl对土壤pH值和可交换态Cd含量的影响效果大于K2SO4。大量研究表明,钾肥对土壤中重金属活性的影响不仅是通过影响土壤pH值,其陪伴离子也产生了极其重要的影响。晏哲等[21]认为Cl-和SO42-易与Cd结合形成络合物,增加固态Cd向土壤溶液迁移,从而增加土壤Cd的生物有效性。ZHAO等[22]通过盆栽试验比较了KCl、K2SO4和KNO33种钾肥对小麦Cd富集的影响,结果表明KCl和K2SO4均明显提高小麦中Cd含量。大量研究认为KCl能促进植物对Cd的吸收,但就K2SO4处理而言,由于陪伴离子SO42-对Cd的影响还不明确,有学者认为因为SO42-与Cd形成的络合物不如Cl-与Cd形成的络合物稳定,所以SO42-对植物Cd的富集不如Cl-显著。另外,水稻在淹水条件下SO42-还原为S2-,S2-与Cd2+生成CdS沉淀,从而降低土壤中Cd的生物有效性[23]。2 a盆栽试验结果表明,K2SO4更有利于土壤中Cd的稳定性。
4 结论
海泡石在2 a内均能对农田Cd污染土壤起到良好的钝化修复效果,即使在没有额外添加海泡石的情况下,糙米中Cd含量和可交换态Cd含量仍显著降低,表明海泡石对农田土壤Cd的钝化作用具有较好的稳定性。
施不同化肥对海泡石钝化土壤Cd的效果及其稳定性有着明显影响,因此,为避免不合理施肥对土壤Cd的钝化产生抵消作用,影响钝化的长期稳定性,在农田Cd污染水稻土钝化修复中,科学合理施肥具有重要意义。综合2 a试验结果,建议在海泡石钝化修复农田Cd污染水稻土时,氮磷钾肥分别施碳铵、钙镁磷肥和K2SO4。
[1] 环境保护部,国土资源部.全国土壤污染状况调查公报[J].中国环保产业,2014(5):10-11.[Ministry of Environmental Protection,Ministry of Land and Resources.Bulletin of National Soil Pollution Survey[J].China Environmental Protection Industry,2014(5):10-11.]
[2] 詹杰,魏树和,牛荣成.我国稻田土壤镉污染现状及安全生产新措施[J].农业环境科学学报,2012,31(7):1257-1263.[ZHAN Jie,WEI Shu-he,NIU Rong-cheng.Advances of Cadmium Contaminated Paddy Soil Research and New Measure of Its Safe Production in China:A Review[J].Journal of Agro-Environment Science,2012,31(7):1257-1263.]
[3] LIANG X F,XU Y,XU Y M,etal.Two-Year Stability of Immobilization Effect of Sepiolite on Cd Contaminants in Paddy Soil[J].Environmental Science and Pollution Research,2016,23(13):12922-12931.
[4] 梁佩筠,许超,吴启堂,等.淹水条件下控释氮肥对污染红壤中重金属有效性的影响[J].生态学报,2013,3(9):2919-2929.[LIANG Pei-jun,XU Chao,WU Qi-tang,etal.Effect of Different Controlled-Release Nitrogen Fertilizers on Availability of Heavy Metals in Contaminated Red Soils Under Waterlogged Conditions[J].Acta Ecologica Sinica,2013,33(9):2919-2929.]
[5] 楼玉兰,章永松,林咸永.氮肥对污泥农用后土壤中重金属活性的影响[J].上海环境科学,2004(1):32-36.[LOU Yu-lan,ZHANG Yong-song,LIN Yan-yong.An Effect of Nitrogenous Fertilizers on Activity of Heavy Metals in Sludge Applied Soil[J].Shanghai Environmental Sciences,2004(1):32-36.]
[6] BOLAN N S,ADRIANO D C,NAIDU R.Role of Phosphorus in (Im)Mobilization and Bioavailability of Heavy Metals in the Soil-Plant System[J].Reviews of Environmental Contamination and Toxicology,2003,177:1-44.
[7] 徐明岗,刘平,宋正国,等.施肥对污染土壤中重金属行为影响的研究进展[J].农业环境科学学报,2006,25(增刊1):328-333.[XU Ming-gang,LIU Ping,SONG Zheng-guo,etal.Progress in Fertilization on Behavior of Heavy Metals in Contaminated Soils[J].Journal of Agro-Environment Science,2006,25(Suppl.1):328-333.]
[8] 肖振林,王果,黄瑞卿,等.酸性土壤中有效态镉提取方法研究[J].农业环境科学学报,2008,27(2):795-800.[XIAO Zhen-lin,WANG Guo,HUANG Rui-qing,etal.Extraction Method for Available Cadmium in Acid Soils[J].Journal of Agro-Environment Science,2008,27(2):795-800]
[9] 吴烈善,曾东梅,莫小荣,等.不同钝化剂对重金属污染土壤稳定化效应的研究[J].环境科学,2015,36(1):309-313.[WU Lie-shan,ZENG Dong-mei,MO Xiao-rong,etal.Immobilization Impact of Different Fixatives on Heavy Metals Contaminated Soil[J].Environmental Science,2015,36(1):309-313.]
[10] 李剑睿,徐应明,林大松,等.水分调控和钝化剂处理对水稻土镉的钝化效应及其机理[J].农业环境科学学报,2014,33(7):1316-1321.[LI Jian-rui,XU Ying-ming,LIN Da-song,etal.Immobilization of Cadmium in a Paddy Soil Using Moisture Management and Amendments[J].Journal of Agro-Environment Science,2014,33(7):1316-1321.]
[11] 孙约兵,王朋超,徐应明,等.海泡石对镉-铅复合污染钝化修复效应及其土壤环境质量影响研究[J].环境科学,2014,35(12):4720-4726.[SUN Yue-bing,WANG Peng-chao,XU Ying-ming,etal.Immobilization Remediation of Cd and Pb Contaminated Soil:Remediation Potential and Soil Environmental Quality[J].Environmental Science,2014,35(12):4720-4726.]
[12] SIMMLER M,CIADAMIDARO L,SCHULIN R,etal.Lignite Reduces the Solubility and Plant Uptake of Cadmium in Pasturelands[J].Environmental Science & Technology,2013,47(9):4497-4504.
[13] SUN Y B,SUN G H,XU Y M,etal.Evaluation of the Effectiveness of Sepiolite,Bentonite,and Phosphate Amendments on the Stabilization Remediation of Cadmium-Contaminated Soils[J].Journal of Environmental Management,2016,166:204-210.
[14] 赵晶,冯文强,秦鱼生,等.不同氮磷钾肥对土壤pH和镉有效性的影响[J].土壤学报,2010,47(5):953-961.[ZHAO Jing,FENG Wen-qiang,QIN Yu-sheng,etal.Effect of Apply Cation of Nitrogen,Phosphorus and Potassium Fertilizers on Soil pH and Cadmium Availability[J].Acta Pedologica Sinica,2010,47(5):953-961.]
[15] 王朋超,孙约兵,徐应明,等.施用磷肥对南方酸性红壤镉生物有效性及土壤酶活性影响[J].环境化学,2016,35(1):150-158.[WANG Peng-chao,SUN Yue-bing,XU Ying-ming,etal.Effects of Phosphorous Fertilizers on Cd Bioavailability and Soil Enzyme Activities in South Acidic Red Soil[J].Environmental Chemistry,2016,35(1):150-158.]
[16] ADRIANO D C,WENZEL W W,VANGRONSVELD J,etal.Role of Assisted Natural Remediation in Environmental Cleanup[J].Geoderma,2004,122(2/3/4):121-142.
[17]SIEBERS N,SIANGLIW M,TONGCUMPOUAND C.Cadmium Uptake and Subcellular Distribution in Rice Plants as Affected by Phosphorus:Soil and Hydroponic Experiments[J].Journal of Soil Science and Plant Nutrition,2013,13(4):833-844.
[18] 刘昭兵,纪雄辉,彭华,等.磷肥对土壤中镉的植物有效性影响及其机理[J].应用生态学报,2012,23(6):1585-1590.[LIU Zhao-bing,JI Xiong-hui,PENG Hua,etal.Effects of Phosphorous Fertilizers on Phytoavailability of Cadmium in Its Contaminated Soil and Related Mechanisms[J].Chinese Journal of Applied Ecology,2012,23(6):1585-1590.]
[19] GAMBRELL R P.Trace and Toxic Metals in Wetlands:A Review[J].Journal of Environmental Quality,1994,23(5):883-891.
[20] 胡星明,袁新松,王丽平,等.磷肥和稻草对土壤重金属形态、微生物活性和植物有效性的影响[J].环境科学研究,2012,25(1):77-82.[HU Xing-ming,YUAN Xin-song,WANG Li-ping,etal.Effects of Phosphate Fertilizer and Rice Straw on Soil Heavy Metal Fraction,Microbial Activity and Phytoavailability[J].Research of Environmental Sciences,2012,25(1):77-82.]
[21] 晏哲,高志强,罗真华,等.不同钾肥对几种烟草吸收累积土壤镉的影响[J].环境化学,2016,35(9):1913-1920.[YAN Zhe,GAO Zhi-qiang,LUO Zhen-hua,etal.Effect of Potassium Fertilizers on the Uptake of Soil Cadmium by Flue-Cured Tobaccos[J].Environmental Chemistry,2016,35(9):1913-1920.]
[22] ZHAO Z Q,ZHU Y G,LI H Y,etal.Effects of Forms and Rates of Potassium Fertilizers on Cadmium Uptake by Two Cultivars of Spring Wheat (TriticumaestivumL.)[J].Environment International,2004,29(7):973-978.
[23] 陈苏,孙丽娜,孙铁珩,等.钾肥对镉的植物有效性的影响[J].环境科学,2007,28(1):182-188.[CHEN Su,SUN Li-na,SUN Tie-heng,etal.Influence of Potassium Fertilizer on the Phytoavailability of Cadmium[J].Environmental Science,2007,28(1):182-188.]
