阻塞性睡眠呼吸暂停综合征并胃食管反流病的影响因素研究
2018-06-12麦热哈巴哈力克赵燕霞杨晓红
麦热哈巴•哈力克,赵燕霞,杨晓红
阻塞性睡眠呼吸暂停综合征(obstructive sleep apnea syndrome,OSAS)是气道狭窄或阻塞引起的呼吸暂停和/或通气不足,可严重影响患者的生活质量。OSAS患者常因连续吸气而导致胸腔压力降低、横膈压力升高,呼吸道阻塞引起深吸气,导致负压升高,进而诱发或加重胃食管返流病(gastroesophageal reflux disease,GERD)[1-2]。GERD是一种胃内容物反流引起的不适症状或并发症。据统计数据显示,西方国家GERD发病率为10%~20%[3]。GERD除具有胃部烧灼感、反酸等典型临床症状外,还表现为反流性咳嗽和/或哮喘等呼吸系统症状,严重者甚至并发睡眠障碍或OSAS[4]。WISE等[5]研究结果显示,约58.6%的OSAS患者伴有GERD症状,OSAS与GERD相互影响并互为因果[6]。本研究旨在分析OSAS并GERD的影响因素,现报道如下。
1 资料与方法
1.1 一般资料 选取2011年3月—2017年6月在新疆维吾尔自治区人民医院呼吸科就诊的OSAS并GERD患者98例作为观察组,均符合OSAS诊断标准[7]及GERD诊断标准[8],另按照体质指数(BMI)(BMI±1.5 kg/m2)1:2比例匹配单纯OSAS患者196例作为对照组。纳入标准:(1)年龄18~75岁;(2)临床资料完整。排除标准:(1)有呼吸道正压通气(CPAP)治疗史或咽喉部整形手术史者;(2)合并上呼吸道疾病、严重心肺疾病者;(3)第1秒用力呼气容积(FEV1)/用力肺活量(FVC)<70%者;(4)合并重症肌无力、格林巴雷综合征等神经肌肉疾病及低钾血症者。
1.2 观察指标
1.2.1 临床资料采集 采集两组患者临床资料,包括年龄、性别、BMI、颈围、打鼾时间、打鼾家族史、冠心病病史、糖尿病病史、高血压病史、咽腔狭窄、扁桃体肿大情况。
1.2.2 睡眠呼吸监测结果 所有患者行夜间睡眠呼吸监测(PSG),监测系统包括脑电图、心电图、胸腹部呼吸运动监测系统、氧饱和度监测系统,记录睡眠呼吸紊乱指数(apnea hypopnea index,AHI)、呼吸暂停指数(apnea index,AI)、最长呼吸暂停时间(longest apnea time,LAT)、平均呼吸暂停时间(mean apnea time,MAT)、夜间最低血氧饱和度(lowest oxygen saturation,LSaO2)、夜间平均血氧饱和度(mean oxygen saturation,MSaO2)、血氧饱和度<90%时间占监测总时间的百分比(TS90%)。
1.3 统计学方法 采用SPSS 22.0统计软件进行数据处理,符合正态分布的计量资料以(±s)表示,两组比较采用两独立样本t检验;不符合正态分布的计量资料以M(QR)表示,采用秩和检验;计数资料分析采用χ2检验;OSAS并GERD的影响因素分析采用多因素Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床资料比较 两组患者年龄、性别、BMI、颈围、打鼾时间、打鼾家族史、冠心病病史、糖尿病病史、高血压病史、咽腔狭窄者所占比例、扁桃体肿大者所占比例比较,差异无统计学意义(P>0.05,见表1)。
2.2 两组患者睡眠呼吸监测结果比较 观察组患者AHI、AI及TS90%高于对照组,LAT、MAT长于对照组,LSaO2和MSaO2低于对照组,差异有统计学意义(P<0.05,见表2)。

表1 两组患者临床资料比较Table 1 Comparison of general information between the two groups
2.3 影响因素分析 将表1~2中有统计学差异的指标作为自变量,将GERD作为因变量(变量赋值见表3)进行多因素Logistic回归分析,结果显示,AHI、AI、LAT、LSaO2、MSaO2是OSAS并GERD的独立影响因素(P<0.05,见表 4)。

表3 变量赋值Table 3 Variable assignment

表4 OSAS并GERD患者影响因素的多因素Logistic回归分析Table 4 Multivariate Logistic regression analysis on influencing factors of GERD in patients with OSAS
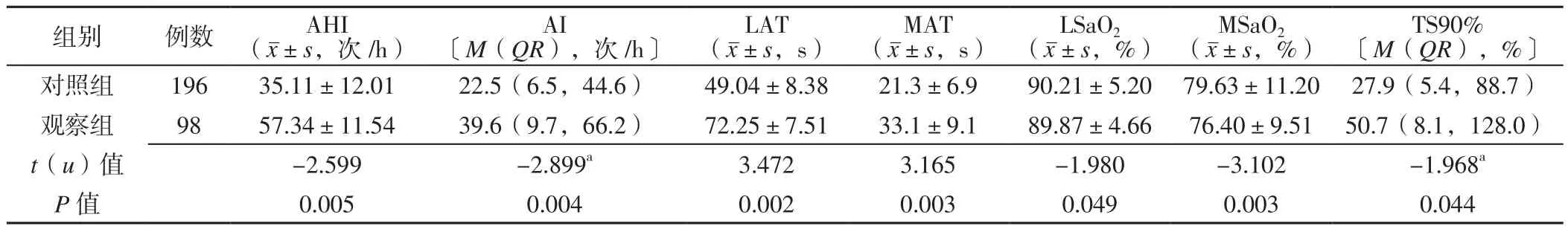
表2 两组患者睡眠呼吸监测结果比较Table 2 Comparison of sleep respiratory monitoring results between the two groups
3 讨论
OSAS和GERD是临床常见疾病,二者具有相似的发病机制。季锋等[9]研究结果显示,腹腔胃底折叠术能有效改善GERD及OSAS症状。ORR等[10]研究证实,OSAS严重程度与GERD内镜下病变程度有关,且睡眠呼吸暂停发作频繁阶段与最长反流持续时间多有重叠,主要原因为OSAS患者睡眠时气道阻塞引起吸气时食管、胸腔负压上升,导致胃内容物反流;GERD患者酸性反流物可直接或间接加重气道痉挛、呼吸道炎症,进而促发OSAS。目前,OSAS与GERD相似的发病机制尚未完全明确,但肥胖是GERD及OSAS共同危险因素已被临床证实[6]。肥胖者食管酸暴露增加,反流性食管炎与食管裂孔疝发生率随之升高[11];此外,肥胖者颈部脂肪沉积导致上气道狭窄,睡眠时软腭松弛,舌根肥大后置,咽腔气道更易发生塌陷而增加OSAS发生风险[10]。本研究对照组是按照BMI进行配对,以减少混杂、偏倚因素。
本研究结果显示,观察组患者AHI、AI及TS90%高于对照组,LAT、MAT长于对照组,LSaO2和MSaO2低于对照组,提示呼吸暂停和缺氧可能与OSAS并GERD有关。既往研究结果显示,口服抑酸类药物能有效控制OSAS并GERD患者GERD症状,减轻咽喉部水肿,降低 AHI[10,12]。SHEPHERD 等[2]研究结果显示,GERD患者酸性食物反流诱发喉痉挛,间接刺激食管远端黏膜感受器而使迷走神经兴奋,引起支气管痉挛,加重OSAS。DOMBKOWSKI等[13]研究结果显示,缺氧可有效降低胃食管括约肌收缩频率,血管活性肽、胰高血糖素样肽升高并作用于消化道,引起消化道括约肌松弛及胃排空减慢,进而增加胃内容物反流频次,诱发或加重GERD。本研究多因素Logistic回归分析结果显示,AHI、AI、LAT、LSaO2、MSaO2是 OSAS 并 GERD 的独立影响因素。AHI、AI、LAT是反映睡眠结构指标,LSaO2可反映低氧血症严重程度,MSaO2可反映机体外周血运输氧及存储氧能力[14],因此OSAS并GERD可能与反复低氧、睡眠结构紊乱有关。分析OSAS并GERD的机制可能如下:(1)缺氧:OSAS患者睡眠期间上呼吸道易发生塌陷、阻塞、舌根后坠,导致气道阻力增加及低氧血症;(2)胸-腹压力差增大:连续用力吸气导致胸腔压力降低、横膈压力升高,而呼吸道阻塞后深吸气可导致负压升高,食管内负压增加;(3)食管酸清除能力降低:夜间睡眠时唾液分泌基本停止,中和物减少,食管酸清除能力下降,故食管酸度增加;(4)夜间反复觉醒:OSAS患者因夜间憋醒而导致食管下括约肌一过性松弛,进而诱发或加重GERD[1]。
综上所述,AHI、AI、LAT、LSaO2、MSaO2是OSAS并GERD的独立影响因素,应积极采取干预措施改善OSAS患者低氧血症及睡眠结构紊乱,以有效预防GERD的发生。
