烟草秸秆低聚木糖的制备和纯化
2018-05-14芦广银吴福芳王珅刘文捷马扩彦戴亚盛良全
芦广银 吴福芳 王珅 刘文捷 马扩彦 戴亚 盛良全

摘要:为优化烟草秸秆低聚木糖制备参数,采用碱解方法提取木聚糖、酶解法制备低聚木糖以及单因素实验法考察了常见因素对工艺的影响。结果表明,木聚糖提取条件为;2.000 g秸秆粉末(≤100目)浸没于20.00 mL浓度为24%NaOH(m/v)和1%NaBH4m/v)碱液中,70℃条件下浸提4h,滤液加3倍乙醇体积用量进行醇沉以及0.2倍乙酸体积用量进行中和。制备低聚木糖的条件为:溶液pH为5.50,温度40℃,时间6h,木聚糖溶液(20 mg/mL)10 mL,木聚糖酶液(0.6%,m/v4.1 U/mL)20 mL。低聚木糖分离提纯条件为:阳离子树脂柱分离纯化,填充高度18.0 cm.直径为4.5 cm:纯化液用高效液相色谱进行定性定量分析。通过上述方法得到的低聚木糖产品纯度较高,对工业制备低聚木糖工艺优化有一定的参考价值。
关键词:烟草秸秆;木聚糖;低聚木糖;纯化
低聚木糖又称木寡糖,由2~7个D-木糖以β-1,4一糖苷键结合而成,以木二糖和木三糖为主,有较强的热稳定性和耐酸性,能够促进肠道内双歧杆菌的增殖,有益于肠胃健康,还有润肠通便,提高免疫力、抗肿瘤、降低血压、血糖、血清胆固醇,防龋齿、清口臭、促进钙吸收等生物学作用,可以用于功能性保健食品中:木聚糖是半纤维素的主要成分,是一种复杂的存在于植物细胞壁的多聚五碳糖,约占植物细胞干重的15%~30%,碳水化合物含量丰富,是自然界中丰富的可再生资源。国内外研究制备低聚木糖的方法主要有酸水解法、热水抽提法、微波降解法、酶解法。酸水解法是利用硫酸或者盐酸直接作用于木聚糖粗品使其发生降解反应,反应周期短、降解效果好,但由于是强酸参与反应,反应进行程度难以控制、容易腐蚀设备以及生成大量有害的副产物,例如糠醛酸等,所以不适宜低聚木糖的产业化生产:热水抽提法以水为原料,通过自水解法制备低聚木糖,但此法需要耐热耐压设备,生产成本高且产率低:微波辅助酸水解法能够更有效地促进酸水解,但仍存在生产成本高和反应不完全的问题:酶解法通过木聚糖酶将木聚糖降解为低聚木糖,木聚糖酶是一种以内切方式作用于木聚糖的β-1,4-糖苷键从而降解木聚糖的水解酶,此法操作简单、副产物少,为后续低聚木糖的分离纯化提供了便利,适合工业上大规模制备低聚木糖。初步统计,我国秸秆年产量达9亿t,综合利用率不到40%,秸秆的综合利用可以解决资源浪费和环境污染问题,国内外研究者致力于从玉米芯、稻壳等原材料中制备低聚木糖,利用烟草秸秆制备低聚木糖的研究鲜有报道。因此本文主要研究从烟草秸秆中制备低聚木糖以及低聚木糖的分离纯化,以期为烟草秸秆的综合利用提供新思路。
1材料与方法
1.1主要试剂和仪器
烟草秸秆生产地:安徽省阜阳市颍泉区周棚镇:生产年份:2016年6月:成分组成:烟草秸秆中纤维素含量42.72%,半纤维素含量24.14%,木质素含量23.01%:
试剂氢氧化钠(AR,西陇化工股份有限公司)、三水合乙酸钠(AR,西陇化工股份有限公司)、冰醋酸(纯度大于99%,天津博迪化工股份有限公司)、工业酒精(95%)、3,5一二硝基水杨酸、苯酚、无水亚硫酸钠、硼氢化钠(纯度大于98%,上海麦克林生化股份有限公司)、酒石酸钾钠、木聚糖酶(纯度大于97%,上海源叶生物科技有限公司)、木糖(纯度大于99.0%,上海展云化工有限公司)、木二糖(纯度大于98%,东京化成工业株式会社)、阳离子树脂、甲醇(色谱级,上海星可高纯溶剂有限公司)、乙腈(色谱级,上海星可高纯溶剂有限公司)。
主要仪器:YB-500A型高速多功能粉碎机(永康市速锋工贸有限公司):UP型超纯水机(优普仪器有限公司):恒温水浴振荡器(南京先欧仪器制造有限公司):SHB-IIIS循环水式多用真空泵(郑州长城科工贸有限公司):PHS-3C型pH计(上海仪电科学仪器股份有限公司);FU-1901型双光束紫外分光光度计(北京普析通用仪器有限责任公司):YL9100高效液相色谱系统;YL9181蒸发光散射检测器(ELSD)(托摩根生物科技有限公司)。
1.2实验流程
1.2.1木聚糖的提取
利用高速多功能粉碎機将烟草秸秆粉碎成粉末,过100目筛,置于干燥洁净的烧杯中,60℃下烘干备用。称取2.000 0 g秸秆粉末于250 mL锥形瓶中,并加入16.00 mL 24%(m/v)功NaOH和1%(m/v)功NaBH4混合溶液,密封后于70℃的恒温水浴振荡器中振荡反应(振荡速度100 r/min)4h,3000 r/min离心20min。取上清液,沉淀用适量蒸馏水洗涤并真空抽滤2次,合并2次滤液于500 mL烧杯中进行浓缩,加入3倍体积的工业乙醇沉淀,再加入0.2倍体积的冰醋酸中和。醇沉完成后真空抽滤,将所得滤渣60℃条件下干燥6 h,即得到黄褐色木聚糖粗产品(图1)。
1.2.2木聚糖酶的配制(0.6%,m/V)
精确称取0.060 0 g的木聚糖酶于洁净的小烧杯中,并加入40.00 mL的乙酸一乙酸钠缓冲液(pH为5.50),磁力搅拌30 min,用pH5.50的缓冲液定容至100.00mL,4℃条件下保存1周,备用。
1.2.3木聚糖的配制(20.00 mg/mL)
精确称取2.000 0 g烟草木聚糖粉末于小烧杯中,并加入40mL的乙酸一乙酸钠缓冲液(pH 5.50),磁力搅拌30min,用pH 5.50的缓冲液定容至100.00 mL,4℃条件下保存。
1.2.4低聚木糖的制备吸取1.2.3中所述木聚糖溶液和1.2_2中所述木聚糖酶液(0.6%,m/V,酶活力为4.1 U/mL)各10.00 mL,再用0.10 mol/L pH5.50的缓冲液定容至30.00 mL,40℃水浴酶解6 h后,100℃条件下5min灭活。
1.2.5还原糖的测定
1.2.6低聚木糖的分离纯化
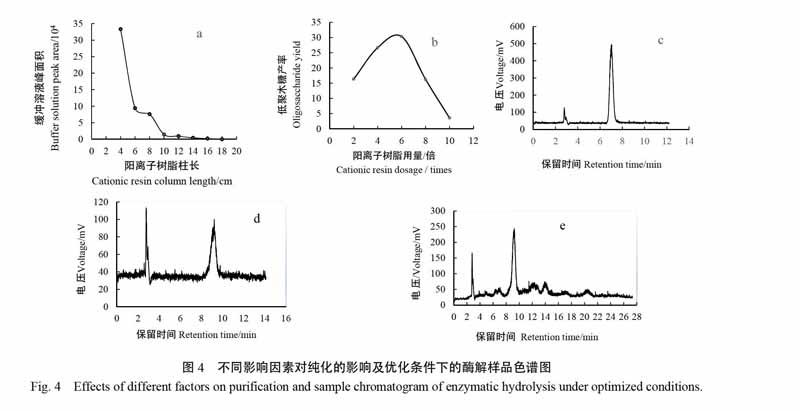
酶解液采取过柱脱盐处理,分别通过阴离子树脂和阳离子树脂柱进行对比发现,阳离子树脂更能有效地脱盐。将经灭酶处理并冷却至室温的酶解液通过阳离子树脂柱进行脱盐处理,0.45 gm滤头过滤后采用HPLC进样检测分析。
(1)色谱条件:色谱柱,安捷伦ZORBAXCarbohydrate(4.6 mmx250mm,5μm)(南昌捷岛科学仪器有限公司):流动相,乙腈/水(V/V=75/25);流速1.0mL/min:恒温器温度25℃:ELSD SprayChamber温度30℃:Drift Tube温度60℃:载气为高纯氮(>99.999%),压力0.5 MPa趱样量20μL。
(2)低聚木糖的浓度计算公式:
(3)阳离子树脂柱长及用量对脱盐的影响:分别取8份酶解后的溶液(25 mL)以流速为1.6mL/min经过填充高度为4.0-8.0 cm、直径为4.5 cm(面积为20.25兀)和体积用量比为2-10倍的阳离子交换树脂柱(732,下同)进行脱盐处理。
1.2.7试验条件优化分别按照1.2.1、1.2.4和1.2.6的方法,选择影响木聚糖提取、酶解和低聚木糖分离纯化的常见因素,进行单因素试验,以确定上述反应的最优条件。
2结果
2.1木聚糖提取条件的优化
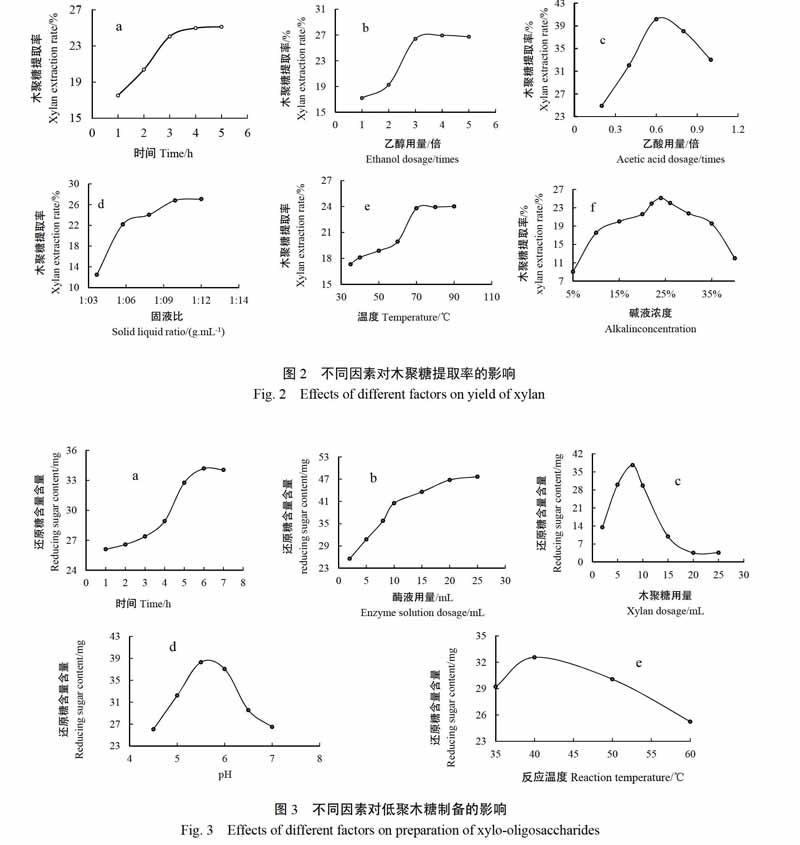
图2表明,在1~4 h内随着提取时间的增加,木聚糖提取率快速增加,而4 h以后提取率增加趋势不明显。在使用1~3倍乙醇体积进行醇沉时,随着乙醇用量的增加,木聚糖的提取率也在快速增加,之后趋于稳定。随着乙酸用量增加,木聚糖提取率大幅增加,0.6倍体积乙酸时,木聚糖提取率最高达到40.17%,但产品颜色加深,杂质增加(见讨论),考虑到产品纯度,采用添加0.2倍体积乙酸中和碱液,此时木聚糖提取率达到24.89%。在固液比为1:10之前,木聚糖提取率随着碱液体积的增加而快速增加,之后趋于稳定。碱解温度在35~70℃,木聚糖提取率快速增加,之后趋于稳定。NaOH浓度在5%-24%(m/v)时,木聚糖提取率快速增加,在浓度为24%时达最大值,高于24%后木聚糖提取率下降。
综合以上结果,优化的木聚糖提取条件为:浓度为24%(m/v)NaOH和1%(m/v)NaBH4的碱液,固液比1:10(m/v),水浴70℃,时间4 h,3倍乙醇体积醇沉和0.2倍乙酸体积中和。
2.2木聚糖制备低聚木糖的酶解条件
图3表明,在1-6 h时间内,随着酶解时间的延长,还原糖含量逐渐增加,之后趋于稳定:酶添加量在2~20 mL(0.6%,4.1 U/mL)时,还原糖含量逐步增加,为20 mL时达到最大值,之后趋于稳定:木聚糖溶液(20 mg/mL)添加量在2~10 mL时,还原糖含量逐渐增加,10 mL达到最大值,之后还原糖量逐步降低:随着pH值的增加,还原糖含量先增加后降低,溶液pH为5.50时,还原糖含量最高:在35-40℃范围内,随着温度的升高,还原糖含量逐渐增加,超过50℃后,还原糖含量逐降低。
综合以上结果,优化的低聚木糖制备条件为:10 mL木聚糖溶液(20 mg/mL),20 mL木聚糖酶液(0.6%,4.1U/mL),缓冲溶液体系pH为5.50,水浴温度40℃,时间6 h。
2.3低聚木糖的分离纯化
本研究采用缓冲溶液色谱峰的面积变化来表征脱盐效果,峰面积越小说明脱盐效果越好,保留时间3 min左右。图4 a为阳离子树脂柱填充高度对脱盐的影响,当树脂柱填充高度高于10 cm时,阳离子树脂柱脱盐效果明显,当高于18 cm,此时阳离子树脂柱可将酶解液中的盐完全脱去:图4 b为阳离子树脂用量对低聚木糖产率的影响,当酶解液分别通过2、4、6、8、10倍体积阳离子树脂柱的低聚木糖的产率分别为16.36%、26.66%、30.32%、16.26%、3.60%,综合脱盐效果和低聚木糖产率两方面考虑,选择用6倍体积的阳离子树脂柱处理酶解液,此时脱盐效果较好,且木糖与木二糖能较好的分开:图4 c为3 mg/mL木糖标准溶液色谱图,保留时间7.5min左右:图4d为0.6mg/mL木二糖标准液色谱图,保留时间9.5 min左右:图4 e为酶解液过6倍体积树脂柱后的色谱图,3 min的色谱峰面积很小,说明此法脱盐效果好,图中每个色谱峰分别表示的是木糖、木二糖、木三糖、木四糖、木五糖、木六糖,其中木二糖含量最高。
3讨论
提取时间增加,烟草秸秆半纤维素(主要是木聚糖)与其他物质之间的共价键容易被破坏,木聚糖充分溶解于碱液中,木聚糖提取率快速提高,结果表明4 h后提取率趋于稳定:而长时间处于高温环境,易生成大量的单糖,故4 h为较适宜的时间。随着乙酸用量增加,木聚糖易出现乙酰化反应,且可溶性木质索等物质在酸性环境中易沉淀,之后采用酸解实验进行木聚糖粗品纯度鉴定,发现产品纯度随乙酸用量增加逐步降低,颜色加深,易潮解有异味,黏性较大,0.2体积用量的产品纯度最高,故使用0.2倍体积用量的乙酸中和碱液。溶液温度升高,增加溶剂和木聚糖分子的动能,加快分子扩散运动,原料充分溶胀,之后温度继续升高,木聚糖提取率增加不到0.5%,但會加重糖的水解和脱水作用,生成一定量的有害物质如糠醛等,颜色加深,因此70℃为较适宜的水浴温度。碱液浓度增加,水解作用增强,半纤维素与纤维素、木质素之间的共价键容易被破坏,但过高的碱液浓度会破坏木聚糖分子的长链结构,图中结果表明,24%的NaOH溶液最为适宜。
由于木聚糖酶与木聚糖分子接触不够充分,随着水解时间增加,还原糖含量逐渐增加,超过6 h后,还原糖含量变化不再明显,说明木聚糖降解完全,故选择的最佳酶解时间为6 h:木聚糖溶液添加量超过10 mL后,还原糖含量开始下降,这是由于木聚糖溶液的黏度较大,不利于木聚糖酶及木聚糖分子的扩散运动,影响彼此接触。pH和温度对蛋白质的结构有影响,所以每一种酶都有一个最佳pH和温度,结果表明该木聚糖酶的最适pH和温度分别为5.50的乙酸一乙酸钠缓冲液和40℃。
提取木聚糖和制备低聚木糖的方法很多,但都存在一定的局限性。酸法提取木聚糖会产生大量的单糖和副产物,反应速度快且难以控制:微波法工艺不成熟,成本高:高温蒸煮法成本高,周期长,副产物多:蒸汽爆破法反应温度太高,产品颜色太深:碱解法得到的木聚糖产率最高,试验中碱性废液处理得当,对环境污染小,与其他方法相比具有产率高,操作简单,成本低等优点。酸水解法制备低聚木糖反应迅速,生成大量木糖:热水抽提法得到的产品颜色深,不利于后续的分离纯化:微波降解法成本高,对设备要求比较严格:与其他方法相比,酶解法反应条件温和,具有专一性,目前我们实验室基本实现了木聚糖酶的固定化,降低了实验成本。后期将通过放大试验,继续探究碱解和酶解法工业上大规模生产低聚木糖以及采用膜分离技术对其进一步分离纯化。
4结论
本研究采用碱解法从烟草秸秆中提取木聚糖和酶解法制备低聚木糖,与其他方法相比,具有简便、快速、安全、污染小的特点,原料(烟草秸秆)来源广泛,成本低,可以循环利用,为烟草秸秆的综合利用提供了新思路,对实现低聚木糖的大规模生产具有一定的参考价值。低聚木糖的纯化分离技术尚处在研究之中,接下来会尝试采用膜分离技术进行低聚木糖的分离纯化,以期掌握简便、快速、无污染的技术制备烟草秸秆低聚木糖,更好地综合利用烟草秸秆。
