高效液相色谱法同时测定介孔SiO2/脂质复合递药系统中紫杉醇、姜黄素的含量
2018-05-10栗婷婷徐彦军林珈好林德贵
栗婷婷,徐彦军,王 倩,林珈好,林德贵
(1.中国农业大学动物医学院,北京 海淀 100193;2.中国农业大学理学院,北京 海淀 100193)
1 仪器与药品
安捷伦1100高效液相色谱仪。TAX(纯度:99.5%);TAX对照品(美仑生物,批号20121213,纯度>99%);CUR(纯度:95%);CUR对照品(中国食品药品检定研究院,批号1100823-201405,纯度:98.9%);正硅酸四乙酯(分析纯,国药集团化学试剂有限公司);十六烷基三甲基溴化铵(化学纯,上海阿拉丁生化科技股份有限公司);大豆卵磷脂(德国Lipoid公司,纯度>94%);胆固醇(美国Amresco分装);甲醇(色谱纯,Fisher公司);乙腈、甲酸(色谱纯,Merck公司)。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液 取TAX、CUR对照品,用甲醇精确配制浓度为600 μg/mL的TAX、CUR混合对照品储备液,记为1号。移液管取1号储备液,以甲醇精确配制得 300 μg/mL、60 μg/mL、30 μg/mL、15 μg/mL、6 μg/mL、3 μg/mL、1.5 μg/mL 系列浓度TAX、CUR对照品溶液,标记为2至8号。各浓度对照品溶液均经0.22 μm微孔滤膜过滤至HPLC进样瓶。
2.1.2 供试品溶液 将3 mg TAX、30 mg CUR 及适量介孔SiO2(MSNs)加入20 mL氯仿中超声混匀。220 r/min摇床震荡19 h后 14 000 r/min离心20 min。 量取0.2 mL 上清,加1.8 mL 甲醇混匀,经0.22 μm滤膜过滤至HPLC进样瓶。药物总量减去上清中药物含量即药物载入量。
2.1.3 阴性对照溶液 精密称取处方量的MSNs,制备空白 MSNs,量取 0.2 mL 参照“2.1.2”项下操作,制备阴性对照溶液。
2.2 色谱条件与系统适用性 色谱柱:Eclipse XDB-C18 柱(150 mm ×4.6 mm,5 μm);流动相:A相为乙腈,B相为0.1%甲酸水溶液,梯度洗脱见表1;流速:1 mL/min;柱温:25℃;检测波长:227 nm;进样体积:5 μL。

表1 流动相梯度洗脱时间
结果见图l,TAX、CUR保留时间分别为14.95 min、14.4 min,峰型良好,无明显前延或拖尾。 分离度为2.81,理论塔板数与拖尾因子均符合要求。MSNs等辅料不影响二者检测。
南京明城墙是明太祖朱元璋(1328-1398)定都南京的产物和象征,是中国历史上唯—建造在江南的统一全国的都城城墙。
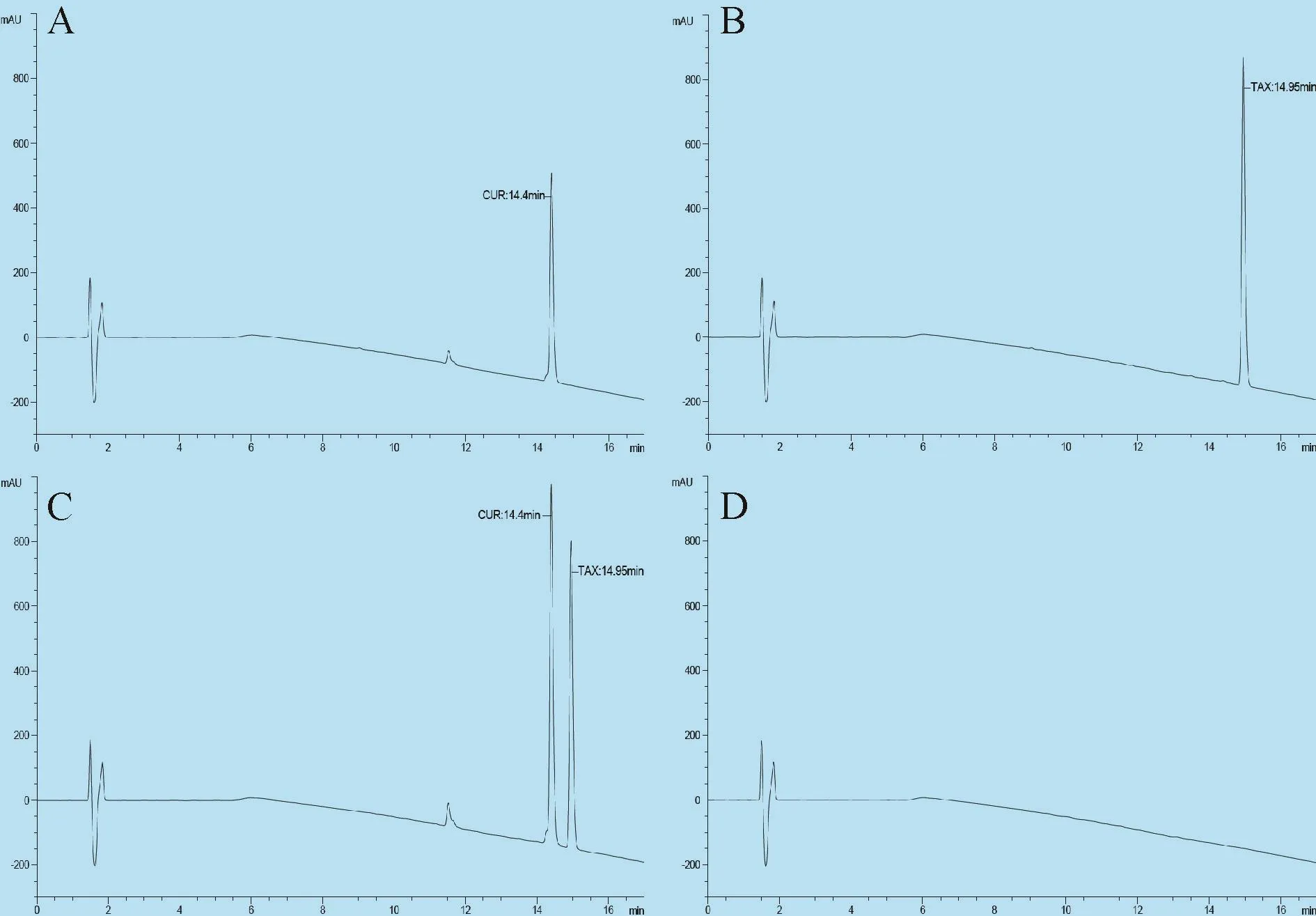
图1 专属性试验高效液相色谱图
2.3 标准曲线绘制 按2.2项下 HPLC方法,取2.1.1 项下 4~8 号(1.5~30 μg/mL)溶液各进样 3次,以峰面积平均值X为横坐标,浓度Y(μg/mL)为纵坐标,绘制标准曲线,回归统计。TAX低浓度回归方程(n=5):Y=(X-1.840 0)/10.860 1,R2=0.999 7。CUR低浓度回归方程(n=5):Y=(X+4.652 0)/10.3471,R2=0.999 9。 取2-6 号(6~300 μg/mL)溶液重复上述操作,得TAX高浓度回归方程(n=5):Y=(X-14.867 4)/10.277 5,R2=1.000 0。CUR高浓度回归方程(n=5):Y=(X+32.374 7)/11.9262,R2=0.999 9。 两药高、低浓度标准曲线见图2。
2.4 精密度试验 取 2.1.1项下 3号溶液(60 μg/mL),经 0.22 μm 滤膜过滤至 HPLC 进样瓶,以建立的HPLC方法,连续进样6次,每次5 μL,记录峰面积。结果TAX、CUR的RSD分别为0.63%、0.34%(n=6),均小于2%,说明此方法精密度良好。

图2 TAX、CUR标准曲线
2.5 稳定性试验 取2.1.1 项下3 号溶液(60 μg/mL),经0.22 μm滤膜过滤至HPLC进样瓶,以建立的 HPLC 方法,分别将样品在0、3、6、9、12、15、18、21 h室温进样测定,记录峰面积。结果TAX、CUR在室温21 h内的 RSD分别为 1.37%、1.76%(n=8),均小于2%,说明样品在21 h内检测性质稳定。
2.6 加样回收试验 取 300 μg/mL、60 μg/mL、6 μg/mL对照品溶液各 0.6 mL,加 0.6 mL 甲醇混匀,制得高、中、低浓度的TAX、CUR混合溶液,每个浓度平行操作3份,以建立的HPLC方法测定TAX、CUR含量,计算加样回收率,结果见表2。
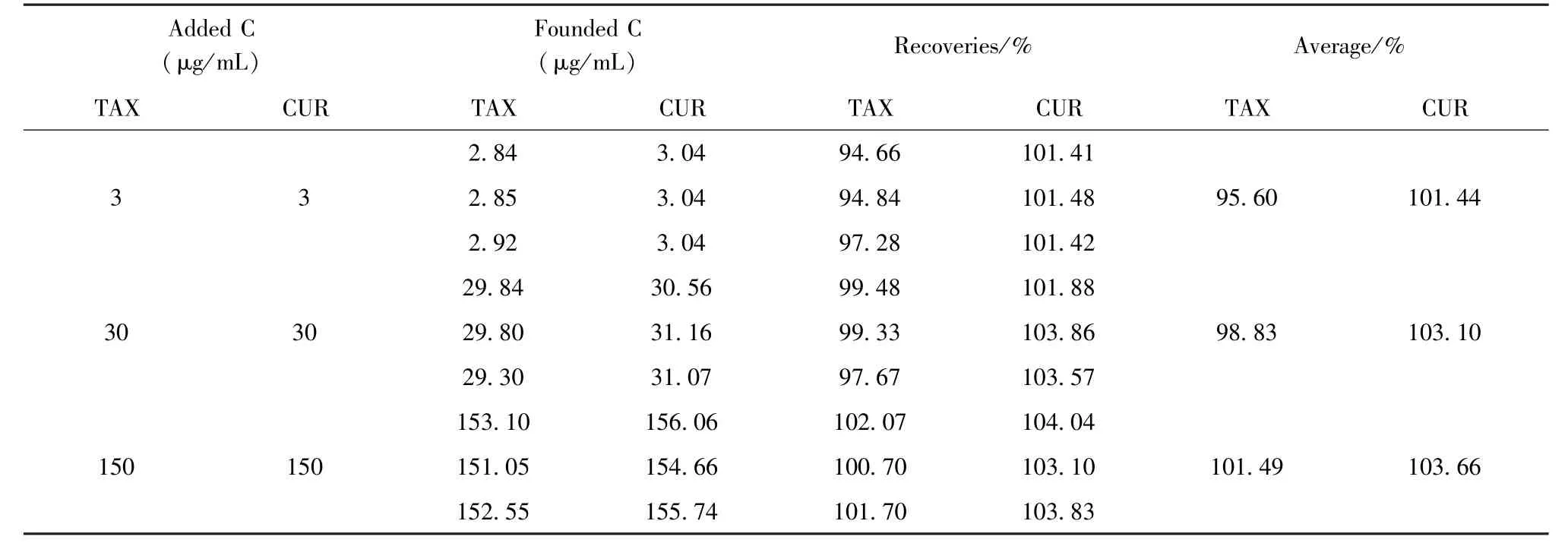
表2 加样回收率试验结果
高、中、低 3个浓度 TAX的 RSD值分别为1.53%、1.02%、0.70%,CUR 的 RSD 值分别为0.04%、1.04%、0.47%,均不超过 2%,方法回收率合格。
2.7 含量测定 取3批MSNs样品离心后上清各0.2 mL,分别按2.1.1项下方法制备供试品溶液,测定其中TAX、CUR含量。结果见表3,3批样品上清中 CUR 含量为(1 051.50 ±43.90)μg/mL(RSD=4.17%,n=3),TAX含量低于最低检测限,故以标准曲线最低浓度计算,为(15 ±0)μg/mL(RSD=0%,n=3)。
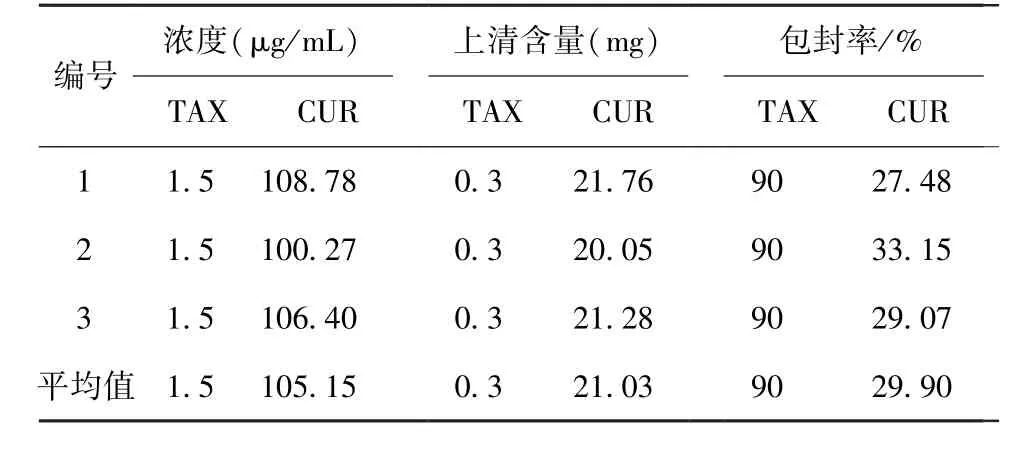
表3 MSNs中TAX、CUR含量及包封率
3 讨论
TAX在甲醇、乙醇、乙腈中的检测波长一般为227 nm左右,CUR在甲醇中的检测波长一般为420 nm左右。为能在同一色谱条件下同时测定TAX与CUR含量,我们在227 nm及420 nm左右摸索了多个检测波长,发现227 nm处两者均有较大吸收,故以其为本方法的检测波长。
选择色谱条件时,根据2010版药典及多篇参考文献[9-11],尝试多种方法。根据文献,检测TAX、CUR均常用C18色谱柱(250 mm或150 mm×4.6 mm,5 μm),考虑仪器条件,最终选择Eclipse XDB-C18柱(150 mm ×4.6 mm,5 μm)。 检测 TAX 常用甲醇、水、乙腈以适当比例组合作为流动相。检测CUR常用乙腈、4%~5%冰醋酸、水以适当比例组合作为流动相。且大多文献采用等度洗脱的方法。因此,我们最初尝试了甲醇、乙腈、甲酸等多种流动相及多种比例组合进行等度洗脱,发现两药不能很好的分离。在此基础上,进一步尝试梯度洗脱的方法,最终确定乙腈-0.1% 甲酸水梯度洗脱系统,分离效果最佳。
本研究建立了HPLC法同时测定TAX-CUR介孔SiO2/脂质复合递药系统中两药含量的方法,该方法操作简便、快速、准确、重复性好,可以用于TAX-CUR介孔SiO2/脂质复合递药系统的质量控制。
参考文献:
[1] Aigner J,Marme F,Smetanay K,et al.Nab-paclitaxel monotherapy as a treatment of patients with metastatic breast cancer in routine clinical practice[J].Anticancer research,2013,33(8):3 407-3 413.
[2] 陈萌.紫杉醇对犬乳腺肿瘤CHMp和CHMm细胞周期调控因子影响的研究[D].哈尔滨:东北农业大学,2012.
[3] Bayet-Robert M,Kwiatowski F,Leheurteur M,et al.Phase I dose escalation trial of docetaxel plus curcumin in patients with advanced and metastatic breast cancer[J].Cancer biology&therapy,2010,9(1):8-14.
[4] Hossain D M,Bhattacharyya S,Das T,et al.Curcumin:the multi-targeted therapy for cancer regression[J].Frontiers in bioscience(Scholar edition),2011,4:335-355.
[5] Si M,Zhao J,Li X,et al.Reversion effects of curcumin on multidrug resistance of MNNG/HOS human osteosarcoma cells in vitro and in vivo through regulation of P-glycoprotein[J].Chinese medical journal,2013,126(21):4 116-4 123.
[6] Sharma R A,McLelland H R,Hill K A,et al.Pharmacodynamic and pharmacokinetic study of oral Curcuma extract in patients with colorectal cancer[J].Clinical Cancer Research,2001,7(7):1 894-1 900.
[7] Gao X,Wang B,Wu Q,et al.Combined delivery and anti-cancer activity of paclitaxel and curcumin using polymeric micelles[J].Journal of biomedical nanotechnology,2015,11(4):578-589.
[8] Zhan Y,Chen Y,Liu R,et al.Potentiation of paclitaxel activity by curcumin in human breast cancer cell by modulating apoptosis and inhibiting EGFR signaling[J].Archives of pharmacal research,2014,37(8):1 086-1 095.
[9] 邓丽.新型二氧化硅—脂质递药系统用于口服递送抗肿瘤药物的研究[D].荣昌:西南大学,2014.
[10] Abouzeid A H,Patel N R,Torchilin V P.Polyethylene glycolphosphatidylethanolamine(PEG-PE)/vitamin E micelles for codelivery of paclitaxel and curcumin to overcome multi-drug resistance in ovarian cancer[J].International journal of pharmaceutics,2014,464(1):178-184.
[11] 陈娜,张祎捷,韩纪昌,等.ZS1肽修饰共载紫杉醇和姜黄素脂质体的构建及其体外靶向性和毒性[J].中国医药工业杂志,2014,45(8):754-757.
