两种微创术式治疗单纯腰椎间盘突出症的疗效比较
2018-05-02吴一民白明银和平李杨赵健
吴一民,白明,银和平,李杨,赵健
(内蒙古医科大学第二附属医院,内蒙古 呼和浩特 010030)
腰椎间盘突出症是骨科常见病、多发病,通过严格保守治疗后不能缓解症状的需要手术治疗。既往的传统后路开窗手术创伤大,肌肉软组织剥离严重,易引起术后下腰部慢性疼痛等并发症。内窥镜技术在腰椎间盘突出症微创治疗中发挥了不可取代的作用,尤其经皮椎间盘镜下髓核摘除术(microendoscopic discectomy,MED)和经椎间孔镜下髓核摘除术(percutaneous endoscopic lumbar discectomy,PELD)在国内得到迅猛发展,被广泛应用于各种类型腰椎间盘突出症的治疗[1-2]。本文回顾总结2012年5月至2015年2月我科随访完整的246例采用微创技术治疗单纯腰椎间盘突出症的患者资料。根据手术方式不同分为两组,A组120例选择椎间盘镜下髓核摘除术,B组126例选择经皮椎间孔镜下髓核摘除术。本研究旨在评估此两种微创手术治疗单纯腰椎间盘突出症患者的手术疗效及并发症情况,现报告如下。
1 资料与方法
1.1 一般资料 本组246例患者,男115例,女131例;年龄32~65岁,平均41.5岁。根据患者的临床表现、病理解剖及影像学表现采用两种微创手术方法,A组120例行后路显微内窥镜下髓核摘除术(microendoscopic discectomy,MED)治疗,B组126例行经皮椎间孔镜下髓核摘除术(percutaneous endoscopic lumbar discectomy,PELD)治疗。两组患者均有腰痛伴有一侧下肢或双侧下肢疼痛麻木的症状,经腰椎CT和MRI检查证实L3~4间盘突出症54例,L4~5间盘突出症112例,L5S1间盘突出症80例。病例选择标准:单节段游离型或包含型椎间盘突出;典型的腰部及下肢根性疼痛症状;系统保守治疗6个月以上,症状无明显缓解,严重影响患者工作和生活。排除标准:同时合并严重的腰椎不稳及滑脱;合并钙化及骨性狭窄;有骨折、肿瘤、感染等病史;合并严重的脊柱侧凸或后凸畸形需要手术干预者。
1.2 手术方法 A组根据患者情况采取硬膜外麻醉或全麻,俯卧位,屈髋屈膝各45°,腹部悬空。C型臂下定位手术间隙后记号笔标记,常规消毒铺巾。MED常规操作定位、建立工作通道,用MED专用椎板钳咬除上位椎板下缘和下位椎板上缘,摘除黄韧带进入椎管,使用神经剥离子探查后使用自动神经牵开器将神经根和硬脊膜一起牵开,显露突出椎间盘,间盘刀切开后即可完成髓核摘除,探查未见游离间盘、神经松紧适度后结束手术,后使用双氧水和碘伏冲洗清除炎性介质,减轻炎症反应,最后大量生理盐水对椎间隙及椎管进行冲洗后缝合并留置引流管,无菌贴粘贴。
B组患者俯卧于可透视的脊柱手术架上,屈髋屈膝45°,使腰椎后凸,腹部悬空。使用G形臂X线机透视下确定手术节段后使用记号笔在体表将穿刺位置标记好,常规消毒铺无菌巾。局部粘贴护皮膜,以穿刺点为中心使用0.5%利多卡因局部浸润麻醉,再使用长针一直穿刺到关节突关节部位继续局部麻醉。局部麻醉效果显现后使用孔镜专用穿刺长针在G型臂监测下经后外侧入路通过安全三角区向椎间盘后1/3穿刺。穿刺针进针点距离后正中线旁约11 cm左右,在侧位透视下应该与终板平行。当针尖正位位于椎弓根内缘连线部位,侧位位于椎体后半部即表示穿刺位置正确,此时进行椎间盘造影(造影剂采用亚甲蓝和碘海醇1︰1的比例混合)及疼痛诱发试验,再次验证诊断。退出穿刺针后距离后正中线14 cm处再次穿刺,当正位透视针尖位于椎弓根内缘连线处,侧位未超过椎体后缘连线即穿刺成功。留置导丝后使用扩张套管逐渐扩张,并使用空心骨钻将关节突腹侧部分切除,最后舌形工作套管沿扩张器推进到椎间盘,直到舌形工作套管末端紧压在纤维环表面。再次透视位置正确后取出扩张器,插入椎间孔镜观察椎间盘髓核和纤维环。退变髓核组织被酸性亚甲蓝优先染成蓝色,而纤维环保持未染色状态,在椎间孔镜下进行选择性摘除椎间盘髓核组织,同时用低温等离子刀头将纤维环及髓核组织消融处理,探查无游离间盘组织、神经根松紧适度后结束手术,局部冲洗,放置1 mL地塞米松后拔出工作套管,局部压迫后无菌贴粘贴。
1.3 术后处理 术后平卧6 h,常规应用神经营养药物和神经脱水肿药物(甘油果糖及地塞米松)3~5 d(防止神经根水肿后引起不适症状)。术后1周时复查腰椎CT或MRI,观察术后髓核摘除情况,同时指导患者进行床上直腿抬高及足背伸功能锻炼。A组术后7~10 d护腰保护下下地活动,B组术后3~5 d护腰保护下下床活动,两组患者3个月内避免剧烈运动及负重。
1.4 观察指标 术中连续监测患者的生命体征。患者术后1周复查腰椎CT或MRI。腰椎功能评分采用日本骨科协会(Japanese orthopaedic association,JOA)评分,所有病例手术前、术后及末次随访时均进行JOA评分(0~29分)。JOA评分改善率=(术后评分-术前评分)/(29-术前评分)×100%。记录两组患者术中出血量、手术时间、住院时间,并根据改良的Macnab标准评定两组优良率。
1.5 统计学分析 应用SPSS 10.0统计软件包进行分析,组间比较采用t检验,数据资料用均数±标准差表示,P<0.05为差异有统计学意义。
2 结 果
两组患者均获随访,随访时间15~18个月。其中A组2例患者因间盘较大且与硬膜囊黏连造成硬膜囊破裂,但通过止血纱布压迫后术后未见脑脊液漏,B组未发生任何并发症。A组术前、术后和末次随访时的JOA评分与B组比较,差异无统计学意义(P>0.05);A组JOA评分组间比较,差异有统计学意义(P<0.05)。B组JOA评分组间比较,差异有统计学意义(P<0.05),见表1。根据改良的Macnab标准评定,两组患者术后3个月和末次随访时近远期临床疗效相似,差异无统计学意义(P>0.05),但术中出血量、手术时间、住院时间等手术指标方面,PELD组均明显优于MED组,差异有统计学意义(P<0.05),见表2。

表1 两组患者JOA评分比较分)

表2 两组患者手术指标比较
典型病例一为45岁女性患者,2013年3月因腰部及左下肢疼痛麻木5个月入院,入院诊断为腰椎间盘突出症,术前CT示L5S1椎间盘突出巨大,偏向左侧,于2013年3月行MED手术,术后3个月复查CT示椎间盘髓核组织完全清除,局部硬膜囊和神经根无压迫,但仍可以看到椎板缺如,术后症状明显缓解(见图1~2)。典型病例二为36岁女性患者,2013年4月因腰部及右下肢疼痛麻木3个月入院,入院诊断为腰椎间盘突出症,术前MRI示L4~5椎间盘突出巨大,于2013年4月行PELD手术,术后1周复查MRI示椎间盘髓核组织完全清除,局部硬膜囊和神经根无压迫,椎板及关节突正常,术后疼痛症状缓解(见图3~4)。

图1 术前CT示L5S1椎间盘突出,偏向左侧

图2 术后3个月CT示椎间盘髓核组织完全清除

图3 术前MRI示L4~5椎间盘突出
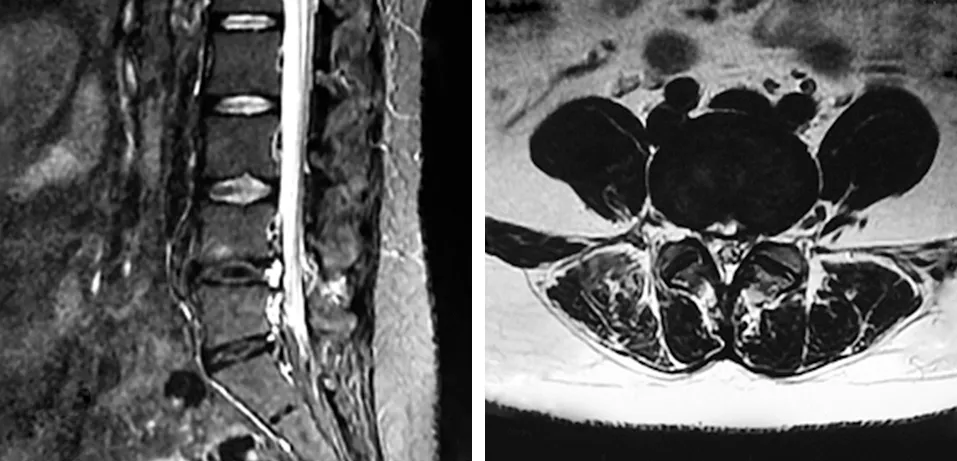
图4 术后1周MRI示椎间盘髓核组织完全清除
3 讨 论
腰椎间盘突出症是骨科常见病、多发病,约占腰腿疼痛患者的20%。系统保守治疗无效者需要手术治疗,本组病例也是在系统保守治疗无效后采用手术治疗。目前针对腰椎间盘突出症的治疗方法很多,尤其是微创治疗方法比较广泛,诸如等离子射频消融、经皮间盘切吸、经皮胶原酶溶盘、经皮臭氧溶解等方法均为间接减压,适应证比较局限,对于突出物较大、压迫严重的患者疗效往往达不到理想效果[3]。传统的后路开放手术,诸如椎板间开窗术、次全椎板切除术、全椎板切除术等,虽然效果比较理想,但是创伤较大,肌肉软组织剥离严重,术后恢复慢,也是引起术后慢性下腰部疼痛的主要原因,且手术需要切除部分关节突关节以及部分椎板,将来可能导致脊柱稳定性破坏和退变加速[4]。
国外学者Foley等[5]首次报道了MED技术,之后被引进国内并广泛推广,比较适合应用于单纯腰椎椎间盘突出症,此外还被应用于腰椎管狭窄、腰椎失稳、腰椎滑脱等腰椎退变性疾病中,被统称为内窥镜技术[6-7],但是MED治疗腰椎间盘突出症仍需要部分破坏脊柱的骨性结构以及后方的软组织,像传统开窗手术一样需要咬除椎板间隙上椎板下缘的骨质、下椎板上缘的骨质、一小部分关节突关节以及椎板间黄韧带,术后会引起患者下腰部疼痛,如果早期下床会出现神经根痛再发等并发症[8],同时还存在硬脊膜损伤、神经根损伤、硬膜外血肿、术中出血、一过性下肢肌力下降等并发症[2]。本研究中A组2例患者因为突出物较大,与硬膜囊黏连,造成硬膜囊破裂,通过止血纱布覆盖后未见术后脑脊液漏等并发症发生。
20世纪90年代美国学者Anthony Yeung医生首创杨氏脊柱内窥镜系统(Yeung endoscopic spine system,YESS)技术,尝试进行了经椎间孔入路手术,而椎间孔镜技术的应用发展改善了以往简单微创疗法的疗效,弥补了传统开放手术的不足,从而大大提高了腰椎间盘突出症的手术治疗效果。YESS技术的原理是使穿刺导管直接进入突出的椎间盘内,由内向外逐渐切除突出髓核进行减压[9-11]。2002年德国Hoogland教授在传统YESS技术基础上提出了经椎间孔脊柱内窥镜系统(transforaminal endoscopic spine system,TESSYS)技术,使经椎间孔镜手术技术进一步成熟完善[12]。THESSYS技术的原理是将工作导管直接置于突出椎间盘表面开始进行手术,由突出物中心向周围逐渐扩大,切除突出间盘组织,最后逐步延伸到椎间盘内进行清理。同时配合使用射频刀头可以将残留间盘组织彻底清理干净,从而达到理想的效果,对骨性结构不会有影响。但是椎间孔镜技术也有一些缺点,因为是水介质下进行,所以有时硬膜囊破裂、脑脊液漏等情况不能及时发现,初学者容易引起患者脊髓及神经根的损伤。同时椎间孔镜技术还有一些并发症,如术中出血、术后感觉异常、术后感染等[13-15]。对于术中出血,笔者认为多为椎间孔动静脉、硬膜囊附近静脉丛等引起,如果不能及时止血,出血过多会影响手术视野,从而影响手术进行,有时出血严重者转为MED手术或传统开放手术。如何避免出血就需要掌握手术部位的解剖层次,操作时动作轻柔,尤其是椎管、硬膜囊及神经根周围血管丛附近要细心操作,使用射频等离子进行彻底止血。术中患者下肢感觉异常多为手术过程干扰硬膜囊及神经根所致,尤其是突出髓核较大与神经根黏连时容易发生,术后对症给予神经脱水肿治疗后逐渐改善。术后椎间隙感染是非常严重的并发症,发生原因不外乎是无菌操作不规范、器械消毒不合格等,极少数情况下是穿刺针在穿刺过程中过度深入腹腔,造成继发污染。发生椎间隙感染时早期开始应用抗生素,如果效果不理想应及早进行手术清创引流。神经根损伤是最严重的并发症,常在穿刺定位、置扩张套管、摘除髓核等操作不当时发生,因此必须严格掌握脊柱神经解剖及手术操作技术,镜下仔细观察好解剖关系后再进行手术,在没有分清楚硬膜囊、神经根及突出间盘组织时绝对不可轻易咬除任何组织,一旦发生神经损伤将难以恢复,所以笔者认为术前进行碘海醇及亚甲蓝的混合液进行造影染色是非常必要的。
本研究中A、B两组患者根据临床表现、病理解剖及影像学表现采用上述两种微创手术方法,对照观察两组的临床效果。结果表明A组JOA评分术前为(18.3±1.2)分,术后为(22.7±1.1)分,末次随访时为(26.5±1.3)分,组间比较差异有统计学意义(P<0.05)。B组JOA评分术前(17.3±1.8)分,术后(24.9±1.3)分,末次随访时为(26.4±1.5)分,组间比较差异有统计学意义(P<0.05),但A、B两组各时间段JOA评分比较,差异无统计学意义(P>0.05)。根据改良的Macnab标准评定,术后3个月及末次随访时临床效果优良率A组分别为90.7%与94.3%,B组分别为89.6%与95.2%,两组数据相比较,差异无统计学意义(P>0.05)。通过手术前后JOA评分及改良的Macnab标准评定分析,两种微创技术效果不分伯仲。A、B两组术中出血量分别为(85±12)mL和(20±8)mL;A、B两组手术时间分别为(45±16)min和(52±14)min;A、B两组住院时间分别为(7±1.2)d和(3.9±1.7)d,住院时间以及术中的出血量等比较结果表明经皮穿刺椎间孔镜下髓核摘除术是一个更加理想的手术方法,相对于椎间盘镜技术它能做到更加微创,更加小的内环境干扰及骨性结构的破坏。分析其中原因主要是因为椎间孔镜技术使用的工作通道更加细,对周围软组织的影响小,术后疼痛轻,可以早下地活动。而后路显微内窥镜下髓核摘除术工作通道达到18 mm,且仍然需要咬除部分上下椎板及关节突内侧部分,相对损伤仍较大,术后患者疼痛程度较B组明显。相对后路椎间盘镜技术,椎间孔镜技术具有创伤更小、术后疼痛更轻、并发症更少、手术时间更短、术后恢复更快、可以早期下地活动等优点。但是要求骨科医生必须通过严格的基础训练和长时间的学习,严格掌握脊柱解剖及镜下手眼配合技术,熟练的掌握微创手术操作技巧才能完成[16]。
在掌握良好手术适应证的前提下,经皮椎间孔镜和后路椎间盘镜在治疗单纯腰椎间盘突出症中均能得到良好的临床效果。经皮穿刺椎间孔镜技术相对更加微创,术中出血更少,住院时间更短。此项技术值得临床推广应用。
参考文献:
[1]徐海栋,赵建宁,付强,等.Spotlight通道系统与显微内窥镜椎间盘切除术治疗腰椎椎间盘突出症临床对比[J].脊柱外科杂志,2013,11(4):193-197.
[2]银和平,李树文,吴一民,等.显微内窥镜技术10年应用经验与思考[J].脊柱外科杂志,2012,10(1):3-5.
[3]赵学军,左玲,傅志俭,等.经皮椎间孔镜下髓核摘除术治疗腰椎间盘突出症[J].中国疼痛医学杂志,2013,19(1):8-12.
[4]赵伟,李长青,周跃,等.经皮椎间孔镜下TESSYS技术治疗腰椎间盘突出症[J].中国矫形外科杂志,2012,20(13):1191-1195.
[5]Chen Z,Zhang L,Dong J,et al.Percutaneous transforaminal endoscopic discectomy compared with microendoscopic discectomy for lumbar disc herniation:1-year results of an ongoing randomized controlled trial[J].J Neurosurg Spine,2018,28(3):300-310.
[6]Khoo LT,Fessler RG.Microendoscopic decompressive laminotomy for the treatment of lumbar stenosis[J].Neurosurgery,2002,51(5):146-154.
[7]Isaacs RE,Podichetty VK,Santiago P,et al.Minimally invasive microendoscopy-assisted transforaminal lumbar interbody fusion with instrumentation[J].Neurosurg Spine,2005,3(2):98-105.
[8]熊英辉,贝抗胜,刘建平,等.显微内窥镜下腰椎间盘髓核摘除术后中远期疗效分析[J].中国矫形外科杂志,2010,18(11):952-953.
[9]周建伟,杨滨,任冬云,等.杨氏椎间孔镜治疗腰椎间盘突出症的远期疗效[J].中国矫形外科杂志,2012,20(17):1537-1540.
[10]Yeung AT.Minimally invasive disc surgery with the Yeung endoscopic spine system(YESS)[J].Surg Technol Int,1999(8):267-277.
[11]李嵩鹏,白一冰,李义凯.侧后路经皮脊柱内镜治疗腰椎间盘突出症的应用进展[J].颈腰痛杂志,2014,35(3):217-220.
[12]Hoogland T,Schubert M,Miklitz B,et al.Transforaminal posterolateral endoscopic discectomy with or without the combination of a low-dose chymopapain:a prospective randomized study in 280 consecutive cases[J].Spine,2006,31(24):890-897.
[13]白一冰,李嵩鹏,王力文,等.改良TESSYS 技术治疗腰椎神经根管狭窄症[J].颈腰痛杂志,2015,36(1):16-19.
[14]张之栋,杜怡斌,储建军.经皮椎间孔镜腰椎间盘摘除术与微创经椎间孔腰椎融合术治疗腰椎间盘突出症的前瞻性随机对照研究[J].中国微创外科杂志,2015,15(7):583-587.
[15]Ahn Y.Transforaminal percutaneous endoscopic lumbar discectomy:tech-nical tips to prevent complications[J].Expert Rev Med Devices,2012,9(4):361-366.
[16]白一冰,徐岭,赵文亮,等.经皮腰椎间孔镜手术的穿刺定位策略[J].中国微创外科杂志,2012,12(6):540-543.
