结核性脑膜炎脑脊液中利褔平浓度与临床疗效相关性分析*
2018-04-24廖小云
廖小云
结核性脑膜炎是结核杆菌所引发的人体脑膜与脊膜出现非化脓性炎症反应的疾病[1],该种疾病的起病比较隐匿,患者的病程较长,在临床上大多表现为持续的发热、头痛、喷射性呕吐等中枢神经症状,如果治疗不及时则有可能导致患者出现意识障碍,诱发癫痫,瘫痪甚至出现死亡,对于患者的身体健康构成严重的威胁[2-3]。对于结核性脑膜炎的治疗原则一般为早期用药、合理用药、联合用药三大原则,临床上常规使用抗结核治疗与降低颅压的方法进行综合治疗[4-5]。但是由于结核性脑膜炎的病变部位主要集中在中枢神经系统,在血脑屏障的保护下,多数药物难以达到该部分发挥效力,所以对于结核病脑膜炎的治疗必须保证脑脊液中的药物浓度[6-7]。而在不同的用药方式下药物浓度会出现较大的差别,本研究选择2010年2月-2017年2月在本院就诊的结核性脑膜炎患者50例的资料进行分析,对结核性脑膜炎患者脑脊液中利褔平的浓度与临床疗效之间的关系进行探讨,现报告如下。
1 资料与方法
1.1 一般资料 选择2010年2月-2017年2月在本院就诊的结核性脑膜炎患者50例。纳入标准:(1)患者符合结核性脑膜炎诊断[8],具有结核病史,外周血白细胞计数显著增高,出现发热、喷射性呕吐、头疼与乏力等典型临床表现,经过头部CT或者MRI检查表现为脑膜的强化,梗阻性脑积水与结核球等;(2)患者接受本院给出的治疗方案并且完成整个疗程;(3)患者及家属对本研究知情同意并且签署知情同意书。排除标准:(1)患者合并有免疫系统,心脑血管等系统的严重性疾病,可能对研究的结果产生影响;(2)患者已经出现脑血管事件或者已经存在结核外的感染;(3)患者对研究中所用药物或器材有过敏现象。患者年龄35~62岁,平均(48.50±11.47)岁,按照随机数字表法分为对照组与观察组,每组25例。本研究已经经过本院医学伦理委员会的批准和通过。
1.2 治疗方法
1.2.1 对照组 首先进行抗结核治疗,给予异烟肼、利福平、乙胺丁醇、吡嗪酰胺的方案。即口服异烟肼[生产厂家:天子福国际药业(江苏)有限公司,批准文号:国药准字H32022309,规格:50 mg/片],8片/次,1次/d;口服利福平(生产厂家:漯河南街村全威制药股份有限公司,批准文号:国药准字H41023790,规格:0.15 g/片),4片/次,1次/d;口服乙胺丁醇(生产厂家:河南省福林制药厂,批准文号:国药准字H41022612,规格:0.25 g/片),1片/次,3次/d;口服吡嗪酰胺[生产厂家:华润三九(北京)药业有限公司,国药准字:H11021652,规格:0.5 g/片],3片/次,3次/d。给予患者糖皮质激素进行治疗,给予地塞米松,每日15 mg进行静脉滴注,患者病情稳定后根据其临床症状与脑脊液和MRI的结果进行酌情的递减。给予患者降颅内压的治疗,根据患者的颅内压情况,可以给予甘露醇、甘油果糖、呋塞米等进行治疗,必要时给予乙酰唑胺,降低脑脊液分泌量,协助降颅内压。给予患者改善脑循环的治疗方法,当患者的情况趋于稳定后,给予一定量的丹参注射液和血塞通等药物。给予营养神经的治疗,如维生素B1和B12等。
1.2.2 观察组 在对照组的治疗方案基础上使用利福平粉针(生产厂家:沈阳双鼎制药有限公司,批准文号:国药准字H20050725,规格:5 mL∶0.3 g)进行静脉滴注,在治疗强化期,每次取2支溶于250 mL 0.9%氯化钠溶液中,在3 h内完成静脉滴注,1次/d。
1.3 观察指标 观察比较两组的脑脊液中利福平浓度、治疗后脑脊液相关指标和效果、不良反应发生情况。(1)脑脊液利福平浓度利用美国Waters公司生产的204型高效液相色谱仪进行测定。(2)治疗后脑脊液相关指标如颅内压、糖、氯化物、蛋白含量和细胞数、脑脊液转阴时间。(3)本研究将治疗效果分为三个级别:治愈、好转和无效。治愈:患者临床症状完全消失,脑脊液连续检查2次结果阴性;好转:患者临床症状好转,脑脊液结果有所改善;无效:患者临床症状未出现变化甚至恶化,脑脊液结果未改善。
1.4 统计学处理 采用SPSS 20.0软件对所得数据进行统计分析,计量资料用(±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用 字2检验,两组等级资料比较采用秩和检验中的Wilcoxon检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。

表1 两组一般资料比较
2.2 两组脑脊液中利福平平均浓度比较 观察组脑脊液利福平浓度为(1.72±0.25)μg/mL,高于对照组的(1.20±0.30)μg/mL,差异有统计学意义(t=6.658,P<0.05)。
2.3 两组治疗后脑脊液相关指标比较 治疗后,观察组颅内压、糖、氯化物、蛋白含量和细胞数、脑脊液转阴时间均低于对照组,差异均有统计学意义(P<0.05),见表 2。
表2 两组治疗后脑脊液相关指标比较(±s)

表2 两组治疗后脑脊液相关指标比较(±s)
组别 颅内压(mm H2O) 糖(mmol/L) 氯化物(mmol/L) 蛋白含量(g/L) 细胞数(×109)脑脊液转阴时间(d)对照组(n=25) 21.34±5.37 56.25±10.38 54.68±11.36 0.65±0.23 64.42±9.76 38.79±6.04观察组(n=25) 13.42±3.27 40.12±8.47 37.49±9.88 0.41±0.21 44.25±8.84 24.85±5.86 t值 6.298 6.02 5.709 3.853 7.659 8.282 P 值 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001
2.4 两组治疗效果比较 观察组治疗效果优于对照组,差异有统计学意义(Z=4.169,P<0.05),见表3。
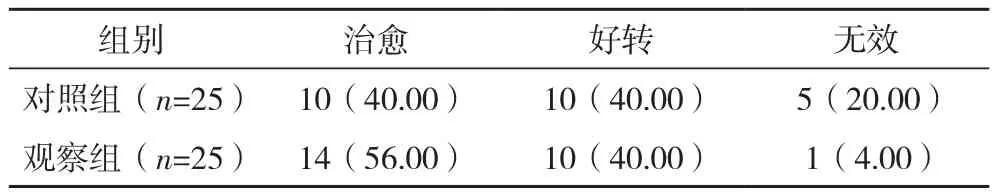
表3 两组患者的治疗效果比较 例(%)
2.5 两组治疗过程中不良反应发生情况比较 两组肝功能损伤、胃肠道反应、白细胞降低发生率比较,差异均无统计学意义(P>0.05),见表4。

表4 两组治疗过程中不良反应发生情况比较 例(%)
3 讨论
结核性脑膜炎属于一种严重性的中枢神经系统疾病,如果不进行及时的正规治疗,容易造成患者的蛛网膜下腔粘连,而脑脊液中蛋白含量的增加可以使脑脊液的循环出现障碍,如果炎症扩散到脊椎的蛛网膜,则可能引发脊髓的损伤[9-12]。脑脊液循环障碍会诱发脑水肿及渗出物刺激使癫痫发作,所以结核性脑膜炎患者即使存活,也容易出现颅神经的遗留损伤和肢体瘫痪的后遗症[13-14]。传统上对于结核性导致的感染大多使用链霉素或者氨基水杨酸等,但是近些年以来结核分枝杆菌的耐药性不断上升,以上药物的治疗效果越来越差。以多药物综合治疗的方法为现在对结核性脑膜炎的治疗原则[15]。
利福平是从利福霉素B中所得到的一种半合成抗生素,该药物通过抑制微生物的DNA转录合成RNA起到灭菌作用[16-17]。利福平是具有广谱抗菌效果的药物,对于结核杆菌、麻风杆菌等诸多革兰阴性菌与革兰阳性菌均具有良好的作用效果。特别对于结核杆菌,利福平对于在细胞内外和任何生长环境与生长状态的结核分枝杆菌均具有杀灭作用,属于完全杀菌剂[18-19]。利福平的抗菌活性为利福霉素B的30倍,而且在人体内可以广泛分布,在许多的器官和组织内均可以达到有效的浓度水平。本研究中对两组患者分别采用了不同的利福平用药方式,对照组仅利用口服方式给药,观察组在治疗的强化期口服给药基础上再利用静脉滴注给药。结果显示,在各项指标的对比中,观察组治疗效果优于对照组,脑脊液中包括氯化物、蛋白含量也均低于对照组。口服利福平后,特别是在饭后服用后,会导致药物的吸收程度降低,生物利用度下降,所以一般利福平均要求进行空腹服用,但是部分患者会产生胃肠道反应,而且结核性脑膜炎患者大多合并有颅内压偏高的症状,如恶心呕吐,造成药物口服困难,药力不能充分发挥。而利用注射剂的方法,尽管药物的作用机制相同,但是生物利用度明显优于口服的制剂,在使用后可以将人体内的血药浓度维持在较高的水准,而且药物直接入血,避免了胃肠道吸收的干扰,也能够避免消化道病理状态和胃内pH值的影响。只有维持较高的血药浓度,才能达到所要求的脑脊液中的药物浓度,人体的血脑屏障会阻碍大多数药物进入脑组织,尽管利福平是目前已知最有效的抗结核药物之一[20],但是其依然存在通过血脑屏障的困难,利用直接静脉滴注的方法可以提高血药浓度,间接提升脑脊液浓度,使治疗效果更佳。两组患者不良反应发生率比较,差异均无统计学意义(P>0.05),也证明了两种方法在治疗的安全性方面没有差异。但是本研究所纳入的患者病例数量较少,希望有机会进行大规模的随机对照研究,对本研究的结果进行深入讨论。
综上所述,利用静脉滴注的方法给药,可以获得更高的脑脊液利福平浓度,脑脊液中利福平浓度的增高可以提高结核性脑膜炎患者的治疗效果,并不增加不良反应发生率,值得在临床推广。
[1]张春艳,池菲,张新,等.不同方法诊断结核性脑膜炎的价值比较[J].疑难病杂志,2017,16(4):356-359,363.
[2]高岭,申改青,王有峰,等.结核性脑膜炎患儿生化及脑脊液检测结果与预后的相关性研究[J].中华医院感染学杂志,2017,27(11):2610-2613.
[3]尹慧敏,贾永林,李燕飞等.结核性脑膜炎患者脑脊液外泌体中let-7d表达的研究[J].中国实用神经疾病杂志,2017,20(6):9-12.
[4]任泽泽,戴伊宁,杨丹红,等.结核性脑膜炎与其他脑膜炎的鉴别诊断[J].国际流行病学传染病学杂志,2017,44(1):32-37.
[5]宋磊,张爱华.护理干预在结核性脑膜炎合并颅内高压患者中的应用效果分析[J].中国实用神经疾病杂志,2017,20(6):134-137.
[6]梁瑞霞,刘新,吴寒,等.观察纤溶酶注射液治疗结核性脑膜炎伴脑积水的临床疗效[J].中国实用神经疾病杂志,2017,20(6):98-100.
[7]岳玉瑛.高压氧联合脑脊液置换加鞘内注药治疗结核性脑膜炎的疗效观察[J].中西医结合心脑血管病杂志,2017,15(4):492-493.
[8]中华医学会.临床诊疗指南·结核病分册[M].北京:人民卫生出版社,2005:19-23.
[9] Qamar F N,Rahman A J,Iqbal S,et al.Comparison of clinical and CSF profiles in children with tuberculous and pyogenic meningitis;role of CSF protein:glucose ratio as diagnostic marker of tuberculous meningitis[J].J Pak Med Assoc,2013,63(2):206-210.
[10] Garg R K,Raut T,Malhotra H S,et al.Tuberculous meningitis and hydrocephalus[J].J Infect,2013,66(6):541-542.
[11]张晓东,李晶超.糖皮质激素联合四联抗结核药物治疗老年结核性脑膜炎的疗效及对脑脊液细胞学的影响[J].中国老年学杂志,2017,37(4):949-951.
[12]汪春雷,张道福,孙金龙,等.脑脊液腺苷脱氨酶、白介素23联合检测在结核性脑膜炎相关疾病诊断中的临床价值[J].中国基层医药,2017,24(3):435-438.
[13] Schmutzhard J,Aregger F C,Otieno A,et al.Release of intracranial pressure leads to improvement of otoacoustic emissions-a case report of a Kenyan child with complicated tuberculous meningitis[J].J Trop Pediatr,2013,59(4):326-329.
[14]余兰.脑脊液置换并椎管内注药治疗结核性脑膜炎的效果[J].临床医学研究与实践,2016,1(8):13-14.
[15] Panagariya A,Sureka R K,Ralot T,et al.Clinicodiagnostic features of tuberculous meningitis and the role of CSF PCR in early diagnosis:a study from north-west India[J].J Indian Med Assoc,2013,111(5):309-312,314.
[16]荆颖,黄淑萍,王倩,等.利福平药动学影响因素的研究进展[J].中国药房,2017,28(12):1726-1728.
[17]张玉华,张国钦,钟达,等.应用Xpert MTB/RIF法对我国肺结核诊断及利福平耐药检测的Meta分析[J].现代预防医学,2017,44(12):2116-2119,2130.
[18]金凤霞,金瑶,黄庆萍,等.初治菌阳肺结核患者异烟肼和利福平原发耐药调查[J].临床肺科杂志,2017,22(5):792-794.
[19]王燕,欧维正,蒙俊,等.应用Xpert MTB/RIF、基因芯片法快速检测结核分枝杆菌对利福平耐药性的研究[J].贵州医药,2017,41(3):249-250.
[20]向敏.结核分枝杆菌耐利福平机制及其研究进展[J].海南医学,2017,28(17):2853-2856.
