石墨烯电化学传感器法快速测定植物油中的苯并(a)芘
2018-04-20冯亚净李书国
冯亚净,李书国*
苯并(a)芘(benzo(a)pyrene,BaP)是由5 个苯环构成的稠环化合物,具有较强的致癌性、致畸性、致突变性[1-2],是世界卫生组织确定的三大致癌物质之一,其普遍存在于环境与食品中,可通过皮肤、呼吸、饮食等多种途径进入人体[3-4]。在一些植物油的制备过程中会产生大量的BaP[5-8],对此,各国对植物油中BaP含量进行了严格的控制,其中欧盟较为严格,规定植物油中BaP的最大限量为2 μg/kg;国际食品法典委员会(Codex Alimentarius Commission,CAC)规定食用油脂中BaP的最大限量为5 μg/kg;而我国食用植物油卫生标准规定最大限量为10 μg/kg,相对较为宽松[9-10]。因此,建立一种简便、快速、准确的BaP检测方法成为研究的重点。
目前,检测BaP的方法主要有荧光分析法、高效液相色谱(high performance liquid chromatography,HPLC)法、气相色谱-质谱联用法及酶联免疫吸附法[11-22]等,前3 种方法虽稳定性好、灵敏度高,但样品处理繁琐、仪器成本高、消耗时间长;酶联免疫吸附法虽简单快速但其灵敏度较低。而电化学方法具有操作简单、成本低、速度快、灵敏度高等特点,受到了广大研究人员的青睐,成为食品安全快速检测技术方法的主流之一[23-25]。Du Chunyuan等[26]采用微分脉冲伏安法,研究了在乙腈-水溶液中BaP在裸玻碳电极(glassy carbon electrode,GCE)上的氧化还原性质,建立了一种用于实际水样中BaP检测的电化学分析方法,检测限为0.67 nmol/L。Keskin等[27]采用方波溶出伏安法进行测定,发现在醋酸缓冲液中BaP在石墨电极上出现了一个明确的伏安响应,检测限为0.002 7 μmol/L。Yardim等[28]采用吸附溶出伏安法,研究了在添加表面活性剂的水溶液中BaP在掺硼金刚石电极上的电化学氧化性质,检测限为2.8 nmol/L。但目前研究BaP在修饰电极上的氧化还原特性的还很少。
本实验采用新型材料石墨烯(graphene,GS)和壳聚糖(chitosan,CS)构建电化学纳米传感器,研究了BaP在修饰电极表面的氧化还原性质,建立了一种快速检测植物油中痕量BaP的纳米传感器方法,并将其应用在实际样品中。
1 材料与方法
1.1 材料与试剂
小磨香油 石家庄市购。
BaP(96%,CAS:50-32-8) 上海阿拉丁生化科技股份有限公司;GS 北京德科岛金科技有限公司;乙腈(分析纯) 天津市大茂化学试剂厂;正己烷(分析纯) 天津市津东天正精细化学试剂厂;甲醇(色谱纯) 天津市康科德科技有限公司。
1.2 仪器与设备
LK98BII型微机电化学分析系统 天津兰力科化学电子高技术有限公司;三电极系统、电解杯 上海CHI仪器公司;LC-10A型HPLC仪 日本岛津公司;FA 2204型电子分析天平 上海菁海仪器有限公司;KQ 2200型超声波清洗仪 昆山市超声仪器有限公司;RE52CS-1型旋转蒸发器 上海亚荣生化仪器厂;TGL-16C型高速离心机 上海安亭科学仪器厂;GZX-9070 MBE型电热鼓风干燥箱 上海博讯实业有限公司医疗设备厂;85-2型控温磁力搅拌器 金坛市恒丰仪器制造有限公司。
1.3 方法
1.3.1 CS-GS修饰液的制备
取0.02 g CS加入到100 mL体积分数1%的乙酸溶液中,持续搅拌至无气泡,得到透明的CS溶液,于4 ℃条件下贮存。取0.01 g GS加入10 mL N,N-二甲基甲酰胺,超声处理20 min,制得均匀分散的GS悬浮液。取5 mL GS悬浮液加入到5 mL CS溶液中,超声处理30 min,使GS均匀地分散在CS溶液中,得到CS-GS修饰液,于4 ℃贮存备用。
1.3.2 电化学传感器的制备
先将GCE用Al2O3粉末(粒径 0.05 μm)打磨抛光,至电极表面成镜面,再依次于体积分数为50%的硝酸溶液、无水乙醇和去离子水中各超声处理3 min,然后在1 mol/L H2SO4溶液中采用快速循环伏安法(电位:-0.5~0.8 V;扫描速率:500 mV/s)扫描至稳定的循环伏安图,从而对GCE进行活化,最后用N2吹干,备用。
取上述修饰液5 μL滴涂到已经过预处理的GCE表面,在红外线灯下烘干,备用。
1.3.3 电化学传感器测定BaP
电化学分析法的测定均采用三电极系统:Φ 3 mm经修饰的玻碳圆盘电极为工作电极、Ag/AgCl为参比电极、铂丝电极为辅助电极,并采用线性扫描伏安法进行测定,扫描电位为0.5~1.3 V,扫描速率为30 mV/s。
电化学检测包含两部分:第1部分是BaP在电极表面的富集,将CS-GS/GCE在开路状态下浸没在含有BaP的乙腈-水(1∶3,V/V)溶液中,并用磁力搅拌器不断搅拌;第2部分是BaP的测定,将富集了BaP的CS-GS/GCE转移到乙腈-水的空白溶液(0.2 mol/L的LiClO4溶液作为电解质,0.1 mol/L的硫酸溶液调节pH值)中,采用循环伏安法与线性扫描伏安法进行测定,测定3 次,并记录相应的峰电流值,并取其平均值作为该BaP浓度所对应的氧化电流值Ip。
1.3.4 植物油样品中BaP的测定
1.3.4.1 样品预处理
称取(1.0±0.05)g香油,然后加入10 mL乙腈饱和正己烷溶液,超声处理30 min后移至分液漏斗中,取30 mL正己烷饱和乙腈萃取3 次,合并下层乙腈层后,用旋转蒸发仪蒸发至干,接着用乙腈分3 次淋洗旋蒸瓶并定容至1 mL。样品提取液以5 000 r/min离心10 min后经0.45 μm滤膜过滤后进行检测。
1.3.4.2 电化学传感器法测定
按照1.3.3节的方法进行测定,将3 次测定结果的平均值带入标准曲线中得到样品中BaP含量。
1.3.4.3 HPLC法测定
色谱条件[29-30]:C18柱(4.6 mm×250 mm,5 μm);流动相为甲醇-水(90∶10,V/V);流速为1.0 mL/min;柱温为35 ℃;进样量为20 μL;激发波长为384 nm,发射波长为406 nm。
准确称取25.0 mg BaP标准品于100 mL 容量瓶中,用乙腈定容,保存于4 ℃条件下备用。配制梯度浓度为10、20、50、100、200、500、1 000 nmol/L的标准溶液,取20 μL标准溶液进样,记录其HPLC图谱,根据所得峰面积与对应的BaP浓度绘制标准曲线。取上述处理好的样品提取液20 μL,进行HPLC检测,取3 次峰面积的平均值作为该样品的图谱峰面积,代入标准曲线计算样品中BaP浓度,并与电化学检测方法的结果进行对比。
1.4 数据处理与统计分析
以上测定均为3 组平行实验,结果取3 组实验数据的平均值。运用SPSS 18.0软件进行数据统计分析,采用单因素方差分析进行显著性差异分析(P<0.05),实验数据图利用 OriginLab Origin Pro v9.0软件绘制。
2 结果与分析
2.1 BaP在不同修饰电极表面的氧化还原行为
采用快速循环伏安法,研究BaP在裸GCE(a)、CS/GCE(b)、GS/GCE(c)、CS-GS/GCE(d、e)上的氧化还原行为,结果见图1。BaP在各GCE上均出现了一个明显的氧化峰,电位也均在1.0 V附近,而没有出现还原峰,说明该反应是不可逆的;修饰了CS后,其氧化峰电流比裸GCE减小了17.37%,这是由于CS在GCE表面形成了一层膜,阻碍了电子之间的传递;而修饰了GS后,峰电流明显增大,增大了3.85 倍,这是由于GS具有相当大的比表面积以及突出的电学性质,为电子与电极之间的电子传递提供了一个微通道;当修饰了CS-GS后,峰电流进一步增大,增大了4.71 倍,这可能是由于CS极好的成膜性将更多的GS固定在GCE的表面。所以CS-GS/GCE具有良好的电化学性质。根据图1d、e比较,可以看出BaP的氧化响应电流随着BaP浓度的增大而增大。

图1 不同电极的循环伏安图Fig. 1 Cyclic voltammograms of different electrodes
2.2 实验条件的优化
2.2.1 修饰液配比与修饰量
修饰液的配比与修饰量对纳米传感器的电子传递具有重大的影响。配制CS溶液与GS悬浮液体积比为1∶4、1∶2、1∶1、2∶1、4∶1的修饰液,取5 μL修饰经处理的GCE,采用线性扫描伏安法测定BaP的氧化电流,结果如图2A所示。当CS溶液与GS悬浮液体积比为1∶2时,峰电流达到最大值,之后在一定范围内随着CS的增加峰电流逐渐减小,这是由于CS的成膜性质会阻碍电子传递的结果。所以选择修饰液的配比为1∶2。分别将1、3、5、7、9 μL的CS-GS修饰液滴涂到GCE上,采用线性扫描伏安法测定其电流的大小,结果如图2B所示。随着修饰量的增加,峰电流逐渐增加,当修饰量为5 μL时,峰电流达到最大,然后随着修饰量的增大,峰电流逐渐减小,这是因为修饰膜太厚影响电子传递的结果。
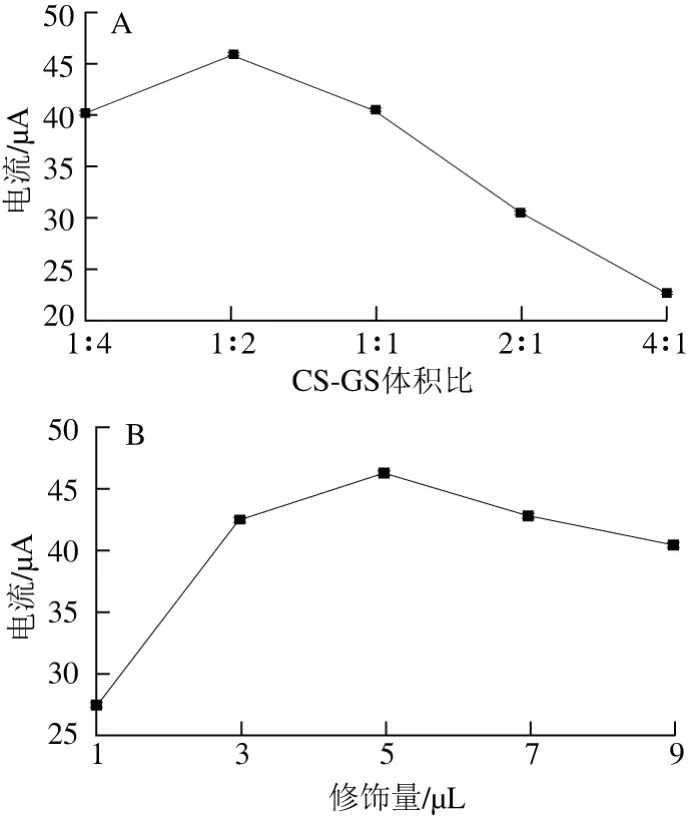
图2 修饰液配比(A)和修饰量(B)对电化学传感器电流的影响Fig. 2 Effects of composition and volume of modified solution on response current of electrochemical sensor
2.2.2 电解质浓度
采用线性扫描伏安法,研究BaP在不同LiClO4浓度(0.05、0.1、0.15、0.2、0.25、0.3 mol/L)的底液条件下的氧化响应电流的变化,结果如图3所示,一开始,峰电流随着电解质浓度的增大而显著增大,当LiClO4浓度为0.2 mol/L时,氧化峰电流值达到最大,LiClO4的浓度继续增大,其峰电流的变化趋向平稳,说明电子之间的传递达到了平衡,导电率达到了最大。所以选择电解质浓度为0.2 mol/L。
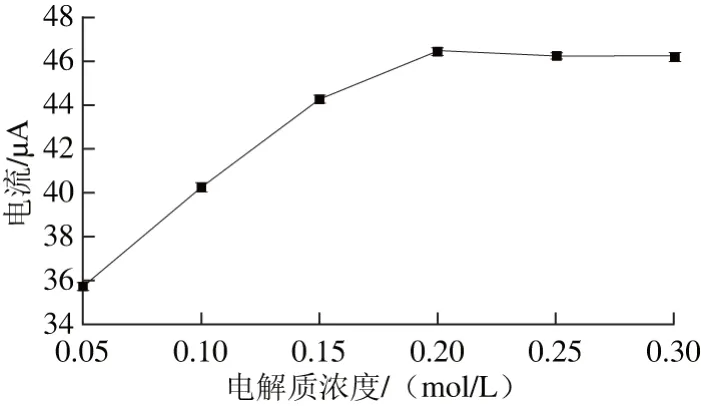
图3 电解质浓度对电化学传感器电流的影响Fig. 3 Effect of electrolyte concentration on response current of electrochemical sensor
2.2.3 硫酸浓度
硫酸浓度与BaP在溶液中的稳定性有着直接的联系,对峰电流也有显著影响。在保证其他实验条件一致的情况下,只改变底液中硫酸浓度(0.05、0.1、0.15、0.2、0.25 mol/L),采用线性扫描伏安法进行BaP的测定,结果如图4所示。BaP的响应电流先随着硫酸浓度的增加而增大,这是由于硫酸可提供质子以促进BaP发生氧化反应;当硫酸浓度为0.1 mol/L时,峰电流的值达到最大,继续添加硫酸,其对峰电流的影响不大,说明此时BaP发生氧化反应所需要的质子的量已达到最大,所以选取硫酸浓度为0.1 mol/L。

图4 硫酸浓度对电化学传感器电流的影响Fig. 4 Effect of sulfuric acid concentration on response current of electrochemical sensor
2.2.4 富集时间
富集时间与电极表面吸附BaP的多少有关,影响着电化学传感器测定的准确性。配制相同BaP浓度的溶液,富集时间分别为5、10、15、20、25 min,在相同的底液中采用线性扫描伏安法进行测定,如图5所示。在5~15 min范围内峰电流随着富集时间的延长而增大,当富集时间达到15 min后,峰电流的变化较小,说明BaP在电极表面的富集达到了饱和状态。实验选择富集时间为15 min。

图5 富集时间对电化学传感器电流的影响Fig. 5 Effect of enrichment time on response current of electrochemical sensor
2.3 电化学测定BaP的分析性能
分别配制0、20、40、60、80、100、200、400 nmol/L的BaP标准溶液,按照1.3.4节进行测定,每个浓度均测定3 次,取其平均值为该浓度的响应电流值,不同浓度BaP的线性扫描曲线,如图6所示。BaP的氧化反应电流Ip值随BaP浓度的增大而增大,且在BaP浓度范围为0~100 nmol/L时Ip值与CBaP之间的关系满足线性关系方程:Ip= 0.116 2CBaP+22.926 2,线性相关系数R2=0.997 8,其检测限为0.103 nmol/L(RSN=3)。可见,本实验构建的电化学传感器具有较好的灵敏度,可作为一种快速测定BaP的分析方法。
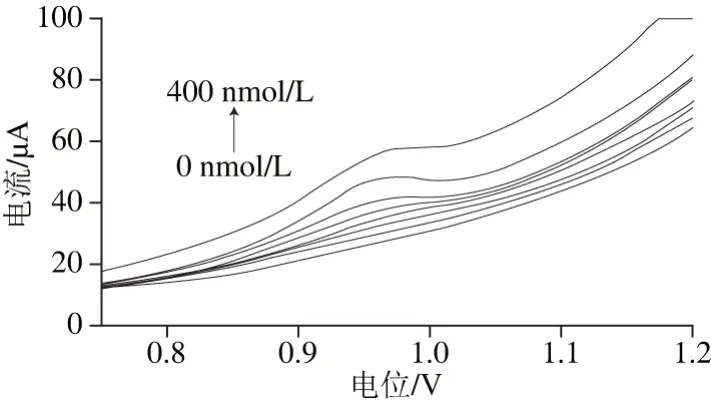
图6 不同浓度BaP的线性扫描曲线Fig. 6 Linear sweeping curves of BaP at different concentrations
2.4 电化学传感器的抗干扰性、稳定性和重复性
考察与BaP性质相同的脂溶性抗氧化剂(VE、TBHQ和PG)对BaP氧化响应电流的影响。分别配制0.1 mol/L的VE、TBHQ和PG溶液,溶剂为乙醇,在4 ℃条件下保存备用。在其他条件相同的情况下,采用线性扫描伏安法分别测定空白的VE、TBHQ和PG溶液、空白的BaP标准溶液以及分别添加3 种抗氧化剂的BaP标准溶液的电化学氧化响应电流,结果如表1所示。该电化学传感器对3 种脂溶性抗氧化剂均可吸附,但其峰位置均在0.35~0.65之间,而BaP的峰位置在1.03左右,互相不影响;且在分别添加VE、TBHQ和PG后,BaP的氧化响应电流变化仅为6.15%、4.72%、4.07%。说明该电化学传感器的抗干扰性较好。
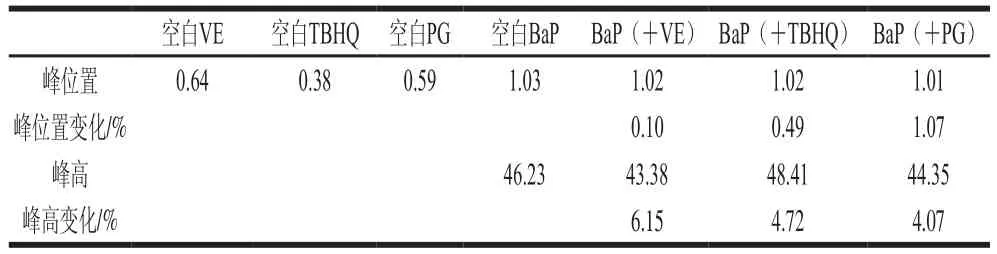
表1 电化学传感器抗干扰性测定结果Table 1 Interference resistance of electrochemical sensor
分别制备3 批电化学传感器(每批3 支),第1批当天进行测定;第2批3 d后进行测定;第3批7 d后进行测定;结果表明,在相同条件下测定同一样品,同一批次的变化率均在3.41%以下,不同批次的变化率不超过6.77%,说明该电化学传感器的稳定性和重复性较好。
2.5 香油样品中BaP的测定
按照1.3.4.1节处理样品,得到样品提取液,分别采用纳米电化学传感器法和HPLC法检测样品中BaP的含量,并进行加标回收实验,按照1.3.5节计算其平均值和相对标准偏差,结果如表2所示,本法测得样品中BaP含量为22.96 nmol/L,而HPLC法测得23.04 nmol/L,二者相差仅0.35%;在分别加有5、10、20 nmol/L的BaP标准品后,本法的回收率在98.51%~100.57%之间,HPLC法则在98.22%~100.58%;另外,两种方法的相对标准偏差均在2.15%~3.16%之间。所以二者基本一致,电化学传感器法快捷方便。
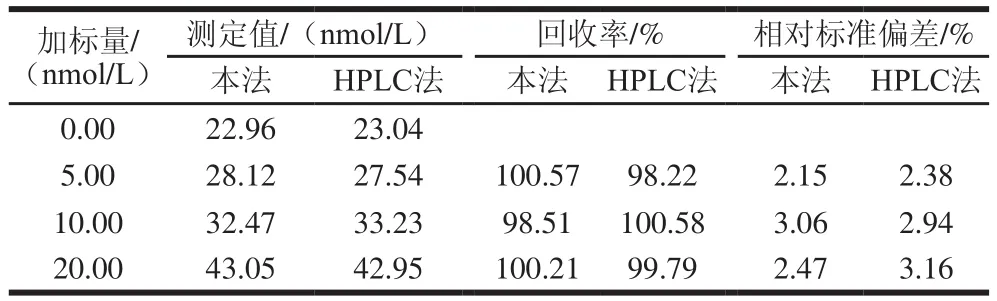
表2 香油样品中BaP回收率测定的结果Table 2 Recovery of BaP from spiked sesame oil
测得市售香油中BaP的含量约为5.76 μg/kg,在我国限量标准(10 μg/kg)之内,但超过了欧盟标准(2 μg/kg)与CAC规定的限量(5 μg/kg)。
3 结 论
BaP具有致癌、致畸、致突变的性质,对身体的危害极大,快速简便的检测方法是及时减小其危害的基本前提。本实验用具有极好成膜性的CS与大比表面积的纳米粒子GS修饰GCE,优化了GCE的导电性能,基于BaP的电化学氧化还原性质,构建了一种速率快、稳定性强、灵敏度高的电化学传感器,并应用于实际样品中BaP的测定。采用循环伏安法与线性扫描伏安法测定BaP的氧化还原电流,发现该反应为不可逆反应,其氧化电流与BaP浓度在0~100 nmol/L范围内呈线性关系。本实验还对其修饰测定条件进行了优化,确定了数学模型、线性范围、检测限等参数,实现了BaP的快速、准确、现场检测。此外,该传感器制作简单、稳定好、重复性好,检测过程抗干扰性强、检测时间短,在食品中BaP快速检测中的开发前景广阔。
参考文献:
[1] 史巧巧, 席俊, 陆启玉. 食品中苯并芘的研究进展[J]. 食品工业科技,2014, 35(5): 379-386. DOI:10.13386/j.issn1002-0306.2014.05.066.
[2] 许琳莉. 苯并芘对小鼠T淋巴细胞的抑制作用及相关信号转导通路的调控[D]. 长春: 吉林大学, 2015: 3.
[3] LIU Y, LIU L B, LIU J M, et al. Distribution and characterization of polycyclic aromatia hydrocarbon compounds in airborne particulates of east Asia[J]. China Particuology, 2006, 4(6): 283-292. DOI:10.1016/S1672-2515(07)60277-2.
[4] 曹梦思, 王君, 张立实, 等. 食品中多环芳烃的研究现状[J]. 卫生研究, 2015, 44(1): 151-157.
[5] 肖苏尧, 车科, 陈雪香, 等. 不同油茶籽油提取工艺中苯并(a)芘形成的溯源[J]. 现代食品科技, 2012, 28(2): 156-159. DOI:10.13982/j.mfst.1673-9078.2012.02.008.
[6] 刘兵戈, 刘国琴, 汪学德. 植物油加工中苯并(a)芘的产生途径及控制措施[J]. 粮油食品科技, 2014, 22(2): 47-51.
[7] 宋怡城. 植物油中苯并芘检测及产生机理研究[J]. 农产品加工,2015(5): 11-13. DOI:10.3969/jissn.1671-9646(X).2015.05.035.
[8] 张小涛, 刘玉兰, 王月华. 食用油脂中多环芳烃的研究进展[J]. 中国油脂, 2012, 37(10): 45-49. DOI:10.3969/j.issn.1003-7969.2012.10.012.
[9] 阿木尔吉日嘎拉, 王玉兰. 食用植物油中苯并(a)芘的测定[J]. 黑龙江畜牧兽医, 2015(9): 263-265. DOI:10.13881/j.cnki.hljxmsy.2015.0739.
[10] 任勇, 汪学德. 焙炒条件对芝麻油中多环芳烃含量的影响[J]. 粮油食品科技, 2016, 24(1): 29-33. DOI:10.16210/j.cnki.1007-7561.2016.01.007.
[11] 李念念, 周光宏, 徐幸莲, 等. 高效液相色谱-荧光法测定腊肉中苯并芘残留[J]. 食品工业科技, 2013, 34(1): 319-322. DOI:10.13386/j.issn1002-0306.2013.01.022.
[12] 王红青, 韩里明, 屠海云, 等. 固相萃取-超高效液相色谱荧光法测定植物油中苯并(a)芘[J]. 食品科学, 2012, 33(14): 216-218.
[13] ESTEFANIA L, MANUEL R, MARIO D. Spanish smoked meat products: benzo(a)pyrene (BaP) contamination and moisture[J].Journal of Food Composition and Analysis, 2015, 37: 87-94.DOI:10.1016/j.jfca.2014.09.004.
[14] ZHAO H F, ZHOU F, QI Y Q, et al. Screening of Lactobacillus strains for their ability to bind benzo(a)pyrene and the mechanism of the process[J]. Food and Chemical Toxicology, 2013, 59(8): 67-71. DOI:10.1016/j.fct.2013.05.040.
[15] 胡加文, 李天宝, 王春利, 等. 固相萃取-液相色谱法测定方便面中苯并芘[J]. 化学分析量, 2014, 23(3): 25-27. DOI:10.3969/j.issn.1008-6145.2014.03.007.
[16] 李敏, 蔡伊莎, 韩宝武, 等. 高效液相色谱法测定水中痕量苯并芘的研究[J]. 四川环境, 2015, 34(4): 71-74. DOI:10.14034/j.cnki.schj.2015.04.014.
[17] HIMANSHU G, BINA G. Photocatalytic degradation of polycyclic aromatic hydrocarbon benzo[a]pyrene by iron oxides and identification of degradation products[J]. Chemosphere, 2015, 138: 924-931.DOI:10.1016/j.chemosphere.2014.12.028.
[18] WU Y H, LIU X Q, ZHANG L, et al. An amperometric biosensor based on rat cytochrome p450 1A1 for benzo[a]pyrene determination[J]. Biosensors and Bioelectronics, 2011, 26(5): 2177-2182. DOI:10.1016/j.bios.2010.09.027.
[19] WANG X, LU X B, CHEN J P. Development of biosensor technologies foranalysisof environmental contaminants[J]. Trends in Environmental Analytical Chemistry, 2014, 2: 25-32. DOI:10.1016/j.teac.2014.04.001.
[20] LIN M H, LIU Y J, LIU C H, et al. Sensitive immunosensor for benzo[a]pyrene detection based on dual amplification strategy of PAMAM dendrimer and amino-modified methylene blue/SiO2coreshell nanoparticles[J]. Biosensors and Bioelectronics, 2011, 26: 3761-3767. DOI:10.1016/j.bios.2011.02.028.
[21] 许丽, 赵鲁. 环境样品中多环芳烃的酶联免疫检测分析[C]//2013中国环境科学学会学术年会论文集(第四卷). 昆明: 轻工业环境保护研究所, 2013: 2241-2245.
[22] 史巧巧, 陆启玉, 席俊. 苯并芘的免疫学快速检测技术研究[D].郑州: 河南工业大学, 2014: 3-6.
[23] 苏招红, 徐孝林, 李朝荣, 等. 植物激素电化学传感技术研究进展[J].中国科学: 化学, 2016, 46(8): 759-767. DOI:10.1360/N032015-00238.
[24] 崔琳. 重金属离子电化学传感器的构建及其应用[D]. 南京: 南京大学, 2015: 15-17.
[25] 周玲. 食品中双酚A检测用新型电化学传感器的研究[D]. 杭州: 浙江大学, 2014: 6-7.
[26] DU C Y, HU Y Q, LI Y C, et al. Electrochemical detection of benzo(a)pyrene in acetonitrile-waterbinary medium[J]. Talanta, 2015, 138: 46-51. DOI:10.1016/j.talanta.2015.02.005.
[27] ERTUGRUL K, YAVUZ Y, ZUHRE S. Voltammetry of benzo[a]pyrene in aqueous and nonaqueous media: adsorptive stripping voltammetric determination at pencil graphite electrode[J]. Electroanalysis, 2010,22(11): 1191-1199. DOI:10.1002/elan.200900527.
[28] YARDIM Y, LEVENT A, KESKIN E, et al. Voltammetric behavior of benzo[a]pyrene at boron-doped diamond electrode: a study of its determination by adsorptive transfer stripping voltammetry based on the enhancement effect of anionic surfactant, sodium dodecylsulfate[J].Talanta, 2011, 85: 441-448. DOI:10.1016/j.talanta.2011.04.005.
[29] 刘艳琴, 王浩, 杨红梅. 凝胶渗透色谱-高效液相色谱法测定植物油中苯并芘[J]. 食品科技, 2013, 38(1): 327-329. DOI:10.13684/j.cnki.spkj.2013.01.026.
[30] 李琴, 楚元卫. 高效液相色谱法快速测定植物油中苯并芘[J]. 农业机械, 2013(23): 42-44. DOI:10.16167/j.cnki.1000-9868.2013.23.002.
