干细胞诱导分化、衍生配子研究及伦理学问题探讨
2018-04-13曾令烽包文虎潘建科关梓桐李晓彦梁伟雄
刘 军,曾令烽,包文虎,曹 烨,潘建科,关梓桐,曹 倩,李晓彦,王 奇,梁伟雄,曾 星
(1.广东省中医院(广州中医药大学第二附属医院),广东 广州 510120;2.广东省中医药科学院,广东 广州 510120;3.世界中医药学会联合会伦理审查委员会,北京 100101;4.中山大学附属肿瘤医院临床研究部/药物临床试验机构,广东 广州 510060)
干细胞,医学界称为“万用细胞”,作为一种具有自我复制能力的多潜能细胞,在一定条件下可分化成多种功能细胞[1-2]。近期有研究小组在干细胞体外诱导和配子形成方面取得了重要进展,初步研究提示此类衍生配子可以来源于成体多能干细胞[3]。日本研究人员在2016年形成了第一个功能性雄性及雌性小鼠生殖细胞,该研究主要通过提取小鼠皮肤细胞、“重编程”为诱导多能干细胞,从而培育出功能完好的卵母细胞;这也是首次全程在体外培育出相应的生殖细胞,且后续通过体外人工授精、获得26个新生小鼠,此类小鼠也能够成功的繁衍出健康的幼崽[4-5]。其次,另一个研究小组通过小鼠胚胎干细胞及原始生殖细胞,建立“类精子细胞”单倍体细胞系,从而培养繁殖后代[6]。通过实验室广泛培育、产生卵母细胞和精子,该过程一般可以用于以下两个方面:①科学性研究活动,例如探索不孕不育症或配子形成过程等;②促进辅助生殖技术的科学发展[7-8]。
当前多数夫妻可以通过自然受孕等常规途径进行孩子生育;可是仍有不少夫妻处于相对不孕症或生育力低下状态,亟待借助辅助生殖技术进行后代繁衍。此类准父母可以通过体外受精或卵泡浆内单精子显微注射(Intracytoplasmic Sperm Injection,ICSI)等方式进行处理;上述过程要求夫妻双方均能够产生可育的配子[9]。然而,目前也存在其他人群,需要经由他人捐赠的配子进行后代生殖,例如化疗、遗传因素、损伤或感染等导致已达生育年龄的异性夫妇出现一方不孕或不育,更年期妇女,(男性或女性)同性夫妇,或者单身人群[10]。在此类背景下,倘若干细胞衍生配子的技术足够安全、有效,在不久的将来很可能便可为上述人群提供一个可行的选项,能够让存有自身基因遗传症状相关的后代得以繁衍;该过程也可允许其他类型的家庭获得最大可能的和谐重建。
鉴于干细胞诱导分化、衍生配子的技术本身安全性等问题,在一定程度上限制了其在临床上的广泛应用。目前该技术仍处在实验室的探索性研究阶段,距离成熟的干细胞临床推广应用尚有很长的路程。然而,该项技术研究的后续开展,亟待对涉及的伦理、法律及社会效应进行充分的权衡评价。本文围绕上述核心问题,针对干细胞衍生配子基础研究及人体生殖研究等层面展开论述,并就隐私保护、知情同意、自主决策等方面进行相关分析,以期为当前干细胞研究利益相关方的权利保护和伦理审查实践提供参考。
1 干细胞衍生配子及伦理学问题
在当今科学技术迅速发展的背景下,科研人员对哺乳动物的配子(卵子、精子等)发育过程进行了系列探索性研究。当前此类工作多数均在老鼠等动物身上开展。倘若人体多能干细胞可以实现体外培育,这将会极大地促进对卵子及精子的研究。近期干细胞研究提示,通过干细胞诱导分化衍生配子是很可能的,此研究对细胞生物学及早期胎儿发育等具有一定的参考价值,而且不少科学探索领域或许也能在该项技术的发展中获益[11-12]。然而,干细胞源配子研究技术的进展也会导致一系列伦理学问题及社会政策性争议,且不同区域文化及社会人群对此很可能也潜存着不同的价值理念与认识。当前比较常见的伦理学问题包括:干细胞衍生配子研究是否体现人们对生命尊重的要求;安全隐患及其商品化问题;遗传伦理学问题,例如与中国传统伦理观的矛盾、与生育权利的矛盾、同性恋以及单身人士有望获得生育能力等,这些涉及伦理学方面的问题亟待进一步探讨。
2 干细胞衍生配子研究的过程管理及控制
针对中国干细胞源配子技术的研究,当前尚未发现相对细化的监管体系。然而,此类辅助生殖技术研究的管理,目前仍存在一系列的不足,亟待在后续优化过程管理及风险控制,统筹兼顾(见图1)。此外,完善干细胞源配子等辅助生殖技术监管体系,需要进一步健全相关法律法规指引,构建长效监管机制,规范行业内部自身管理,同时应强化干细胞/生殖伦理委员会的监管职能,并妥善协调社会公众参与和媒体舆论监督(见表1)。
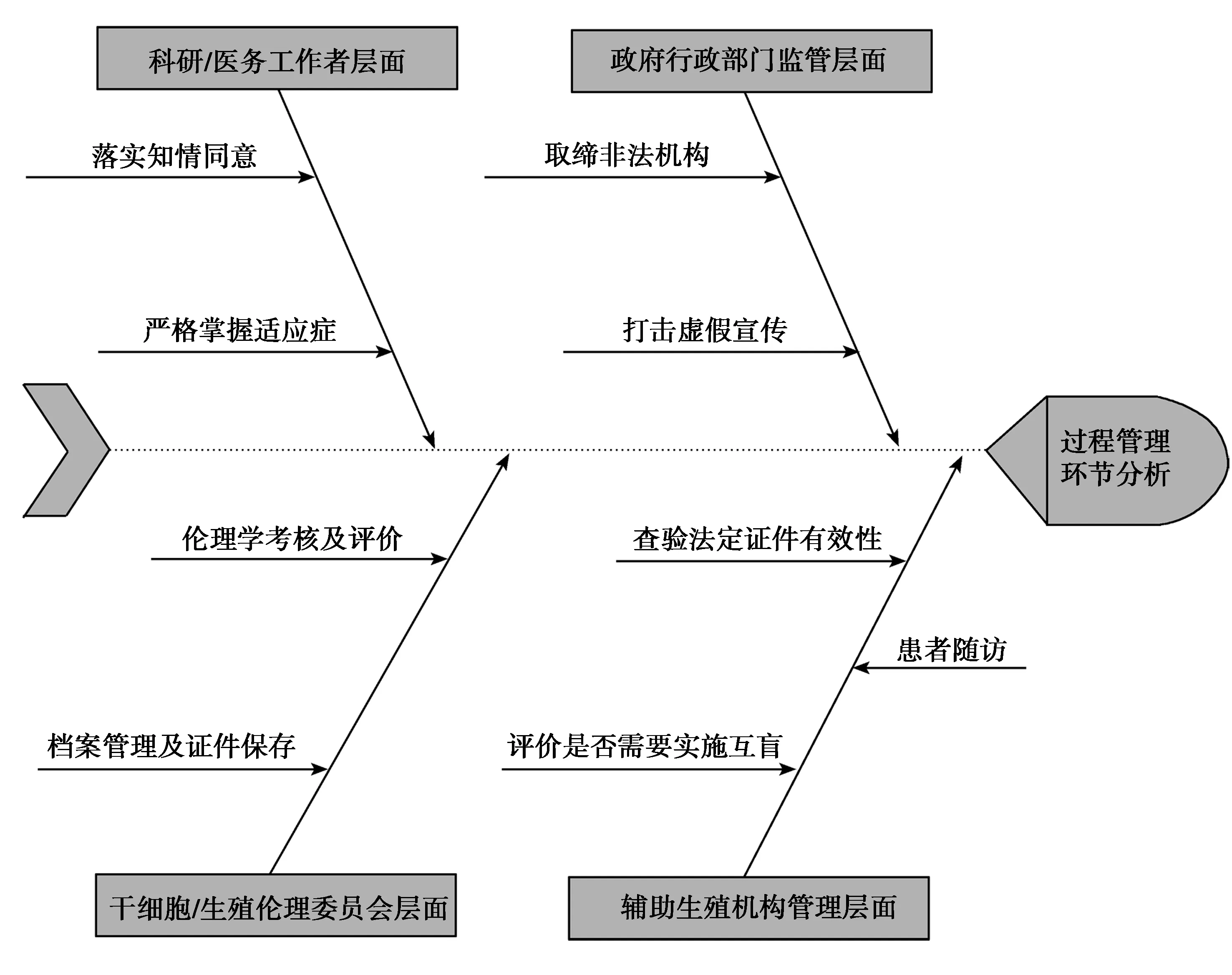
图1 干细胞源配子等辅助生殖技术的过程管理及控制
3 干细胞衍生配子研究中的伦理学问题优化策略
3.1 基础研究方面的伦理学问题优化
第一,通过建立体外培育体系、衍生配子的基础及临床前研究,涉及卵母细胞和胚胎的生成、使用及销毁等程序。例如,干细胞来源的卵母细胞,需要使用自然精子进行功能检测,导致胚胎的形成。该过程类似于线粒体替换技术活性研究,在孕育新生命的同时,很可能也潜在生殖细胞的基因修饰。然而,在科学研究中建立和使用人类胚胎,该命题是否符合伦理道德尚存有很大争议及不同解读。基于此,不少国家采取了渐进的立场,即授予早期胚胎一定的“道德地位”,并随着其后续发育及妊娠有所强化。在此背景下,胚胎伦理“14天规则”便应运而生,即规定人体胚胎若应用于干细胞研究务必限制时间跨度在14天之内。此胚胎发育14天的临界时点,也被认为将出现原始脊索条纹的标志;而在此之前,胚胎可潜在分裂成两个或融合在一起[13-14]。鉴于14天之前人胚尚未分化形成神经等结构,还没有体现出人的特征,故暂未涉及伦理学问题。当前大多数国家地区均遵循为期14天的准则,并在严格的限制范围之内从事人体胚胎的相关研究;然而仍有不少区域国家对此类科研活动缺乏必要的监管[15]。出于科学研究初衷所需要的胚胎生成,在当前大多数被认为必须采取有效的措施进行管控,以符合相应的伦理道德法规。然而,在不孕治疗等人体生殖方面,通常也在广泛使用体外受精的技术操作,该过程也牵涉到多余的或不适合医学治疗的人胚生成及毁弃问题。相比于以研究为目的的胚胎形成(例如探索不孕治疗新方法或其他致命疾患医疗条件等),用以治疗不孕的人胚生成及销毁行为,在当前往往更容易接受[16]。
第二,干细胞衍生配子的初始临床应用研究,在当前依然充满着风险及不确定性。因此,有必要采取必要措施,针对人体胚胎进行全面、广泛的临床前研究,以保证该项技术本身的安全性及有效性。例如在临床之前展开试验,检测与对照胚胎相比,研究胚胎是否已具备正常的身体分化可塑性及胚层形成等。上述过程研究很可能最终需要展开超过14天期限的胚胎体外培养。然而,“14天规则”在目前仍被各个国家研究机构视为符合实际且合法的底线,也常作为政策性评价手段用于衡量胚胎研究的道德地位。此外,“类器官”研究等其他科学活动的最新发展,也对“14天规则”提出了质疑。因此,当前亟待对14天期限之外涉及的伦理学问题及相关监管性法规进行重新审视[13,16]。

表1 干细胞源配子研究的伦理学问题、过程管理及策略优化要点
第三,国际干细胞研究伦理学相关指南法规明确规定,用于“研究”的人体生物材料必须通过合理的途径及方式获取[17-18]。其中一个重要原则是,用于建立新型干细胞系的人体材料,需要将相关情况明确告知捐赠者,给予其足够的尊重,并获得自愿的知情同意签署;而且此知情同意内容应与将开展的材料研究情况相一致。鉴于上述高标准的准入要求,部分国家在实际操作层面很可能并未确切考虑到相应的知情同意程序。例如,美国联邦研究法案条例对涉及病理切片或诊断标本等人体生物材料予以同意开展研究,然而该条例明确要求应满足以下条件[19]:此类资源可以公开获取;或者已采取措施对相关“敏感信息”实施妥善保存,而患者通过常规途径无法进行识别或与患者相衔接的标识符已做特殊处理。这意味着倘若区域国家缺乏严谨的法规政策指引规范,在临床实践中任何被丢弃的组织均可以用于上述类型的研究;而这一过程无需获得患者过多的知情同意,只要符合匿名化的组织或者患者以手术状态入院、做诊断性程序或手术流程相关知情方式,均可以在患者接受治疗的过程中采集相应的生物材料,并冠以做“教育或科学研究”。在此背景下,当前在使用人体生物材料用于构建诱导多能干细胞系、衍生配子的研究中,科学研究人员有责任、有义务加强自身的道德素养,规范科研行为实践。此外,对于作为这些配子基因来源的患者而言,是否同意让临床中丢弃的组织用于此类研究,往往多数情况下根本没有相关的意识,更加不用说去做周详的考虑。因此,有必要采取可行的措施构建信息交互平台,保持研究人员与患者之间的互动、沟通与协调,同时应设法保证研究的公开透明化,为社会公众所获悉参与,促进公众的信任与支持。
第四,干细胞衍生配子的出现,可为以研究为初衷的卵母细胞科研活动提供可能。出于研究目的的卵母细胞移植,在当前大多数国家均视为可接受的科研实践。国际干细胞研究学会(International Society for Stem Cell Research,ISSCR)也规定了卵子捐赠的条件、程序及相关规范性指南[17,20]。然而,卵母细胞的获取,包括了捐赠女性所承受的一系列风险、负担及不便,故卵母细胞相关研究长期处于欠缺或不足状态。基于此,干细胞诱导分化衍生配子,可作为一个期待的替代选择。然而,此类卵母细胞的便捷供应也可能导致另一个极端,即胚胎研究规模的大范围增殖性拓展,业界多称之为“胚胎农场”[21]。因此,有必要针对干细胞衍生配子的形成及使用,设定最低限度的初始需求,并构建可行的监管机制及法规,实施过程管理及风险规避。
第五,干细胞诱导分化、衍生配子,可以通过基因组编辑工具(例如CRISPR/Cas9技术)进行转基因处理[22],该过程可用于科学研究及遗传疾患预防,以达到不断改进完善的效果。尽管生殖系基因组编辑不在本研究论述的范畴,可针对其后续应用进行广泛的社会探讨。
3.2 人类辅助生殖研究方面的伦理学问题优化
第一,干细胞诱导分化、衍生配子技术,可以为那些迄今仍依赖捐赠者来繁衍后代的夫妇提供一个潜在的辅助生殖选择。例如,癌症化疗后导致生育能力丧失的幸存者、受累于基因遗传疾患的病人、排卵障碍或其他原因导致不孕的患者等。对于上述不孕不育夫妇而言,干细胞源配子很可能实现其后代培育的渴望。此外,该项技术的出现对于其他人群,例如同性夫妇等不能生育存血亲关系小孩等,也可以起到解放思想及缓解压力的效用。从某种意义来说,此类后代繁衍概率的均等再现,很可能会引发社会群体“人人皆可生育”[23]。
与传统范式应用不同,干细胞诱导分化、衍生配子技术,可以实现两个以上不同基因的父母亲系共同繁衍一个小孩,也称为“多重亲代”[24]。单一小孩的诞生,很可能通过几个基因遗传后代的快速演替繁殖而成。首先,两个体外胚胎可以通过夫妇自身配子或干细胞源配子的形式进行体外受精实现,该过程可来源于两个不同的夫妇;接着,通过上述胚胎可形成胚胎干细胞系,分化产生一系列潜在的可育配子,从而创建繁育一个新的胚胎。在此假设的情况下,4个不同的个体作为祖父母身份一起产生繁殖了一个小孩,该过程很可能也体现他们渴望的初衷,希望保留维系着与后代的遗传亲缘关系。
鉴于此类应用形式有悖于自然属性或存有其他缺陷,当前在学术界仍然饱受伦理学争议及道德偏见[25]。因此,在进行相关研究时应持谨慎的态度,同时避免采用“人造”配子或“合成”配子等术语,因为这些标签很可能会引发贬义倾向或歧视性印象,即干细胞源配子在伦理学层面不如或劣于其他类型的体外受精。其次,当前国际区域的相关法律法规,多数适用于由双亲( 父亲和母亲)及其孩子构成的核心家庭[26];然而通过上述形式产生的新型现代家庭,当前有必要从伦理学及法律等方面进行综合评估,兼顾衡量。
此外,这种新兴技术也亟待从社会学层面进行研究。对通过此类技术产生的小孩群体,应从其长远的福利受益情况进行综合评价。当前的普遍共识为,小孩的幸福安康应该作为优先考虑的伦理要素,特别针对体外受精等形式产生的后代。同时,应保证辅助生殖其医学方面的合理化,力趋让这一过程达到合理的福利标准,即未来诞生的小孩将有适当的机会获得可接受的生活质量[27]。当然,对于此类新型技术情况还需要做进一步的细化分析,但未来小孩的福利考虑可以作为此类研究的经验法则来参考。
第二,干细胞诱导分化、衍生配子研究的出现,给不孕患者带来不少潜在的社会压力,因为该项技术可以让他们实现繁衍“属于自己”小孩的愿望,该过程也可能会导致片面聚焦于基因遗传相关的小孩生育问题[28]。然而,此类问题应该引起足够的重视,因为配子衍生相关技术同样可以应用于体外受精的临床实践。而多数情况下,人类更倾向于养育存有自身血亲相关的后代,唯有获悉此抉择变得有现实困难或不可能实现的时候,很可能才会转向考虑其他选项。其次,是否生育小孩或者如何生养小孩等决定,在一定程度上也受限于夫妻双方的生育自主权利。尽管如此,在当前应该对不孕不育研究的社会价值进行细化监管,例如是否有必要将有限的财政经费及科研资源投资在日趋精确细化的生育研究当中[29-30]。
第三,倘若配子可以来源于皮肤细胞,这不仅会出现研究捐赠者不知情的情况,而且很可能会导致潜在父母的不知情,因为作为“捐赠者”或许根本无法获悉此类配子源自其本人的组织[26]。鉴于此类问题,有必要强化立法监管,对干细胞衍生配子的生成及使用进行操作流程规范化。此外,对辅助生殖技术涉及干细胞衍生配子的医学专家与父母,必须明确落实相关责任,统筹兼顾,综合衡量。
参考文献:
[1]钱万强,陈涛,江海燕.基于文献计量学的国内外干细胞研究热点分析[J].中国科技论坛,2012(2):152-159.
[2]陈涛,钱万强.国内外干细胞研究和产业发展态势分析[J].中国科技论坛,2011(10):150-153.
[3]HAYASHI K,OGUSHI S,KURIMOTO K,et al.Offspring from oocytes derived from in vitro primordial germ cell-like cells in mice[J].Science,2012,338(6109):971-975.
[4]HIKABE O,HAMAZAKI N,NAGAMATSU G,et al.Reconstitution in vitro of the entire cycle of the mouse female germ line[J].Nature,2016,539(7628):299-303.
[5]CYRANOSKI D.Mouse eggs made from skin cells in a dish[J].Nature,2016,538(7625):301.
[6]ZHOU Q,WANG M,YUAN Y,et al.Complete meiosis from embryonic stem cell-derived germ cells in vitro[J].Cell stem cell,2016,18(3):330-340.
[7]王珊珊,王宏起,高翔.我国干细胞产业技术标准化模式与策略研究[J].中国科技论坛,2014(10):54-59.
[8]高翔,王宏起,李玥.基于粗糙集的干细胞技术产业化潜力评价研究[J].中国科技论坛,2014(6):56-62.
[9]ISHII T,PERA R A.Creating human germ cells for unmet reproductive needs[J].Nature biotechnology,2016,34(5):470-473.
[10]HENDRIKS S,DONDORP W,DE WG,et al.Potential consequences of clinical application of artificial gametes:a systematic review of stakeholder views[J].Human reproduction update,2015,21(3):297-309.
[11]徐婕,周宁.公共财政支持的科研项目如何保障公众利益——来自美国加州干细胞研究项目的启示[J].中国科技论坛,2012(9):148-152.
[12]刘长秋.生物经济发展的法律需求及其立法原则研究[J].中国科技论坛,2014(3):48-52.
[13]HYUN I,WILKERSON A,JOHNSTON J,et al.Embryology policy:revisit the 14-day rule[J].Nature,2016:169-171.
[14]刘长秋,马彦.论人类遗传资源的国际法律地位——兼对中国立法之启示[J].中国科技论坛,2016(9):104-109.
[15]HYUN I.Policy:regulate embryos made for research[J].Nature,2014,509(7498):27-28.
[16]BREDENOORD A L,CLEVERS H,KNOBLICH J A.Human tissues in a dish:the research and ethical implications of organoid technology[J].Science,2017,355(6322).
[17]DALEY G Q,HYUN I,APPERLEY J F,et al.Setting global standards for stem cell research and clinical translation:the 2016 ISSCR guidelines[J].Stem cell reports,2016,6(6):787-797.
[18]《干细胞临床研究管理办法(试行)》解读.中华人民共和国国家卫生与计划生育委员会,2015[EB/OL].(2017-04-30).http://www.nhfpc.gov.cn/zwgk/jdjd/201508/e941634d667c4e25bae62566da537363.shtml.
[19]US Government 2009,Code of Federal Regulations Title 45,Part 46.101.b.2[EB/OL].(2017-04-30).https://www.hhs.gov/ohrp/sites/default/files/ohrp/policy/ohrpregulations.
[20]王太平,徐国彤,周琪,等.国际干细胞研究学会《干细胞临床转化指南》[J].生命科学,2009(5):747-756.
[21]COHEN I G,DALEY G Q,ADASHI E Y.Disruptive reproductive technologies[J].Science translational medicine,2017,9(372):eaag2959.
[22]罗会宇,雷瑞鹏.我们允许做什么?——人胚胎基因编辑之反思平衡简[J].伦理学研究,2017,38(2):111-117.
[23]TESTA G,HARRIS J.Ethics and synthetic gametes[J].Bioethics,2005,19(2):146-166.
[24]PALACIOSGONZáLEZ C,HARRIS J,TESTA G.Multiplex parenting:IVG and the generations to come[J].Journal of medical ethics,2014,40(11):752-758.
[25]NUSSBAUM M C.Hiding from humanity:disgust,shame,and the law[J].Dissent,2013,60(2):18.
[26]SMAJDOR A,CUTAS D.Artificial gametes and the ethics of unwitting parenthood[J].Journal of medical ethics,2014,40(11):748-751.
[27]BREDENOORD A L,PENNINGS G,WERT G D.Ooplasmic and nuclear transfer to prevent mitochondrial DNA disorders:conceptual and normative issues[J].Human reproduction update,2008,14(6):669-678.
[28]ILIOI E C,GOLOMBOK S.Psychological adjustment in adolescents conceived by assisted reproduction techniques:a systematic review[J].Human reproduction update,2014,21(1):84-96.
[29]CUTAS D,DONDORP W,SWIERSTRA T,et al.Artificial gametes:perspectives of geneticists,ethicists and representatives of potential users[J].Medicine,health care and philosophy,2014,17(3):339-345.
[30]HENDRIKS S,DONDORP W,DE W G,et al.Potential consequences of clinical application of artificial gametes:a systematic review of stakeholder views[J].Human reproduction update,2015,21(3):297-309.
