磁性聚苯乙烯-苯甲氨二乙酸对Cu2+富集性能的研究
2018-04-09张慧娟刘王玮吕浩永刘惠玲
张慧娟, 刘王玮, 吕浩永 , 刘惠玲,2
(1 中南民族大学 化学与材料科学学院,武汉430074;2中南民族大学 实验教学与实验室管理中心,武汉 430074)
铜元素是人体蛋白质和酶的重要组成部分,若缺乏或有过量的铜均会产生不同的病症[1]. 环境中过量的铜离子对人类造成极大的危害,因此监控环境中的铜离子含量十分重要.目前,测定痕量铜离子的常用分析方法有分子吸收光度法、原子吸收光谱法[2]、阳极溶出伏安法[3]、电感耦合原子发射光谱法[4]等.这些分析方法容易受到样品基质影响,通常都需要对样品进行复杂的前处理,因此发展快速简洁处理水样中铜离子的固相分离富集材料十分重要.
近年来,由于磁性固相分离富集材料具有较高的分离效率和重用性得到了广泛应用[5].聚合物复合材料在环境保护领域应用显示巨大潜力[6].其中聚苯乙烯类材料具有廉价易得[7]、刚性好、低吸水性、易于合成且耐酸碱的优点[8],使磁性聚苯乙烯修饰材料同时具有磁性纳米材料与聚合物的双重优势,已应用于废水处理[9]、食品检测[10]、新兴污染物检测[11]等领域.但聚苯乙烯材料上能与金属离子发生配位或者离子交换的活性基团较少,因此通过选择性质各异单体制备适用于富集金属离子的磁性聚苯乙烯类材料,对拓展其在有害金属治理及监测方面的应用有一定的实用性和优越性.
基于此,本文以磁性硅胶微球(Fe3O4@SiO2-MPS)为基质,N-(4-乙烯基)-苯甲氨二乙酸(VBIDA)为单体,m(PEG2000)∶m(甲苯)=2∶1的混合溶液为制孔剂,二乙烯基苯为交联剂在偶氮二异丁腈引发下合成了磁性聚苯乙烯-苯甲氨二乙酸(Fe3O4@SiO2@PS-BIDA)材料.通过透射电子显微镜(TEM)、傅里叶红外光谱(FT-IR)和热重分析(TG)等对材料的结构和形貌进行了表征,并以Cu2+为研究对象,考察了磁性聚苯乙烯-苯甲氨二乙酸材料对金属离子的富集性能.
1 实验部分
1.1 试剂与仪器
偶氮二异丁腈(AIBN)、亚氨基二乙酸(IDA)、γ-甲基丙烯酰氧基丙基三甲氧基硅烷(MPS)购于上海阿拉丁生化科技股份有限公司;四氧化三铁(Fe3O4)纳米粒子、正硅酸四乙酯(TEOS)、聚乙二醇(PEG)2000、4-氯甲基苯乙烯(VBC)、二乙烯基苯(DVB)、乙二胺四乙酸(EDTA)、甲苯、无水硫酸铜、氢氧化钾(KOH)、甲醇、乙醚、盐酸(HCl)、异丙醇、乙醇、磷酸、二水合磷酸二氢钠均购自国药集团化学试剂有限公司.所有试剂均为分析纯.
智能傅里叶红外光谱仪(NEXUS 470,美国Thermo Nicolet),热重分析仪(TG-209F3型,德国NETZSCH),原子吸收分光光谱仪(AA-6300型,日本岛津),透射电子显微镜(JEM-100CX II型,日本Jeol).
1.2 复合材料的制备
1.2.1VBIDA的制备
将0.959 g IDA加入含有50 mL(0.2 mol·L-1)KOH的甲醇溶液的三口烧瓶中,60 ℃下搅拌并逐滴加入蒸馏水使之溶解.加入465 μL VBC和10 mL(1 mol·L-1)KOH的甲醇溶液,30 min后继续加入等量的VBC.反应24 h后,蒸发部分溶剂并用乙醚萃取,取下层溶液,逐滴加入少量盐酸直至生成大量沉淀.将沉淀抽滤后在50 ℃下真空干燥12 h后得到产品.
1.2.2磁性聚苯乙烯-苯甲氨二乙酸材料的制备
合成过程如图1所示.称取1.0 g制备的VBIDA,分多次加入V(异丙醇)∶V(二甲亚砜) =10∶1的混合溶液30 mL,直至完全溶解,并加入2.5 mL DVB和0.96 mL的m(PEG2000)∶m(甲苯)=2∶1的混合溶液,超声5 min后转入三口烧瓶.磁性MPS修饰硅胶微球的方法参照文献[12].加入250 mg磁性MPS修饰硅胶微球和30 mg AIBN,氮气保护,70 ℃下反应10 h后用乙醇洗净并在50 ℃下真空干燥12 h得到产品.
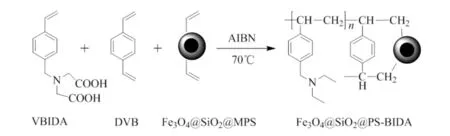
图1 Fe3O4@SiO2@PS-BIDA的合成示意图Fig.1 Synthetic schematicdaiageam of Fe3O4@SiO2@PS-BIDA
1.2.3Cu2+的吸附实验
准确称取一定量的复合材料于刻度试管中,用5 mL甲醇活化两次.加入10 mL一定pH值的 25 mg·L-1的Cu2+标准溶液中,25 ℃下涡旋一定时间后用磁铁分离.用火焰原子吸收分光光度法测定吸附前后溶液中Cu2+浓度,依下式计算吸附量qt:
(1)
式中:V为Cu2+溶液体积(mL);m为吸附剂重量(mg);ρ0和ρt分别为吸附前、吸附t分钟后Cu2+浓度(mg·L-1) .依下式计算吸附率η:
(2)
式中:mt为不同时间吸附Cu2+的质量;me为理论上吸附Cu2+的质量.
1.2.4Cu2+浓度测定方法
火焰原子吸收分光光度法测定Cu2+,仪器检测波长325 nm,灯电流2 mA,燃烧头高度5 mm,空气流量2.5 L·min-1,乙炔流量0.5 L·min-1,狭缝宽度0.2 nm.分别配制浓度为1, 25, 50, 75, 100 mg·L-1的Cu2+溶液,并用火焰原子吸收分光光度法测定溶液的吸光度,以吸光度对Cu2+浓度作图得到Cu2+工作曲线.线性方程为A= 0.02399ρ-0.00816,线性方程的相关系数R2为0.9991.在吸附实验后,可通过测定的吸光度,由线性方程计算对应的Cu2+浓度.通过Cu2+的浓度利用公式(2)计算吸附率.
1.2.5Cu2+的洗脱实验
将吸附后的材料用外磁场收集,用5 mL的蒸馏水洗净富集材料,氮气吹干.再加入2 mL洗脱液,室温下涡旋震荡15 min后在外磁场存在下移走洗脱液,测定其吸光度值A,依下式计算洗脱率D.R:
(3)
式中:m为洗脱液中Cu2+的质量;m0为水溶液中Cu2+的初始质量.
2 结果与讨论
2.1 磁性聚苯乙烯-苯甲氨二乙酸材料的表征
2.1.1傅里叶红外光谱
Fe3O4@SiO2MPS和Fe3O4@SiO2@PS-BIDA的红外光谱图见图2.由图2可知:在Fe3O4@SiO2MPS中,3443 cm-1处为―OH的伸缩振动峰,1083 cm-1处为Si―O键的不对称伸缩振动峰,1710 cm-1处为C==O双键的伸缩振动特征峰,590 cm-1处为Fe―O的伸缩振动峰.将Fe3O4@SiO2@PS-BIDA的红外谱图与之比较发现:在2927 cm-1处具有明显峰,这是亚甲基的特征吸收峰;而3443 cm-1处峰强度明显增大,因为包覆的VBIDA上含有两个羧基使得材料上―OH含量增大,导致峰强度增加.而1639,1619 cm-1处出现强吸收峰,这是由材料上含有的苯环基团所引起;1210 cm-1的峰则是由C―N的伸缩振动引起的.从红外光谱来看,材料具有苯环、叔胺基、羧基等特征基团.
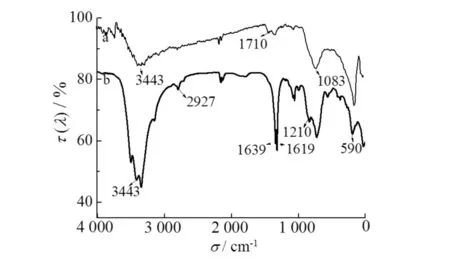
a) Fe3O4@SiO2MPS;b) Fe3O4@SiO2@PS-BIDA图2 磁性聚合材料的红外光谱图Fig.2 FTIR spectra of magnetic polymer materials
2.1.2热重分析
为了考察材料的热稳定性和组分,通过热重分析仪对材料进行了表征,结果见图3.由图3可知:制备材料在100~480 ℃有两个明显失重阶段,223, 430 ℃质量损失最明显;当温度升至223 ℃时,复合物材料上功能基团如羧酸基团分解;430 ℃时,材料上聚苯乙烯基质部分燃烧,引起质量较大损失;948.3 ℃时,仍有质量分数为46.32%的物质未被分解,因为剩余的磁性粒子和硅胶基质未达到分解温度而残留.
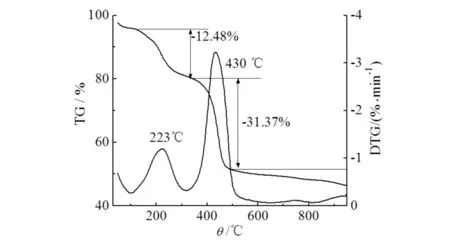
图3 Fe3O4@SiO2@PS-BIDA的热重图Fig.3 TGDTG curves of Fe3O4@SiO2@PS-BIDA
2.1.3透射电子显微镜
为观察材料的微观形貌特征,利用TEM对材料进行了表征,结果见图4.由图4可见:材料呈球状,粒径范围约为30~120 nm.球状内核深黑色部分为磁性Fe3O4纳米粒子,浅灰色部分为包覆上去的聚合物,证明聚合物已经成功地包覆在了Fe3O4纳米粒子表面.

图4 Fe3O4@SiO2@PS-BIDA的透射电镜图Fig.4 TEM image ofFe3O4@SiO2@PS-BIDA
2.2 磁性聚苯乙烯-苯甲氨二乙酸材料吸附及洗脱性能的考察
2.2.1吸附剂用量对材料吸附性能的影响
不同吸附剂用量对Cu2+的吸附性能影响结果见图5.
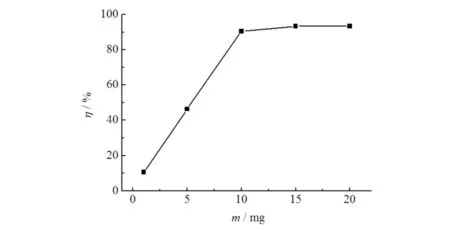
图5 吸附剂用量对Cu2+吸附效果的影响Fig.5 Effect of adsorbent amount on adsorption of Cu2+
图5中,当采用10 mL,pH为5 的Cu2+溶液(25 mg·L-1)时,材料对Cu2+吸附率随其用量的增大先增大而后趋于稳定.因为随着吸附剂用量的增加,与Cu2+作用的活性位点增多;但当吸附剂用量超过10 mg后,材料对Cu2+吸附率达93%,溶液中Cu2+基本被完全吸附,再增加吸附剂用量,吸附率不再明显增加.故吸附剂用量选10 mg更合适.
2.2.2pH值对材料吸附性能的影响
在pH 3.0~9.0内考察pH值变化对材料吸附Cu2+效果的影响,结果见图6. 由图6可见:材料用量为10 mg,其他条件不变时,pH值对材料吸附Cu2+影响不大,吸附率均在80%以上.当pH值为4.0~6.0时,吸附率最大;当pH值较小时,材料上的羧酸基团不易电离,降低了Cu2+与吸附位点之间的离子交换作用力;随着溶液pH值增大至碱性时,溶液中OH-增加,与Cu2+形成配合物,影响Cu2+与吸附位点结合,不利于材料对Cu2+的吸附.故选择pH=5.0作为吸附的最佳pH值.
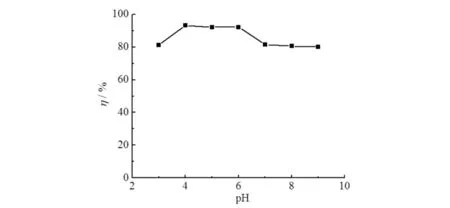
图6 pH值对Cu2+吸附效果的影响Fig.6 Effect of pH value on adsorption of Cu2+
2.2.3Cu2+初始浓度对材料吸附性能的影响
当材料用量为10 mg,Cu2+溶液的体积为10 mL,其他条件不变时,测定了5组不同初始浓度下材料的吸附率和吸附量,结果见图7.如图7所示:除了浓度为1 mg·L-1的Cu2+溶液外,其余吸附达到平衡的时间约为15 min;随Cu2+初始浓度的增大,吸附量也随之增大(见图7a).因为材料吸附能力较强,当初始浓度较低时吸附速度很快,达到平衡所需时间短.随着Cu2+浓度增大,材料与Cu2+发生吸附的几率增大,吸附量增加.但材料对Cu2+的吸附率基本保持不变(见图7b),只有当Cu2+的初始浓度为100 mg·L-1时,才发生了明显降低,由于材料上的吸附位点在高Cu2+浓度下趋于饱和,出现吸附率降低.
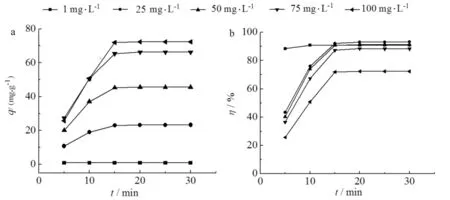
a) 不同吸附量;b) 不同吸附率图7 Cu2+的初始浓度对材料吸附能力的影响Fig.7 Effect of initial Cu2+ concentration on material adsorption capacity
2.2.4吸附动力学研究
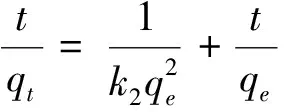

表1 磁性聚苯乙烯苯甲氨二乙酸材料对Cu2+的吸附动力学Tab.1 Adsorption kinetic of Cu2+ onto Fe3O4@SiO2@PS-BIDA materials
2.2.5共存离子对吸附性能的影响
为考察共存离子对Cu2+吸附性能的影响,将2 mg·L-1Cu2+和一定浓度的共存离子混合,在最佳吸附条件下,测定Cu2+的吸附率,结果如表2所示.由表2可知:不同共存离子对Cu2+吸附率的干扰程度不同;Zn2+和Mn2+对吸附率影响较小,其他4种离子影响略大.但总体来说,在复杂金属离子环境中,材料对Cu2+的富集具有较大优势,同时推测材料对其他金属离子也具有一定的富集能力.
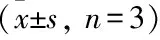

共存离子ρ/(mg·L-1)η(Cu2+)/%Na+6076±0.5K+4076±0.5Ca2+4070±1.6Mg2+4070±1.6Mn2+4085±0.2Zn2+4090.7±0.1
2.2.6洗脱条件的考察
分别以HCl和EDTA为洗脱液,其他条件不变,洗脱15 min,考察了它们对制备材料的洗脱能力,结果见图8. 如图8所示:0.1 mol·L-1的EDTA相比于1 mol·L-1HCl和0.01 mol·L-1EDTA,在洗脱能力上具有明显优势;当第2个1 mL的洗脱液洗脱时,0.1 mol·L-1的EDTA洗脱率达到了95%,而1 mol·L-1HCl和0.01 mol·L-1的EDTA的洗脱率分别为59%和15%;需要4 mL HCl才能将83%的目标物洗脱.因此选择2 mL EDTA(0.1 mol·L-1)作为洗脱液.
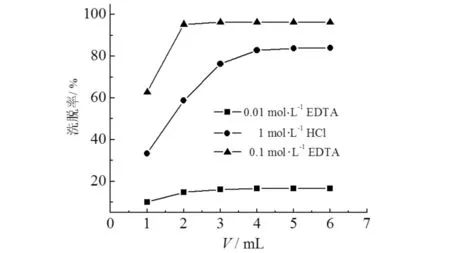
图8 不同洗脱剂对Fe3O4@SiO2@PS-BIDA洗脱效果的考察Fig.8 Eluting effect of different eluent forFe3O4@SiO2@PS-BIDA
3 结语
本文以N-(4-乙烯基)-苯甲氨二乙酸为单体,以二乙烯基苯为交联剂,m(PEG2000)∶m(甲苯)=2∶1的混合溶液为致孔剂,在偶氮二异丁腈引发下合成了磁性聚苯乙烯-苯甲氨二乙酸材料.通过透射电镜、傅里叶红外光谱和热重分析表征证实了聚合物成功地包覆在Fe3O4纳米粒子表面,材料呈球状,有一定的机械强度. 当Cu2+溶液浓度为25 mg·L-1、体积为10 mL, pH值为5时,10 mg吸附剂在15 min达到吸附平衡且吸附率可达93%.采用2 mL(0.1 mol·L-1)乙二胺四乙酸溶液在15 min可对其完成小体积快速洗脱,洗脱率可达95%.Cu2+在材料上的吸附行为与准二级动力学模型拟合较好,其吸附由多种机理共同作用.该材料作为固相分离富集材料在水体中金属离子的检测中具有较好的应用前景,后期可对材料进行改性,利用金属亲和蛋白质和氨基酸的作用将材料的应用范围拓宽.
[1]Huang D,Kong J,Seng Y. Effects of the heavy metal Cu2+on growth,development,and population dynamics ofSpodopteralitura(Lepidoptera: Noctuidae)[J]. J Econ Entomol,2012,105(1): 288-294.
[2]Al Othman Z,Unsal Y E,Habila M,et al. Determination of copper in food and water by dispersive liquid-liquid microextraction and flame atomic absorption spectrometry[J]. Anal Lett,2015,48(11): 1738-1750.
[3]Liang Y,Liu Y,Guo X,et al. Phytate functionalized multi-walled carbon nanotubes modified electrode for determining trace Cu (II) using differential normal pulse anodic stripping voltammetry[J]. Sensor Actuat B-Chem,2014,201(4): 107-113.
[4]Yilmaz V,Arslan Z,Hazer O,et al. Selective solid phase extraction of copper using a new Cu (II)-imprinted polymer and determination by inductively coupled plasma optical emission spectroscopy (ICP-OES)[J]. Microchem J,2014,114: 66-72.
[5]Tang S C N,Lo I M C. Magnetic nanoparticles: essential factors for sustainable environmental applications[J]. Water research,2013,47(8): 2613-2632.
[6]Fan J,Zhang S. Facile preparation of Fe3O4/mesoporous TiO2,nanoparticles shell on polystyrene beads and its effective absorption of cyanobacteria in water[J]. J Polym Res,2015,22(9):1-5.
[7]陈胜慧,李林,张道洪.表面功能化聚苯乙烯纳米球的制备及其性能[J].中南民族大学学报(自然科学版),2017,36(3):6-9
[8]Yan X,He Q,Zhang X,et al.Magnetic polystyrene nanocom-posites reinforced with magnetite nanoparticles[J]. Macromol Mater Eng,2014,299(4): 485-494.
[9]Gu H,Lou H,Ling D,et al. Polystyrene controlled growth of zerovalent nanoiron/magnetite on a sponge-like carbon matrix towards effective Cr (VI) removal from polluted water[J]. RSC Adv,2016,6(111): 110134-110145.
[10]Yu Y,Fan Z.Determination of Rhodamine B in beverages using a polystyrene-coated magnetite nanocomposite for magnetic solid phase extraction[J]. Anal Lett,2016,49(12): 1835-1846.
[11]Gu H,Lou H,Tian J,et al. Reproducible magnetic carbon nanocomposites derived from polystyrene with superior tetrabromobisphenol A adsorption performance[J]. J Mater Chem A,2016,4(26): 10174-10185.
[12]胡静荣,吕浩永,刘惠玲,等. 磁性聚苯乙烯-氯甲基苯乙烯材料的合成及其对蒽的吸附性能研究[J]. 分析测试学报,2017,36(4):464-470.
