基于《欧洲药典》和《中华人民共和国药典》中黄芪质量控制的比较研究
2018-03-11姜庆华林评兰谢瑞芳李瑶周昕
姜庆华+林评兰+谢瑞芳+李瑶+周昕
摘 要 目的:对《欧洲药典》和《中华人民共和国药典》中黄芪部分进行比较。方法:根据《欧洲药典》和《中华人民共和国药典》,对国内和巴黎购买的3批次黄芪饮片进行质量控制。结果:这3批次饮片均符合《欧洲药典》和《中华人民共和国药典》要求。结论:虽然《中华人民共和国药典》与《欧洲药典》对黄芪的质量控制的要求有一定区别,但是无论是性状鉴别、指标成分的含量,还是安全性检查,《中华人民共和国药典》均不低于《欧洲药典》。
关键词 欧洲药典 中华人民共和国药典 黄芪 质量控制
中图分类号:R921 文献标识码:A 文章编号:1006-1533(2018)03-0077-06
Comparison of the quality control of Astragalus mongholicus Radix based on European Pharmacopoeia and Chinese Pharmacopoeia*
JIANG Qinhua1**, LIN Pinglan1,2** , XIE Ruifang1, LI Yao1, ZHOU Xin1***
(1. Department of pharmacy, Longhua Hospital affiliated to Shanghai University of Traditional Chinese Medicine, Shanghai 200032, China; 2. Department of nephrology, Shuguang Hospital affiliated to Shanghai University of Traditional Chinese Medicine; TCM institute of kidney disease, Shanghai University of Traditional Chinese Medicine; Shanghai Key Laboratory of Traditional Chinese Clinical Medicine, Shanghai 201203, China)
ABSTRACT Objective: To compare the quality control of Astragalus mongholicus Radix based on European Pharmacopoeia and Chinese Pharmacopoeia. Methods: The quality control was performed to three batches of Astragalus mongholicus Radix from China and Paris, France based on European Pharmacopoeia and Chinese Pharmacopoeia. Results: The results showed they all met the requirements of both European and Chinese Pharmacopoeias. Conclusion: Although some differences exist between two Pharmacopoeias, the quality criteria of Chinese Pharmacopoeia for Astragalus mongholicus Radix are not inferior to those of European Pharmacopoeia in the identification of characteristics, the content of mark ingredient and safety examination.
KEY WORDS European Pharmacopoeia; Chinese Pharmacopoeia; Astragalus mongholicus Radix; quality control
虽然中药有较好的临床效果,但在法国和欧盟的范围内传统中药仅能以保健品、食品的名义合法销售,而非药品。在欧盟药典中,黄芪也有专论,这就意味着,其相关饮片在欧洲应用,也需符合《欧洲药典》的要求。本文以黄芪饮片为例,探讨了《欧洲药典》和《中华人民共和国药典》的异同,为我国中药饮片进入国际市场提供参考。
1 实验仪器与材料
1.1 实验仪器
台式显微镜,分析天平,高效液相色譜、二级阵列管检测器,超声仪,台式离心机,旋转蒸发仪,超高效液相色谱、ELSD检测器,Waters色谱柱。
1.2 试剂与材料
50%甘油,正丁醇,正庚烷,冰醋酸,甲醇,乙醇,乙腈,磷酸,氨水,乙酸乙酯;硅胶薄层色谱板gel 60 F254,刻度毛细管,十八烷基甲硅烷硅胶小柱(40~60 μm)。
1.3 对照品
黄豆苷(≥99%),黄豆苷元(≥99%),黄芪甲苷对照品,人参皂苷(≥99%)。
1.4 饮片
黄芪饮片分不同时间购买,其产地、来源等如表1所示。上述饮片基源由生药学专家何波鉴定为蒙古黄芪(Astragalus mongholicus var. Mongholicus)的干燥根。这些饮片均符合《中华人民共和国药典》对黄芪的质量要求。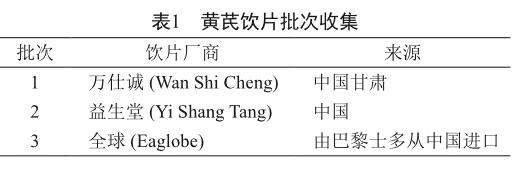
2 实验方法与结果
2.1 黄芪饮片粉末显微鉴定
将黄芪饮片样本打粉,过355号筛(药筛孔径为355 μm,相当于《中华人民共和国药典》中规定的3号药筛),形成黄白色粉末,滴加水合氯醛溶液在显微镜下检视。endprint
显微特征结果表明,木纤维独立散在或成簇,表面隔板增厚或纵裂增厚,初生细胞壁与次生细胞壁分开,两者末尾破碎(批次1,批次2)或成批次3的流苏状,或者被轻微截断。无色或橘色具缘纹孔导管紧密排列,木栓组织多层,多数伴有(栓内层)厚角组织化。石细胞多数可见,圆形、椭圆形、不规则形,细胞壁轻微增厚。滴加50%甘油溶液,置于显微镜下检视,小型圆形或卵圆形淀粉颗粒,通常单个或2、3个复粒散在分布,符合《欧洲药典》质量要求。
2.2 黄芪饮片薄层色谱定性研究
供试品溶液:称取3 g饮片粉末,加入50 ml甲醇加热回流50 min,滤过。滤液减压蒸干溶剂,加入1 ml水复溶。溶液加于预先以3 ml甲醇和3 ml水预洗过含有6 ml十八烷基硅烷键硅胶的固相提取柱中,以水15 ml洗脱,弃去水液,再用30%甲醇25 ml洗脱,弃去洗脱液,继用20 ml甲醇洗脱,收集洗脱液,减压蒸干后以2 ml甲醇复溶;对照品溶液:1 mg/ml大豆苷元,2 mg/ml大豆苷混合溶液;薄层板:TLC硅胶F254,硅胶粒径为2~10 μm;流动相:水-甲醇-乙酸乙酯(10∶13.5∶100 V/V/V);点样:取样3 μl,8 mm条带,溶剂展开7 cm;检测:挥干,于254 nm紫外灯下检测,茴香醛溶液处理后,100 ℃加热3 min,至365 nm紫外灯下检测。
结果表明,在254 nm紫外灯下(图1Ⅰ),供试液与对照溶液中大豆苷元在上方相同位置显示荧光斑带,与对照溶液中大豆苷在下方相同位置显示荧光斑带;在365 nm紫外灯下(图1Ⅱ),对照溶液中大豆苷和大豆苷元显示蓝白色荧光斑带,供试品溶液在相同位置显示棕色斑带,同时供试溶液在点样板上方区域显示多条紫色斑带,在点样板下方区域显示多条棕色斑带,符合《欧洲药典》要求。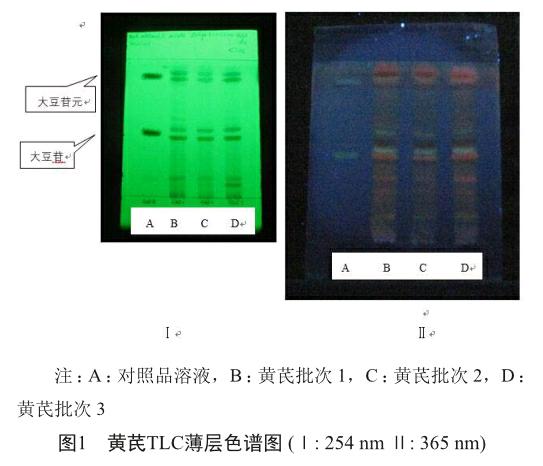
2.3 黄芪指标化合物定量研究
2.3.1 两种提取方法供试品溶液的制备
按照《欧洲药典》8.0版,取黄芪饮片,干燥后,打成中粉,取约4 g粉末,精密称定,置索氏提取器中,加甲醇40 ml,冷浸过夜,再加甲醇适量,加热回流4 h,提取液回收溶剂并浓缩至干,残渣加水10 ml,微热使溶解,用水饱和的正丁醇振摇提取4次,每次40 ml,合并正丁醇液,用氨水充分洗涤2次,每次40 ml,弃去氨水,正丁醇液蒸干,残渣加水5 ml使溶解,放冷。溶液通过预先以5 ml甲醇和5 ml水预洗过的含有1 g十八烷基硅烷键硅胶的固相提取柱中,以水20 ml洗脱,再用25%乙醇25 ml洗脱,弃去洗脱液,继用70%乙醇25 ml洗脱,收集洗脱液,蒸干,残渣加甲醇溶解,转移至5 ml量瓶中,加甲醇至刻度,摇匀,溶液经过0.45 μm尼龙滤膜过滤,取续滤液,即得。
按照《欧洲药典》修订版27.4取供试品粉约4 g,精密称定,加甲醇40 ml,80 ℃超声提取30 min,离心7 min取上清液,残渣加甲醇25 ml,80 ℃超声提取30 min,离心7 min取上清液,重复上述提取离心过程,合并所有上清液,提取液回收溶剂并浓缩至干,残渣加水10 ml,微热使溶解,用水饱和的正丁醇振摇提取4次,每次40 ml,合并正丁醇液,用氨水充分洗涤2次,每次40 ml,弃去氨水,正丁醇液蒸干,残渣加甲醇溶解,转移至5 ml量瓶中,加甲醇至刻度,摇匀。溶液经过0.45μm尼龙滤膜过滤,取续滤液,即得。
2.3.2 对照溶液的制备
精密称取10 mg黄芪甲苷对照品,用甲醇溶解配成1 mg/ml的对照品溶液(a),稀释成不同浓度的对照品溶液(b)、(c)、(d);精密称取5 mg人参皂苷rb1对照品,用5 ml甲醇溶解,用对照品溶液(a)定容至10 ml,得到对照品溶液(e)。
2.3.3 液相条件
C18色谱柱(0.1 m× 2.1 mm×1.8 μm)。温度:40 °C;流速:0.6 ml/min;进样量:2 μl;用Waters蒸发光散射检测器检测(漂移管温度:40 °C,载气:空气);流动相:0.1%甲酸水溶液-0.1%甲酸乙腈溶液(13∶87,V/ V),具体比例见表2。
2.3.4 色谱结果
结果表明(图2,3),在现有色谱条件下,均得到了良好分离。在对照品溶液中,人参皂苷与黄芪甲苷先后出峰,峰型对称,保留时间分别为6.12 min和6.75 min,两峰的分离度为6.3,符合药典要求;两种不同提取方式处理的单个批次的供试品溶液中,黃芪甲苷出峰时间均为6.75 min,峰型对称。
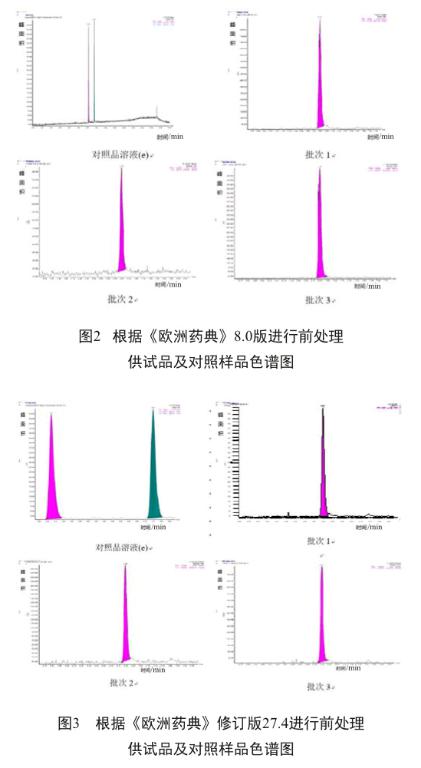
将对照品溶液浓度对数为横坐标,峰面积对数为纵坐标绘制对照品浓度-峰面积双对数标准曲线,结果表明(表4),黄芪甲苷在0.097 8~0.489 mg/ml的范围内有良好的线性,相关系数为0.996。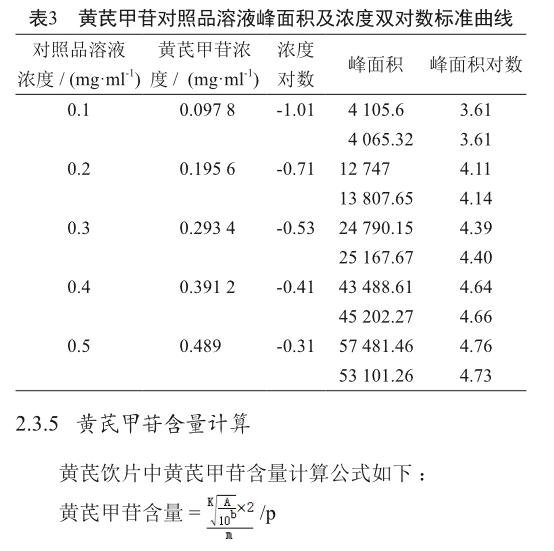
A=样品溶液中黄芪甲苷色谱峰面积;K=黄芪甲苷对照品溶液峰面积及浓度双对数标准曲线斜率;b=黄芪甲苷对照品溶液峰面积及浓度双对数标准曲线截距;m=干燥的黄芪供试品粉末质量(g);p =药典黄芪甲苷对照品中黄芪甲苷的纯度(97.8%)。
黄芪饮片粉末根据《欧洲药典》和修订版27.4中两种方法进行前处理之后。结果表明,3批饮片样品中,黄芪甲苷含量测定结果均符合0.040%的最低定量限要求。相同批次的黄芪两次测得含量并不相同,但结果无明显数量级的差异(表4)。endprint
分析原因可能是由样品前处理中提取、转移等操作步骤引起。故无法单从已知的测定结果中简单判定两种方法的优劣。两种方法皆采用水饱和正丁醇萃取并用饱和氨水洗涤,可除去溶液中酚、酸性成分并富集皂苷类成分[1]。《欧洲药典》方法中,供试品溶液通过十八烷基硅烷键硅胶的固相提取柱,富集和纯化溶液中皂苷类成分,所得溶液相比步骤简化的《欧洲药典》修订版27.4的提取方法所得供试品溶液外观更为澄清透明,但是,作为药典质量控制的专论,《欧洲药典》修订版27.4采用的超声波加热回流提取方法,操作更为简便、节省时间,在实际检测工作中具有更大的优势。至于两种方法中,批次1的数据降低与批次2、3的升高的趋势相反,可能是操作的误差引起的。
黄芪中含有大量以黃芪甲苷为代表的环黄芪醇皂苷,均为三萜皂苷,如黄芪皂苷Ⅰ、黄芪皂苷Ⅱ和异黄芪皂苷等[2-3]。环黄芪醇皂苷含有相同的苷元母核,因配糖体部分不同而分为多种皂苷,环黄芪醇皂苷的配糖体上有3个取代位置,黄芪甲苷糖体3个位置均与OH相连,而其它环黄芪醇皂苷配糖体上联接OH或OAc,故工业提取中采用皂化反应原理,在氢氧化钾的作用下,将所有的环黄芪醇皂苷、乙酰化转化为黄芪甲苷,可增加提取率。而在中国与欧洲药典黄芪甲苷提取中,均不采用乙酰化反应,体现了专论方法的专一性和稳定性,精确有效地测量饮片中有效成分的含量。
黄芪甲苷仅有紫外末端吸收,用紫外(203 nm)检测时杂质干扰大、溶剂背景吸收难以消除[4-5],故采用ELSD检测器,样品颗粒与蒸发光发生多个类型的散射过程[6],直接以峰面积值和相对应的样品浓度计算标准曲线时,得到线性结果较差,而将峰面积与样品浓度值分别取自然对数后可得更理想的线性关系(r=0.998 2) [7]。ELSD 检测器为质量型检测器,不受外部环境干扰,试剂在检测器中全部蒸发,不干扰检测,灵敏度、稳定性及重现性亦能符合含量测定的要求。
2.42.5 《欧洲药典》与《中华人民共和国药典》黄芪专论标准和方法的比较研究
根据《欧洲药典》8.0版与《中华人民共和国药典》2015年版中的黄芪部分质量和标准的比较,归纳整理如表5。
可得到如下结论:①两药典规定的黄芪饮片基源、采收时间以及加工方式有一定的区别。②在性状鉴定方面,《中华人民共和国药典》对于黄芪的干燥饮片外观、性状有详细的描述与要求,并对饮片横截面有具体显微结构描述,而《欧洲药典》对饮片横截面没有具体要求。③在薄层色谱鉴定方面,《欧洲药典》中黄芪采用大豆苷与大豆苷元进行饮片鉴定,以区别于含量测定中所使用的阿魏酸与黄芪甲苷,避免重复。而《中华人民共和国药典》中,饮片薄层色谱鉴定与含量测定采用的对照品均为黄芪甲苷。此外,《中华人民共和国药典》薄层鉴别还使用黄芪对照饮片。④在其他测试方面,《中华人民共和国药典》具有浸出物、重金属及有害元素、有机氯农药含量的限制要求;而《欧洲药典》将上述内容归纳为杂质及酸不溶性灰分。⑤在含量测定方面,两者对于黄芪中的黄芪甲苷要求是相同的。《欧洲药典》在黄芪对照品溶液中加入人参皂苷rb1,用以确定液相系统检测条件的适用性,使测量结果更为准确可信。《中华人民共和国药典》中对于对黄芪有毛蕊异黄酮苷含量至少为0.020%的要求,而《欧洲药典》则没有。
3 结语
本文根据《欧洲药典》和《中华人民共和国药典》对国内以及在巴黎十三区华人街购买的黄芪饮片进行初步的质量研究,结果表明这3批次饮片符合《欧洲药典》和《中华人民共和国药典》要求。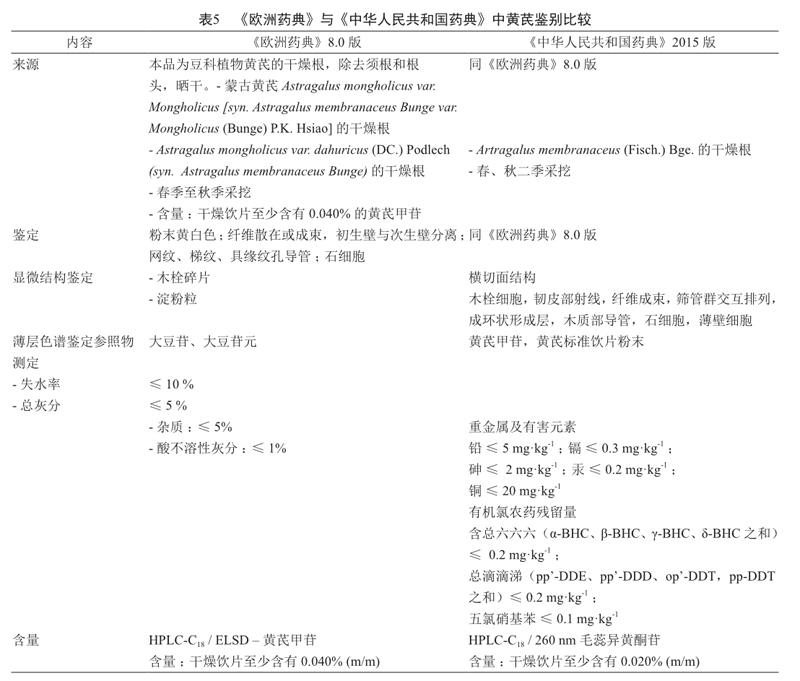
我们将《欧洲药典》与《中华人民共和国药典》中对黄芪饮片质量要求进行比较,可以看出,虽然《中华人民共和国药典》与《欧洲药典》对黄芪的质量控制的要求有一定区别,但是无论是性状鉴别、指标成分的含量,还是安全性检查,《中华人民共和国药典》均不低于《欧洲药典》。
参考文献
[1] 刘浩文, 刘嘉仪, 杨妙荣, 等. 黄芪药材中黄芪甲苷含量测定的两种方法的比较研究[J]. 中药新药与临床药理, 2011, 22(6): 659-662.
[2] 王金山. 黄芪中有效成分环黄芪醇皂苷和黄芪甲苷的含量测定[J]. 海峡药学, 2009, 21(2): 39-41.
[3] 刘正磊, 冯素香, 李娟,等. 高效液相-蒸发光散射检测法测定黄芪药材中黄芪甲苷含量[J]. 中医学报, 2012, 27(3): 334-335.
[4] 邬成华. 高效液相色谱-蒸发光散射检测法测定黄芪注射液中黄芪甲苷含量[J]. 上海医药, 2001, 22(2): 83-84.
[5] 张凯, 尹子郡, 张跃进, 等. HPLC法测定复方乌骨藤胶囊中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J]. 西北林学院学报, 2016, 31(1): 250-253.
[6] 李翔, 朱臻宇, 朱东亮, 等. 高效液相色谱-蒸发光散射检测梯度洗脱法测定黄芪药材中黄芪甲苷的含量[J]. 第二军医大学学报, 2006, 27(3): 331-333.
[7] 王建舫, 胡格, 张涛, 等. 高效液相色谱-蒸发光散射法测定芪参口服液中黄芪甲苷的含量[J]. 中兽医医药杂志, 2012, 31(5): 11-14.endprint
