罗丹明B酰肼柱前衍生—高效液相色谱—质谱联用法测定蜂蜜中的苯甲醛残留量
2018-03-11陈栎颖朱贵萍曹瑞芳钟婷婷申光辉罗擎英张志清黎杉珊
彭 雪 韩 瑞 陈栎颖 王 玥 朱贵萍 曹瑞芳 钟婷婷 申光辉 罗擎英 张志清 黎杉珊
(四川农业大学食品学院,四川 雅安 625014)
随着生活水平的提高,人们对蜂蜜的需求量迅速增长,对其食用品质要求也越来越高[1]。蜂蜜的质量标准由Codex Alimentarius标准(CODEX Stan 12,2001)和欧盟蜂蜜指令(Council Directive,2001)定义,该标准规定蜂蜜中不应添加任何成分[2]。然而,目前市售的蜂蜜中常会存在天然苯甲醛的残留。苯甲醛具有苦杏仁特殊气味,存在于无花果、杏仁等天然植物中,同时也可人工合成,被作为食品添加剂广泛用于食品工业中[3]。由于其对眼和上呼吸道黏膜有刺激作用,对神经有麻醉作用,能引起过敏性皮炎[4],因此建立蜂蜜中残留苯甲醛的检测方法,具有十分重要的意义。对于蜂蜜中苯甲醛的检测已有文献报道,如:超声辅助萃取和电子气相色谱捕获检测(GC-ECD)、固相微萃取与气相色谱—质谱联用测定光谱测定(SPME-GC/MS)等[5]。这些方法虽准确、可靠,但灵敏度尚有不足。近年来,化学衍生化—高效液相色谱—质谱检测技术(HPLC-MS)被广泛关注,该方法以化学衍生试剂对分析物进行衍生化,并采用HPLC-MS检测,是一种具有高灵敏度的分离检测技术,具有选择性好,分析速度快,定性能力强[6]等特点,在痕量分析中有显著优势,该技术为发展高灵敏的苯甲醛检测分析方法提供了可能。
罗丹明类化合物是一种氧杂蒽类荧光染料[7],其基本骨架主要由带有 3,6 位取代氨基的氧杂蒽母体(简称母环)和 9 位碳原子所连接的芳环(简称底环)两个片段组成。罗丹明类物质具有优异的理化性能,是制备HPLC-MS化学衍生试剂的一种理想材料:一方面,疏水性强,可有效改善分析物的反相HPLC的分离效果;另一方面,摩尔消光系数高、光稳定性好[8-10],易雾化,易质子化[11],有利于提高分析物分子离子化效率,能同时放大色谱和质谱响应信号;此外,罗丹明 B 分子结构中含有一个季铵型的正电荷,其衍生产物呈现正离子状态,从而提高信噪比和分析灵敏度[12]。目前,吕涛[13]曾合成了4′-羧基罗丹明,并应用于人参二醇的质谱增敏研究,但对醛酮类物质的质谱增敏研究还没有相关报道。本试验拟研究一种新型化学衍生试剂罗丹明B酰肼(Rhodamine B hydrazide,RBH),并建立RBH柱前衍生—高效液相色谱—质谱联用法,以实现蜂蜜中残留苯甲醛含量的高灵敏检测。
1 材料与方法
1.1 试剂与仪器
罗丹明B(96%)(RB):分析纯,梯希爱(上海)化成工业发展有限公司;
水合肼(98%)、苯甲醛(98%):分析纯,北京百灵威科技有限公司;
无水乙醇:色谱纯,成都市科隆化学品有限公司;
甲醇:色谱纯,成都凌微科技有限公司;
甲酸:优级色谱纯,西格玛奥德里奇有限公司;
洋槐蜂蜜:购自雅安市红旗超市;
高效液相色谱仪:Agilent 1260型,安捷伦科技有限公司;
质谱仪:Agilent 6120型,安捷伦科技有限公司;
反相色谱柱(250 mm×4.6 mm,5 μm):Agilent Zorbax SB-C18型,安捷伦科技有限公司;
核磁共振波谱仪:Bruker AVIII 600 MHz型,布鲁克科技有限公司;
傅里叶变换红外光谱仪:Thermo Scientific NicoletIS10型,赛默飞世尔科技有限公司。
1.2 RBH的合成及表征
1.2.1 RBH的合成 合成路线如图1所示。称取0.48 g罗丹明B溶于12 mL无水乙醇,逐滴加入85%水合肼1.2 mL,剧烈搅拌回流2 h,反应液由深紫色变为澄清的淡桔色。反应液冷却,减压抽除溶剂。向所得的固体中加入1 mol/L HCl溶液20 mL,得澄清红色溶液。再在搅拌条件下向溶液中慢慢滴加约1 mol/L NaOH溶液28 mL至溶液pH 9~10,将所得沉淀用6 mL超纯水洗涤3次,干燥,蒸除溶剂,得到粉色固体产物RBH 0.45 g[14]。产率为93.8%。
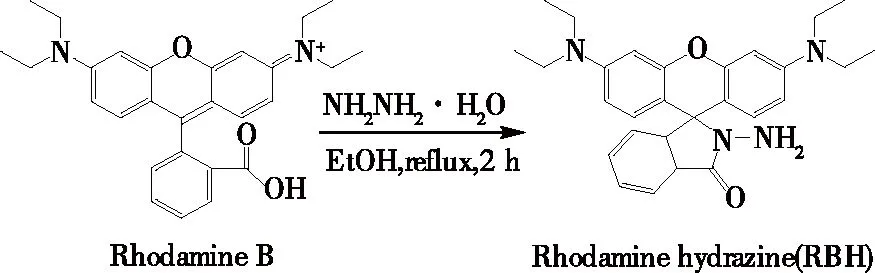
图1 罗丹明B酰肼(RBH)的合成路线Figure 1 Synthetic route of Rhodamine B hydrazide (RBH)
1.2.2 核磁共振氢谱表征(1H-NMR) 以氘代乙腈为溶剂测定RBH的1H-NMR,NMR谱仪质子共振频率为600.13 MHz,TMS为内标,试验温度为298 K。
1.2.3 傅里叶红外光谱(FTIR)表征 用压片法测定。以KBr为背景,压力为15 kPa,仪器分辨率为4 cm-1,扫描次数为32 次[15]。
1.3 样品前处理
称取10 g 洋槐蜂蜜样品(精确到0.1 g)置于100 mL三角瓶中,加入10 mL甲醇,在液体混匀器上高速混合并放置30 min以上。转入50 mL容量瓶中,用水洗涤三角瓶,并入容量瓶中,再用超纯水稀释至刻度,混合均匀后为样品提取溶液[16]。
1.4 标准溶液的配制
称取10.6 g苯甲醛标准品置于100 mL容量瓶中,用无水乙醇溶解并定容至刻度,摇匀,制得浓度为1.0 mg/mL的储备液,于低温避光处存放。根据试验需要,用无水乙醇将标准储备液配制成不同浓度的标准工作溶液,现配现用。
1.5 苯甲醛的衍生化
称取一定量RBH溶于无水乙醇,制得浓度为0.156 mol/L 的衍生化试剂。将25 mL衍生化试剂于磁力加热搅拌下逐滴加入至0.4 mL苯甲醛标准溶液或样品溶液中,10 min滴完,于50 ℃水浴反应1 h[17],反应液用0.22 μm滤膜过滤,供HPLC-MS分析。
1.6 高效液相色谱—质谱联用条件
1.6.1 色谱条件 色谱柱:Agilent Zorbax SB-C18反相色谱柱(250 mm×4.6 mm,5 μm);流动相A为甲醇+0.1% HCOOH;流动相B为H2O+0.1% HCOOH;梯度洗脱0~6 min,70%~95% A,6~12 min,95% A;进样量5 μL;流速1 mL/min;柱温35 ℃;DAD检测波长560 nm。
1.6.2 质谱条件 扫描方式:电喷雾离子源(ESI)正离子扫描;检测模式:SIM扫描;雾化气体:N2;干燥气流速:12.0 L/min;雾化器压力:275.8 kPa;干燥气温度:350 ℃。以分子离子和碎片离子荷质比定性,质谱峰面积外标法定量。
1.7 数据处理
采用Excel 2003软件对试验数据进行统计,并应用Origin 8.5软件对数据进行作图分析。
2 结果与讨论
2.1 RBH的结构表征
利用1H-NMR对合成的RBH进行结构研究并与RB对比,表1列出了RBH和RB在CD3CN中的质子化学位移(δH)及其位置归属。由表1可见,RBH与RB分子上各质子的δH值及峰裂分情况有明显差异,与RB相比,RBH在0.003 8‰ 处多出现一个2H的宽单峰,可归属于酰肼基团中的—NH2,这一特征值可表明RB底环上的羧基已转化为酰肼基团,RBH合成成功。
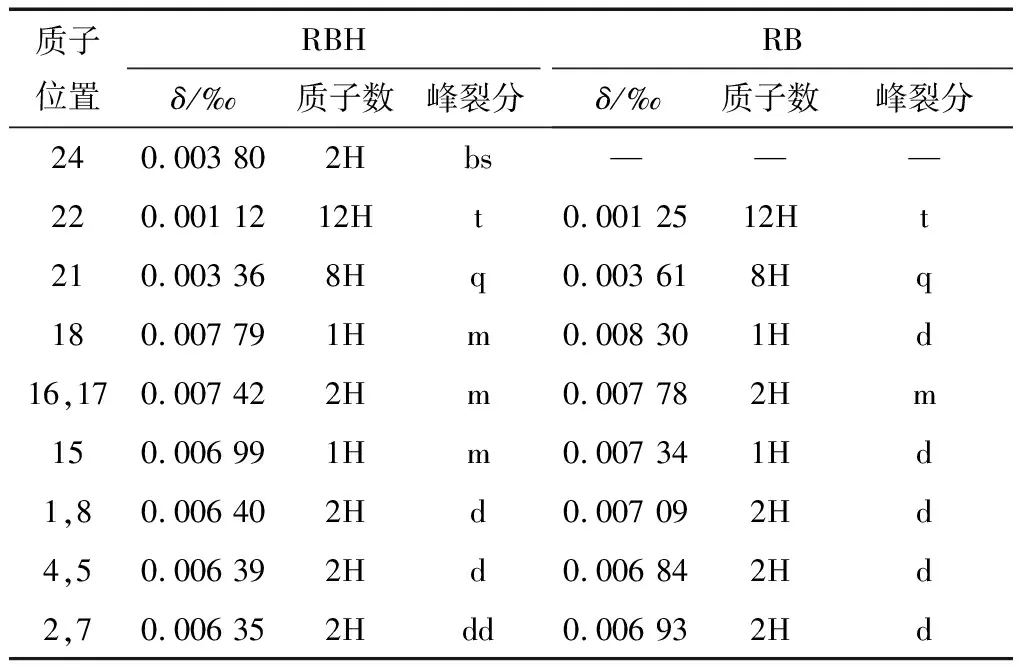
表1 RBH、RB的核磁共振氢谱1H-NMRTable 1 Nuclear magnetic resonance spectroscopy 1H-NMR of RBH, RB
此外,对RBH还进行了FTIR表征。如图2所示,3 437.69 cm-1处的峰为—NH2的伸缩振动吸收峰;2 973.55,2 931.90 cm-1处的峰可归属于母环顶端与氮原子相连的—CH3的伸缩振动;邻近的一个双峰则归属于—CH2— 基团;1 697.86 cm-1处为酰胺上羰基C═O的吸收峰;1 634.53,1 615.63,1 515.08 cm-1的峰为苯环C═C键的特征吸收峰;1 375.61 cm-1的峰为顶端—CH3的弯曲振动吸收峰;1 220.05 cm-1的峰归属于顶端叔胺取代基;1 119.05 cm-1处的峰归属于—C—O—C—;819.50,789.75,700.50 cm-1处的峰为取代苯C—H变形振动的吸收峰。以上数据进一步证实了RBH合成成功。
2.2 RBH对苯甲醛的衍生化
RBH对苯甲醛的衍生化反应如图3所示。酰肼类化合物可与含有羰基的醛类或酮类化合物发生亲核加成反应生成酰腙类化合物[18],由于肼类化合物其结构本身具有大的共轭结构,使得生成的腙类化合物相对更加稳定。该反应灵敏且具有高度的选择性,被广泛地应用于醛酮类物质的标记[19]。因此,RBH可以作为化学衍生试剂用于苯甲醛的衍生化,进而进行HPLC-MS检测。
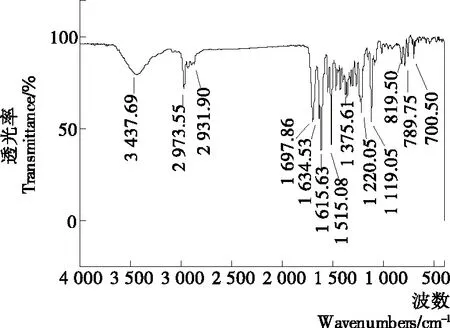
图2 RBH的傅里叶变换红外光谱图Figure 2 Fourier transform infrared spectrum of RBH
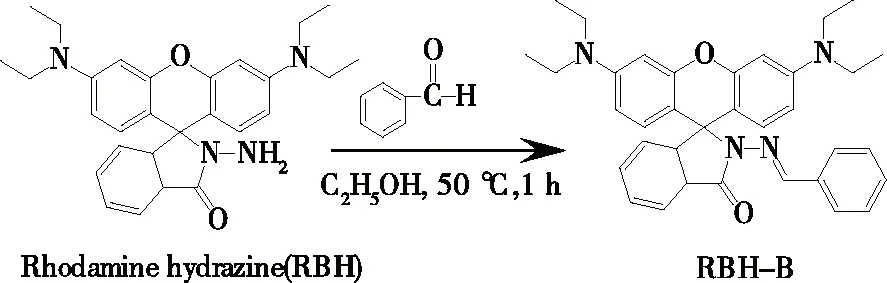
图3 RBH对苯甲醛的衍生化Figure 3 Derivatization of RBH and benzaldehyde
2.2.1 RBH-B的鉴定 对RBH及其与苯甲醛(RBH与苯甲醛的摩尔比为1∶1)反应后的溶液进行HPLC-MS分析。图4是RBH的HPLC及MS谱图。HPLC图中,12.50 min处的峰是RBH的峰;MS谱图中,m/z=457.3的峰为RBH的[M+H]+峰,m/z=229.3的峰为RBH的[M+H]2+峰,进一步证实RBH结构正确,合成成功。图5是RBH-B的HPLC及MS谱图。HPLC图中,在9.12 min处出现一个新峰,而12.50 min处RBH的峰基本消失,证实衍生化反应中RB反应完全,有新物质生成,且反应转化率高,选择性好,无副产物。通过MS谱图对9.12 min处的峰进行分析,其中m/z=545.3的峰可归属为RBH-B的[M+H]+峰,m/z=273.3为RBH-B的[M+H]2+峰,由此可判断RBH对苯甲醛衍生化反应是成功的。
2.2.2 衍生条件的优化
(1) 衍生溶剂:分别采用乙腈和无水乙醇为溶剂进行衍生化,以无水乙醇为反应溶剂时,反应充分且效率高。因此,选择无水乙醇为反应溶剂。
(2) 衍生温度:分别在常温和50 ℃水浴加热条件下使RBH和苯甲醛完全反应,试验表明,在50 ℃水浴加热条件下,其反应时间短,转化率高。
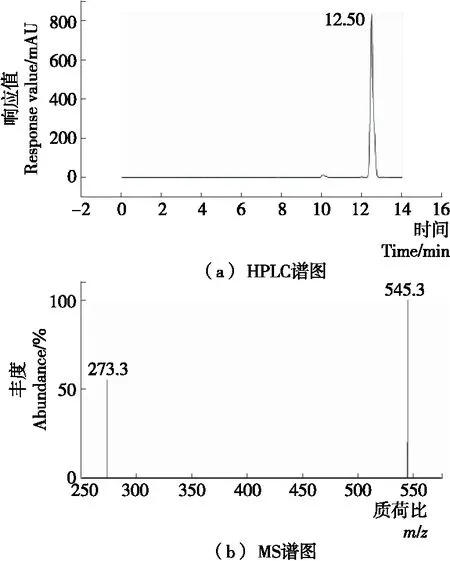
图4 RBH的HPLC及MS谱图Figure 4 HPLC and MS spectra of RBH
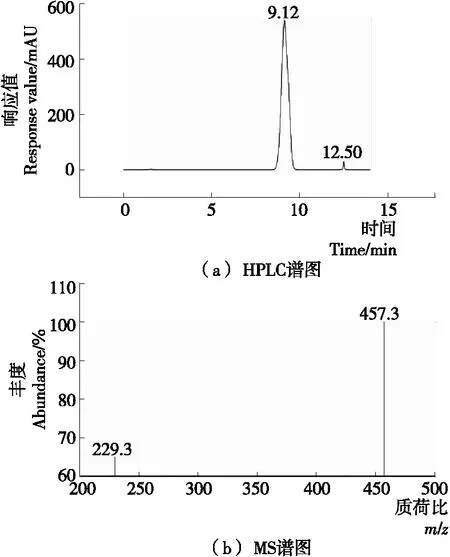
图5 RBH-B的HPLC及MS谱图Figure 5 HPLC and MS spectra of RBH-B
(3) 衍生时间:在8 h内研究了反应时间对衍生效率的影响。结果表明,反应1 h时反应效率最大且稳定,1 h后反应效率随着时间的延长逐渐变低。因此,反应时间选定为1 h。
结果表明,在最优条件下,分别测定RBH和RBH-B的色谱峰面积ARBH和ARBH-B,由ARBH-B/(ARBH+ARBH-B)计算可得衍生化反应的转化率为95.2%。
2.2.3 质谱条件的优化 将配制的浓度为0.1 ng/mL的苯甲醛标准溶液,与RBH衍生化后,进入质谱系统进行质谱参数优化。由于化合物RBH-B含有杂环原子,在正离子模式下易得到H+形成准分子离子峰[M+H]+。因此,本试验选用正离子模式。首先采用全扫描模式选择母离子,再采用SIM扫描模式找出响应较高的两个碎片离子峰,对碰撞诱导解离等条件进行优化(表2),最后选定定性离子和定量离子。
2.3 方法线性范围、检出限和定量限
本试验采用线性回归分析,以浓度为横坐标、定量离子峰面积为纵坐标进行计算。采用加标回收法测定检出限(LOD)和定量限(LOQ),分别根据最低测定浓度的信噪比S/N=3 和S/N=10 确定。结果表明,本方法在0.05~6.00 ng/mL 浓度范围内呈良好的线性关系,线性方程为Y=7 416.1X+5.03×105,相关系数为0.996 2,LOD和LOQ分别为0.80×10-3,2.71×10-3ng/mL。与已报道的方法以及GB/T 18932.14—2003中高效液相色谱荧光法(表3)相比较,本方法的LOD和LOQ明显更低,该方法在灵敏度方面具有显著优势。因此,RBH柱前衍生结合HPLC-MS法可用于苯甲醛高灵敏的定量检测。此外,RBH还可用于其他醛酮类物质的分析检测,对于高灵敏分析方法的开发具有一定的理论及实践价值。
2.4 样品加标回收率与精密度
加标回收试验是对空白样品进行3个不同浓度的添加并测定,添加浓度分别为0.1,1.0,3.0 ng/mL,每个添加浓度平行测定3 次。方法精密度以3次平行结果的相对标准偏差(RSD)进行分析评估。测得回收率为93.3%~104.0%,RSD为0.8%~2.6%,如表4所示。说明该方法的准确性和精密度较好。采用本方法测得洋槐蜂蜜中的苯甲醛含量为0.7 ng/mL, 蜂蜜样品和加标蜂蜜样品的SIM扫描谱图如图6 所示。
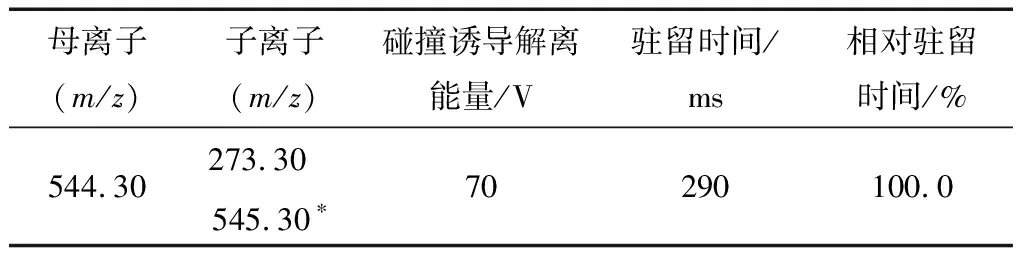
表2 RBH-B的质谱采集参数†Table 2 Mass spectrometry acquisition parameters for RBH-B
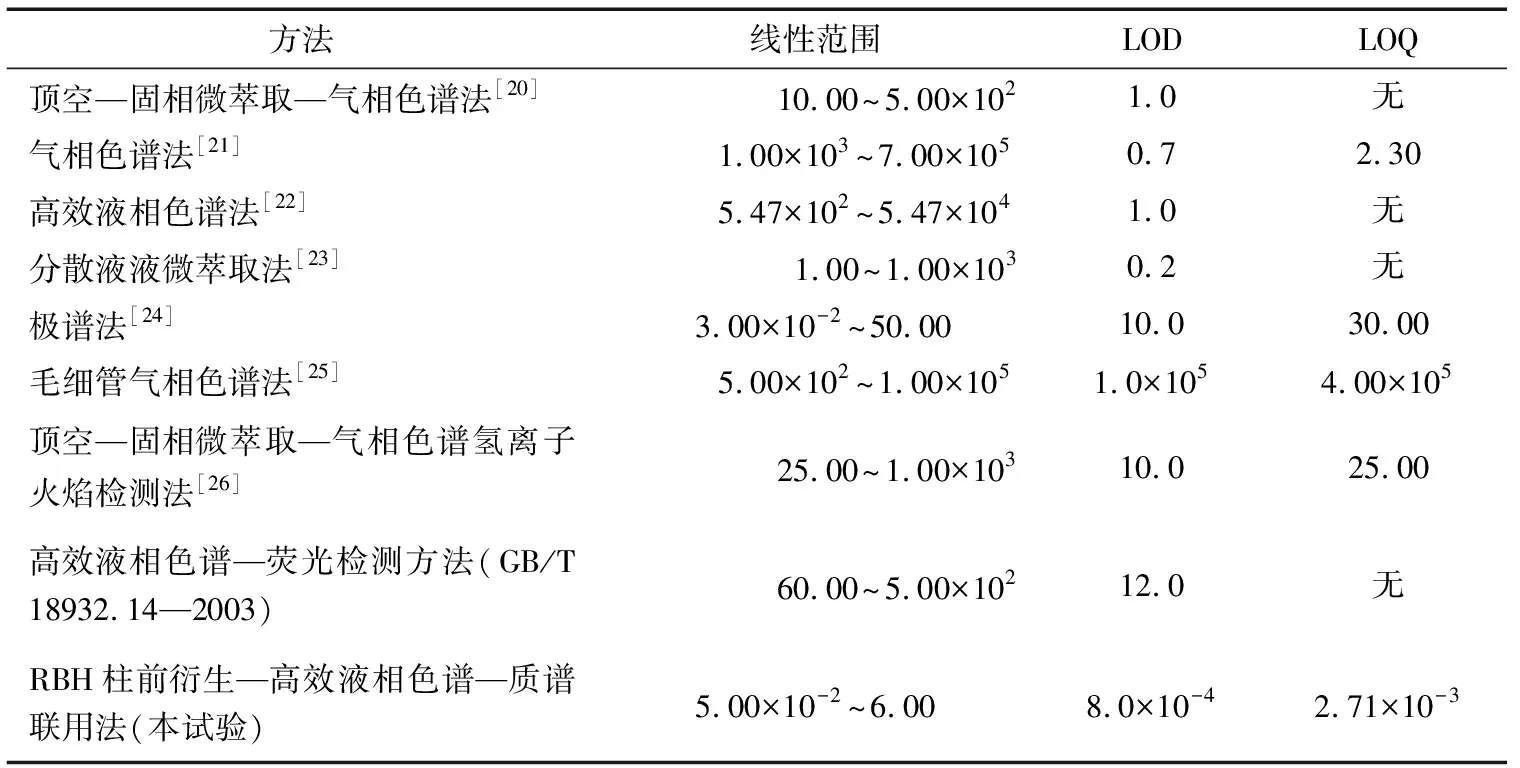
表3 检测苯甲醛不同方法的线性范围、LOD和LOQTable 3 Linear range, LOD and LOQ for different methods of detecting benzaldehyde ng/mL
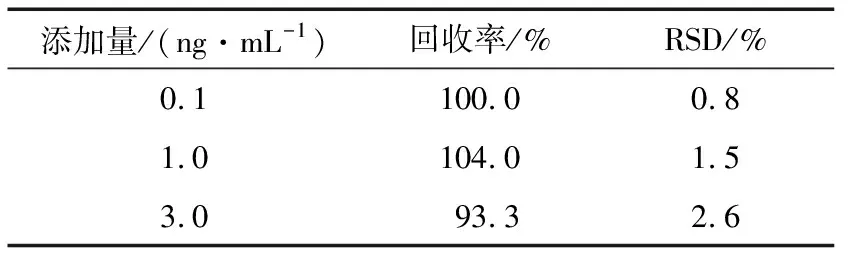
表4 LC-MS法测定蜂蜜样品中的加标回收率和相对标准偏差Table 4 Recovery and relative standard deviations (RSD) of honey samples in LC-MS (n=3)
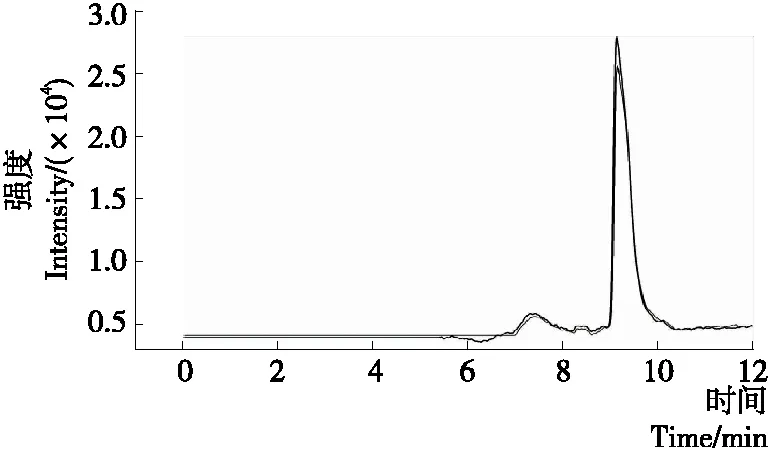
图6 空白样品和加标样品(3 ng/mL)中苯甲醛的SIM扫描图Figure 6 SIM scan of benzaldehyde in sample and spiked sample(3 ng/mL)
3 结论
本研究以RB为母体,设计合成了新型酰肼类化学衍生试剂RBH。基于RBH与醛酮类物质反应灵敏、快速、选择性好的特点,及HPLC-MS技术分析范围广、灵敏度高的优点,建立了RBH柱前衍生HPLC-MS联用法对蜂蜜中的苯甲醛残留进行检测分析。结果表明,与已报道的其他方法相比,该方法具有选择性好、灵敏度高、衍生化时间短、检测限低等优点,可为醛酮类物质的检测分析提供有利、可靠的方法,并对开发超灵敏LC-MS新方法具有重要意义。但本试验没有对多个醛酮类物质同时检测,今后可以进一步对其他醛酮类物质衍生化,并采用多反应监测模式进行HPLC-MS测定。
