多西紫杉醇血药浓度监测在乳腺癌化疗中的临床应用
2018-03-06曾乌查黄铃铃
曾乌查, 施 烯, 黄铃铃
多西紫杉醇是肿瘤科常见的紫杉烷类化疗药物,在乳腺癌、头颈部肿瘤、肺癌、卵巢癌等领域中广泛应用。血液学毒性是多西紫杉醇给药剂量限制性毒性[1]。研究显示,在含多西紫杉醇的化疗方案中,亚裔人群的重度中性粒细胞减少的发生率较非亚裔人群明显增高[2]。本研究在乳腺癌患者应用含多西紫杉醇方案化疗过程中进行血药浓度-时间曲线下面积(area under concentration-time curve,AUC)的检测,观察其近期疗效和不良反应与AUC的关系,希望能寻找一个合适的多西紫杉醇的药代动力学参数来指导临床应用。
1 对象与方法
1.1对象 选取2016年3月-2017年10月收治的78例经病理确诊的乳腺癌患者,均为女性,年龄中位数49岁(31~65岁)。78例患者均为新辅助治疗或姑息一线化疗,其中10例存在骨转移,但排除存在脊柱或骨盆多发骨转移患者;9例为晚期内分泌治疗后进展患者。所有待检测患者均签署了知情同意书,避免服用可能干扰多西紫杉醇代谢的CYP3A4的食物和药物。
1.2方法
1.2.1治疗 所有入选乳腺癌患者的治疗均采用含多西紫杉醇(上海创诺制药有限公司,国药准字 H20113165,20 mg)的联合化疗方案,其中56例为序贯表阿霉素+环磷酰胺方案、14例为联合卡铂方案、8例联合卡培他滨方案。多西紫杉醇均按体表面积75 mg/m2给药,静脉输注时间1 h。在多西紫杉醇用药前1天开始给予地塞米松8 mg bid,持续3 d。化疗前30 min给予5-羟色胺受体拮抗剂预防性止吐,在化疗结束后48 h给予重组人粒细胞集落刺激因子150 μg qd 预防性升白治疗,连续3 d。患者最多接受6个周期的化疗。用药期间进行多西紫杉醇AUC的检测,用药后每周观察中性粒细胞减少、血小板减少、贫血、乏力、肝功能异常、恶心呕吐等毒副反应指标。
1.2.2样本检测 多西紫杉醇血药浓度检测采用胶乳免疫比浊法[3],试剂盒购自江苏长星医疗科技有限公司,经CS-600B全自动生化分析仪检测。分别在输注多西紫杉醇结束前10 min内及输注结束后30~60 min内采集血样3 mL至K2EDTA抗凝采血管中,准确记录药物输注起始时间、实际采样时间和输注结束时间,若血样未能及时检测,应放置在2~8 ℃冰箱保存。将收集完成的样本在1 h内送至实验室统一进行离心(2 000 r/min,10 min),分离血浆,进行样本血药浓度的检测,通过非线性混合效应模型软件(NONMEM)估算多西紫杉醇的AUC[AUC(mg·h-1·L-1)=给药剂量(mg)/清除率(L/h)]。计算软件采用Mycare TM药物暴露软件。推荐多西紫杉醇75 mg/m2给药时AUC正常范围为1.0~2.5 mg·h-1·L-1[4]。设定AUC<1.0 mg·h-1·L-1为低AUC组、AUC1.0~2.5 mg·h-1·L-1为正常AUC组,AUC>2.5 mg·h-1·L-1为高AUC组。
1.2.3 评价标准 不良反应评价标准按照美国国立癌症研究院通用不良事件术语标准4.0版(Common Terminology Criteria Adverse Events,CTCAE v4.0)确定。疗效评价标准采用RECIST 1.1 版标准[5]:完全缓解(CR):所有目标病灶消失;部分缓解(PR):基线病灶长径总和缩小≥30%;进展(PD) :基线病灶长径总和增加≥20%或出现新病灶;稳定(SD):基线病灶长径总和有缩小但未达PR或有增加但未达PD。
有效率(%)=(CR+PR)/总例数×100%
临床获益率(%)=(CR+PR+SD)/总例数×100%
1.3统计学处理 采用IBM SPSS Statistics 20统计软件处理。计数资料采用χ2检验或Fisher精确概率法进行显著性检验,等级资料如不良反应等使用秩和检验,检验水准α=0.05,P<0.05为差别具有统计学意义。
2 结 果
2.1基线特征 根据检测得到的多西紫杉醇AUC水平,将患者分为低AUC、正常AUC、高AUC 3组,其中低AUC组4例、正常AUC组63例、高AUC组11例。各组的基线特征比较,差别无统计学意义(P>0.05,表1)。
2.2疗效评价 患者接受(4.36±1.07)个(2~6个)周期的化疗,低AUC组、正常AUC组和高AUC组在有效率、临床获益率等方面比较,差别无统计学意义(P>0.05,表2)。
2.3不良反应发生情况 3组患者在不同程度的粒细胞减少发生率比较,差别有统计学意义(Z=7.653,P=0.022),其中高AUC组的Ⅰ~Ⅳ度粒细胞减少发生率、Ⅲ+Ⅳ度粒细胞减少发生率明显高于正常AUC组(Z=-2.763,P=0.017)。而各组间贫血、血小板减少、乏力、肝功能异常、恶心呕吐等不良反应发生率差别无统计学意义(P>0.05,表3)。以不同化疗方案为分层因素进行统计分析,结果显示,3种不同化疗方案组别之间粒细胞减少发生率差别无统计学意义(P>0.05)。
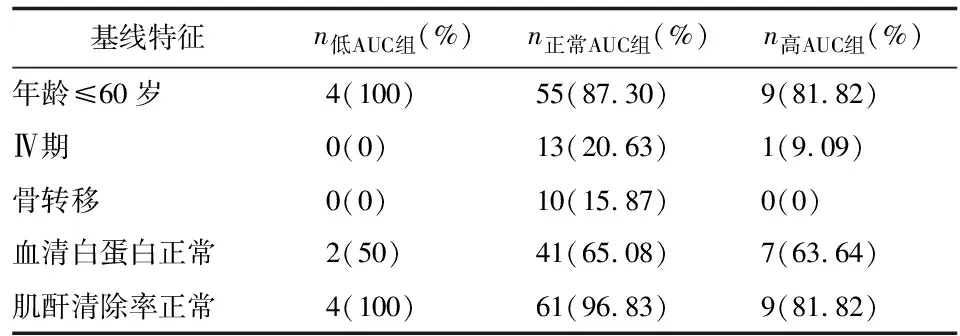
表1 3组AUC患者基线特征比较
AUC:血药浓度-时间曲线下面积.
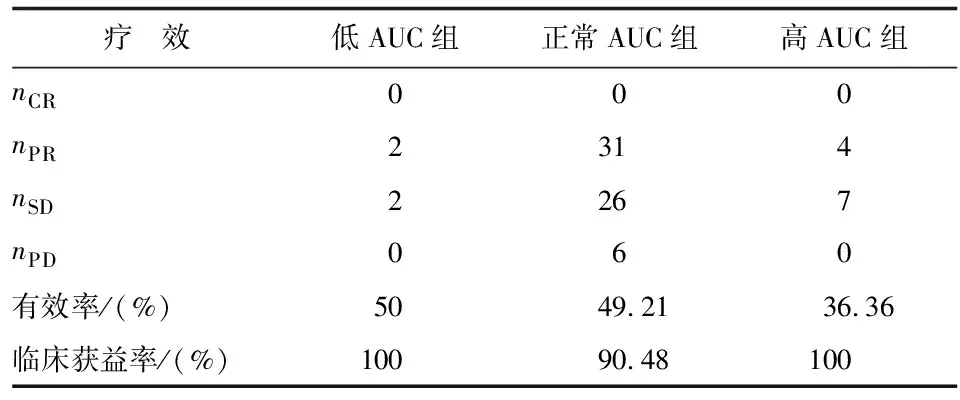
表2 3组AUC患者化疗近期疗效比较
AUC:血药浓度-时间曲线下面积; CR:完全缓解; PR:部分缓解;SD:稳定;PD:进展.
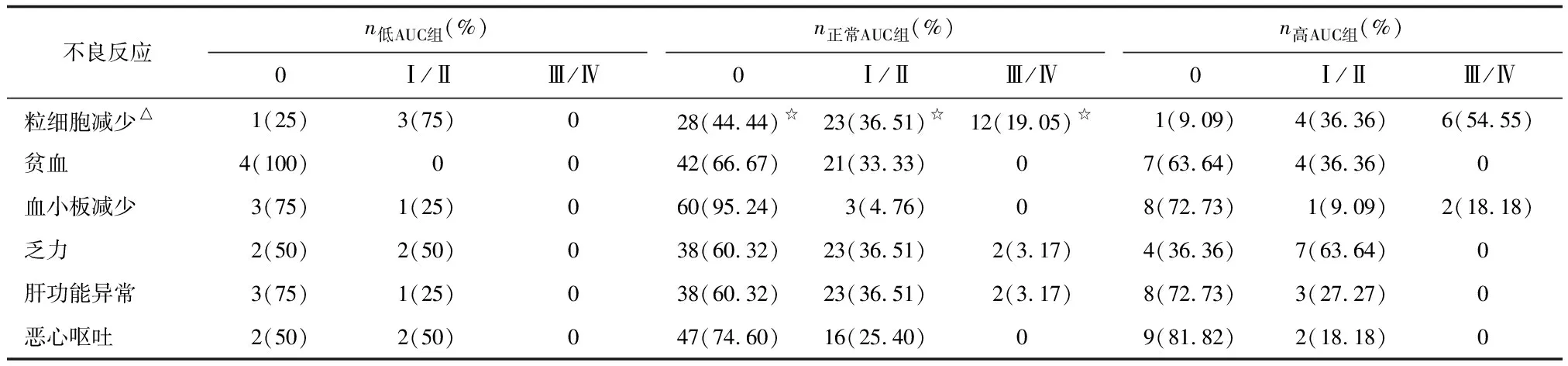
表3 3组AUC患者不良反应比较
AUC:血药浓度-时间曲线下面积; CR:完全缓解; PR:部分缓解;SD:稳定;PD:进展. 3组间不同程度粒细胞减少发生率比较,△:P<0.05;正常AUC组与高AUC组不同程度粒细胞减少发生率比较,☆:P<0.05.
3 讨 论
乳腺癌是常见恶性肿瘤之一,多西紫杉醇作为一种半合成的紫杉烷类抗肿瘤药物,在乳腺癌的早期辅助化疗和晚期姑息化疗方面都占据了重要的地位,单药有效率约为40%[6]。目前,临床上推荐的多西紫杉醇给药剂量都是根据体表面积(body surface area,BSA)计算的。一项Ⅲ期临床试验证实,在一定的剂量范围内(60~100 mg/m2)增加多西紫杉醇的剂量可以增加肿瘤的治疗反应率[7]。但Engels等认为,基于BSA给药的多西紫杉醇,其药代动力学参数的变异系数可达30%~40%,甚至部分报道可达50%[8]。研究表明,75 mg/m2的多西紫杉醇联合卡铂一线治疗晚期乳腺癌,Ⅲ/Ⅳ级中性粒细胞减少的发生率达94%,其中15%的患者出现粒缺性发热[9]。而在相同甚至更低给药剂量的情况下,中国人的重度骨髓抑制发生率高于欧美国家[2]。在这种情况下,基于BSA给药的多西紫杉醇实际的药物暴露量存在比较大的差别,而这种差别可能导致部分患者在不良反应发生方面存在较多的不可测因素,甚至因不良反应导致治疗失败,影响效益-风险比,尤其亚裔患者。寻找一个更合适的参数指标指导多西紫杉醇的临床应用就显得尤为重要。
多项研究认为,AUC是唯一一个能够预测多西紫杉醇严重毒副反应的参数[10-11]。Bruno等收集了6个Ⅱ期研究的数据指出,高AUC水平与应用多西紫杉醇后严重不良反应发生率正相关[11]。一些关于亚裔的研究也证实了这一点[12-13]。Yamamoto等的研究发现,相比按体表面积给予多西紫杉醇得出的AUC,根据清除率及目标AUC[(2.66±0.91) mg·h-1·L-1] 计算得出的多西紫杉醇的个体化剂量能显著减少AUC的变异率[14]。多项研究认为,不同水平的AUC并不影响多西紫杉醇的临床疗效[14-15]。Harvey等推荐2.9 mg·h-1·L-1为接受多西紫杉醇联合环磷酰胺治疗的中国乳腺癌患者的最佳AUC范围[7]。但是目前国内在这方面的数据并不成熟,没有一个统一的AUC标准范围。本研究大部分患者测得的AUC值均<2.5 mg·h-1·L-1,根据公司推荐及一些相关研究数据,按AUC有效范围为1.0~2.5 mg·h-1·L-1进行分组[4],结果表明,在基于体表面积给予多西紫杉醇后,虽然不同患者最终AUC值不同,但不同水平AUC组间的有效率、临床获益率统计学上并没有差别,这与大部分研究的结论一致。而在不良反应方面,即使治疗中已经给予G-CSF预防性升白处理,本研究中仍出现23.08%的Ⅲ/Ⅳ度粒细胞减少,并且随着AUC值的升高,粒细胞减少的发生率显著上升,而研究中3.85%的患者发生粒缺性发热,且均发生于AUC>1.0 mg·h-1·L-1组,这提示不同AUC的水平可预测应用多西紫杉醇后粒细胞减少的发生率,制定合适的AUC范围有利于指导多西紫杉醇的临床应用。本研究在贫血、血小板减少的血液学不良反应方面各组间比较,差别无统计学意义,这可能与样本量不足,发生贫血、血小板减少的病例较少有关,尤其是低AUC组,结果值得进一步扩大数据研究。
因此,根据相关研究数据,中国患者应用多西紫杉醇AUC值的正常范围可考虑为1.0~2.5 mg·h-1·L-1。根据AUC正常范围值调整多西紫杉醇用量有望减少毒副反应的发生,可更加合理地指导多西紫杉醇的临床应用,也期待更大型的国内研究来寻找一个合适的多西紫杉醇的药代动力学参数水平。
