氧化乐果在绿化废弃物厌氧发酵过程中的降解
2018-02-02邵一心顾平道
邵一心,顾平道
(东华大学环境科学与工程学院,上海 201600)
近年来,在绿化面积不断增长的同时,园林绿化废弃物的回收利用问题逐渐凸显。现阶段园林绿化废弃物的处理主要停留在焚烧及填埋2种手段上,造成了极大的浪费,少部则分用来进行堆肥,使之转化成有机肥料[1]。然而,利用废弃物进行厌氧发酵产沼气的研究较少。在进行城市园林绿化废弃物厌氧发酵的同时,发现发酵系统中农药浓度对于发酵的产气量、产气时间等指标有影响。因此笔者探究了农药与发酵过程之间的关系,并使用气相色谱技术对发酵体系的农药含量进行检测[2-3],研究有机磷在绿化废弃物厌氧发酵过程中的降解。
1 材料与方法
1.1供试废弃物与接种物以上海某大学校园内常见园林作物——悬铃木(英国梧桐)树叶作为厌氧发酵底物,采用实验室中式中温厌氧发酵反应系统中驯化良好的猪粪作为厌氧发酵系统的接种物[4]。底物的总固形物(TS)含量为88.1%,挥发性固体(VS)含量为25.6%;接种物的TS含量为13.35%,VS含量为76.25%。
1.2试剂与仪器气相色谱仪:天美GC9700,检测器FID;色谱柱:TD-5,30 m×0.25 mm×0.5 μm,C18SPE柱,真空固相萃取装置,隔膜真空泵,氮吹仪,氢气发生器,空气进样器。农药标准品:中国计量科学研究院。化学试剂:NaCl,乙腈,正己烷,丙酮,乙酸乙酯,甲醇,正丁醇,所有试剂均为分析纯级别。
1.3试验装置采用自行研发的厌氧发酵系统(图1),建立批量式发酵产沼气装置,为了便于收集沼液并维持反应系统的厌氧状态,反应发生装置为特制的下口瓶,替代了从瓶口取样的传统方式。用HH-4型恒温水浴锅为反应过程提供恒温条件,选择中温环境发酵,发酵温度为35 ℃[5-6]。产生的气体采用排饱和食盐水法收集。下口瓶规格为500 mL,试验开始前,将发酵底物悬铃木树叶机械粉碎至1 mm3形状碎片,随后向瓶中加入30 g发酵底物、70 g接种物及347 mL蒸馏水,使得整个厌氧发酵体系的总体积达到400 mL,TS含量为8%[7]。测量沼气中甲烷含量的仪器为进口高灵敏度甲烷二氧化碳检测器。试验中滴加的农药为市面上常见的有机磷农药氧化乐果乳油(20%)。氧化乐果量为0、20、40、60、80、100、120、140、160、180、200、220、240、260、280、300、320 mg(每个浓度设置3个平行)。发酵系统对应滴加量及浓度见表1。
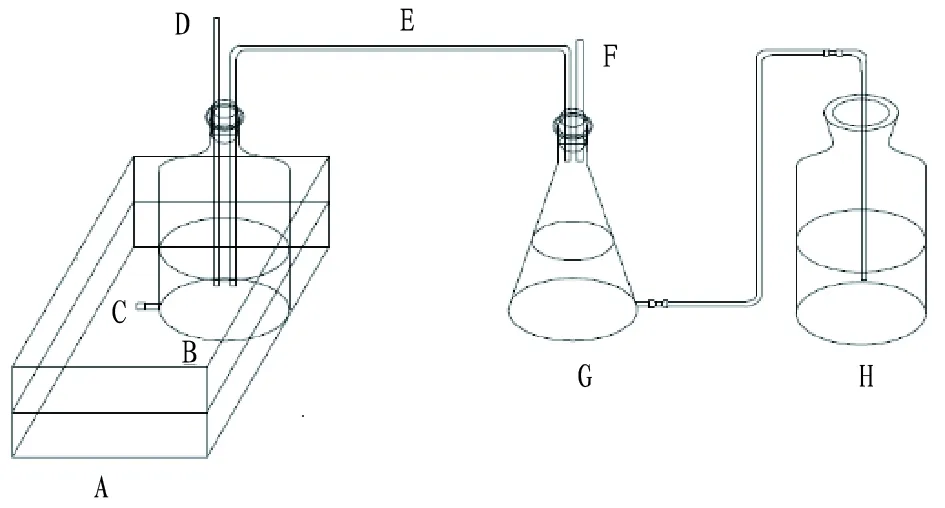
注:A.温度计;B.发酵罐;C.取样口;D.温度计;E.导气管;F.气体取样口;G.集气瓶;H.大口瓶Note:A.thermometer;B.fermentor;C.sampling port;D.thermometer;E.trachea;F.gas sampling;G.collector;H.large bottle图1 厌氧发酵系统反应装置Fig.1 Reaction device of anaerobic fermentation system
1.4固相萃取操作
1.4.1水样预处理。先从下口瓶瓶口取出3~4 mL沼液,放入离心机中以9 000 r/min离心30 min,目的是分离杂质。提取上层清液2 mL,加入缓冲液调整水样pH至7~8,并加入2% NaCl,于水样中加入2%~3%乙腈进行SPE填料活化[8]。
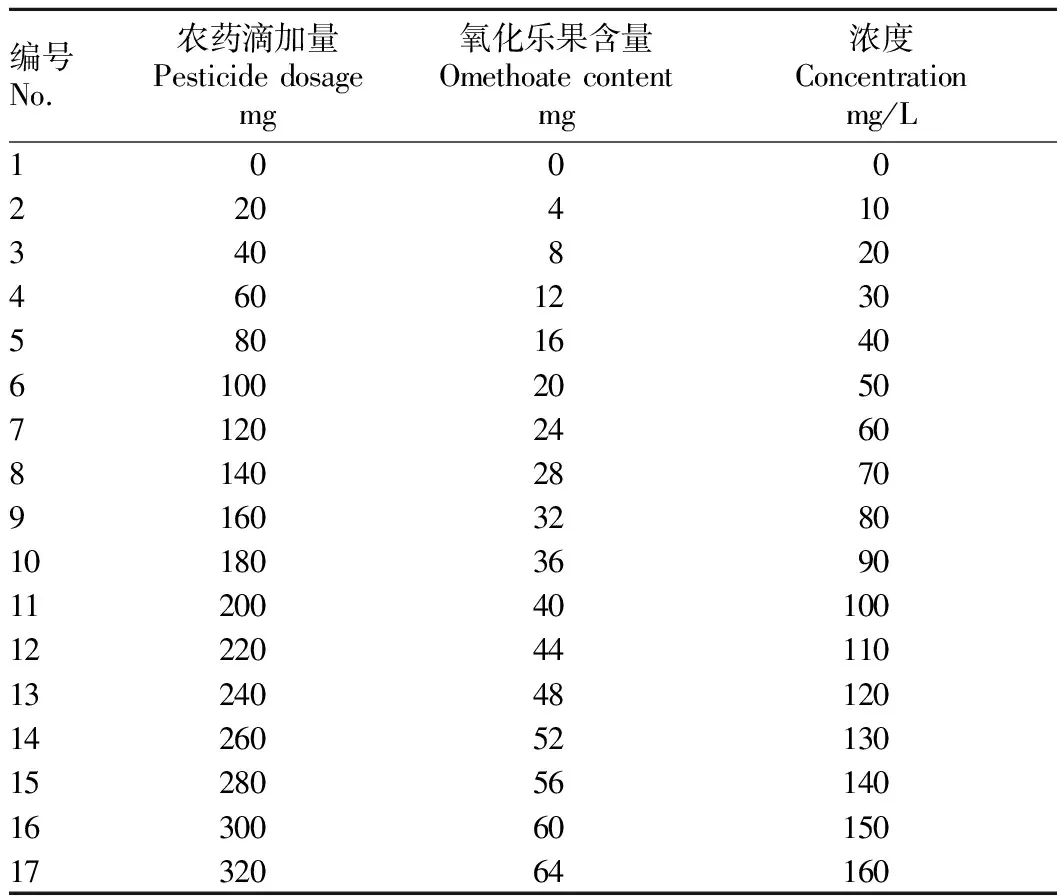
表1 农药滴加量及对应浓度
1.4.2SPE柱活化。常压状态下,先用5 mL蒸馏水洗涤SPE柱,再向柱中加入用5 mL丙酮,并保持溶液以1 mL/min的速度通过填料,即将抽干时再加入5 mL乙酸乙酯,仍保持1 mL/min的速度通过填料。在溶液抽干前加入少量蒸馏水保持填料湿润。
1.4.3样本富集。加入蒸馏水后,在蒸馏水抽干之前加入处理好的上层清液,在小于20 Mpa的压力下,控制流速为1 mL/min[9],在填料接触空气之前加入5 mL蒸馏水洗涤SPE柱。
1.4.4样本洗脱。在蒸馏水抽干前加入5 mL甲醇,使甲醇保持1 mL/min的速度通过填料,再加入5 mL丙酮,保持相同的速度,注意加入丙酮前避免填料接触空气。
1.5色谱条件载气:高纯氮气(纯度>99.999%),柱流速:1 mL/min;进样口温度:280 ℃;不分流进样,分流比为1∶40;载气压力为306.138 kPa。
柱温程序:初始温度50 ℃,保持1 min;以30 ℃/min升温至130 ℃,保持2 min;以20 ℃ /min 升温至180 ℃,保持1 min;以20 ℃/min 升温至240 ℃,保持1 min;以3 ℃ /min升温至280 ℃,保持1 min。
1.6氧化乐果标准浓度曲线绘制农药含量检测参照国家标准GB 13192—91《水质 有机磷农药的测定 气相色谱法》,采用外标法定量[10]。首先将农药标准品配置成0.1、10、40、80、120、160 mg/L一系列浓度梯度的标准溶液,随后进行色谱分析,记录氧化乐果的保留时间,根据浓度和对应的峰面积大小绘制出标准曲线[11]。在上述色谱条件下,用气相色谱仪中检测农药标准品,并以浓度为横坐标,峰面积为纵坐标绘制标准浓度曲线(图2)。回归方程为y=25.214x+2 764.680,相关系数R2=0.992 27。

图2 农药标准曲线Fig.2 Standard curve of pesticide
试验启动后,于每日18:00准时测量收集到的厌氧发酵产气,记录甲烷和二氧化碳含量,每天收集并测量一次发酵沼液中农药浓度,并进行记录[12]。
2 结果与分析
2.1厌氧发酵系统中氧化乐果浓度的变化整个厌氧发酵系统总反应时间为35 d,产气周期结束时,滴加的氧化乐果也得到了有效降解。从图3可以看出,氧化乐果的降解周期与滴加的浓度存在着明显的关系,10 mg/L农药的降解只需4 d,随着浓度的增加,降解所需的周期也增大为8、9、11、13、15、18、19、20、22 d。试验开始进行前10 d,浓度低于20 mg/L的氧化乐果已经被完全降解,试验开始20 d后,120 mg/L以下浓度的农药完全被降解。而当浓度达到130 mg/L时,降解周期已经明显增大,尤其当初始浓度为140 mg/L时,经过35 d的产气周期,仍有少量氧化乐果未被彻底降解。由此可知,绿化废弃物厌氧发酵可以促进氧化乐果的降解,降解所需的时间与农药的浓度呈正相关关系,浓度越大,周期越长。在该试验的设计条件下,整个发酵体系可承受的负荷浓度为140 mg/L。

图3 氧化乐果浓度随时间的变化Fig.3 The change of Omethoate concentration with time
2.2日产气量和累计产气量由图4可知,在发酵初期,产气量虽然高,但甲烷含量低,因此发酵初期甲烷累计产气量不高,发酵进入第5天之后,各浓度产生的气体中甲烷含量逐渐升高,进入终期之后,甲烷含量降低。从图4可以看到浓度对于日产气高峰的影响,浓度为0 mg/L时,发酵体系在第6天达到日产气高峰,随着浓度的不断升高,产气高峰不断向后推移。60 mg/L以下浓度的厌氧发酵体系中,日产气量和未滴加农药的体系相比差别不大,并且产气高峰都集中在5~12 d,在该浓度梯度内,氧化乐果对日产气量和产气高峰并无太大影响,当浓度达到80 mg/L时,最大日产气量已降至0 mg/L的50%。80~120 mg/L时,氧化乐果已经对产气的高峰值产生了明显影响,且将产气高峰推到15 d之后。而当浓度达到130~140 mg/L时,农药的存在已经严重影响到整个厌氧发酵系统的正常反应,日产气峰值仅为20 mL,而达到产气高峰的时间需要21 d,接近反应周期的末期。可以推断造成这种现象的原因可能是产甲烷菌对环境要求较高,而高浓度的氧化乐果会破坏产甲烷菌的生活环境,甚至会杀死这些细菌,从而大大降低产气性能。
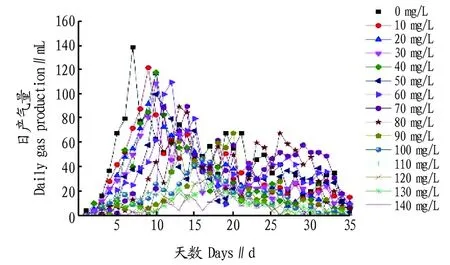
图4 氧化乐果浓度对日产气高峰的影响Fig.4 The effect of Omethoate concentration on the peak of daily gas production
图5反映了累计产气量随时间的变化情况,累计产气量直接受到日产气量的影响,可以看到累计产气量斜率最大的地方,也就是累计产气量增长最快的地方,正好对应图4中日产气量的高峰时段。从图5可以看出,氧化乐果的存在在一定程度上抑制了正常的厌氧发酵。产气总量大致分为3个区域,第1区域为1 600 mL,对应为未滴加农药的发酵系统,第2个区域为1 000~1 300 mL,对应的浓度为10~80 mg/L,第3个区域为200~600 mL,对应的浓度为90 mg/L,这表明高浓度的氧化乐果已经严重抑制了发酵系统的产气量。

图5 氧化乐果浓度对累计产气量随时间变化的影响Fig.5 The effect of Omethoate concentration on the change of cumulative gas production
2.3甲烷含量和pH变化从图6可以看出,在0~90 mg/L浓度范围内,甲烷含量并无特别大的差距,农药的存在并未对产气产生特别大的影响。然而,当农药的浓度达到120 mg/L时,甲烷含量大幅降低,仅为0 mg/L系统的50%,说明高浓度的氧化乐果会对厌氧消化系统产生的沼气质量造成持续性的影响。

图6 氧化乐果浓度对甲烷含量变化的影响Fig.6 The effect of Omethoate concentration on the change of methane content
从图7可以看出,滴加农药的量越多,发酵液的初始pH越低,所有发酵系统的初始pH均低于6.2,呈酸性,其原因是氧化乐果遇水呈酸性。随着发酵的进行,pH不断上升,证明氧化乐果的性质和结构在发酵的作用下发生了改变。氧化乐果的降解使得发酵体系的pH不断恢复到6.5~7.3,此为产甲烷菌最适宜的生存环境。

图7 氧化乐果浓度对pH变化的影响Fig.7 The effect of Omethoate concentration on the change of pH
3 结论与展望
(1)该试验探究了有机磷农药氧化乐果在绿化废弃物厌氧发酵反应体系中的降解情况,得到如下结论:①氧化乐果可在以城市绿化废弃物为底物的厌氧发酵体系中得到有效降解,在该试验条件下,设置的所有浓度梯度的农药均被完全降解,在厌氧发酵周期的前5 d,农药的降解速率最快;②氧化乐果的存在对日产气量峰值和总产气量均有抑制作用,产气高峰的出现也会延迟;农药浓度低于80 mg/L时,影响并不明显,浓度达到90 mg/L时,产气量会受到严重影响;③氧化乐果浓度在10~100 mg/L时,甲烷含量相比于无农药的发酵系统差别不大,但在高浓度(>100 mg/L)条件下,产气质量明显受到影响;④氧化乐果溶液会使发酵液呈酸性,
不利于产甲烷菌的生长,但随着发酵反应的不断进行,氧化乐果被降解,pH稳步升高,最终会稳定在利于细菌生长的pH范围内。
(2)该研究结果表明,利用城市绿化废弃物厌氧发酵降解农药的方法是可行的,该方法不仅可以处理废物,生产沼气,还可以促进农药的降解。因此,可以在以厌氧消化为主要工艺的沼气工程设置试点,进一步研究农药降解的最大负荷,观察实际效果,并推广该方法。
[1] ALI G,NITIVATTANANON V,ABBAS S,et al.Green waste to biogas:Renewable energy possibilities for Thailand’s green markets[J].Renewable and sustainable energy reviews,2012,16(7):5423-5429.
[2] 涂忆江.我国农药残留快速检测技术的研究与应用现状[J].农药科学与管理,2003,24(4):14-16.
[3] 朱赫,纪明山.农药残留快速检测技术的最新进展[J].中国农学通报,2014,30(4):242-250.
[4] 陈荣艳.新能源沼气在农村发展中的利用[J].农业与技术,2013(9):7.
[5] 成官文,朱宗强,胡乐宁,等.几种常见农业有机废物产沼气研究[C]//第十届中国科协年会论文集(二).北京:中国科学技术协会学会学术部,2008.
[6] 孙树贵,任广鑫,翟宁宁,等.中温下3种落叶厌氧发酵产气量研究[J].安徽农业科学,2010,38(19):10164-10166.
[7] 刘荣厚,郝元元,武丽娟.温度条件对猪粪厌氧发酵沼气产气特性的影响[J].可再生能源,2006(5):32-35.
[8] 高玲,杨元,景露,等.水中13种有机磷农药的固相萃取-气相色谱-质谱测定法[J].环境与健康杂志,2009,26(8):723-725.
[9] 刘丰茂,钱传范,江树人.水中12种农药的固相萃取及GC-MS测定方法研究[J].农药学学报,2000,2(2):89-93.
[10] 钟宁,曾清如,姜洁凌,等.有机磷农药的降解及其研究进展[J].现代农药,2005,4(6):1-6.
[11] 陈少华,罗建军,林庆胜,等.农药残留降解方法研究进展[J].安徽农业科学,2009,37(1):343-345.
[12]吉喜燕.有机磷农药在厌氧消化系统中的降解研究[D].昆明:云南师范大学,2016.
