TiO2/g-C3N4复合物的光催化性能测试及机理研究
2018-01-23高敏,王蒙,肖霞,刘伟
高 敏,王 蒙,肖 霞,刘 伟
(1.西安近代化学研究所,陕西 西安 710065;2.陕西延长石油(集团)有限责任公司 碳氢高效利用技术研究中心,陕西 西安 710075)
二氧化钛(TiO2)作为一种常见的半导体光催化材料,因其具有良好的机械性能、光热稳定性、耐腐蚀性以及无毒等特性,被认为是一种最有前景的光催化剂[1-4]。但是,其禁带宽度大(Eg=3.2 eV),光生电子空穴复合率高等缺陷致使其光催化性能不太理想[5-7]。石墨相氮化碳(g-C3N4)是一种禁带宽度窄(2.75 eV,450 nm)、电子性能优异的二维半导体材料[8-10]。因其与TiO2之间存在导带电势差,能够有效阻止光生电子与空穴的复合,因此研究者制备出了多种TiO2/g-C3N4复合物[11-12]。Burapat[13]等人制备了对亚甲基蓝的降解率可达到70%的高活性g-C3N4/TiO2可见光催化剂;Wei[14]等人制备了g-C3N4/TiO2异质结,其光解水制氢速率明显高于纯g-C3N4和TiO2。虽然这些研究有效提高了半导体复合物的光催化性能,但在提高载流子传递效率的基础上,同时提高自然光的利用效率和抑制光生电子和空穴的复合这方面的研究却鲜有报道。
本研究通过将块体g-C3N4剥离成少层g-C3N4来减少光生电子的传递路径,使体相中的载流子快速迁移至g-C3N4表面。然后,将该少层g-C3N4与TiO2复合,利用g-C3N4的导带价位(-1.13 eV)比TiO2(-0.3 eV)更负,使光生电子快速从g-C3N4表面迁移到TiO2上,同时导带电势差可以抑制光生电子从TiO2上逆向迁移至g-C3N4上,实现在提高载流子传递效率的基础上,同时提高自然光的利用效率和抑制光生电子和空穴复合的构想。
1 实验方法
1.1 实验原料
TiO2购于国药集团化学试剂有限公司,三聚氰胺(AR,质量分数≥99.0%)来自于天津市化学试剂四厂。无水乙醇购于红涯化学试剂有限公司,所用去离子水由娃哈哈公司提供。超声剥离所用仪器为昆山舒美科技有限公司生产的KBS-150~KBS-2800型细胞粉碎仪。
1.2 样品制备
少层g-C3N4的制备 本文采用高温热聚合法制备块体g-C3N4。称取10 g三聚氰胺加入到带盖子的刚玉坩埚,并将三聚氰胺平铺在坩埚里,在马弗炉中120 min升温至550℃并在此温度下恒温反应180 min,自然冷却至室温后研磨、过筛,所得黄色样品即为块体g-C3N4。取0.5 g制备好的块体g-C3N4在300 mL去离子水中超声剥离后,采用离心法去除未剥离的g-C3N4,所得样品即为少层g-C3N4,记为Sg-C3N4。
TiO2/g-C3N4复合物的制备 称取适量TiO2粉末加入到100 mL 制备好的Sg-C3N4悬浮液,并搅拌均匀,在80℃下搅拌蒸干。将蒸干后的样品在400℃下煅烧2h,自然冷却即为TiO2/g-C3N4复合物。其中,TiO2质量分数为1%~5%的样品,分别记为1-TiO2/g-C3N4,2-TiO2/g-C3N4,3-TiO2/g-C3N4,4-TiO2/g-C3N4和5-TiO2/g-C3N4。
1.3 催化剂表征
样品的晶体结构利用Rigaku D/Max 2550 VB/PC型X-射线衍射仪分析;样品的形貌采用JSM-6390A型场发射扫描电子显微镜和Tecnai G2F20S-TWIN型透射电子显微镜;红外光谱采用PerkinElmer Frontier仪器分析;紫外可见吸收光谱采用日本岛津公司生产的Shimadzu UV-3600 UV/vis/NIR光谱仪分析;光致发光光谱采用日本日立公司生产的Hitachi F-7000 fluorescence型荧光光谱仪分析。
1.4 光催化降解罗丹明B
将0.1 g制备好的催化剂加入100 mL罗丹明B (10 mg/L)溶液,采用300W的氙灯作为模拟光源。光照前暗搅拌30 min以达到吸附脱附平衡。吸附平衡样品的浓度记为C,以后每隔20 min取样一次并离心处理,其浓度记为Ci(i=1,2,3,…)。最后通过测量样品在最大吸收波处的吸收强度计算Ci/C并作图来评价样品的降解性能。
1.5 光催化分解水制氢
分别取0.1g制备好的样品分散于100 mL含有H2PtCl6的乙醇/水溶液(10%,体积分数)中,在自制光催化反应装置内进行光催化分解水制氢实验,并采用300W的氙灯作为模拟光源,光源自上而下照射到反应器中。首先用N2将系统中的空气去除,并将样品在模拟太阳光下照射30 min后再次用N2将系统中的气体排干。然后开始计时,每隔60 min取样一次,用气相色谱分析样品中的H2含量。
2 结果与讨论
2.1 XRD表征
图1为g-C3N4,TiO2和3-TiO2/g-C3N4的XRD图。可以看出,纯g-C3N4在13.5°和27.5°处分别有一个峰。其中,13.5°处的宽峰对应的是g-C3N4(100晶面)二维平面上N原子和C原子之间的平面衍射峰,而27.5°处的高峰对应是g-C3N4(002晶面)层与层之间堆砌衍射峰。在TiO2中2478°对应的是锐钛矿型TiO2的220晶面的衍射峰。在复合物样品中,锐钛矿型TiO2的衍射峰和g-C3N4上(002)的衍射峰都可以检测到,说明TiO2和g-C3N4已经很好的复合在一起。另外,g-C3N4(002)晶面的衍射峰减弱说明g-C3N4层间距变大,同时TiO2的衍射峰也减弱,说明TiO2被g-C3N4包裹住,从而减弱了其衍射峰。
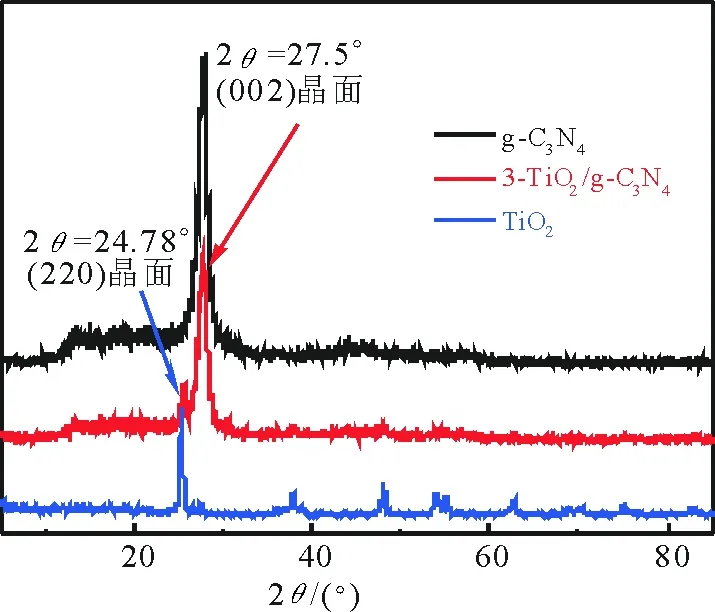
图1 g-C3N4,TiO2和3-TiO2/g-C3N4样品的XRD图Fig.1 XRD patterns of g-C3N4, TiO2 and 3-TiO2/g-C3N4
2.2 形貌表征
图2分别为所得纯TiO2,g-C3N4以及复合样品3-TiO2/g-C3N4的SEM图和TEM图。其中,图a为纯TiO2的SEM图,可以看出,所购TiO2的尺寸约为80 nm左右。图b为Sg-C3N4的SEM图,可以看出该样品为二维片状材料。图2(c)和图2(d)为复合物样品3-TiO2/g-C3N4的SEM图。可以看出,粒状的粉末状物质为TiO2颗粒,底部的块状物质则为Sg-C3N4,并且TiO2均匀地负载在g-C3N4的表面。将图2(c)局部放大后,可以看出TiO2均匀地包覆在Sg-C3N4表面(图2(d))。图2(e)和图f为复合样品3-TiO2/g-C3N4的TEM图,其中图f为图e的放大图。可以看到,黑色斑点为TiO2纳米颗粒,底部的灰色片状物质则为少层g-C3N4纳米片。

图2 (a) TiO2,(b) Sg-C3N4的SEM图,(c)和(d) 3-TiO2/g-C3N4复合物的SEM图(e)和(f) 3-TiO2/g-C3N4复合物的TEM图Fig.2 SEM images of (a) TiO2, (b) g-C3N4, (c) and (d) 3-TiO2/g-C3N4 composites.(e) and (f) TEM images of 3-TiO2/g-C3N4 composites
2.3 UV-vis表征
图3为纯g-C3N4,TiO2以及复合样品3-TiO2/g-C3N4的紫外可见吸收光谱图。可以看出,纯g-C3N4的吸收边带与复合物的吸收边带相近,大约在460 nm,对应的禁带宽度约为2.70 eV, 可以将纯TiO2的吸收带边从紫外光区拓展至可见光区。从吸收强度来看,纯g-C3N4在可见光区的吸收比较强,而TiO2在紫外光区的吸收比较强。对复合物来说,其在紫外区域的吸收强度虽然弱于TiO2,但强于纯g-C3N4,在可见光区的吸收弱于纯g-C3N4,但又强于TiO2。因此,可以推断,该复合物既克服了纯TiO2在可见光吸收不强的弱点,同时增强了纯Sg-C3N4在紫外光区吸收的吸收强度。综上所述,该复合物可以有效利用可见光的同时,也可以增强其在紫外光区的吸收强度,将更多的光能转化成化学能用来进行光催化反应。
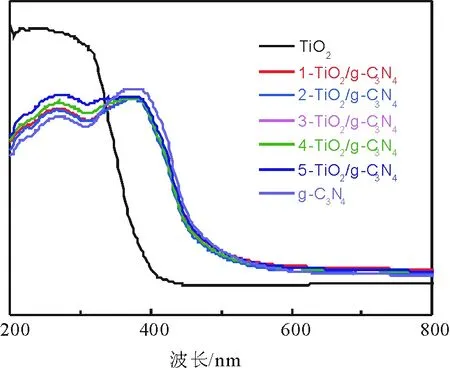
图3 不同样品的UV-vis图Fig.3 UV-vis spectra of different samples
2.4 FT-IR表征
图4为纯g-C3N4, TiO2以及复合物样品3-TiO2/g-C3N4的傅里叶变换红外光谱。 对于g-C3N4,803 cm-1处为三嗪环骨架的特征吸收峰, 在1 200~1 650 cm-1之间的吸收峰为g-C3N4杂环上C—N和CN的伸缩振动峰。 介于2 800~3 300 cm-1之间的强吸收峰为g-C3N4表面或者边缘上的未聚合的—NH或—NH2的伸缩振动峰。对于TiO2来说,在650 cm-1左右有一个强的吸收峰。3-TiO2/g-C3N4的复合样品,在803 cm-1左右的吸收峰没有发生变化,说明Sg-C3N4的主体结构在复合物的制备过程中没有被破坏。在2 800~3 300 cm-1之间的吸收峰明显变宽且强度增加,说明TiO2负载在Sg-C3N4表面,使其表面上未聚合的—NH或—NH2与Sg-C3N4表面的结合更加牢固。
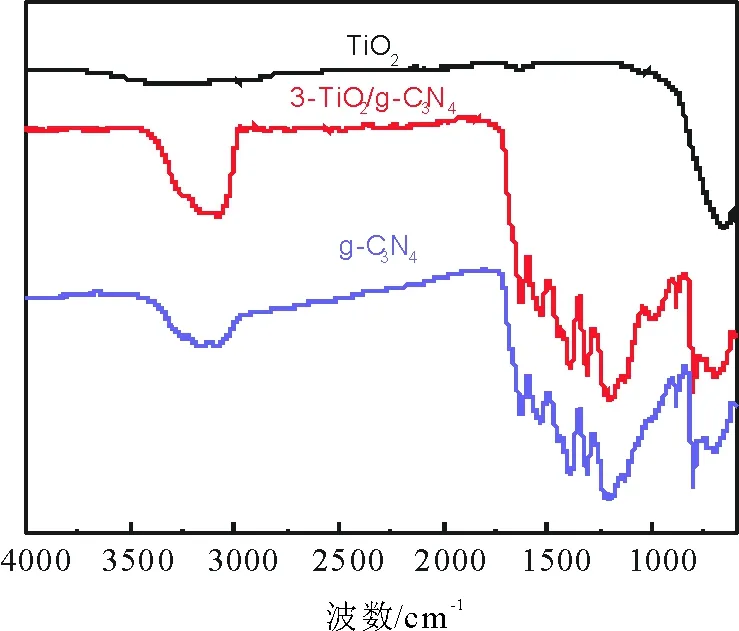
图4 纯g-C3N4,TiO2和3-TiO2/g-C3N4样品的FT-IR图Fig.4 FT-IR spectra of g-C3N4, TiO2 and 3-TiO2/g-C3N4 composites
2.5 PL表征
图5为纯g-C3N4以及复合物1-TiO2/g-C3N4,2-TiO2/g-C3N4,3-TiO2/g-C3N4,4-TiO2/g-C3N4,5TiO2/g-C3N4的光致发光光谱图。可以看出,光致发光的强度与样品的光生电子空穴的复合率密切相关。峰越强表示该样品的光生电子空穴的复合率越高。因此,所有的复合物都可以有效地抑制光生电子空穴的复合。在复合物中,随着TiO2的含量不断增加,其荧光强度先减弱、后增加。其中,在TiO2质量分数为3%时荧光强度最弱,即3-TiO2/g-C3N4可以有效抑制光生电子和空穴的复合,从而改善光催化性能。
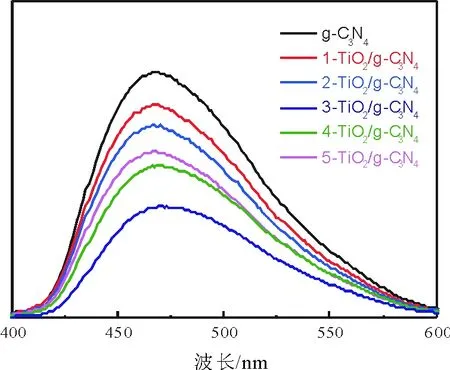
图5 纯g-C3N4以及复合物样品的PL谱图Fig.5 PL spectra of g-C3N4 and composites samples
2.6 光催化降解罗丹明B
样品的光催化性能采用罗丹明B的降解来评价,如图6所示。在没有催化剂或者无光照的条件下,其降解率可以忽略不计,表明罗丹明B降解是光催化作用。对于纯g-C3N4和TiO2来说,其降解率均不如复合样品好,纯g-C3N4的降解率大约为40%,TiO2降解率大约为30%。对于复合物样品来说,1-TiO2/g-C3N4,2-TiO2/g-C3N4,3-TiO2/g-C3N4,4-TiO2/g-C3N4,5TiO2/g-C3N4的降解率分别为56.8%,66.6%,87.7%,74.4%,63.6%。当TiO2质量分数为3%时降解率最高,当TiO2质量分数超过3%时,其降解率反而降低。这是因为过量的TiO2团聚在g-C3N4表面,从而阻止了罗丹明B分子与g-C3N4的接触,因此其降解效率反而随着TiO2的增加而降低。
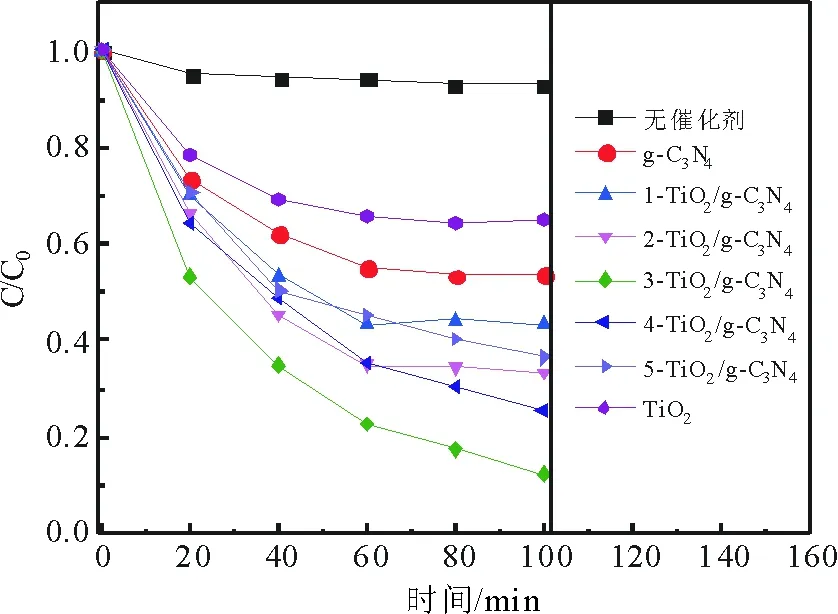
图6 不同光催化剂降解罗丹明B性能曲线Fig.6 The performance of different samples on RhB degradation
2.7 光催化分解水制氢
复合样品的光催化降解罗丹明B实验说明在3-TiO2/g-C3N4复合样中留下的空穴比较多,可以很快将有机染料氧化成二氧化碳和水。同时,光生电子的利用率采用光催化分解水制氢试验来测试。从图7中可以看出,纯g-C3N4的产氢速率为36.86 μmol/h,当TiO2的质量分数为1%,2%,3%和4%的产氢速率分别为45.81 μmol/h,53.69 μmol/h,68.62 μmol/h和21.25 μmol/h。其中,TiO2质量分数在3%时产氢速率最高,当质量分数不足3%产氢速率随着TiO2的质量分数增加而升高,当超过3%时,产氢速率反而下降。其主要原因为TiO2的质量分数不足3%时,其产氢速率主要受光生电子的分离速率影响,由于TiO2的含量较少,不能充分地将g-C3N4的光生电子全部转移到TiO2上,因此制氢速率会随着TiO2的含量增加而升高。当TiO2质量分数超过3%时,产氢速率主要由TiO2表面的光生电子势能影响。由于TiO2的导带电势只有-0.3 eV,远低于g-C3N4的-1.13 eV,因此当TiO2的质量分数超过3%时,其产氢速率反而下降的特别明显,甚至不如纯g-C3N4的产氢速率。
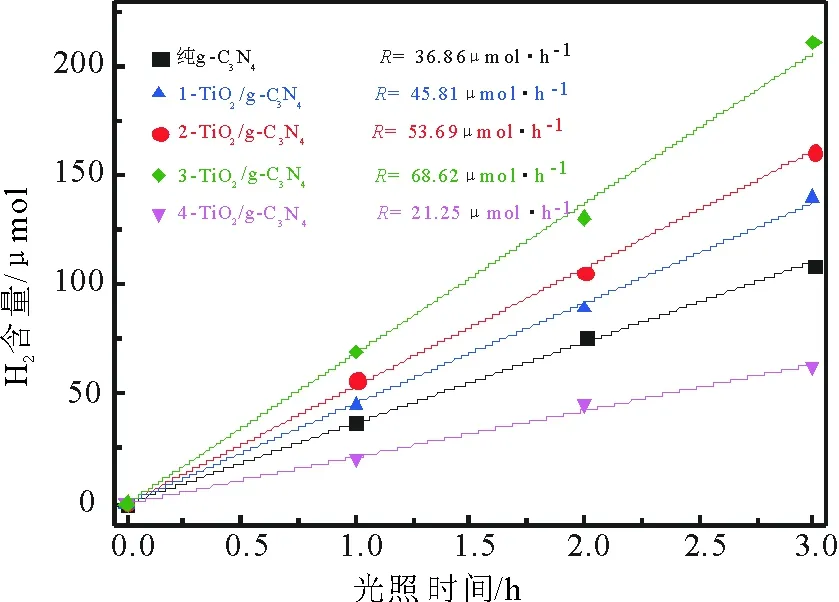
图7 不同样品的产氢速率曲线Fig.7 The performance of different samples on H2 production
3 光催化机理分析
3.1 稳定性分析
为了测试所制备3-TiO2/g-C3N4的稳定性,将该样品循环用于罗丹明B的降解实验,其降解条件与之前条件完全相同,所得结果如图8所示。可以看出,该样品在经过5次循环降解试验后,其降解性能并没有出现明显的减弱,表明该样品的稳定性比较好。在5次循环实验中,其降解率分别为87.7%,84.3%,82.5%,80.2%以及78.3%。因此,该复合样品稳定性比较好,有很好的应用潜力。

图8 3-P25/g-C3N4样品降解罗丹明B的循环实验Fig.8 The performance of 3-P25/g-C3N4 on RhB degradation with five times circulation
3.2 活性因子检测实验
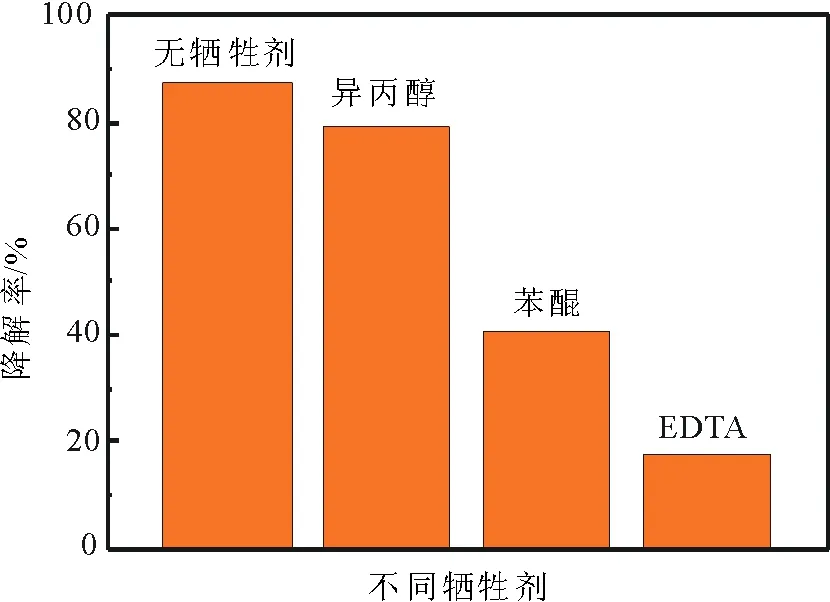
图9 活性因子捕获实验Fig.9 The performance of 3-P25/g-C3N4 on RhB degradation with different captures
在罗丹明B的降解实验中分别加入异丙醇,苯醌以及EDTA-2Na作为·OH,·O2-以及h+的捕获剂,其结果如图9所示。在没有加入任何捕获剂时,其降解率为87.7%,当加入异丙醇时,其降解率有所降低,但不太明显。当加入苯醌时,其降解率明显降低,说明·O2-在罗丹明B的降解中也是主要的活性物种。然而,当加入EDTA-2Na时,其降解率明显被抑制,说明h+在降解过程中是最主要的活性物种。因此,在罗丹明B的降解过程中,最主要的活性物种为h+,·O2-次之,·OH对降解的抑制作用最弱。从该实验结果可以推测3-TiO2/g-C3N4的复合样可以有效的将电子和空穴分离,从而提高光催化效果。
3.3 降解机理分析
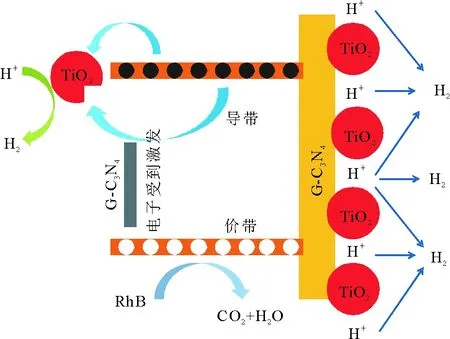
图10 复合物的光催化增强机理Fig.10 The enhanced mechanism of composites on RhB degradation
在光催化过程中,影响其光催化活性的主要因素有3个方面,光生电子的产生效率,载流子的传递效率,光生电子和空穴复合。光催化总效率为三者的乘积,即η总=η1×η2×η3。因此,改善以上3个方面中的任意一个都可以提高光催化效果。对于该复合样品来说,主要是通过抑制光生电子和空穴的复合,同时提高载流子的传递速率和光吸收范围来提高光催化活性。其主要机理如图10所示,g-C3N4的基态电子接受光能量后变成激发态并聚集形成导带(方程1中的e),而留下的空穴聚集形成价带(方程1中的h+)。价带则具有一定的氧化性(方程2,3)而导带具有一定的还原性(方程4,5)而,降解罗丹明B则是h+起主要作用,制氢过程则是光生电子和质子氢的作用。该机理可以解释为光生电子很快的从g-C3N4体相迁移到表面后转移至TiO2上而空穴的则留在g-C3N4表面,而光生电子转移到TiO2上以后因为电势差(g-C3N4的导带电势(-1.13 eV)比TiO2的导带电势(-0.3 eV)更负)的作用很难再回到g-C3N4表面。所以,该复合物可以有效地提高载流子的传递速率,同时可以抑制光生电子和空穴的复合、拓宽光吸收范围,从而提高光催化活性。
Samples+hv↔e-+h+
(1)
h++TEOA→oxidation products
(2)
h++OH-↔·OH
(3)
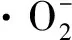
(4)
e-+H+→H2
(5)
4 结 论
1) 通过超声剥离法和二次煅烧法地制备了TiO2和g-C3N4的复合物,且TiO2均匀分散在g-C3N4表面,TiO2与g-C3N4之间通过化学键结合。
2) 当TiO2的质量分数为3%时光催化活性最强,过量的TiO2反而阻止了被降解物分子和g-C3N4的接触,从而抑制其光催化活性。不足量的TiO2则不能将g-C3N4产生的光生电子完全转移,达不到最好光催化效果。
3) 少层g-C3N4可以减少载流子的传输距离,通过和TiO2复合可以很快将g-C3N4上的光生电子转移至TiO2并且抑制电子和空穴的复合几率,从而提高催化活性。
[1] FAN X, FAN J, HU X Y, et al. Preparation and characterization of Ag deposited and Fe doped TiO2nanotube arrays for photocatalytic hydrogen production by water splitting[J]. Ceramics International, 2014, 40(10):15907-15917.
[2] CAO S W, YU J G. g-C3N4-based photocatalysts for hydrogen generation[J]. The Journal of Physical Chemistry Letters, 2014, 4(5):2101-2107.
[3] WANG X J, YANG W Y, LI F T, et al. In Situ Microwave-Assisted Synthesis of Porous N-TiO2/g-C3N4heterojunctions with enhanced visible-light photocatalytic properties[J]. Industrial & Engineering Chemistry Research, 2013, 52(48):17140-17150.
[4] WU F, HU X Y, FAN J, et al. Photocatalytic activity of Ag/TiO2nanotube arrays enhanced by surface plasmon resonance and application in hydrogen evolution by water splitting[J]. Plasmonics, 2012, 8(2):501-508.
[5] 吴树新, 马智, 秦永宁, 等.过渡金属掺杂二氧化钛光催化性能的研究[J] 影像科学与光化学, 2005, 23(2):94-101.
[6] 王丽, 陈永, 赵辉,等.非金属掺杂二氧化钛光催化剂的研究进展[J] 材料导报, 2015, 29(1):147-151.
[7] WU H T, FAN J, LIU E Z, et al. Facile hydrothermal synthesis of TiO2nanospindles-reduced graphene oxide composite with a enhanced photocatalytic activity[J]. Journal of Alloys & Compounds, 2015, 623:298-303.
[8] ZHONG Z, YIN Y, GATES B, et al. Preparation of mesoscale hollow spheres of TiO2and SnO2by templating against crystalline arrays of polystyrene beads[J]. Advanced materials, 2000, 12(3):206-209.
[9] WANG Y, WANG X, ANTONIETTI M.Polymeric graphitic carbon nitride as a heterogeneous organocatalyst: From photochemistry to multipurpose catalysis to sustainable chemistry[J]. Angewandte Chemie, 2012, 51(1):68-89.
[10] MA Y N, LIU E Z, HU X Y, et al. A simple process to prepare few-layer g-C3N4nanosheets with enhanced photocatalytic activities[J]. Applied Surface Science 2015, 358:246-251.
[11] BOONPRAKOB N, WETCHAKUN N, PHANICHPHANT S, et al. Enhanced visible-light photocatalytic activity of g-C3N4/TiO2films[J]. Journal of Colloid and Interface Science, 2014, 417(3):402-409.
[12] LI G, NIE X, ChEN J, et al. Enhanced visible-light-driven photocatalytic inactivation of Escherichia coliusing g-C3N4/TiO2hybrid photocatalyst synthesized using a hydrothermal-calcination approach[J]. Water research, 2015,86:17-24.
[13] WEI X, SHAO C, LI X, et al. Facile in situ synthesis of plasmonic nanoparticles-decorated g-C3N4/TiO2heterojunction nanofibers and comparison study of their photosynergistic effects for efficient photocatalytic H2evolution[J]. Nanoscale, 2016, 8(21):11034-11043.
[14] LI J, LIU E Z, MA Y N, et al. Synthesis of MoS2/g-C3N4nanosheets as 2D heterojunction photocatalysts with enhanced visible light activity[J]. Applied Surface Science, 2016, 364:694-702.
