β-环糊精修饰CdSe量子点关-开型荧光探针法测定药品中锌离子
2018-01-22刘秋文李满秀
刘秋文,李满秀,丁 茹,胡 艳
(忻州师范学院化学系,忻州034000)
锌是人体生命活动中不可缺少的微量元素,是介导脑缺血损伤的一种金属离子,参与生命细胞的多项生理生化功能,对人体的生命活动和健康有着极其重要的作用。因此准确测定药品中锌离子的含量十分必要。
CdSe量子点具有发射峰窄、激发光谱连续等优点[1],存在量子限域效应,具有既不同于体相材料又别于一般分子的光学和电子学性质,被广泛用作生物体系的荧光标记物[2-3]。β-环糊精具有疏水空腔和众多羟基,可以对许多分子进行多位点识别[4]。但由于β-环糊精本身缺乏测量信号,对于那些具有光学惰性或经β-环糊精包合未能引起光学信号显著改变的客体而言,用直接吸光光度法和荧光法进行测定就受到了限制[4-5]。CdSe量子点作为荧光探针可在药物分析中应用[6-7],但未见基于环糊精修饰后的CdSe量子点测定锌离子含量的报道。本工作考虑量子点的荧光特性并基于β-环糊精的包合特性[8],合成具有荧光信号的β-环糊精修饰的CdSe量子点(CdSeβ-CD QDs)并对锌离子进行标记,实现对样品中锌离子的测定。
1 试验部分
1.1 仪器与试剂
F-4500型荧光分光光度计;UV-2500型紫外分光光度计;pHS-3B型酸度计;78-2型磁力加热搅拌器;微量进样器;HK-2A型超级恒温水浴。
锌标准储备溶液:1.0×10-3mol·L-1,称取硫酸锌0.028 8g,用水溶解,并转移至100mL容量瓶中定容,摇匀待用。
根皮素标准溶液:3.7×10-4mol·L-1,称取根皮素10mg,用无水甲醇溶解,并转移至100mL容量瓶中,用无水甲醇稀释至刻度,摇匀待用。
四硼 酸 钠-硼 酸 缓 冲 溶 液 (pH 8.0):将0.05mol·L-1四硼酸钠溶液和0.2mol·L-1硼酸溶液混合,调节溶液的pH至8.0。
硫酸锌为光谱纯,巯基丙酸、根皮素、β-环糊精、硼氢化钠、硒粉、CdCl2·5/2H2O为分析纯,试验用水为超纯水。
1.2 仪器工作条件
激发和发射狭缝宽度均为10nm,激发和发射波长分别为321,520nm。
1.3 试验方法
1.3.1 巯基丙酸包被的CdSe量子点的制备[9]
分别称取硒粉0.127 6g和硼氢化钠0.080 0g加入三颈瓶中,在氮气保护下迅速注入水3mL。在冰水浴中、强磁力搅拌下反应4h,静置10min,上层无色溶液即为NaHSe溶液。
将1.25×10-3mol·L-1CdCl2溶液100mL加入250mL三颈烧瓶中,随后通高纯氮气30min,注入巯基丙酸26μL,并用1mol·L-1NaOH 溶液调pH至11,在氮气保护下迅速注入新制备的还原剂NaHSe溶液75μL,在96℃水浴中回流3h,即获得颜色透明的CdSe量子点。
1.3.2 CdSeβ-CD QDs的合成[10]
向CdSe量子点前体溶液中加入等体积的2.5×10-3mol·L-1的β-环糊精溶液,控制回流温度为96℃,在氮气氛围中、磁力搅拌下反应1h,得到CdSeβ-CD QDs溶液,密封避光保存备用。
1.3.3 样品分析
称取葡萄糖酸锌样品粉末0.131 0g,用水溶解后转至100mL容量瓶中,以水定容,摇匀备用。
在10mL比色管中加入CdSeβ-CD QDs溶液1.0mL,再向其中加入3.7×10-4mol·L-1根皮素溶液0.6mL,摇匀后再加入葡萄糖酸锌溶液0.2mL,用pH 8.0的四硼酸钠-硼酸缓冲溶液定容至5mL,反应10min后测量荧光强度。
2 结果与讨论
2.1 量子点光学性质表征
对于合成的CdSe量子点和CdSeβ-CD QDs用紫外光谱进行表征,结果见图1。图1(曲线1)代表水溶性CdSe量子点的紫外吸收光谱图,两个吸收峰分别位于400,600nm;图1(曲线2)代表CdSeβ-CD QDs的紫外吸收光谱图,两个吸收峰分别位于320,400nm。对合成的CdSe量子点和CdSeβ-CD QDs用荧光光谱表征结果见图2。图2(曲线1)表示在激发波长410nm时,CdSe量子点在550nm处有一较窄而强发射峰;图2(曲线2)表示在激发波长为321nm时,CdSeβ-CD QDs在550nm处也有一窄而强的发射峰,相比未修饰的量子点来说,荧光强度明显增强。
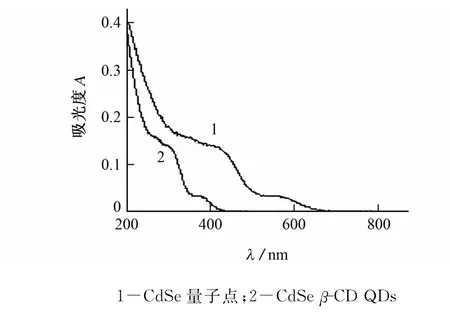
图1 紫外吸收光谱图Fig.1 UV adsorption spectra
2.2 CdSeβ-CD QDs与根皮素的作用
在9支10mL比色管中分别加入CdSeβ-CD QDs溶液1mL,再依次加入不同体积的3.7×10-4mol·L-1根皮素溶液,摇匀使其充分混合,静置后用pH 8.0的四硼酸钠-硼酸缓冲溶液定容,放置10min,在仪器工作条件下测量其荧光强度,结果见图3。
由图3可知:随着溶液中根皮素的浓度增大,CdSeβ-CD QDs的荧光强度会明显下降。根皮素对CdSeβ-CD QDs的荧光强度具有猝灭作用,其机理不是因为分子间碰撞引起的,可能是由于根皮素属于黄酮类物质,黄酮类物质和量子点以非共价键形式结合成某种不发光的配合物而形成荧光猝灭[11]。
试验数据显示:根皮素浓度在3.6×10-6~5.1×10-5mol·L-1内与荧光强度呈线性关系,且猝灭后的荧光强度随着根皮素浓度的增加而减小,荧光强度(F)和根皮素浓度(c)之间的线性回归方程为F=-8.271×106c+6.089×102,相关系数为0.993 7。

图2 荧光发射光谱图Fig.2 Fluorescence emission spectra

图3 根皮素浓度对CdSeβ-CD QDs荧光强度的影响Fig.3 Effect of the concentration of phloretin on the fluorescence intensity of CdSeβ-CD QDs
2.3 Zn2+对CdSeβ-CD QDs猝灭体系荧光恢复的影响
在7支10mL比色管中分别加入CdSeβ-CD QDs溶液1mL,再加入3.7×10-4mol·L-1根皮素溶液1.4mL,振荡摇匀,静置10min,然后依次向比色管中加入1.0×10-3mol·L-1Zn2+溶液0,0.06,0.08,0.4,0.6,0.8,0.9mL,振荡使溶液充分混合,静置后用pH 8.0的四硼酸钠-硼酸缓冲溶液定容,放置10min,在仪器工作条件下测量其荧光强度。
试验表明:在上述根皮素-CdSeβ-CD QDs猝灭体系基础上加入不同量的锌离子,CdSeβ-CD QDs的荧光强度会得到恢复,见图4。其原因可能是锌离子和黄酮类物质发生结合,将量子点表面的根皮素释放出来。因此随着量浓度锌离子的加入,CdSeβ-CD QDs的荧光强度会得到不同程度的恢复。

图4 Zn2+浓度对CdSeβ-CD QDs荧光强度的影响Fig.4 Effect the concentration of Zn2+ on the fluorescence intensity of CdSeβ-CD QDs
2.4 缓冲溶液及酸度的影响
在上述选定的根皮素-CdSeβ-CD QDs猝灭体系,根皮素-CdSeβ-CD QDs-Zn2+恢复体系基础上,考察不同酸度四硼酸钠-硼酸缓冲溶液(pH 7.4,8.0,8.4,9.0)和四硼酸钠-氢氧化钠缓冲溶液(pH 9.5,10.0)对猝灭体系和恢复体系荧光强度的影响,结果见图5。
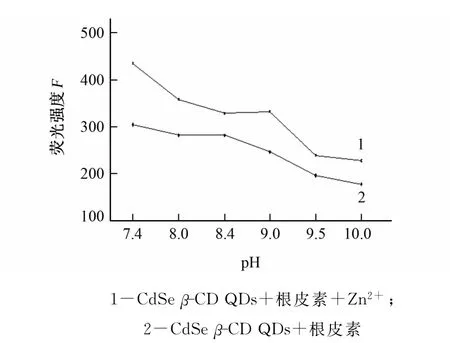
图5 酸度对CdSeβ-CD QDs荧光强度的影响Fig.5 Effect of acidity on the fluorescence intensity of CdSeβ-CD QDs
由图5可知:在pH 8.0的四硼酸钠-硼酸缓冲体系中荧光强度变化最大。试验选择pH 8.0的四硼酸钠-硼酸缓冲溶液为反应介质。
2.5 反应时间和温度的影响
在确定溶液pH的条件下,考察了反应时间对CdSeβ-CD QDs猝灭体系和恢复体系的影响。在时间为10,20,30,60,90,120min条件下测定体系的荧光强度。结果表明,CdSeβ-CD QDs与根皮素混合后10min后,体系发光强度达到平衡,因此选择10min后测定量子点猝灭的荧光强度。当Zn2+加入猝灭体系后荧光强度会增大,且10min后发光强度趋于稳定,所以选择在10min时测定量子点的荧光恢复强度。通过考察15,25,35,45,55℃的温度对猝灭体系和恢复体系荧光强度的影响,表明在15~25℃时测定荧光强度最为合适,试验选择室温(25℃)下测定。
2.6 CdSeβ-CD QDs用量的影响
试验 表 明:当 加 入 CdSeβ-CD QDs 溶 液1.0mL时,量子点的荧光强度适中且荧光稳定性比较好;加入量小于1.0mL时,荧光猝灭以及荧光恢复的效果都不明显;当加入量大于1.0mL时,虽然荧光猝灭以及荧光恢复的效果有明显提升,但分析灵敏度较低。综合考虑灵敏度、线性范围、背景干扰等因素,试验选用CdSeβ-CD QDs溶液1.0mL。
2.7 根皮素浓度对猝灭的量子点恢复的影响
试验探讨了根皮素浓度对猝灭后量子点恢复的影响。结果表明,根皮素浓度直接影响CdSeβ-CD QDs恢复体系荧光强度的测定。当根皮素浓度为5.1×10-5mol·L-1时,荧光的恢复效率较高、检测背景低、线性范围宽。当根皮素浓度低于5.1×10-5mol·L-1或高于5.1×10-5mol·L-1时,CdSe β-CD QDs荧光猝灭的效率会降低,检测背景高,恢复线性范围窄。因此,试验选用5.1×10-5mol·L-1根皮素溶液作为量子点猝灭剂对Zn2+进行测定。
2.8 干扰物质对荧光强度的影响
用含5.1×10-5mol·L-1根皮素和8.0×10-5mol·L-1Zn2+的溶液,对共存物质进行干扰试验。当相对误差在±5%内时,各共存物质的允许量如下(以μmol·L-1计):K+、Mg2+、Cl-、葡萄糖、L-精氨酸(100),苯酚(80),L-半胱氨酸(50),果糖(20),Mn2+、Al3+、Hg2+、SO42-、硬 脂酸 镁 (10),Ca2+(7.5),Cd2+(5),Pb2+(1.5),Cr3+(1),Cu2+、Fe3+、Ni2+(0.5),Co2+(0.3),Ag+、NO3- (0.05)。
2.9 标准曲线和检出限
按试验方法对Zn2+标准溶液系列进行测定,Zn2+浓度在6.0×10-6~9.0×10-5mol·L-1内与F/F0(F 为根皮素-CdSe-β-CD QDs猝灭体系基础上加入不同量的锌离子时的荧光强度;F0为CdSeβ-CD QDs加入根皮素时体系的荧光强度)具有良好的线性关系,线性回归方程为F/F0=3.063×106c+1.665×102,相关系数为0.990 6。
对2.0×10-5mol·L-1锌离子溶液进行10次平行测定,测定值的相对标准偏差为1.1%,以3倍标准偏差法计算方法的检出限(3s)为3.8×10-6mol·L-1。
2.10 样品分析
按试验方法测定葡萄糖酸锌片中的锌[12],并进行加标回收试验,结果见表1。葡萄糖酸锌片中锌含量标示值为10mg,试验测得每片中锌含量为9.5mg。

表1 样品分析结果(n=5)Tab.1 Analytical results of samples(n=5)
本工作合成了CdSeβ-CD QDs,在优化体系酸度、反应温度、反应时间等条件的基础上,以CdSeβ-CD QDs为关-开型荧光探针,成功测定了药片中锌离子的含量,此方法操作简便、快速、准确,丰富了CdSe量子点的应用范围。
[1] 朱明雪,徐建萍,张晓松,等.CdSe/CdS核壳纳米晶微波水热法一步合成与发光光谱分析[J].发光学报,2014,35(8):950-955.
[2] 刘星,罗阳.量子点生物传感器中的表面修饰技术及其医学应用[J].分析化学,2014,42(7):1061-1069.
[3] 李巍,刘峥,赖丽燕,等.荧光量子点的制备及分析应用[J].理化检验-化学分册,2014,50(4):518-524.
[4] 吴双双,梁耀珍,俞英,等.CdSe/巯基-β-环糊精量子点的纯化及应用[J].华南师范大学学报(自然科学版),2011(3):82-86.
[5] 韩翠平.环糊精的纳米界面组装及分子识别性能研究[D].武汉:华中师范大学,2012.
[6] 陈晓英,李芳,沈茂,等.基于KMnO4修饰的硒化镉量子点关-开型荧光探针法测定尿样中的抗坏血酸[J].科学技术与工程,2011,11(21):4969-4971.
[7] 杨昆,陈林情,赵慧凯,等.CdSe量子点“开关”的构建及其在药物分析中的应用[J].发光学报,2015,36(3):312-316.
[8] 刘春玲,侯长军,霍丹群,等.环糊精修饰的量子点功能材料及其选择性识别研究进展[J].功能材料,2015,46(9):9007-9010.
[9] 李满秀,邸慧霞,张媛,等.基于CdTe量子点荧光猝灭-恢复方法测定磷酸根[J].化学研究与应用,2015,27(3):335-338.
[10] 杨虹,杨成雄,严秀平.环糊精修饰CdTe量子点荧光探针用于检测茶叶中咖啡因[J].分析科学学报,2014,30(5):619-624.
[11] 周柳金,赵晓艺,田建袅,等.三种黄酮药物对CdSe/CdS量子点荧光影响研究[J].光谱学与光谱分析,2010,30(11):303-304.
[12] 汤家华,王玉文,张家庭,等.5′-硝基水杨基荧光酮-溴化十六烷基三甲胺-柠檬酸光度法测定锌[J].应用化工,2014,43(12):2307-2309.
