高效液相色谱法测定纺织品中3种短链对特辛基苯酚乙氧基化物
2018-01-22任清庆保琦蓓傅科杰
任清庆,保琦蓓,2*,傅科杰,3,吴 丰,钱 丹
(1.宁波出入境检验检疫局 纺织品检测中心,宁波315100; 2.宁波检验检疫科学技术研究院,宁波315012;3.浙江理工大学 材料与纺织学院,杭州310018)
对特辛基苯酚乙氧基化物是由辛基酚与环氧乙烷在碱催化剂存在下缩聚而成。在纺织行业中主要被用作液体洗涤剂、染料色泽改进剂或乳化剂。2012年12月17日,在欧盟化学品管理局(ECHA)官方网站上公布的REACH法规第八批高度关注物质(SVHC)候选清单中增加了对特辛基苯酚乙氧基 化 物 [4-(1,1,3,3-tetramethylbutyl)phenol,ethoxylated],限制了这类物质在纺织品与皮革产品中的使用,并要求物品中此类物质质量分数不超过0.1%[1]。世界上已有很多国家开始对该类物质进行了单独的研究和监控。不同聚合度的对特辛基苯酚乙氧基化物的特性、应用范围及毒性有很大的差别。特别是含有1~3个乙氧基单元的短链对特辛基苯酚乙氧基化物是纺织品及环境中此类聚合物自然降解而形成的难进一步降解的中间产物,其具有比母体更大的生态毒性[2]。因此,建立能够同时分离不同聚合度的对特辛基苯酚乙氧基化物的方法非常必要,特别是该类短链对特辛基苯酚乙氧基化物的检测方法,将为纺织品的生态安全和我国纺织品顺利出口提供强有力的保障。
从国内外的研究文献来看,对此类物质的定量分析方法主要有气相色谱-质谱法(GC-MS)、高效液相色谱法(HPLC)、高效液相色谱-串联质谱法(HPLC-MS/MS)等[3-6],但由于其具有一定的极性且挥发性低,采用GC-MS需要进行衍生化处理,否则容易出现色谱峰拖尾及灵敏度低等情况。液相色谱法不需进行衍生化,目前纺织品检测实验室配置较多,但其灵敏度很大程度上取决于所选择的检测器。HPLC-MS/MS近年来发展迅速,可较好地定性定量分析目标物,既可以提供较高的灵敏度,又可以最大限度避免假阳性结果,但由于仪器昂贵,能配备的实验室较少,应用范围受到一定限制。用于测定非离子表面活性剂及其同系物最为合适的方法是高效液相色谱法,一般能用正相色谱柱进行测定[6]。文献[3]采用GC-MS的方法测定了皮革中的烷基酚类聚乙氧基化表面活性剂。文献[7]采用正相液相色谱-紫外检测器与反相液相色谱-质谱检测器测定了纺织品中的烷基酚聚乙氧基化物。文献[2]又采用反相HPLC测定了废水及其他环境样品中的聚乙氧基化烷基酚的总量。文献[8]提出应用LCMS/MS进行测定,通过向流动相中加入一种有足够挥发性的离子试剂可以达到很高的灵敏度。文献[9]采用正相液相色谱-质谱法分离了废水样品中具有3~10个乙氧基单元的壬基酚乙氧基化物。文献[10]在研究4-t-辛基酚的降解动力学时使用反相高效液相色谱配合紫外检测器测定了水中的此类物质。文献[11]使用C1柱的反相液相色谱达到了对日用化学品中对辛基酚类非离子表面活性剂的快速分离和测定,并对其同系物的分布进行了一些研究。
由于反相液相色谱法鉴别类似物质技术已较为成熟,本工作首先尝试使用反相液相色谱法,但3种物质无法区分开来,因此本工作在优化索氏萃取、超声波萃取与微波萃取3种前处理方法的基础上,采用正相液相色谱法对纺织品中的对特辛基苯酚单乙氧基化物、对特辛基苯酚二乙氧基化物与对特辛基苯酚三乙氧基化物等3种生态毒性较大的短链对特辛基苯酚乙氧基化物含量的测定方法进行了探讨。
1 试验部分
1.1 仪器与试剂
Waters e2695型高效液相色谱仪,配荧光检测器(FLD);KQ 2200E型超声波发生器,工作频率为40kHz;AE 260型分析天平;RV 10型旋转蒸发仪;Multiwave 3000SOLV型微波萃取仪。
标准储备溶液:称取对特辛基酚单乙氧基化物、对特辛基酚二乙氧基化物与对特辛基酚三乙氧基化物的标准品,分别用异丙醇配制成质量浓度为1 000mg·L-1的单组分标准储备溶液。再分别移取各单组分标准储备溶液适量,用异丙醇稀释,配制成混合标准溶液。
对特辛基酚单乙氧基化物标准品(纯度不小于98%);对特辛基酚二乙氧基化物标准品(纯度不小于99%);对特辛基酚三乙氧基化物标准品(纯度不小于99%)。
所用甲醇、乙腈、正己烷、异丙醇等有机试剂均为色谱纯,试验用水为一级水。
1.2 仪器工作条件
Dikma platisil silica 硅 胶 柱 (250mm ×4.6mm,5.0μm);柱温度35℃;流动相 A为正己烷-异丙醇(85+15)混合液,流动相B为异丙醇-水(85+15)混合液。梯度洗脱程序:0~10min时,A为100%;10~15min时,A由100%降为85%;15~20min时,A由85%降为80%;20~25min时,A由80%降为70%。荧光检测器,激发波长230nm,发射波长296nm;流量0.5mL·min-1;进样量10μL。
1.3 试验方法
选取试样,剪碎至5mm×5mm的碎片,混匀。称取试样2.00g置于具塞锥形瓶中,加入甲醇50mL于常温下在超声波发生器中萃取40min,将萃取液转入圆底烧瓶中,再用甲醇20mL对锥形瓶中的样品重复提取20min,合并两次萃取液,然后用甲醇10mL洗涤残渣,并入萃取液中。在旋转蒸发仪上于(40±2)℃,浓缩至1~2mL,然后用异丙醇定容至10.0mL。溶液经有机相过滤膜过滤后,作为样液供正相高效液相色谱检测。
2 结果与讨论
2.1 色谱柱的选择
试验选择了Kromasil氨基液相色谱柱(250mm×4.6mm,5μm),Dikma platisil silica硅胶柱(250mm×4.6mm,5μm),Kromasil氰基液相色谱柱(250mm×4.6mm,5μm)等3种正相色谱柱进行目标物分离。结果表明:在氨基液相色谱柱与氰基液相色谱柱中对特辛基酚单乙氧基化物与对特辛基酚二乙氧基化物的出峰效果较差,仪器响应较低,且对特辛基酚三乙氧基化物的峰形有严重拖尾现象。因此,试验采用Dikma platisil silica硅胶柱分离。
2.2 流动相的选择
根据相似相溶原理,利用不同乙氧基(EO)单元的辛基酚聚氧乙烯醚(OPEO)的极性差异进行正向柱的试验。起始采用100%正己烷为流动相A,但是极性太小导致高效液相色谱仪不能完成前平衡过程,因此加入少量异丙醇增强流动相A的极性。选择水作为流动相B,其极性虽然更强,但出峰效果不佳,所以加大流动相B中异丙醇的比例而减少了水的配比。流动相B中异丙醇可以使短链对特辛基苯酚乙氧基化物的保留值降低,缩短分离时间,却使疏水性较强的对特辛基酚单乙氧基化物与对特辛基酚二乙氧基化物的分离度降低。当异丙醇含量降低,整个流动相的极性减弱时,虽然各个主要样品峰能达到基线分离,但使疏水性较弱的对特辛基酚三乙氧基化物在分析柱上的保留性加强,导致峰展宽,峰高降低,较难检测。采用正己烷-异丙醇(85+15)混合液为流动相A,异丙醇-水(85+15)混合液为流动相B,3个目标物基本能够达到基线分离。
图1为3种短链对特辛基苯酚乙氧基化物混合标准溶液的正相色谱图,3种物质的保留时间分别为9.939,12.539,15.134min。
2.3 前处理条件的优化
通常用于提取固体样品中待测成分的方法主要有索氏萃取法、超声萃取法与微波萃取法。分别采用这3种萃取方法对不同材质的市售纺织品中的3种对特辛基酚乙氧基化物进行萃取,比较其萃取效果。采用玫红色机织棉布、黑色机织涤纶布、粉红色机织羊毛面料等3个样品进行前处理方法的选择试验。
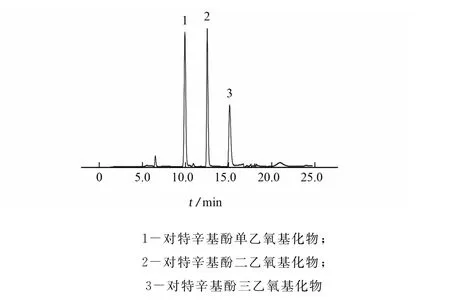
图1 3种短链对特辛基苯酚乙氧基化物混合标准溶液的色谱图Fig.1 Chromatogram of the mixed standard solution of 3kinds of short chain 4-(1,1,3,3-tetramethylbutyl)phenol,ethoxylated
2.3.1 索氏萃取法
1)萃取时间
取玫红色机织棉布样品,以甲醇作为萃取溶剂,分别索氏萃取2,3,4,5h后,按试验方法进行测定,计算萃取效率。结果发现:萃取时间在2h后萃取效率基本无变化。因此,试验选择索氏萃取时间为2h。
2)萃取溶剂
试验选用二氯甲烷、甲醇、石油醚、三氯甲烷、正己烷等5种溶剂对3个样品进行索氏萃取。根据各溶剂的沸点,索氏萃取的温度比各溶剂的沸点高10℃。萃取效果见图2。
由图2可知:对于3种不同材质的纺织样品,甲醇的萃取效果均最佳,其次为二氯甲烷和正己烷。综合考虑,试验选择索氏萃取法的条件为:甲醇作为萃取溶剂,在80℃下索氏萃取2h。
2.3.2 超声萃取法
1)萃取时间
取黑色机织涤纶布样品,以甲醇为萃取剂,以1∶25的固液比分别超声10,20,30,40,50,60,70min,萃取液转移至烧瓶中旋转蒸发浓缩至近干,用异丙醇定容至10.0mL后进行液相色谱法分析,结果见图3。
2)萃取温度
取黑色机织涤纶布样品,分别在30,40,50,60℃下超声萃取40min,旋转蒸发至近干后用异丙醇定容后进行高效液相色谱法测定。结果发现超声温度对萃取效果的影响不大,因此,试验选择在室温下进行超声萃取。
3)萃取溶剂
试验选择甲醇、异丙醇、乙酸乙酯、丙酮、正己烷-丙酮(1+1)混合液等5种常用溶剂作为萃取溶剂,萃取3个样品中的3种目标物,萃取结果见图4。

图2 不同溶剂对3种样品中3种对特辛基乙氧基化物的索氏萃取效果Fig.2 Efficiency of Soxhlet extraction for 3kinds of 4-(1,1,3,3-tetramethyl(butyl)phend,ethoxylated in 3samples with different solvents

图3 超声萃取时间对萃取效果的影响Fig.3 Effect of microwave extraction time on extraction efficiency
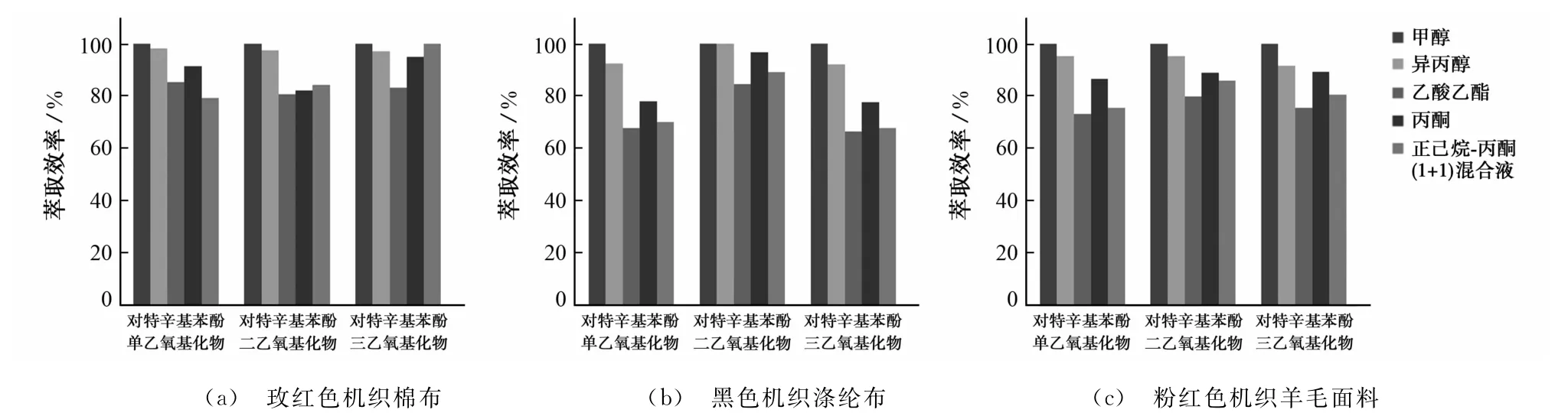
图4 不同溶剂对3个样品中3种对特辛基乙氧基化物的超声萃取效果Fig.4 Efficiency of ultrasonic extraction for 3kinds of 4-(1,1,3,3-tetramethyl(butyl)phenol,ethoxylated in 3samples with different solvents
由图4可知:对3种不同材质的纺织品样品,甲醇的萃取效果均最佳,其次为异丙醇。
因此,超声萃取法的条件为:以甲醇作为萃取溶剂,以1∶25的固液比超声40min后将萃取液转移至烧瓶中,再加入1∶10固液比的萃取剂超声20min,以萃取样品中残留的目标物,将两次超声萃取的萃取液合并后旋转蒸发浓缩至近干,用异丙醇定容至10.0mL后进行液相色谱法分析。
2.3.3 微波萃取法
(一)在目前国内绝大多数高校中,专业教师在教学过程中,已然形成了一种思维定式,教师强调知识的传授,与学生缺乏思想和情感的交流,下课后更是难有接触。另外一方面是绝大多数高校对目前的这种现状更是一种“默许”的现状,如何改变专业教师的观念、注入协同育人的理念,如何加强高校对专业教师与思想政治教育工作者协同育人的重视将会是本课题研究的重点难点,任何举措和制度都应得到专业教师的认可和接受才能接地气,才能真正有所改变。
根据微波萃取理论,影响微波萃取的效率主要取决于萃取溶剂种类、萃取时间和萃取温度。采用不同的溶剂萃取时,其萃取效率相差较大。有研究表明,固定萃取溶剂和温度时,微波萃取效率会随着萃取时间的延长而有所提高,但提高幅度不大,可以忽略不计。一般情况下,萃取时间在20~30min基本可以满足萃取要求。在有机物的萃取过程中,将有机物从基质的活性位脱附是整个萃取过程的关键,较高的萃取温度有助于提高溶剂的溶解能力,更好地破坏有机物和基团活性位之间的作用力;同时,温度的提高使溶剂的表明张力和黏度下降,保持溶剂和基质之间的良好接触。通常情况下,萃取温度越高,有机物内部活动程度越剧烈,越有利于有机物的萃取。
试验选用二氯甲烷、甲醇、乙酸乙酯、丙酮、正己烷-丙酮(1+1)混合液等5种常见溶剂作为萃取剂,萃取玫红色机织棉布样品中的3种目标物质,考察其萃取效果。微波萃取时,萃取管内的压力随着萃取溶剂和温度的变化而变化,一般可达几个至十几个大气压,这时萃取溶剂的沸点也随之上升。试验中,采用每种萃取溶剂时的萃取温度均设定为比相应溶剂的沸点温度高20℃,升温速率均设为5℃·min-1,温度保持时间均为30min。采用不同溶剂的萃取效果见图5,结果可知,甲醇的萃取效果均最好,其次为丙酮。
综合考虑,确定微波萃取法的条件为:以甲醇为萃取溶剂,在80℃下微波萃取30min。
2.3.4 最优萃取条件的确定
试验综合考察了索氏萃取法、超声萃取法与微波萃取法对3种目标物的最优提取条件,考虑到实验室操作的方便性,采用超声萃取法进行样品的前处理。
2.4 标准曲线、检出限与测定下限
在仪器工作条件下对不同质量浓度的混合标准溶液进行测定,结果表明:3个目标物的色谱峰面积y与其质量浓度x在一定范围内呈线性关系。线性范围、线性回归方程和相关系数见表1。
试验采用在标准布中加标进行测定以确定方法的检出限,以3倍信噪比计算得到方法的检出限(3S/N),以10倍信噪比计算得到方法的测定下限(10S/N),结果见表1。

图5 不同溶剂对3种对特辛基苯酚乙氧基化物的微波萃取效果Fig.5 Efficiency of microwave extraction of 3kinds of 4-(1,1,3,3-tetramethyl(butyl)phenol,ethoxylated with different solvents

表1 线性参数、检出限和测定下限Tab.1 Linearity parameters,detection limits and lower limits of determination
2.5 精密度与回收试验
在玫红色机织布样品中分别添加2.50,5.00,10.00mg·kg-1等3个水平的标准物质,按试验方法各进行6次平行测定,计算加标回收率和测定值的相对标准偏差(RSD),结果见表2。
由表2可知:在3个添加水平下,回收率在94.4%~106%之间,RSD均小于6.0%。
2.6 样品分析
按照试验方法对实验室内部送检的26批样品进行测定,结果表明:26个样品中有2个阳性样品,分别是黑色涤纶机织布检出含对特辛基酚单乙氧基化物6.7mg·kg-1,粉红色羊毛针织布检出含对特辛基酚二乙氧基化物54.2mg·kg-1。图6为两个阳性样品的色谱图。

表2 精密度与回收试验结果(n=6)Tab.2 Results of tests for precision and recovery(n=6)

图6 阳性样品的色谱图Fig.6 Chromatograms of positive samples
本工作采用超声萃取-正相HPLC同时分离测定了纺织品中对特辛基苯酚单乙氧基化物、对特辛基苯酚二乙氧基化物与对特辛基苯酚三乙氧基化物等3种生态毒性较大的短链对特辛基苯酚乙氧基化物的含量。本方法具有较高的准确度和精密度,灵敏度高,检出限低,可对单乙氧基化物、二乙氧基化物与三乙氧基化物的质量分数高于1.1,1.2,1.5mg·kg-1的 样 品 进 行 定 量 分 析,能 满 足REACH法规中SVHC清单对该类物质的管控要求。
[1] 欧洲化学品管理局(ECHA).化学品注册、评估、授权和限制法规(REACH法规)附件17限制物质清单[Z].2012.
[2] AHEL M,GIGER W,KOCH M.Behaviour of alkylphenol polyethoxylate surfactants in the aquatic environment-I.Occurrence and transformation in sewage treatment[J].Water Research,1994,28(5):1143-1152.
[3] MA H W,CHENG Y.Determination of free and ethoxylated alkylphenols in leather with gas chromatography-mass spectrometry[J].Journal of Chromatography A,2012,1217(50):7914-7920.
[4] VEGA-MORALES T,SOSA-FERRERA Z,SANTANA-RODRIGUEZ J J.Determination of alkylphenol polyethoxylates,bisphenol-A,17α-ethynylestradiol and 17β-estradiol and its metabolites in sewage samples by SPE and LC/MS/MS[J].Journal of Hazardous Materials,2010,183(1/3):701-711.
[5] DATLA V M,BECK K,SHIM E.Reverse phase HPLC analysis of commercial surfactants used as melt additives[J].Tenside,Surfactants,Detergents,2010,47(3):142-150.
[6] VANHOENACKER G,SANDRA P.High temperature liquid chromatography and liquid chromatographymass spectroscopy analysis of octyphenol ethoxylates on different stationary phases[J].Journal of Chromatography A,2005,1082(2):193-202.
[7] WANG C,MA Q,WANG X.Determination of alkylphenol ethoxylates in textiles by normal-phase liquid chromatography and reversed-phase liquid chromatography/electrospray mass spectrometry[J].Journal of AOAC International,2007,90(5):1411-1417.
[8] LOOS R,HANKE G,UMLAUF G,et al.LC-MSMS analysis and occurrence of octyl-and nonylphenol,their ethoxylates and their carboxylates in Belgian and Italian textile industry,waste water treatment plant effluents and surface waters[J].Chemosphere,2007,66(4):690-699.
[9] MART NEZ E,GANS O,WEBER H,et al.Analysis of nonylphenol polyethoxylates with 3to 10ethoxy units in water samples by normal-phase liquid chromatography with electrospray mass spectrometry detection[J].Fresenius Environmental Bulletin,2005,14(8):681-689.
[10] 吴彦霖,余炎,袁海霞,等.185nm紫外光下薄液层中4-t-辛基酚的降解动力学:持久性有机污染物论坛2010暨第二届持久性有机污染物全国学术研讨会论文集[C].[出版地不详]:[出版者不详],2010:174-175.
[11] 王振地,默文芬戈斯,姚晨之,等,用C1柱的反相液相色谱对辛基酚聚氧乙烯醚型非离子表面活性剂快速分离和测定氧乙烯聚合物分布(英)[J].日用化学品科学,1999(6):9-12.
