离子液体-银纳米粒子修饰电极的制备及其在测定维生素C中的应用
2018-01-19,
,
(1. 天津职业大学 生物与环境工程学院, 天津 300410; 2. 天津大学 化工学院, 天津 300072)
维生素C是维持人体健康必需的维生素,对于防御感染性疾病有重要意义,研究表明维生素C缺乏可导致多种疾病,其含量测定被用于疾病诊断及营养分析中[1-2]。维生素C的测定方法包括碘量法、比色法等,但这些方法步骤繁琐,不利于快速分析。有报道利用电化学伏安法测定维生素C的含量[3],这种方法多采用聚合物及无机化合物薄膜修饰电极,能够快速、准确地测定维生素C的含量,但存在检出限偏高、测定灵敏度较低的缺点。因此需开发灵敏度高、快速、准确的电化学方法。
离子液体(IL)由于具有电化学稳定性、较宽的电化学窗口及良好的导电性,已被作为传感材料应用于电化学中[4]。纳米粒子具有大比表面积和良好的电子迁移性,其在电化学传感器中的应用近年来成为热点[5-6]。纳米粒子与离子液体结合应用于电化学传感器中,具有广泛的应用前景。
银纳米粒子(AgNPs)具有良好的导电性及生物兼容性,AgNPs应用于电化学传感器中可极大地提高电极表面电荷迁移速率,有效改善电化学响应信号,提高传感器的灵敏度[7-8]。离子液体[BMIM]BF4具有良好的离子化及导电性能,同时可作为稳定剂附着在纳米粒子表面,对AgNPs有很好的分散作用,防止AgNPs的团聚。
本工作利用离子液体-银纳米粒子复合材料修饰玻碳电极,考察银纳米粒子及离子液体对修饰电极性能的影响规律,对修饰电极的动力学进行研究,计算不同银浓度修饰电极的反应扩散系数,并对药剂中的维生素C含量进行测定。
1 试验部分
1.1 仪器与试剂
CHI 650型电化学分析仪,配三电极系统(修饰玻碳电极为工作电极,饱和甘汞电极为参比电极,Pt电极为辅助电极);TU-1810PC型紫外-可见分光光度仪;IRPrestige-21 SHIMADZU型岛津傅里叶变换红外光谱仪;JEM-2100F型场投射电子显微镜。
硝酸银、氯化钾、维生素C、甲基咪唑、溴代正丁烷、硼氢化钠、柠檬酸钠为分析纯,试验用水为去离子水。
1.2 离子液体的制备
取一定量甲基咪唑与溴代正丁烷,以甲苯为溶剂,回流反应3 h;用丙酮、乙酸乙酯抽滤后,得到中间体溴代甲基咪唑[BMIM]Br;在常温条件下,加入NaBF4搅拌6 h,直至反应完全,即得离子液体[BMIM]BF4。
1.3 银纳米粒子的制备
取0.1 mol·L-1柠檬酸钠溶液3 mL,加入氢氧化钠溶液调pH至12,加入到三口烧瓶中;再加入0.1 mol·L-1硝酸银溶液3 mL,电动搅拌,溶液呈褐色;再加入2 g·L-1维生素C溶液70 mL,于30 ℃水浴下,搅拌30 min后,停止反应。用水及乙醇溶液对银纳米粒子进行离心清洗,清洗多次,利用紫外-可见分光光度仪扫描,直至光谱图中250~650 nm处只有银纳米粒子峰即可。将清洗后的银纳米粒子在60 ℃进行真空干燥2 h。
1.4 修饰电极的制备
称取干燥后的银纳米粒子,配制一系列浓度的银纳米粒子溶液,并与离子液体按照一定体积比混合,配制成一系列浓度的银纳米粒子-离子液体混合溶液。
首先将玻碳电极依次用0.1,0.3,0.05 μm的Al2O3粉抛光,而后用水清洗。进行裸电极测试,确定电极表面打磨好后,浸泡于0.1 mol·L-1半胱氨酸溶液中1 h后取出,用水冲洗后,分别取上述银纳米粒子-离子液体混合溶液,滴于抛光后的玻碳电极上,于30 ℃真空干燥5 min。
1.5 试验方法
维生素C片剂处理:取标示量为0.1 g·片-1维生素C片于研钵中研细,称取粉末若干,用水溶解,过滤后,在100 mL容量瓶中定容备用。
选取上述修饰电极为工作电极,饱和甘汞电极为参比电极,Pt电极为辅助电极,电极优化测试在10,80 μmol·L-1维生素C的PBS溶液中进行,扫描范围为-0.4~0.8 V。测定了药剂中的维生素C含量,并进行了抗干扰试验。
2 结果与讨论
2.1 离子液体及银纳米粒子的表征
将制备的离子液体进行傅里叶变换-红外光谱(FT-IR)表征,谱图见图1。

图1 离子液体[BMIM]BF4的傅里叶变换-红外光谱图Fig. 1 FT-IR spectrum of ionic liquid [BMIM]BF4
由图1可知:所制备的离子液体的主要特征峰为3 413,1 628,1 570,1 167,1 050 cm-1。其中3 413 cm-1归属为芳香环上C-H的伸缩振动峰,1 628,1 570 cm-1归属为芳香环骨架振动峰,1 167 cm-1归属为芳环C-H面内振动峰,1 050 cm-1归属为BF4基团的B-F振动峰,与离子液体标准品谱图基本一致,证明合成的离子液体纯度较高。
制备的银纳米粒子溶液呈深绿色,其紫外-可见吸收光谱图见图2。

图2 银纳米粒子的紫外-可见吸收光谱图Fig. 2 UV-Vis absorption spectrum of silver nanoparticles
由图2可知:银纳米粒子的最大吸收峰出现在402 nm处,说明银纳米粒子尺寸较小。利用场投射电子显微镜表征银纳米粒子尺寸,见图3,银纳米粒子尺寸在20 nm左右。

图3 银纳米粒子的透射电子显微镜图片Fig. 3 TEM image of silver nanoparticles
2.2 维生素C在修饰电极中的电化学行为
2.2.1 银纳米粒子浓度对修饰电极性能的影响
方波伏安法测试在浓度为80 μmol·L-1维生素C的PBS溶液中进行,首先以裸玻碳电极为工作电极,测试结果见图4(曲线1),维生素C在裸电极中无氧化峰出现。试验分别测定了维生素C在不同浓度银纳米粒子修饰的玻碳电极的电化学行为,见图4(曲线2~7)。

1-裸电极;2~7对应银纳米粒子的浓度依次为0,0.2, 0.6,1.0,1.5,3.0 mol·L-1图4 维生素C在不同浓度银纳米粒子修饰电极的方波伏安图Fig. 4 SWV diagrams of Vitamin C at the electrodes modified with AgNPs of various concentrations
由图4可知:当只有离子液体修饰电极时,峰电流信号不明显;当修饰溶液中银纳米粒子浓度增大时,维生素C氧化峰电流逐渐增大;当修饰溶液中的银纳米粒子浓度继续增大至3.0 mol·L-1后,峰电流消失。
结合交流阻抗图5(曲线2~6)可知:高频区半圆直径即Rct值随银纳米粒子浓度增大而变小。这是由于随银纳米粒子在电极表面增多,电荷转移速率加快。因此,随着银纳米粒子浓度增大,对应图4(曲线6)中峰电流最大。

1-裸电极;2~7对应银纳米粒子的浓度依次为0,0.2, 0.6,1.0,1.5,3.0 mol·L-1图5 不同浓度银纳米粒子修饰电极的阻抗图Fig. 5 Impedance diagrams of the electrodes modified with AgNPs of various concentrations
由图5(曲线7)可知:对于由高浓度3.0 mol·L-1银纳米粒子-离子液体混合溶液修饰的电极,高频区Rct值虽然较小,但低频区直线斜率显著变小,电极表面的物质扩散变得不利,这成为反应速率的控制步骤。因此,维生素C的电化学反应不能发生,从而导致图4(曲线7)中银纳米粒子浓度增大至3.0 mol·L-1时峰电流消失。
2.2.2 离子液体浓度对修饰电极性能的影响
试验考察了银纳米粒子-离子液体混合修饰溶液中离子液体的体积分数(0~10%)对于修饰电极性能的影响。
如图6(曲线1)所示,当不加离子液体时,即只有银纳米粒子修饰玻碳电极时,有一定的峰电流相应;当修饰溶液中添加一定量的离子液体,可增强峰电流信号,如图6(曲线3)所示,当修饰液中离子液体的体积分数为4%时,修饰电极的性能最好。这是由于适当地添加离子液体有利于增强电极表面的导电性。但当离子液体比例过高时,反而不利于峰电流的增大,这与离子液体黏度大、极性强有关,离子液体的比例过高,抑制了反应物及产物的扩散,因而降低了修饰电极的性能。

曲线1~5对应离子液体的体积分数分别为0,2%, 4%,8%,10% 银纳米粒子在电极修饰溶液中的浓度均为1.0 mol·L-1图6 维生素C在不同体积分数离子液体修饰电极上的方波伏安图Fig. 6 SWV diagrams of Vitamin C on the electrodes modified with ionic liquid of various volume ratios
2.2.3 扫描速率对修饰电极电化学行为影响
对修饰电极进行优化后,在浓度为10 μmol·L-1维生素C溶液中,考察了扫描速率(v)对峰电流(Ip)的影响,见图7。
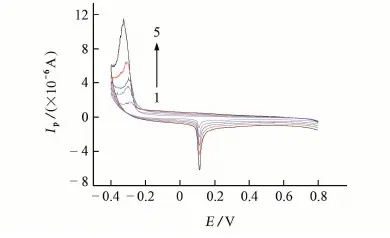
曲线1~5对应的扫描速率依次为0.02,0.04, 0.06,0.08,0.1 V·s-1图7 不同扫描速率下维生素C在修饰电极上的循环伏安曲线Fig. 7 CV curves of Vitamin C on the modified electrodes under different scan rates
通过计算可知:Ip与v1/2呈线性关系,相关系数为0.996 7。
2.3 修饰电极的电化学动力学测定
根据Randles-Savcik公式(1),计算修饰电极的有效面积。
Ip=2.69×105n3/2AD1/2cv1/2(1)
式中:Ip为峰电流,A;n为电子转移数;A为电极有效面积,cm2;D为扩散系数,cm2·s-1;v为扫描速率,V·s-1;c为浓度,mol·L-1。
测定了不同扫描速率下修饰电极在0.1 mol·L-1KCl及2×10-4mol·L-1K3[Fe(CN)6]溶液中峰电流,对Ip-v1/2进行了回归,回归方程为Ip=46.90v1/2+3.120×106,已知0.1 mol·L-1KCl中K3[Fe(CN)6]的扩散系数D为6.3×10-6cm2·s-1,由回归方程直线斜率可得出电极有效面积,利用计时电量法(CC)计算扩散系数。
利用CC法测出不同浓度的维生素C的Q-t1/2关系式,由公式(2)计算出维生素C不同浓度的扩散系数D,见表1。
(2)
式中:Q为计时电量法电量,C;n为电极反应的电子转移数;F为法拉第常数,96 485 C·mol-1;A为电极面积,cm2;D为扩散系数;cm2·s-1;t为电解时间,s;Qdl为双电层的充电电量,C。

表1 CC法测定扩散系数D的结果Tab. 1 Determination results of diffusion coefficiet D by CC method
由表1可知,随着维生素C浓度的增大,扩散系数减小。
2.4 片剂中的维生素C含量测定
2.4.1 线性范围及灵敏度考察
利用修饰电极测定了方波伏安法中峰电流随维生素C浓度变化的曲线图。当维生素C浓度在5~100 μmol·L-1内,峰电流与浓度呈线性关系,Ip(μA)=-0.424 7c(μmol·L-1)-0.443 8,相关系数为0.998 7,灵敏度为0.4 μA/μmol·L-1。
2.4.2 抗干扰试验
在10 μmol·L-1维生素C的PBS溶液中加入10倍的葡萄糖及过氧化氢,当相对误差在±5%以内均不干扰测定。
2.4.3 维生素C片剂测定及精密度考察
将处理的维生素C片剂样品按试验方法测定,平行测定5次,测定值与文献[9]基本一致,测定值的相对标准偏差(RSD)小于2.0%,方法具有较高的精密度。
以离子液体-银纳米粒子复合材料修饰玻碳电极,并对维生素C溶液进行了电化学测试。通过方波伏安法及交流阻抗法测试了不同浓度银纳米粒子及离子液体修饰电极的性能,结果表明:银纳米粒子浓度为1.5 mol·L-1,离子液体体积分数为4%的修饰溶液修饰电极性能最佳。利用修饰电极考察了扫描速率及维生素C浓度对峰电流变化的影响。对维生素C溶液的电化学扩散系数进行了计算,扩散系数随维生素C溶液的浓度增大而减小。利用优化电极测定了药剂中的维生素C含量,结果与文献值较为接近,方法准确度、精密度较高。
[1] 周闻云,陈艳玲,韩清,等.抗坏血酸在纳米银DNA修饰电极上的电化学行为研究[J].分析科学学报, 2009,25(2):169-172.
[2] 莫润宏,王富民,倪张林.离子排斥色谱-双检测器法同时测定果蔬中的糖、有机酸和维生素C[J].现代食品科技, 2016,32(4):276-278.
[3] 王琦,吴俊森.电化学分析法测定抗坏血酸的研究与应用[J].山东师范大学学报(自然版), 2005,20(4):38-40.
[4] 刘艳.离子液体在电化学生物传感器中的应用[J].辽宁化工, 2010,39(12):12-16.
[5] BAGHERI A, EMAMI F, NATEGHI M R. Direct measurment of traces of Vitamin C in urine using a modifed glassy carbon electrode[J]. Analytical letters, 1997,30(11):2023-2028.
[6] NASIRIZADEH N, SHEKARI Z, DEHGHANI M. Delphinidin immobilized on silver nanoparticles for the simultaneous determination of ascorbic acid, noradrenalin, uric acid, and tryptophan[J]. J Food Drug Anal, 2016,4:406-416.
[7] RASTOGI P K, GANESAN V, AZAD U P. Electrochemical determination of nanomolar levels of isoniazid in pharmaceutical formulation using silver nanoparticles decorated copolymer[J]. Electrochim Acta, 2016,188:818-824.
[8] WANG H, ZHANG Y, LI H. A silver-palladium alloy nanoparticle-based electrochemical biosensor for simultaneous detection of ractopamine, clenbuterol and salbutamol[J]. Biosens Bioelectron, 2013,49:14-19.
[9] 张爱菊,戴兴德,张小林.碘-淀粉显色液褪色光度法测定药剂中的维生素C[J].理化检验-化学分册, 2016,52(3):339-341.
