正交试验优化头孢噻肟钠原料药有关物质检查中溶液制备条件
2018-01-18张涛豆东海杨鹏波安阳市食品药品检验检测中心河南安阳455000河南康达制药有限公司河南周口46600
张涛,豆东海,杨鹏波(.安阳市食品药品检验检测中心,河南安阳455000;.河南康达制药有限公司,河南周口 46600)
头孢噻肟钠属于第三代头孢菌素类衍生物,对革兰氏阴性菌的抗菌活性高于第一代和第二代,因其耐酶和广谱的特点而在临床上广泛使用[1],其质量标准收载于2015年版《中国药典》(二部)[2]。笔者依照《中国药典》检验标准对头孢噻肟钠原料药进行质量分析时,发现有关物质检查重复性较差,结果不稳定。笔者参考相关文献[3-6],发现放置时间、放置温度、磷酸盐缓冲液pH、光照这4个因素均对溶液稳定性有较大影响,单因素考察试验显示随着供试品溶液放置时间增加、试验温度提高、磷酸盐缓冲液pH增加、光照强度增加这些因素的改变,头孢噻肟钠原料药杂质总量会变化;但未见有综合上述4个因素进行影响分析的报道。鉴于此,笔者采用单因素和正交试验法,以该原料药中的杂质总量为指标,优化有关物质检查中溶液的制备条件,以期为完善该原料药有关物质检查方法提供参考。
1 材料
1.1 仪器
LC-2030C型高效液相色谱(HPLC)仪,包括自动进样器、柱温箱、紫外检测器(日本Shimadzu公司);MS105DU型电子分析天平(瑞士Mettler-Toledo公司);HYC-390 2~8℃海尔医用冷藏箱(青岛海尔公司);Labonce-380GS 4~65℃恒温箱(北京兰贝石恒温技术有限公司);Milli-Q Advantage A10型超纯水仪(美国Millipore公司)。
1.2 药品与试剂
头孢噻肟钠原料药(河南某制药厂,批号:201160701、201160702、201160703);头孢噻肟系统适用性对照品(中国食品药品检定研究院,批号:130619-201402);甲醇为色谱纯,其余试剂均为分析纯,水为实验室纯化水。
2 方法与结果
2.1 头孢噻肟钠有关物质检查
2.1.1 色谱条件的确定 色谱柱:Hypersil ODS2(200 mm×4.6 mm,5 μm);流动相:流动相A为0.05 mol/L磷酸盐缓冲液(取7.1 g无水磷酸氢二钠至1 000 mL量瓶中,加水溶解并稀释至刻度,用磷酸调节pH为6.50)-甲醇(86∶14,V/V),流动相B为0.05 mol/L磷酸盐缓冲液(用磷酸调节pH为6.50)-甲醇(60∶40,V/V);进样时,均先以流动相A-B(95∶5,V/V)等度洗脱,待头孢噻肟峰洗脱完毕后再进行梯度洗脱(梯度洗脱程序:0~2 min,95%→75%A;3~8 min,75%A;9~23 min,75%→0 A;24~28 min,0 A;29~33 min,0→95%A;34~43 min,95%A);检测波长:235 nm;柱温:5 ℃;进样量:10 μL。
2.1.2 溶液的制备 ①供试品溶液。取样品原料药25.10 mg,置于25 mL棕色量瓶中,用置于冰箱中降温到5℃的流动相A为溶剂进行溶解并定容。溶解过程中,应避光操作,供试品溶液温度应尽量保持5℃。②系统适用性对照品溶液。取头孢噻肟系统适用性对照品25.14 mg,置于25 mL棕色量瓶中,用置于冰箱中降温到5℃的流动相A为溶剂进行溶解并定容,即得。③空白溶液。取空白溶剂适量为空白溶液。
2.1.3 系统适用性试验 取“2.1.2”项下溶液各适量,按上述色谱条件进样分析,结果主峰与各杂质峰、各杂质峰间均能达到基线分离,分离度均>1.5,色谱见图1。
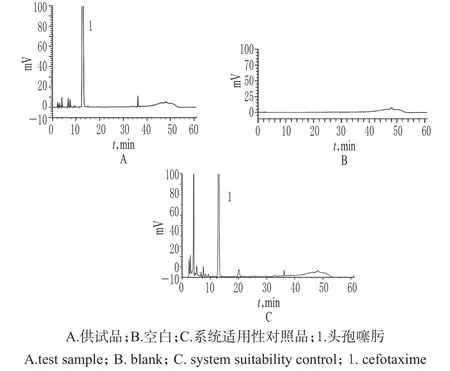
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.2 单因素试验
2.2.1 放置时间 取“2.1.2”项下供试品溶液(批号:201160701)适量,分别于放置5、30 、60、120 、240 min时按“2.1.1”项下色谱条件进样测定,放置时间与杂质总量的关系见图2。由图2可知,杂质总量随着时间的递增呈上升趋势,但在60 min后杂质总量增加变平缓,所以取5、30、60 min为考察因素。
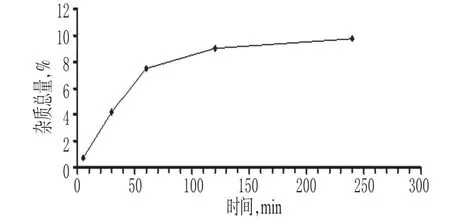
图2 放置时间Fig 2 Standing time
2.2.2 放置温度 取“2.1.2”项下供试品溶液(批号:201160701)适量,分别放置于5、15、25、35、45 ℃环境中,各按“2.1.1”项下色谱条件进样测定,放置温度与杂质总量的关系见图3。由图3可知,杂质总量随着放置温度的增加呈上升趋势,但在35℃以后杂质总量增加变平缓,所以取5、15、30℃为考察因素。

图3 放置温度Fig 3 Placing temperature
2.2.3 磷酸盐缓冲液pH 精密称取样品原料药(批号:201160701)适量,按2015年《中国药典》(二部)[2]现行质量标准有关物质检查项操作制成单因素试验溶液,流动相A为0.05 mol/L磷酸盐缓冲液(取7.1 g无水磷酸氢二钠至1 000 mL量瓶中,加水溶解并稀释至刻度,用磷酸分别调节pH为6.0、6.25、6.5、7.0、7.25)-甲醇(86∶14,V/V);流动相B为0.05 mol/L磷酸盐缓冲液(用磷酸分别调节 pH 为 6.00、6.25、6.50、7.00、7.25)-甲醇(60∶40,V/V),供试品溶液中磷酸盐缓冲液的pH也相应变化;检测波长:235 nm;试验环境及样品温度:25℃;进样量:10 μL。并按“2.1.1”项下梯度洗脱程序进行梯度洗脱,按上述条件测定杂质总量,结果见图4。由图4可知,当磷酸盐缓冲液pH为6.00~7.25时,杂质总量降低,但考虑到甲醇也呈碱性,所以流动相A和B混合后流动相pH会接近8,达到了常规色谱柱的高限,所以取pH为6.0、6.25、6.5为考察因素。
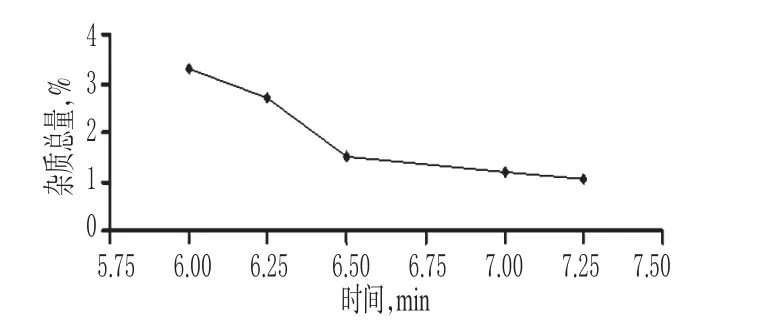
图4 磷酸盐缓冲液pHFig 4 pH value of phosphate buffer solution
2.2.4 光照条件 分别在避光环境下(1)、棕色量瓶(2)、正常环境(3)下,按“2.1.2”项下供试品溶液制备方法制备供试品溶液(批号:201160701),再按“2.1.1”项下色谱条件进样测定,光照条件与杂质总量的关系见图5。由图5可知,杂质总量随着光照强度的增强呈上升趋势。所以取避光环境、棕色量瓶、正常环境为考察因素。
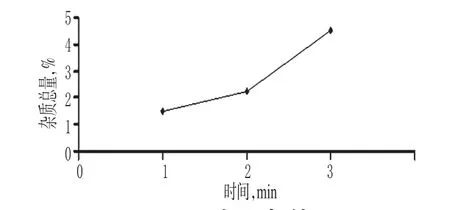
图5 光照条件Fig 5 Illumination condition
2.3 正交试验
2.3.1 正交试验设计 在单因素试验的基础上,以头孢噻肟钠含量(%)为指标,对磷酸盐缓冲液pH(A)、放置温度(环境温度及溶液制备时温度)(B)、供试品溶液从制备完成到进样前的放置时间(C)以及光照条件(D)4个因素进行考察,各因素均取3个水平(见表1),L(934)正交试验设计与结果见表2(表中杂质总峰面积=总峰面积-主峰面积);方差分析结果见表3。
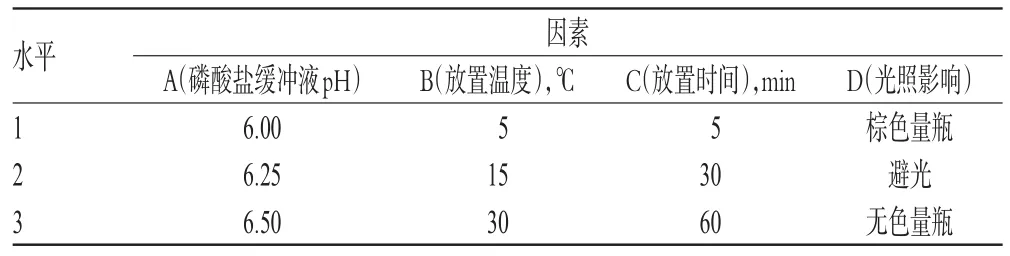
表1 正交实验因素与水平Tab 1 Factors and levels of orthogonal test
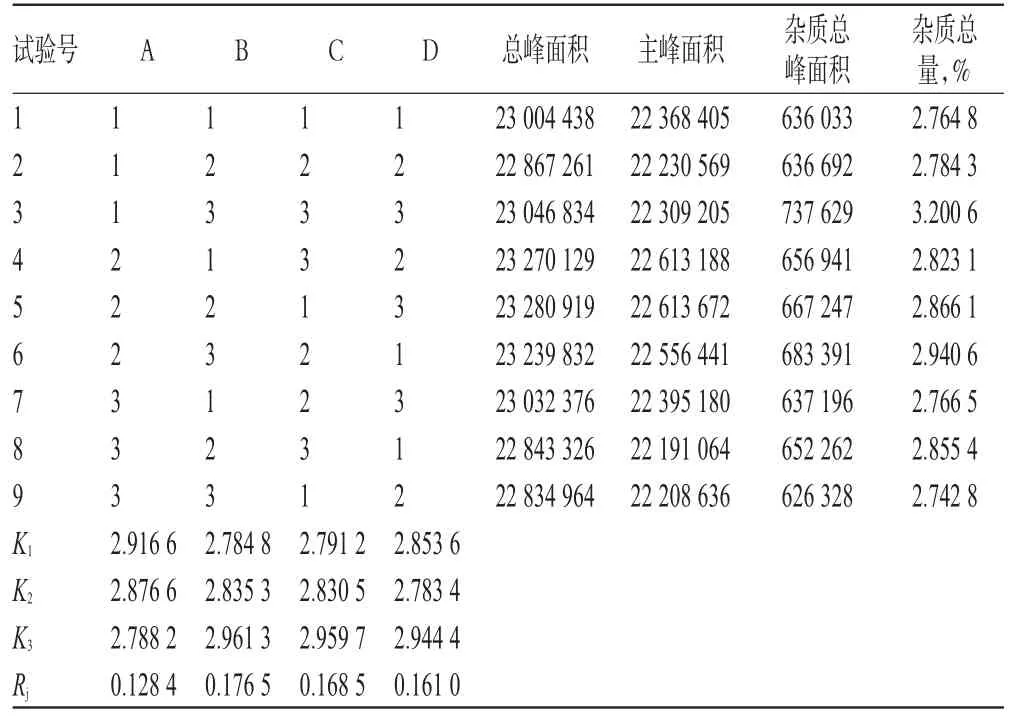
表2 正交试验设计与结果Tab 2 Design and results of orthogonal test
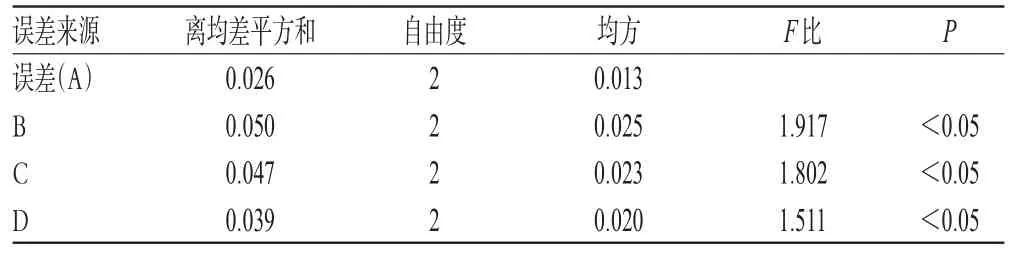
表3 方差分析结果Tab 3 Variance analysis results
2.3.2 数据处理 由表2可知,影响因素主次顺序为B>C>D>A,各因素水平较优的搭配是A3B1C1D2,即供试品溶液制备时溶液温度为5℃时(HPLC仪带柱温箱和放置温度取同样水平),5 min内进样,试验过程避光操作,磷酸盐缓冲液的pH为6.50。
2.3.3 验证试验 取3批样品适量,按2015年《中国药典》(二部)的方法和本文优化的方法进行试验,结果见表4。由表4可知,正交试验结果可靠。
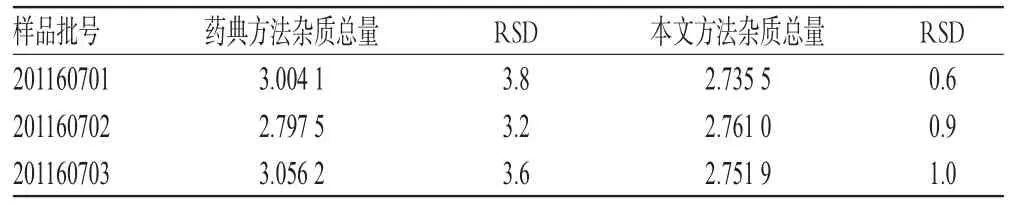
表4 样品有关物质测定结果(n=3,%)Tab 4 Results of the relevant substances in the sample(n=3,%)
3 讨论
3.1 评价指标的选择
温度、湿度、日光、空气等外界条件会引起药物发生水解、氧化、分解、异构化等变化,使药物产生有关物质[6],导致主成分含量降低而杂质总量增加,因此可以以杂质总量[即杂质总峰面积/总峰面积(%)]为评价指标优选头孢噻肟钠有关物质检查中的溶液制备条件。
3.2 有关物质对照品
我国头孢噻肟钠现行质量标准有关物质检查是不加校正因子的自身对照法,且我国只发行了头孢噻肟对照品和头孢噻肟系统适用性对照品(混合有关物质对照品和主成分对照品),未对头孢噻肟钠原料药及分析中可能存在的单个有关物质进行结构确证,有关物质检查以有关物质峰面积及杂质总峰面积和头孢噻肟主峰面积进行比较。
3.3 方法学说明
由于没有单一有关物质对照品,在本研究优化过程中未作单一有关物质的含量测定及线性考察。还因本试验对头孢噻肟钠有关物质的稳定性进行了单因素考察,数据表明随试验时间变化,稳定性有所改变,所以在本研究优化过程中未再对稳定性进行考察。
3.4 其他
本试验在模拟光照因素时使用的是玻璃量瓶,紫外线不能穿透玻璃容器,没有完全模拟纯紫外线影响。在质量分析工作中,应尽量避免称量、过滤等步骤中样品完全暴露在日光下,以免紫外线影响。
综上所述,优化后的方法重复性好,结果可靠。
[1]张海涛.头孢噻肟钠结晶技术研究[D].天津:天津大学,2008.
[2]国家药典委员会.中华人民共和国药典:二部[S].2015年版.北京:中国医药科技出版社,2015:286-297.
[3]刘海燕,蒋红霞.关于《中国药典》中注射用头孢噻肟钠含量测定方法的讨论[J].数理医药学杂志,2010,23(5):594.
[4]朱建平,高燕霞,梁立革,等.关于头孢噻肟钠测定方法的商榷[J].中国药事,2005,19(1):40-41.
[5]于力.抗生素头孢噻肟钠的杂质研究[D].济南:山东大学,2004.
[6]Lerner DA,Bonnefond G,Fabre H,et al.Photodegradation paths of cefotaxime[J].J Pharm Sci,1988,77(8):699-703.
