正负极电解液对钒电池能量衰减的影响研究
2018-01-17李君涛史小虎余龙海
李君涛,史小虎,余龙海,彭 穗
(1.大力电工襄阳股份有限公司,湖北襄阳441057;2.攀钢集团研究院有限公司,四川成都610303)
全钒氧化还原液流电池具有能量转换效率高、容量可调节、使用寿命长、安全性高和环境友好等优点,主要用于太阳能、风能等可再生能源的发电系统配套储能设备、电网的调峰填谷装置、不间断电源和应急电源系统[1]。
全钒液流电池在充电时,将电能转化为化学能储存在不同价态的钒离子中,正极VO2+氧化为VO2+,负极中V3+还原为V2+;放电时将化学能转化成电能,正极VO2+转化为VO2+,负极中V2+转化为V3+[2],钒离子浓度越高,比能量越大[3]。
全钒液流电池正负极初始电解液一般分为两种:一种是以硫酸氧钒的硫酸水溶液为初始电解液,由于初始钒价态为四价,为使正负极在充电过程中达到电荷的匹配,在正负极钒浓度相同的前提下,正极电解液体积为负极电解液体积的2倍[4];另外一种则是以三价钒与四价钒浓度比1∶1的硫酸水溶液为初始液,此时正负极钒浓度及电解液的体积均相同[5]。
一般情况下,全钒液流电池正负极初始电解液是同一种,即钒离子的价态、浓度、硫酸浓度均相同。但是,随着电池系统充放电循环的进行,电解液中钒离子和水可能透过离子传导膜由电极一侧向另一侧迁移,导致正负极电解液的体积、钒离子浓度、硫酸根浓度发生变化,从而使电池容量发生衰减[6]。
电池在循环运行过程中,电解液中的水从负极迁移到正极,本文设置负极电解液的体积大于正极电解液的体积,使得电解液从负极向正极的迁移得到改善,进而改善循环过程中电池的容量衰减。
以下三组钒电池进行充放电实验:正负极同体积、钒浓度均为1.7 mol/L、硫酸根浓度均为4.5 mol/L(以下简称对称实验);正极电解液与负极电解液的总钒量相同,正极电解液钒浓度为1.7 mol/L、硫酸根浓度为4.5 mol/L,负极电解液钒浓度为1.55 mol/L、硫酸根浓度为4.1 mol/L(以下简称不对称Ⅰ);正极电解液与负极电解液的总钒量相同,正极电解液钒浓度为1.7 mol/L、硫酸根浓度为4.5 mol/L,负极电解液钒浓度为1.55 mol/L、硫酸根浓度为4.7 mol/L(以下简称不对称Ⅱ)。考察三组电池的衰减率及能量效率,并通过测试正极电解液钒离子的浓度,考察三组电池钒离子的迁移情况。实验表明负极电解液在较高的硫酸浓度和较低的钒浓度下,钒离子迁移量较小,电池的容量衰减较小,能量效率也较高。
本文分别对钒浓度1.7 mol/L、硫酸根浓度4.5 mol/L的电解液,钒浓度1.55 mol/L、硫酸根浓度4.1 mol/L的电解液,以及钒浓度1.55 mol/L、硫酸根浓度4.7 mol/L的电解液进行循环伏安测试,考察了不同钒浓度及硫酸浓度配比下电解液的氧化还原可逆性。实验表明在较低的硫酸浓度下,电解液的氧化还原可逆性降低。
1 实验
1.1 电解液制备装置及充放电测试系统
电解液制备装置如图1所示,电解液充放电测试系统如图2所示。

图1 电解装置
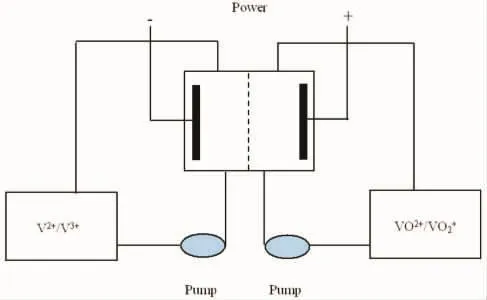
图2 钒电池系统
1.2 实验仪器
实验所用仪器与试剂:电池充放电测试仪,CT-3008W-10V10A-NA(深圳新威尔);恒温恒湿实验箱,JK-K-500Z(上海江凯机械);电化学工作站,CHI660C(上海辰华);紫外分光光度计,UV/VIS-4802(上海尤尼科)。
1.3 电解液制备
配置浓度4.5 mol/L的硫酸溶液4 000 mL,装入图1所示的电解槽阳极室和阴极室各2 000 mL,并在电解槽的阴极室一侧加入V2O5粉末。利用电解助溶,随着V2O5的溶解,不断补充V2O5粉末,直到不再溶解为止,控制电解时间,分别得到溶液中三价钒与四价钒比例为1∶1(平均价态3.5),总钒浓度为1.7 mol/L的电解液2 000 mL。采用紫外分光光度计对制备的电解液进行钒价态及浓度测试。
取出制备好的钒浓度为1.7 mol/L、硫酸浓度为4.5 mol/L的电解液400 mL,分别调节钒浓度为1.55 mol/L、硫酸根浓度为4.1 mol/L的电解液200 mL,和钒浓度为1.55 mol/L、硫酸根浓度为4.7 mol/L的电解液200 mL。
1.4 循环伏安测试
采用光谱纯石墨电极做工作电极,铂电极为辅助电极,选取饱和甘汞电极为参比电极,分别对三、四价钒比例为1∶1、钒浓度为1.7 mol/L、硫酸根浓度为4.5 mol/L的电解液,钒浓度为1.55 mol/L、硫酸根浓度为4.1 mol/L的电解液,和钒浓度为1.55 mol/L、硫酸根浓度为4.7 mol/L的电解液进行循环伏安测试。
1.5 电池性能测试
利用图2所示的钒电池系统,分别对正负极同体积、钒浓度均为1.7 mol/L、硫酸根浓度均为4.5 mol/L(对称实验);正极电解液与负极电解液的总钒量相同,正极电解液钒浓度为1.7 mol/L、硫酸根浓度为4.5 mol/L,负极电解液钒浓度为1.55 mol/L、硫酸根浓度为4.1 mol/L(不对称Ⅰ);正极电解液与负极电解液的总钒量相同,正极电解液钒浓度为1.7 mol/L、硫酸根浓度为4.5 mol/L,负极电解液钒浓度为1.55 mol/L、硫酸根浓度为4.7 mol/L(不对称Ⅱ)的三组钒电池进行充放电实验,考察三组电池的衰减率及能量效率。
2 结果与讨论
2.1 电解液制备
V2O5在4.5 mol/L的硫酸中电解,发生以下反应:

通过上述化学反应可得到含有三价和四价钒离子的硫酸溶液。
将三、四价钒比例为1∶1的电解液,加入到电池中进行充电电解,发生以下反应:

通过上述化学反应可得到含有二价和五价钒离子的硫酸溶液。
2.2 循环伏安测试
为了考察不同钒离子浓度和不同硫酸浓度电解液对电极反应的影响,对3种不同钒离子和硫酸根浓度的溶液做了循环伏安实验,结果如图3所示。扫描电压相对饱和甘汞电极为-1.0~+1.5 V,扫描速率是50 mV/s。
图3中的1、2、3号曲线分别对应钒浓度1.7 mol/L、硫酸根浓度4.5 mol/L的电解液,钒浓度1.55 mol/L、硫酸根浓度4.1 mol/L的电解液,和钒浓度1.55 mol/L、硫酸根浓度4.7 mol/L的电解液,通过对峰电流和峰电压的观察可以看出,2号电解液峰电流较小,说明其钒氧化还原可逆性比其他两组电解液差。
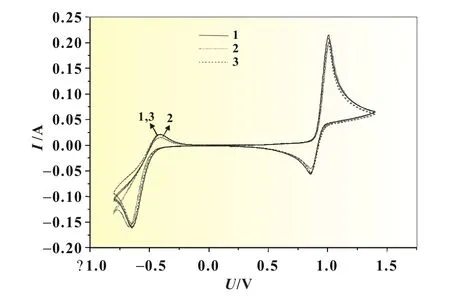
图3 三种电解液的循环伏安曲线
2.3 电池充放电测试
将三组不同电池进行充放电测试,考察电池的基本性能,测试结果见表1。可以看出,采用不对称Ⅱ的模式,电池的能量效率较高,而且电池的衰减降低。
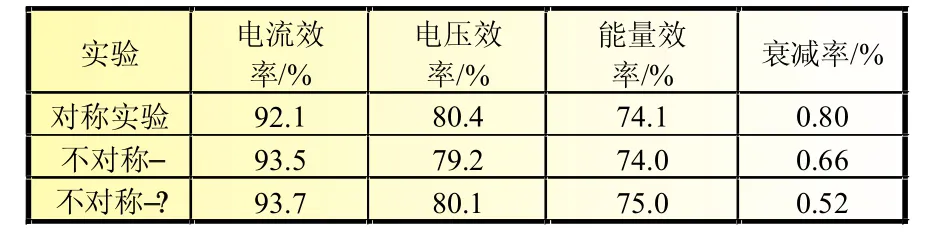
表1 正、负极电解液不同的三组电池充放电实验结果
2.4 钒离子迁移量的测试
对三组电池进行充放电测试,分别选取第10、50和第100次循环,对每组电池的正极电解液取样,检测钒离子的含量,考察三组电池钒离子的迁移量,测试结果如表2所示。
从表2的数据可以看出,随着电池充放电次数的增加,负极电解液钒离子通过隔膜,不断渗透到正极电解液中。降低负极电解液初始钒离子浓度,增加负极电解液体积,可以有效减缓钒离子的渗透,其中,加大负极电解液硫酸浓度、降低负极钒离子浓度,钒离子渗透量降低明显。
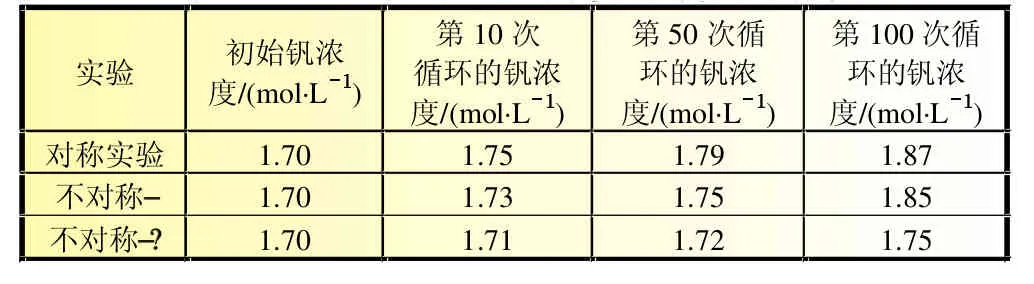
表2 三组电池正极钒离子浓度测试结果
3 结论
本文设置负极电解液的体积大于正极电解液的体积,使电解液从负极向正极的迁移得到改善,进而改善循环过程中电池的容量衰减。通过对三组电池的充放电实验可以看出,负极电解液在降低钒离子浓度的同时,稍微提升电解液的硫酸含量,可以增加负极液渗透压,从而减小钒离子和水分子迁移、降低电池容量衰减。
通过对三组不同钒离子浓度和硫酸浓度的电解液进行循环伏安测试,可以得出较低的硫酸含量会降低电解液中钒离子的氧化还原可逆性,从而降低电池的电压效率和能量效率。
[1]朱厚军,郎俊山.全钒液流电池研究进展[J].船电技术,2012,32(6):5-8.
[2]范永生,陈晓,徐冬清,等.全钒液流电池荷电状态检测方法研究[J].华南师范大学学报,2009(11):112-114.
[3]罗冬梅,许茜,隋智通.添加剂对钒电池电解液性能的影响[J].电源技术,2004(2):94-96.
[4]彭声谦,许国镇,杨华铨,等.从石煤中提取的V2O5研制全钒氧化还原液流电池[J].矿产综合利用,1998(2):42-45.
[5]陈孝娥,崔旭梅,王军.V(Ⅲ)-V(Ⅳ)电解液的化学合成及性能[J].化工进展,2012,31(6):1330-1332.
[6]KNEHR K W,KUMBUR E C.Role of convection and related effects on species crossover and capacity loss in vanadium redox flow batteries[J].Electrochemistry Communications,2012,23:76-79.
