自供电植入式神经电刺激器的制作与应用
2018-01-10赵婷婷党永辉刘红忠西安交通大学第一附属医院神经内科陕西西安7006机械制造系统国家重点实验室陕西西安70049医学部法医学院陕西西安7006
贾 蕊,赵婷婷,刘 鹏,党永辉,刘红忠(西安交通大学:. 第一附属医院神经内科,陕西西安 7006;. 机械制造系统国家重点实验室,陕西西安 70049;. 医学部法医学院,陕西西安 7006)
自供电植入式神经电刺激器的制作与应用
贾 蕊1,赵婷婷2,刘 鹏3,党永辉3,刘红忠2
(西安交通大学:1. 第一附属医院神经内科,陕西西安 710061;2. 机械制造系统国家重点实验室,陕西西安 710049;3. 医学部法医学院,陕西西安 710061)
目的探讨一种自供电植入式神经刺激器的可行性。方法基于热释电效应和红外光的穿透性,构建一种植入式神经刺激器,测试其在体外红外光驱动下的电学性能;并进行体内和体外的生物实验,观察电刺激下的蛙腓肠肌的电刺激响应,以及小鼠心脏的电刺激响应。结果构建的植入式神经刺激器在红外光的间歇照射下会产生可控的神经电刺激信号,输出的神经电刺激电压可达到1.2 V;用该神经电刺激器分别直接刺激小鼠心脏和蛙腓肠肌,可见小鼠心电图的变化,蛙腓肠肌会发生明显收缩,且张力值随体外控制光强度的增大而增大;在体外控制光的驱动下,植入蛙皮下的该神经电刺激器能有效刺激蛙的腓肠肌,使之发生可控收缩。结论体外光驱动的植入式神经电刺激器可以实现电刺激器的自供电,且电刺激幅值、波形可随光照强度和频率可调,为植入式设备的供电提供了解决方案。
植入式刺激器;红外光;热释电;自供电;电刺激响应
植入式电子设备相比较传统的便携式医疗器械在外型和使用上更为灵巧,方便,不仅能够实时监测健康状况[1],甚至可以替代某些功能衰竭的器官[2]。然而,人体植入式电子设备同样面临着许多问题,其中如何提供一个可靠、高效的能量供给单元一直是其研究的关键与难点[3]。目前有三类主要的能量供给方式:电池,非接触能量传输以及基于能量采集技术的供电方式。电池具有安全可靠和高能量密度的优势,但始终存在寿命有限的缺点[4]。经表皮非接触能量传输[5]解决了电池电能耗尽后需手术更换的问题,但是电源所使用的材料一般为金属,满足不了柔性的需求,而且会导致患者无法进行一些医疗检测。基于能量采集技术的供电方式是将人体或外界环境中的能量,如人体的运动、肌肉的伸缩、血管的收缩与舒张等机械能、声波或超声波等震动能直接转换成电能给植入式器件供电[6-7]。由于其供电方式的灵活性,基于能量采集技术的新型供电方式为研究者们提供了一个新的思路。
光能不仅可以实现能量远程操控,且具有低噪声、无复杂电路等很多优点。红外光具有热效应且穿透能力较强,短波红外线(波长1.5 μm以内)透入组织最深,可达10 mm,能直接作用到皮肤的血管、淋巴管、神经末梢及其他皮下组织[8-10]。对于具有自发极化的材料,当材料受热或冷却,由于温度变化而导致其自发极化强度随之改变,从而在材料表面上会产生电荷,该现象称为热释电效应[11]。人们常利用热释电效应将变化的温度转化成电能来使用。我们设想利用红外光作为激励源,结合热释电效应,提出一种红外驱动的自供电植入式刺激器的方案,实现植入式设备的能量自供,这对于植入式医疗设备的能量供应具有重要意义。
1 材料与方法
1.1热释电型植入式刺激器的设计和制备依据热释电原理,本文设计了如图1所示的热释电型刺激器,采用红外光源作为体外能量源,利用快门控制红外光的光照频率,为体内热释电单元提供一个变化的温度场,从而产生电信号。该热释电单元是由功能材料-聚偏二氟乙烯(PVDF)和电极材料-石墨烯组成的。PVDF是一种质轻、成本低、具有良好柔性和生物兼容性的热释电材料[12],且对红外光具有较强的吸收率[13]。石墨烯是一种具有高导电和高导热系数[15]的电极材料,同时它对红外光具有高透过率[14],使用石墨烯作为电极材料可提高功能层对红外光的吸收,本文使用的是用化学气相沉积法在铜箔上生长的单层石墨烯。首先在石墨烯上旋涂一层2%的PMMA溶液,烘干后将铜箔漂浮在0.5 mol/L的三氯化铁溶液上,待铜箔被完全腐蚀,用载玻片将石墨烯捞起放入去离子水中清洗,最后用PVDF薄膜一面将石墨烯捞起,重复上述过程使PVDF薄膜的另一面也转移上石墨烯,最后用导电银浆将铜导线固定于上下石墨烯电极上,引出正负电极线,完成热释电单元的制备。
图1基于红外驱动的热释电型刺激器原理图
Fig.1 The schematic diagram of pyroelectric stimulator manipulated by infrared ray
1.2热释电型刺激器的性能测试热释电型刺激器的性能测试所用到的仪器有:红外光源;示波器(Tektronix DPO 3034);电流放大器(SR570);红外热成像仪(SC7300M)。测试刺激器在红外光源间歇照射下器件的电学性能和温度变化。
1.3生物实验验证本研究在严格遵守西安交通大学医学伦理委员会要求的条件下完成。分别进行了体外和体内的动物实验来验证该热释电型器件在功能性电刺激上的应用。首先进行蛙坐骨神经-腓肠肌的电刺激实验,将刺激器引出的两根电极线与坐骨神经连接,采用不同光照强度的红外光照射刺激器时,观察腓肠肌的收缩和张力值变化。为了验证红外驱动的热释电器件作为植入式电子器件的可行性,进行了体内实验,捣毁蛙的脑和脊髓,使后肢的坐骨神经暴露,剪开蛙的表皮,将用聚二甲基硅氧烷(PDMS)封装好的刺激器(封装的作用是避免体液导致上下电极导通)放入皮下,并使刺激器的两根电极通过皮下连接到后肢的坐骨神经上。将蛙的表皮缝合。直接用红外光照射蛙体,观察后肢的运动。另外,我们利用该刺激器刺激小鼠的心肌,首先将小鼠用1%的水合氯醛麻醉,固定在手术台上。四肢皮下插入心电图导联线,记录正常标准肢体导联心电图。然后将小鼠心脏暴露,使植入皮下的刺激器的电极与心脏相连接。观察光照下小鼠心电图的变化。
2 结 果
2.1热释电型刺激器的性能表征热释电型刺激器面积为25 mm×25 mm,厚度30 μm,如图2A、B所示该器件在光强密度3 W/cm2,光照频率0.125 Hz的红外光下产生的热释电信号,可产生600 mV的开路电压和6 nA的短路电流。采用红外热成像仪测量器件的温度变化,如图2C所示,器件的温度在红外光照瞬间会从16.4 ℃升高到20.9 ℃,光照停止,温度会降到17.1 ℃,最大温升为5.3 ℃。

图2电刺激器在红外光照射下的电压信号(A)电流信号(B)和温度变化(C)
Fig.2 The voltage signal (A), the current signal (B) and the temperature (C) of pyroelectric stimulator under illumination of infrared ray
如图3A所示,刺激器的输出电压与红外光的光强密度成正比,当光强密度达到5 W/cm2时,输出的电压幅值能达到1.2 V。根据热释电理论,热释电电流I与受热的电极面积A、材料的热释放系数p以及温度的变化率dT/dt有关,Q是产生的自由电荷[15]。
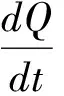
(1)
从公式(1)中可以看出当电极面积和材料一定时,产生的热释电电流和温度变化率成正比。当热释电材料暴露在能量密度为W(J s-1m-2)的辐射下一段时间Δt后,材料吸收辐射会导致一定的温升ΔT(K),假设材料吸收辐射后的热量在材料内部迅速传导,且忽略温升过程的散热,从而使得材料整体温升均一,可以得到公式(2)[16],

(2)
CE是材料的比热容(J m-3K-1),δ是材料的厚度(m)。公式(2)对时间求导可以得到材料在辐射下的温度变化率,如公式(3):

(3)
由公式(1)和(3)可以得到:

(4)
从公式(4)可以看出产生的电流和辐射强度成正比。因此器件的输出电压随红外光的光强密度可调。另外,当非光照时间固定(6 s),改变不同的光照时间会输出如图3B的电压波形。从图中可见,当非光照时间一定时,不同光照时间下输出的电压值是相同的,时间越短,脉宽越窄。当光照时间为0.1 s时,输出电压的脉宽大概为500 ms。但是光照时间越长,降温过程中产生的负电压会越大,由于非光照时间一致,所以非光照期间的波形一致。根据零维不稳定导热微分方程,红外光关闭时的温度变化率为:

(5)
h是对流换热系数(W m-2K-1),其中:

(6)
由公式(5)和(6)可以得到:

(7)
从公式(7)中可以看出,非光照时的温度变化率与光照时间Δt成正比,因此光照时间越长,非光照时的电压值越大。波形的可调控对神经刺激而言非常重要,因为不同神经纤维的兴奋性存在差异,所以对电刺激的强度和脉宽等要求也不同。

图3红外光照强度与输出电压的关系(A)及不同光照时间下的电压波形(B)
Fig.3 The relationship between power intensity of infrared ray and output voltage (A) and the voltage waveform under different irradiation period (B)
由于刺激器只会在治疗的时间段内使用,并不会一直开启,所以只需要满足使用过程中电量的稳定性即可。如图4所示为热释电器件连续工作1 h的电压输出结果,可见器件连续工作1 h输出的电压基本没有变化,因此证明了该刺激器输出电量具有一定的稳定性。

图4热释电器件连续工作1h的电压输出
Fig.4 The output voltage of pyroelectric stimulator during 1 h
2.2蛙的腓肠肌刺激实验结果为了验证提出的热释电型刺激器在植入式医疗应用中的可行性,我们进行了蛙的腓肠肌电刺激实验。对于蛙的腓肠肌,当输入的电压超过其动作电位的阈值,腓肠肌即会发生收缩[17]。
首先利用生物信号采集与处理系统标定出制备的坐骨神经腓肠肌标本的刺激阈值,刺激方式为单刺激,刺激强度从10 mV开始,逐渐增加刺激强度。可观察到该坐骨神经腓肠肌标本的刺激阈值为290 mV,最适刺激强度为390 mV。使用红外光强为2 W/cm2的红外光间歇照射刺激器时,能达到300 mV的输出电压,可见腓肠肌明显收缩,张力值随之改变。从图3A中可见刺激器的输出电压随红外光强可调,当红外光强达到2.5 W/cm2时,输出电压接近390 mV,达到腓肠肌的最适刺激强度。之后再增加光照强度,张力值也不会发生变化了。因此,通过调控红外光强来改变刺激器输出电压的大小,可得到不同刺激强度下的张力值变化,如图5所示。
2.3植入式实验验证为了进一步验证红外驱动植入体内刺激器的可行性,我们进行了蛙的皮下植入实验,把刺激器植入到蛙的皮下,并使引出的双电极经由皮下连接到左后肢的坐骨神经上。用红外光照蛙体,可见左后肢明显收缩运动。如图6所示,左后肢收缩运动后可见α2明显大于α1。但是,目前PVDF和石墨烯尚不属于可靠的生物植入材料,其在体内的安全性还有待进一步验证。

图5不同光照强度下的张力图
Fig.5 Tension profile during stimulation by controllable power intensity of infrared ray

图6刺激器植入蛙皮下后的红外刺激
Fig.6 The device was implanted subcutaneously in frog
2.4小鼠的心肌刺激实验结果热释电型刺激器在红外光照下输出的电压还可以直接刺激小鼠心肌,如图7所示。首先记录小鼠正常的心电图,如图7B蓝色结果所示。将刺激器的电极直接插入被麻醉小鼠的心脏,光照下观察小鼠的心电图,如图7B中黑色结果所示。小鼠的心电图上呈现出频率与光照频率相同的波形,说明该刺激器输出的电能可以影响小鼠的心电功能。
3 讨 论
针对植入式医疗设备供电系统存在的问题,本文提出采用对人体有益的近红外光作为激励,基于热释电原理,制作热释电型植入式刺激器,为植入式医疗设备提供能量。

图7小鼠心肌刺激照片(A)及小鼠正常的心电图(蓝色)和光照刺激下的心电图(黑色)(B)
Fig.7 The heart stimulation on a live rat (A) and the normal ECG and the recorded real-time ECG in a live rat during heart stimulation by electrical pulse generated by the battery-less device (B)
采用红外光作为激励源,与电/热驱动相比,光驱动可以实现无线驱动,低噪声、无复杂电路等很多优点。红外光具有热效应且穿透能力较强。所以采用红外光作为远程能量操控的激励源,可用于植入式医疗设备。
红外光操控的热释电型器件依据红外间歇光照提供的温度变化产生电能,这不同于其他的能量转换装置,它无运动部件,因此减少了如压电器件在不断运动后产生的疲劳,提高了耐受性。所使用的PVDF和石墨烯材料柔性好,可与生物组织随型,更适合用于植入式设备。热释电型器件的输出幅值随红外光强度可调,提高了可控性。
本文对提出的红外光操控的热释电型刺激器进行了生物实验验证,输出的电压可对小鼠心肌和蛙的坐骨神经腓肠肌进行刺激,且通过调控红外光照强度,可使腓肠肌获得不同程度的收缩。最后进行了初步的植入实验,验证了刺激器植入的可能性。但是所使用材料目前尚不属于可靠的生物植入材料,其在体内的安全性还有待进一步验证。
[1] FAMM K, LITT B, TRACEY K J, et al. A jump-start forelectroceuticals[J].Nature, 2013, 496(7444):159-161.
[2] REARDON S. Electroceuticals spark interest[J]. Nature, 2014, 511(7507):18.
[3] WEI XJ, LIU J. Power sources and electrical recharging strategies for implantable medical devices[J]. Front Energy Power Eng China, 2008, 2(1):1-13.
[4] DAGDEVIREN C, YANYB D, SU Y, et al.Conformal piezoelectric energy harvesting and storagefrom motions of the heart, lung, and diaphragm[J]. Proc Natl Acad Sci USA, 2014,111(5):1927-1932.
[5] NEIHARTN M, HARRISON RR. Micropower circuits for bidirectional wireless telemetry in neural recording applications[J]. IEEE Trans Biomed Eng, 2005, 52(11):1950-1959.
[6] DIAO LW, ZHENG J, PAN XD, et al. Application of piezoelectric nanogenerator in medicine: Bio-experiment and theoretical exploration[J]. J Thora Dis, 2014, 6(9):1300-1306.
[7] KARAMI MA, INMAN DJ. Powering pacemakers from heartbeat vibrations using linear and nonlinear energy harvesters[J]. Appl Phys Lett, 2012, 100(4):042901(1-4).
[8] CUI S S, YIN D Y, CHEN YQ, et al.Invivotargeted deep-tissue photodynamic therapy basedon near-infrared light triggered upconversion nanoconstruct[J]. Acs Nano, 2013, 7(1):676-688.
[9] VINCH E, CAGNIE B, COOREVITS P, et al. Pain reduction by infrared light-emitting diode irradiation: A pilotstudy on experimentally induced delayed-onset muscle sorenessin humans[J]. Lasers Med Sci, 2006, 21(1):11-18.
[10] WEISSLEDER R. A clearer vision forinvivoimaging[J]. Nat Biotech, 2001, 19(4):316-317.
[11] LANGS B. Pyroelectricity: From ancient curiosity to modern imaging tool[J].Physics Today, 2005, 58(8):31-36.
[12] ZABEK D, TAYLOR J, BOULBAR E L, et al. Micropatterning of flexible and free standing polyvinylidene difluoride (PVDF) films for enhanced pyroelectric energy transformation[J]. Adv Energy Mater, 2015, 5(8).
[13] KULKARNI ES, HEUSSLER SP, STIER AV, et al. Exploiting the IR transparency of graphene for fast pyroelectric infrared detection[J]. Adv Optical Mater, 2015, 3(1):34-38.
[14] CHOI D, CHOI MY, CHOI WM, et al. Fully rollable transparent nanogenerators based on graphene electrodes[J]. Adv Mater, 2010, 22(19):2187-2192.
[15] WHATMORE RW, Pyroelectric devices and materials[J]. Rep Prog Phys, 1986,49(12):1335.
[16] BOWEN CR, TAYLOR J, BOULBAR EL, et al. A modified figure of merit for pyroelectric energy harvesting[J]. Mater Lett, 2015, 138:243-246.
[17] GU L, CUIN Y, CHENG L, et al. Flexible fiber nanogenerator with 209 V output voltage directly powers a light-emitting diode[J]. NanoLett, 2013, 13(1):91-94.
Theself-poweredandimplantablestimulatordrivenbyinfraredray
JIA Rui1, ZHAO Ting-ting2, LIU Peng3, DANG Yong-hui3, LIU Hong-zhong2
(1. Department of Neurology, the First Affiliated Hospital of Xi’an Jiaotong University,Xi’an 710061; 2. State Key Laboratory for Manufacturing Systems Engineering,Xi’an Jiaotong University, Xi’an 710049; 3. College of Medicine & Forensics,Xi’an Jiaotong University Health Science Center, Xi’an 710061, China)
ObjectiveTo explore the feasibility of fabricating a self-powered and implantable stimulator.MethodsBased on pyroelectric effect and high penetrability of infrared ray, an implantable stimulator was designed and fabricated. The electrical performance of stimulator was measured under infrared ray illumination. We conducted the animal experimentsinvitroandinvivoto observe the response of gastrocnemius contraction under stimulation.ResultsThe stimulator could output the electrical signal under the periodical infrared ray illumination. The output voltage and current were proportional to the intensity of infrared ray, which could reach up to 1.2 V. A real-time electrical stimulation of frog gastrocnemius was conducted and obvious contraction was observed. The tension values increased with the increase of infrared intensity. We further carried out theinvivoexperiment with a frog in order to evaluate the performance of the stimulator after being implanted into the body. The gastrocnemius would also be made to contract even though the infrared intensity decayed when through the skin.ConclusionThe proposed pyroelectric stimulator can be self-powered and controlled through near-infrared illumination. This study can provide some guidance for solving the problems of implantable power.
implantable stimulator; infrared ray; self-powered; response
2017-01-13
2017-05-22
陕西省国际科技合作与交流计划项目(No.2015KW-051)
Supported by International Scientific and Technological Cooperation Program in Shaanxi Province (No.2015KW-051)
贾蕊,住院医师/助理研究员. E-mail: jiarui029@163.com
优先出版:http://kns.cnki.net/kcms/detail/61.1399.R.20171220.1142.002.html(2017-12-20)
O121.8;G558
A
10.7652/jdyxb201801029
(编辑 卓选鹏)
