壳聚糖纳米复合物的制备及对甲基橙吸附性能研究
2018-01-02贾琬鑫芦冬涛焦媛赵秀阳李梦丹原郝楠武玲玲刘佳朋董川
贾琬鑫,芦冬涛,焦媛,赵秀阳,李梦丹,原郝楠,武玲玲,刘佳朋,董川
(山西大学 化学化工学院 环境科学研究所,山西 太原 030006)
壳聚糖纳米复合物的制备及对甲基橙吸附性能研究
贾琬鑫,芦冬涛,焦媛,赵秀阳,李梦丹,原郝楠,武玲玲,刘佳朋,董川*
(山西大学 化学化工学院 环境科学研究所,山西 太原 030006)
采用简便的一步水热方法合成磁性壳聚糖纳米复合物(Fe3O4-CS MNPs)。用透射电子显微镜、红外光谱仪、热重分析仪、多功能振动样品磁强计对其进行了表征,并通过紫外可见吸收光谱考察了其对甲基橙染料的吸附行为。结果表明,磁性壳聚糖纳米复合物对甲基橙染料的吸附遵循二级反应动力学和Freundlich吸附模型。最大吸附量为 93.84 mg/g。吸附后的磁性壳聚糖纳米复合物可通过 NaOH溶液进行脱附,脱附率为 92.98%,且4次吸附-脱附行为后,吸附量仍能达到 77.04 mg/g,表明该吸附剂具有良好的循环利用能力。
磁性壳聚糖纳米复合物;甲基橙;吸附;解吸附
0 引言
染料废水具有水质复杂、有机污染物含量高、化学需氧量高和难降解等特点,且严重破坏水体自净能力,其中污染最为严重的是染料残留[1]。各种技术已经被开发并应用到印染废水的处理中,主要有生物法[2]、吸附法[3]、氧化法[4]、化学混凝法[5]等,其中吸附法是处理印染废水的常用方法之一。然而吸附剂通常成本高,合成工艺复杂,不易回收。因此,开发来源广、高效、无二次污染的吸附材料成为当前水处理研究的热点。
壳聚糖作为一种资源丰富的天然高分子聚合物,具有生物相容性、环境友好性等特点,而且其分子链上含有丰富的羟基、氨基[6-7]等,对于金属离子、染料、蛋白质等物质有良好的亲和力,被广泛应用于生物工程、医药、食品、化工、环境等众多领域。四氧化三铁因其具有磁性,与壳聚糖复合后可以在外加磁场作用下快速回收,有效减少二次污染[8-11]。目前,许多方法已经用于合成磁性壳聚糖纳米复合物。Wu等[12]采用交联法,用三聚磷酸钠作为交联剂进行反应合成磁性壳聚糖纳米复合物;Ma等[13]采用两步共沉淀法合成了磁性壳聚糖纳米复合物(MFe3O4/CS NPs),其中沉淀剂为氨水;Zhi等[14]采用微乳液法在氢氧化钠的作用下合成磁性壳聚糖纳米复合物,但是这些方法程序复杂、所需试剂较多。我们采用简便的一步水热法合成磁性壳聚糖纳米复合物(Fe3O4-CS MNPs),并且考察了其对甲基橙染料的吸附行为,实验表明,吸附性能良好,可以应用于偶氮染料吸附领域。
1 实验部分
1.1 主要试剂和仪器
仪器:红外光谱仪(TenSorⅡ,德国Bruker optics公司);热重分析仪(Q50,美国TA公司);透射电子显微镜(Tecnai G2,FEI香港有限公司);多功能振动样品磁强计系统(VersaLab,美国Quantum Design公司);紫外-可见分光光度计(TU-1901型,北京普析通用仪器有限责任公司);酸度计(FE20,梅特勒-托利多仪器有限公司),恒温振荡摇床(M205444型,北京中西远大科技有限公司)。
1.2 磁性壳聚糖纳米复合物(Fe3O4-CS MNPs)的制备
分别称取1.500 g 三氯化铁与1.789 g壳聚糖于烧杯中,加入 25 mL乙二醇,超声 10 min均匀分散,再加入 2 mL(1.800 mol/L)的己二胺溶液搅拌均匀。然后将上述溶液转移至 50 mL聚四氟乙烯反应釜中,加热到 220℃反应8 h。反应完毕冷却至室温,用乙醇和二次水洗涤3次后,放入真空干燥箱中60℃干燥24 h,即获得产物 Fe3O4-CS MNPs。并用透射电子显微镜(TEM)、红外光谱仪(FTIR)、热重分析仪(TGA)、多功能振动样品磁强计(VSM)对其进行了表征。
1.3 甲基橙的吸附实验
1.3.1 pH的影响
将初始浓度为40 mg/L甲基橙溶液,用BR缓冲调节pH值在2.0~12.0范围内。称取2.0 mg Fe3O4-CS MNPs加入到上述不同pH值的5 mL初始浓度的甲基橙溶液中,在摇床中震荡90 min,用磁铁分离吸附剂,分别测量吸附前后溶液的吸光度值。
1.3.2 Fe3O4-CS MNPs质量的影响
分别称取0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0 mg的 Fe3O4-CS MNPs加入到5 mL浓度为40 mg/L的甲基橙溶液中,在摇床中震荡90 min,用磁铁分离吸附剂,分别测量吸附前后溶液的吸光度值。
1.3.3 吸附等温线
配制5 mL浓度为6.667、13.33、20.00、26.67、33.33、40.00、46.67、53.33、60.00、66.67 mg/L的甲基橙溶液,分别加入 2.0 mg Fe3O4-CS MNPs,在摇床中震荡 90 min,用磁铁分离吸附剂,分别测量吸附前后溶液的吸光度值。
1.3.4 吸附动力学
称取 24.0 mg的 Fe3O4-CS MNPs 加入到 60 mL 40 mg/L的甲基橙溶液中,在摇床中震荡,在吸附过程中,每个时间隔点(0、10、20、30、40、50、60、70、80、90、100、110、120 min)取 5 mL溶液,迅速用磁铁分离吸附剂,测量溶液的吸光度值。
1.3.5 脱附与重复性实验
称取2.0 mg的Fe3O4-CS MNPs加入到5 mL 40 mg/L的甲基橙溶液中,在摇床中震荡,在吸附过程中,用磁铁分离吸附剂,分别测量吸附前后溶液的吸光度值。然后用磁铁分离收集吸附剂后再用于下一次循环吸附实验。共进行了4次吸附3-脱附循环实验。
2 结果与讨论
图1为磁性壳聚糖纳米复合物(Fe3O4-CS MNPs)的制备及对甲基橙吸附性能研究的完整流程。首先,将三氯化铁和壳聚糖通过简便的水热法合成 Fe3O4-CS MNPs。然后将 Fe3O4-CS MNPs 加入到一定浓度的甲基橙染料溶液中进行吸附,吸附完全之后用外加磁铁将 Fe3O4-CS MNPs 和甲基橙进行分离。通过加入 NaOH 溶液进行解吸附,再次得到 Fe3O4-CS MNPs。
2007年无锡供水危机后,国家下决心进一步治理太湖,2008年出台了《太湖流域水环境综合治理总体方案》,以减污治污为中心,以节水调水为手段,工程措施与社会管理相结合,对太湖流域进行综合治理和管理。《条例》明确太湖流域管理应当遵循全面规划、统筹兼顾、保护优先、兴利除害、综合治理、科学发展的原则,并赋予了太湖局统筹协调、监督和管理职责。
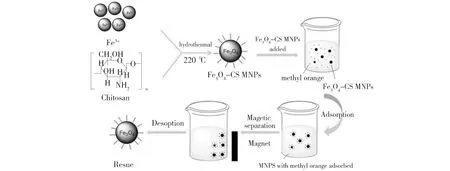
Fig.1 Synthesis routes of Fe3O4-CS MNPs and their application for methyl orange adsorption图1 Fe3O4-CS MNPs的合成及吸附甲基橙的路线
2.1 Fe3O4-CS MNPs的表征
图2为壳聚糖与Fe3O4-CS MNPs的FTIR光谱。FT-IR光谱中,Fe3O4-CS MNPs (b)的红外光谱在593 cm-1处有强吸收,是Fe—O键的伸缩振动峰,证明了磁性纳米粒子Fe3O4的存在。3 400~3 500 cm-1处的吸收峰为壳聚糖表面O—H和N—H的伸缩振动,1 579 cm-1处的吸收峰为壳聚糖表面N—H的弯曲振动,均表明在Fe3O4已经成功连结上了壳聚糖[15]。
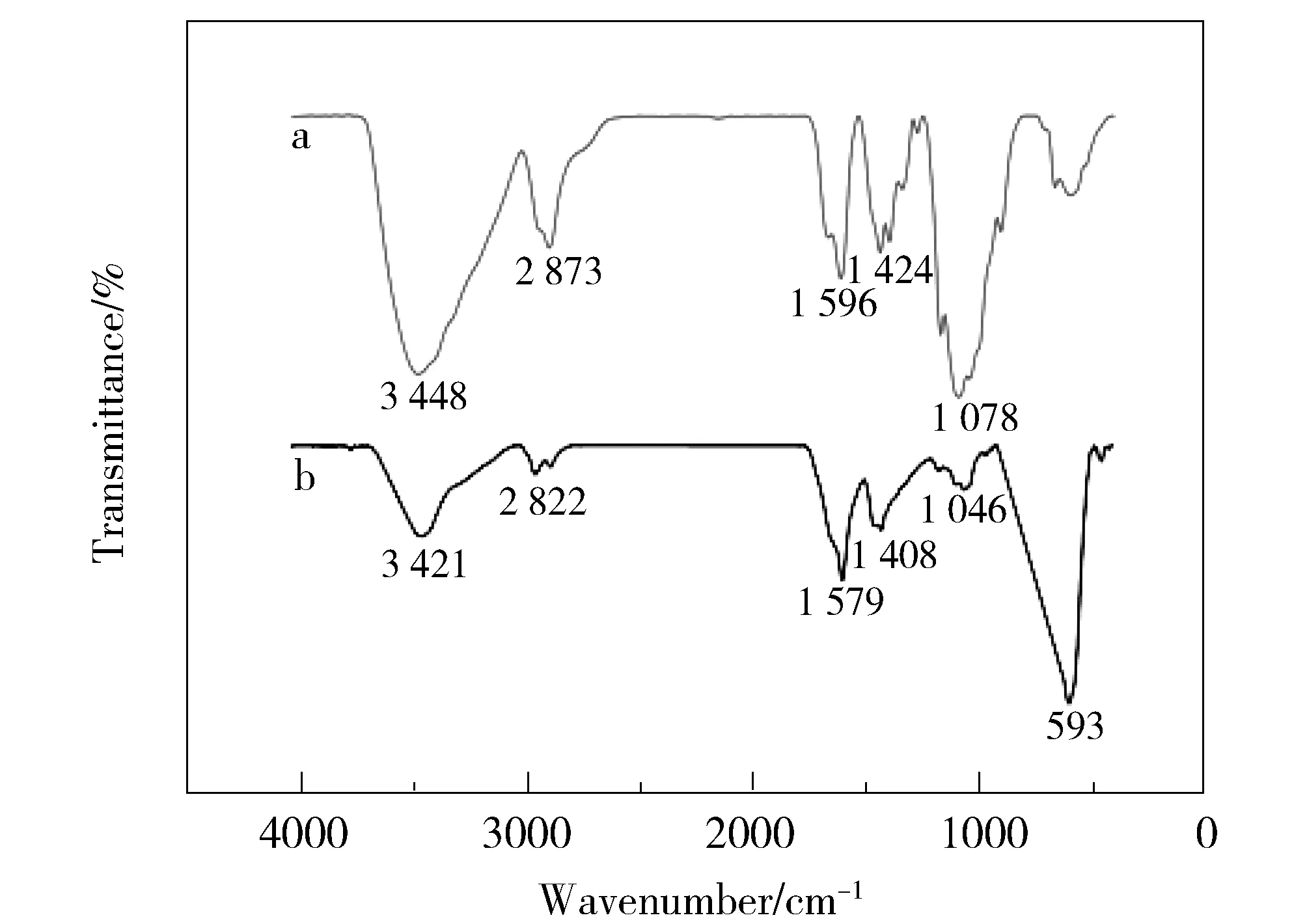
Fig.2 FTIR spectra of CS (a) and Fe3O4-CS MNPs (b)图2 壳聚糖 (a)和Fe3O4-CS (b) MNPs的傅里叶红外光谱

Fig.3 TGA curves of CS (a) and Fe3O4-CS MNPs (b)图3 壳聚糖(a)和(b)和Fe3O4-CS MNPs的热失重曲线
图3为壳聚糖与Fe3O4-CS MNPs的热失重曲线。曲线a中200℃以下失去7%的质量,主要是由于失去粒子表层水;280~550℃失去大部分的质量,主要是由于壳聚糖自身的分解。曲线b中200℃以下失去7%的质量,主要由于失去粒子表层水;200~600℃失去的质量是因为失去含氧基团;600~700℃失重是由于壳聚糖的分解[16]。
图4为壳聚糖与Fe3O4-CS MNPs的TEM谱图。通过TEM电镜分析观察Fe3O4-CS MNPs的微观形貌和尺寸,Fe3O4-CS MNPs粒子外形呈近似圆形,具有规则的核壳结构,核为黑色的Fe3O4纳米粒子,壳层为壳聚糖,粒径大约为10 nm。

Fig.4 TEM microgragh of Fe3O4-CS MNPs图4 Fe3O4-CS MNPs的TEM谱图
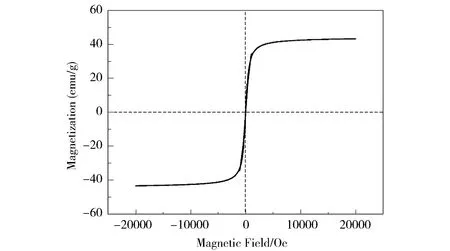
Fig.5 Hysteresis loop of Fe3O4-CS MNPs measured at room temperature图5 Fe3O4-CS MNPs的磁化率曲线
图5为Fe3O4-CSMNPs的磁化曲线。由图5可见,Fe3O4饱和磁化强度为43.32 emu·g-1,表明Fe3O4-CS MNPs对外界磁场具有良好的磁响应,可以在外磁场下快速分离与富集[17]。
2.2 甲基橙的吸附实验
2.2.1 pH的影响
如图6(a)所示,Fe3O4-CS MNPs对甲基橙的吸附量随着pH的增大而逐渐减小,所以pH为2.0时吸附效果最佳;如图6(b)所示,pH从2.0至5.0时电势电位为正值,从6.0至12.0时电势电位为负值。酸性条件下吸附效果最佳是因为酸性条件下 Fe3O4-CS MNPs表面带正电,而甲基橙表面由于带有负点的磺酸基[18],二者产生静电吸引从而引起吸附。
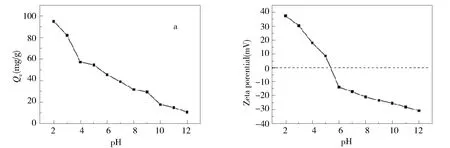
Fig.6 (a) Effect of initial pH on adsorption of methyl orange by Fe3O4-CS MNPs (b) Zeta potentials of Fe3O4-CS MNPs in Britton-Robinson buffer at different pH values图6 (a)pH对 Fe3O4-CS MNPs对吸附甲基橙的影响;(b)不同pH下Fe3O4-CS MNPs的电势电位值
2.2.2 Fe3O4-CS MNPs质量的影响
如图7所示,Fe3O4-CS MNPs对甲基橙的吸附量先是随着Fe3O4-CS MNPs质量的增加而逐渐增大,当Fe3O4-CS MNPs质量达到0.001 5 g时,又逐渐减少。而Fe3O4-CS MNPs对甲基橙的吸附效率从0.000 5 g 至0.002 0 g逐渐增大之后趋于稳定,所以选用0.002 0 g作为最佳条件。
2.2.3 吸附等温线
如图8所示,Fe3O4-CS MNPs对甲基橙吸附量随着甲基橙溶液浓度的增加从10.04 mg/g增加至91.45 mg/g,为了进一步了解其吸附特性,对吸附等温线分别进行了Langmuir(1)和Freundlich(2)拟合。

(1)
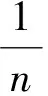
(2)
其中:Qe为平衡吸附量(mg/g);Qm为饱和吸附量(mg/g);b为解离常数(g/L);KF为Freundlich常数;1/n为Freundlich组分因数。

Fig.7 Effect of adsorbent amount on adsorption of methyl orange图7 Fe3O4-CS MNPs质量对吸附甲基橙的影响
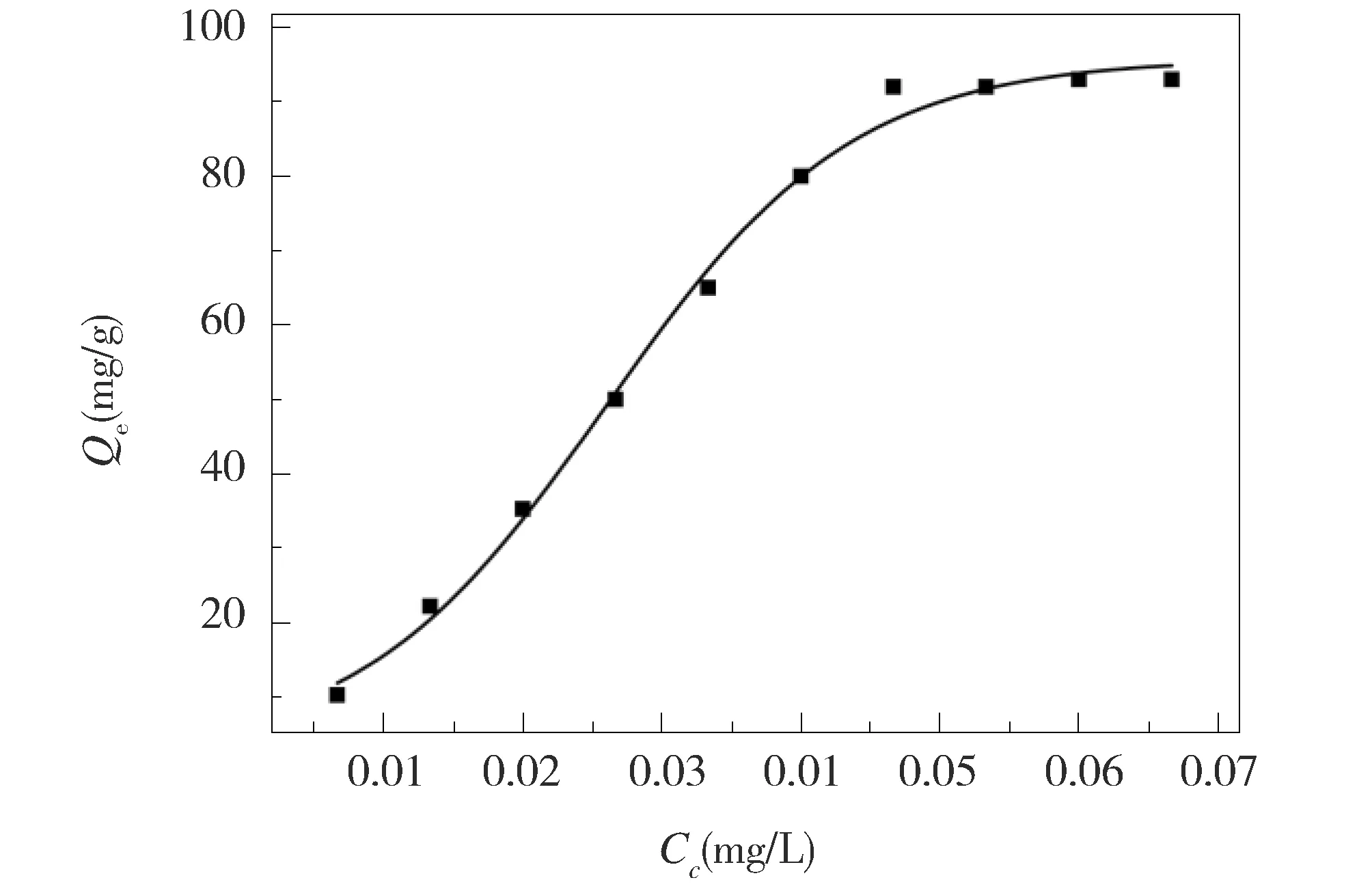
Fig.8 Adsorption isotherms of methyl orange on Fe3O4-CS MNPs图8 Fe3O4-CS MNPs对甲基橙的吸附等温线
如图9所示,拟合后,Langmuir方程所得直线线性相关系数为0.950 4,Freundlich方程所得直线线性相关系数为0.999 1,所以Fe3O4-CS MNPs对甲基橙吸附过程更符合Freundlich吸附模型。表明Fe3O4-CS MNPs对甲基橙的吸附是多层吸附过程,在多个活性位点上均有吸附。
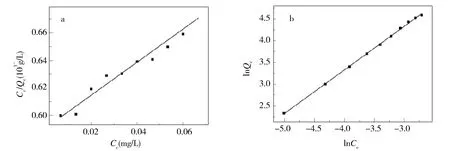
Fig.9 Fitting of adsorption isotherm data with Langmuir (a), Freundlich (b) models图9 Fe3O4-CS MNPs对甲基橙的Langmuir(a)和Freundlich(b)吸附曲线
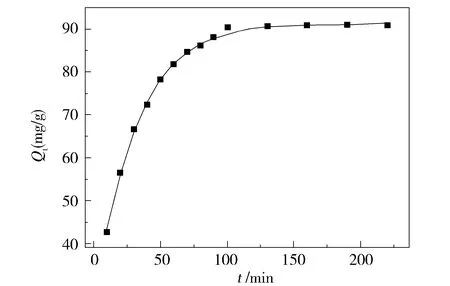
Fig.10 Adsorption kinetic of methyl orange on Fe3O4-CS MNPs图10 Fe3O4-CS MNPs对甲基橙的吸附动力学曲线
2.2.4 吸附动力学
如图10所示,Fe3O4-CS MNPs对甲基橙吸附能力在100 min内迅速增强,然后逐渐稳定,最后达到吸附平衡。进一步对动力学曲线分别进行准一级动力学方程(3)和准二级动力学方程(4)拟合。
ln(Qe1-Qt)=lnQe=k1t
(3)

(4)
其中:t为吸附时间;Qt为t时刻的吸附量;Qe为平衡吸附量;k1、k2为动力学吸附常数。
如图11所示,拟合后,准一级动力学方程所得直线线性相关系数为0.979 3,准二级动力学方程所得直线线性相关系数为0.999 2,所以Fe3O4-CS MNPs对甲基橙吸附过程更符合准二级动力学吸附过程。
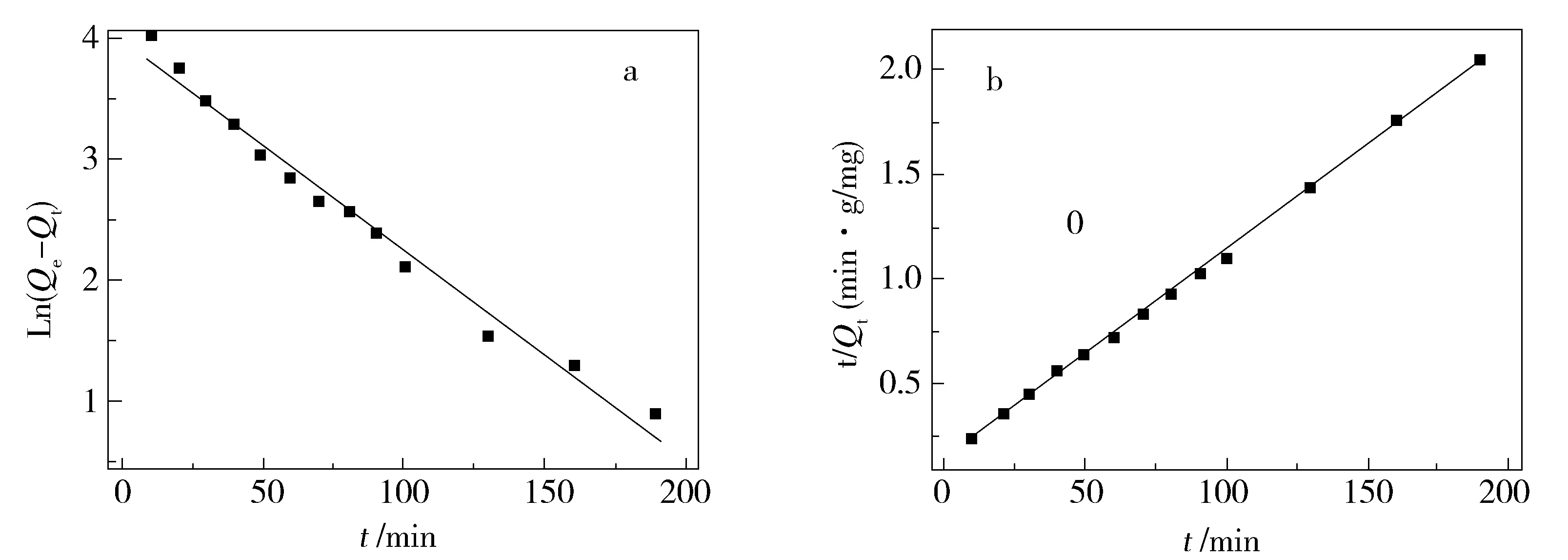
Fig.11 Fitting of adsorption kinetic data with Pseudo-first-order (a),Pseudo-second-order models(b)图11 Fe3O4-CS MNPs对甲基橙的准一级动力学(a)和准二级动力学(b)的线性拟合

Fig.12 Recycling of Fe3O4-CS MNPs in the removal of methyl orange图12 Fe3O4-CS MNPs对甲基橙的循环吸附
2.2.5 脱附与重复性实验
采用 NaOH溶液对已经吸附甲基橙的 Fe3O4-CS MNPs进行脱附实验,加入 NaOH 1 min后甲基橙脱附明显,表明Fe3O4-CS MNPs对甲基橙的吸附是一个可逆的过程。碱性条件下解吸附是因为碱性条件下 Fe3O4-CS MNPs表面不带电,而甲基橙表面由于带有负点的磺酸基,二者之间静电吸引消失从而引起解吸附。在吸附-脱附四次之后,吸附量仍能达到 77.04 mg/g,表明Fe3O4-CS MNPs吸附剂是一种环保的,可重复使用的染料吸附剂。
3 结论
通过简化的一步水热法,合成了磁性壳聚糖纳米复合物(Fe3O4-CS MNPs)。磁性壳聚糖微球对甲基橙溶液的吸附符合Freundlich等温吸附模型,表明Fe3O4-CS MNPs对甲基橙的吸附是多层吸附过程。其吸附过程符合准二级动力学吸附过程。经过吸附-解吸附4次后,吸附量仍能达到 77.04 mg/g,表明Fe3O4-CS MNPs吸附剂是一种环保的,可重复使用的染料吸附剂,所以该吸附剂材料在偶氮染料吸附领域有一定的应用前景。
[1] Robati D,Mirza B,Rajabi M,etal.Removal of Hazardous Dyes-BR 12 and Methyl Orange using Graphene Oxide as an Adsorbent from Aqueous Phase[J].ChemEngJ,2016,284:687-697.DOI:10.1016/j.cej.2015.08.131.
[2] Neamtu M,Yediler A,Siminiceanu I,etal.Oxidation of Commercial Reactive Azo Dye Aqueous Solutions by the Photo-Fenton and Fenton-like Processes[J].JPhotochPhotobioAChemistry,2003,161:87-93.DOI:10.1016/S1010-6030(03)00270-3.
[3] Chen A B,Li Y T,Yu Y F,etal.Synthesis of Mesoporous Carbon Nanospheres for Highly Efficient Adsorption of Bulky Dye Molecules[J].JMaterSci,2016,51:7016-7028.DOI:10.1007/s10853-016-9991-7.
[4] Pandey A,Singh P,Iyengar L.Bacterial Decolorization and Degradation of Azo Dyes[J].IntBiodeterBiodegr,2006,59:73-84.DOI:10.1016/j.ibiod.2006.08.006.
[5] Kim T H,Park C,Yang J,etal.Comparison of Disperse and Reactive Dye Removals by Chemical Coagulation and Fenton Oxidation[J].JHazardMaterB,2004,112:95-103.DOI:10.1016/j.jhazmat.2004.04.008.
[6] Wang J Z,Zhao G H,Jing L Y,etal.Facile Self-assembly of Magnetite Nanoparticles on Three-dimensional Graphene Oxide-chitosan Composite for Lipase Immobilization[J].BiochemEngJ,2015,98:75-83.DOI:10.1016/j.bej.2014.11.013.
[7] Cao C H,Xiao L,Chen C H,etal.In Situ Preparation of Magnetic Fe3O4/Chitosan Nanoparticles Via a Novel Reduction-precipitation Method and Their Application in Adsorption of Reactive Azo Dye[J].PowderTechnol,2014,260:90-97.DOI:10.1016/j.powtec.2014.03.025.
[8] Xu P,Zeng G M,Huang D L,etal.Use of Iron Oxide Nanomaterials in Wastewater Treatment:A review[J].SciTotalEnviron,2012,424:1-10.DOI:10.1016/j.scitotenv.2012.02.023.
[9] Gao J R,Wei W,Shi M J,etal.A Controlled Solvethermal Approach to Synthesize Nanocrystalline Iron Oxide for Congo Red Adsorptive Removal from Aqueous Solutions[J].JMaterSci,2016,51:4481-4494.DOI:10.1007/s10853-016-9760-7.
[10] Yang H,Yuan B,Lu Y B,etal.Preparation of Magnetic Chitosan Microspheres and Its Applications in Wastewater Treatment[J].SciChinaSerBChem,2009,52:249-256.DOI:10.1007/s11426-008-0109-1.
[11] Zhang Y R,Zhang S L,Wang S Q,etal.A Dual Function Magnetic Nanomaterial Modified with Lysine for Removal of Organic Dyes from Water Solution[J].ChemEngJ,2013,239:250-256.DOI:10.1016/j.cej.2013.11.022.
[12] Wu Y,Wang Y J,Luo G S,etal.In Situ Preparation of Magnetic Fe3O4-chitosan Nanoparticles for Lipase Immobilization by Cross-linking and Oxidation in Aqueous Solution[J].BioresourceTechnology,2009,100:3459-3464.DOI:10.1016/j.biortech.2009.02.018.
[13] Ma W,Ya F Q,Han M.Characteristics of Equilibrium,Kinetics Studies for Adsorption of Fluoride on Magnetic-chitosan Particle[J].JHazardMater,2007,143:296-302.DOI:10.1016/j.jhazmat.2006.09.032.
[14] Zhi J,Wang Y J,Lu Y C.In Situ Preparation of Magnetic Chitosan/Fe3O4Composite Nanoparticles in Tiny Pools of Water-in-oil Microemulsion[J].Reactive&FunctionalPolymers,2006,66:1552-1558.DOI:10.1016/j.reactfunctpolym.2006.05.006.
[15] Cai Y L,Zheng L C,Fang Z Q,etal.Selective Adsorption of Cu (ii) from an Aqueous Solution by Ion Imprinted Magneticchitosan Microspheres Prepared from Steel Pickling Waste Liquor[J].RSCAdv,2015,5:97435-97445.DOI:10.1039/c5ra16547d.
[16] Zhu H Y,Jiang R,Xiao L,etal.A Novel Magnetically Separable Gamma-Fe2O3/Crosslinked Chitosan Adsorbent:Preparation,Characterization and Adsorption Application for Removal of Hazardous Azo Dye[J].JHazardMater,2010,179:251-257.DOI:10.1016/j.jhazmat.2010.02.087.
[17] Song W,Gao B Y,Xu X,etal.Adsorption-desorption Behavior of Magnetic Amine/Fe3O4Functionalized Biopolymer Resin Towards Anionic Dyes from Wastewater[J].BioresourceTechnol,2016,210:123-130.DOI:10.1016/j.biortech.2016.01.078.
[18] Beppu M M,Santana C C.Influence of Calcification Solution on in Vitro Chitosan Mineralization[J].MaterRes,2002,5:47-50.DOI:10.1590/S1516-14392002000100008.
SynthesisofChitosanModifiedFe3O4MagneticNanoparticlesforMethylOrangeAdsorption
JIA Wanxin,LU Dongtao,JIAO Yuan,ZHAO Xiuyang,LI Mengdan,YUAN Haonan,WU Lingling,LIU Jiapeng,DONG Chuan*
(InstituteofEnvironmentalScience,andSchoolofChemistryandChemicalEngineering,ShanxiUniversity,Taiyuan030006,China)
Magnetic chitosan nanoparticles (Fe3O4-CS MNPs) were synthesized by a simple one-pot hydrothermal method and applied for methyl orange adsorption. The Fe3O4-CS MNPs were characterized by TEM, FTIR, TGA and VSM. The adsorptive behavior of methyl orange on Fe3O4-CS MNPs was investigated using the UV-vis spectrophotometric technique. The adsorption process followed the pseudo-second-order kinetic model. The adsorption equilibrium data fitted well with the Freundlich isotherm model with the saturated adsorption capacity of 93.84 mg/g. The desorption experiment could be carried out using NaOH with the recovery of 92.98 %. After four cycles, adsorption efficiency still reached 77.04 mg/g. The results showed that Fe3O4-CS MNPs possessed a simple synthesis route and excellent reusability, which have potential application in the adsorption of dye in environmental effluents.
magnetic chitosan nanoparticles;methyl orange;adsorption;desorption
10.13451/j.cnki.shanxi.univ(nat.sci.).2017.04.025
2016-11-25;
2016-12-22
国家自然科学基金(21475080;21575084);山西省高等学校科技创新项目(2015114);山西省自然科学基金(2015011030);山西省高等学校大学生创新创业训练项目(201610108018)
贾琬鑫(1991-),女,山西阳泉人,硕士研究生,从事分析化学方面研究。
*通信作者:董川(DONG Chuan),E-mail:dc@sxu.edu.cn
O647.3
A
0253-2395(2017)04-0809-07
