氯金酸修饰对再生电极检测性能的影响
2017-12-27刘永玲李文娇
刘永玲 ,李 立,李文娇,赵 勇,卢 瑛 ,4,5*
1.上海海洋大学 食品学院,上海 201306
2.上海水产品加工及贮藏工程技术研究中心;农业部水产品贮藏保鲜质量安全风险评估实验室,上海 201306
3.食品热加工技术研究发展中心(亚洲),上海 201306
4.食品科学与工程国家级实验教学示范中心(上海海洋大学),上海201306
5.国家淡水水产品加工技术研发分中心,上海201306
近年来,纳米材料的电化学免疫传感器以其快速、灵敏、可在线检测等特点,在致病菌,抗生素残留,农、兽药残留和毒素检测等方面已成为一种快速、方便、可靠的食品安全检测方法[1,2],并受到越来越多的关注和研究。但这些传感器往往都是一次性的,大大影响了免疫传感器在实际生产应用中的竞争力,且增加了制作的难度和成本。因此寻找有效的传感器再生方法可是很有必要的。对电极进行再生是传感器发展中重要的一部分[3,4]。由于抗原抗体之间的结合具有可逆性的特点,因此,传感器的再生主要是将形成的免疫复合物解离开,但是抗原抗体结合后不易分开,要一些具有降低两者间亲和力的物质对其进行处理。常用的有柠檬酸-柠檬酸钠缓冲液、尿素[5]、甘氨酸-盐酸缓冲液、乙二胺、盐酸胍缓冲液[6]、强酸强碱及超声清洗等[7]。此外,在再生过程中要尽可能的保持抗原抗体的活性,这也就要求对使用的再生溶液浓度或pH及再生时间等进行优化[8,9]。再生后电极的电流响应会有所下降[10],为了提高其可用性,本文对其进行了氯金酸修饰。氯金酸修饰电极的方法参考纳米金对电极的修饰方法,主要有恒电位沉积法[11,12]、自组装法[13,14]、LB膜法[15,16]及种子媒介法。由于氯金酸修饰量较大时,会在电极的表面形成结晶块,使修饰电极的比表面积减小、导电性降低[17],故需对其修饰量和修饰时间进行优化。
在本研究中,我们采用柠檬酸-柠檬酸钠缓冲液作为再生液对电极上的免疫复合物进行解离,优化了再生液的解离条件;此外,对再生电极的氯金酸修饰条件进行了优化,并探讨了氯金酸修饰对再生电极检测性能的影响作用。
1 材料与方法
1.1 材料
1.1.1 试剂与耗材 使用过的多壁碳纳米管纤维电极,根据实验室之前的研究制备[18],硫堇购自江莱生物;辣根过氧化物酶(HRP)抗体标记试剂盒购自英国Innova Biosciences;EDC(1-乙基-3-二甲基氨基丙基碳酰二亚胺盐酸盐)、NHS(N-羟基琥珀酰亚胺)购自美国PIERCE公司;氯金酸溶液(10 mmol/L)、H2O2购自国药集团化学试剂有限公司;牛血清白蛋白(BSA)购自上海生工生物工程技术服务有限公司;柠檬酸-柠檬酸钠缓冲液、磷酸盐缓冲液(PBS)为本实验室自行配制;单增李斯特菌ATCC19115,购自中国科学院微生物研究所;单增李斯特菌多克隆抗体为本实验室制备;实验用水均为去离子水,试剂均为分析纯。
1.1.2 实验仪器 电化学工作站(chi660D上海辰华仪器有限公司);铂丝对电极(盐城骄远分析仪器有限公司);参比电极(232型上海精密科学仪器有限公司);恒温振荡培养箱(上海知楚仪器有限公司);垂直混合器(HS-3,宁波新芝生物科技股份有限公司);Synergy™2多功能酶标仪购自美国博腾仪器有限公司。
1.2 方法
1.2.1 检测流程 采用循环伏安法进行电化学测试。在实验中,Relative Percentage(RP%)表示电极再生或氯金酸修饰前后电流变化的相对百分比RP%=(Ia-Ib)/Ia×100%,其中,Ia为电极再生液或氯金酸处理后的电流,Ib为电极再生或氯金酸处理前的电流。Current percentage(CP%)表示再生处理或氯金酸修饰后电极电流达到其原始电流的百分比,CP%=Id/Ic×100%,其中:Id为再生或氯金酸处理后电极的电流,Ic为电极的原始电流。
在氯金酸修饰前后再生电极的比较中,△Ipc=I1-I2。I1为免疫反应前电极的电流,I2为免疫反应后电极的电流。电化学测量是在一个含有三电极体系的电化学池中进行,电化学池中含有0.1 M PBS,0.1 M NaCl和1 mM的硫堇。测试的工作电压为-1.0 v~0.5 v相对于Ag/AgCl参比电极,扫描速率为0.1 v/s。单增李斯特菌的检测是基于抗原抗体结合前后循环伏安曲线中还原峰峰电流的变化值△Ipc。
1.2.2 柠檬酸-柠檬酸钠再生液的条件优化 为使再生液有更好的再生效果,本研究对再生液的相关条件进行了优化,主要包括再生液浓度(0.05、0.1、0.15、0.20 mmol/L)、再生液pH(2.2、2.4、2.6、2.8、3.0)和再生时间(10、15、20、30、40 min)的优化。优化结果根据再生前后后电极电流的DP%及达到原始电流的C%进行选择。
1.2.3 氯金酸修饰条件的优化 根据碳纳米管纤维电极本身的大小特点,选取适量的氯金酸修饰量(25、50、75、100 μL)和修饰时间(30、60、90、120 min)进行梯度优化。根据修饰前后电极电流的RP%及修饰后电极的电流达到其原始电流的CP%来选择氯金酸的修饰条件。
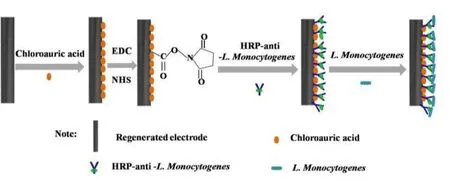
图1 氯金酸修饰的酶免疫电极的制备Fig.1 The preparation of an enzyme immune electrode modified by chloroauric acid
1.2.4 基于氯金酸修饰的酶免疫电极的制备 制作过程如图1所示。将经再生液处理过的电极用0.01 mol/L、pH7.4的PBS缓冲液清洗3次,晾干后将一定量的氯金酸溶液覆盖在碳纳米管纤维表面静置2 h,并清洗表面。然后根据化学键共价交联法将经过EDC、NHS活化后的氯金酸修饰电极置于HRP标记的抗单增李斯特菌抗体中3 h,并用0.2%的BSA对未结合位点进行30 min封闭,最后将清洗后的电极至于4°C冰箱中备用。再生免疫电极的制备方法与氯金酸修饰后制备免疫电极的方法相同。
1.2.5 氯金酸修饰对再生电极检测性能的影响 电极在修饰了氯金酸之后在信号增强、偶联抗体等方面都有所提升,为了验证这一作用,本研究将再生免疫电极和氯金酸再生免疫电极分别置于5 mL的102~107cfu/mL单增李斯特菌稀释液中,PBS做阴性对照,室温孵育30 min后进行循环伏安测试检测,对单增李斯特菌的检测灵敏度进行了评价。此外,通过分别将不同时期制作的两种免疫电极置于几份平行(n=5)的5 mL的1×105cfu/mL的单增李斯特菌溶液中室温孵育30 min后检测电极的电流响应,进行了重现性分析。最后,在25 d内对两种免疫电极分别进行第1、2、5、7、10、15、20、25 d的连续测试,观察电流的变化,对电极的长期稳定性进行了评价。
2 结果与讨论
2.1 柠檬酸-柠檬酸钠再生液的优化
2.1.1 柠檬酸-柠檬酸钠浓度优化 再生液柠檬酸-柠檬酸钠的浓度对电极电流的影响如图2所示。随着再生液浓度的增大,电极再生前后电流变化的RP%也随之增大,在0.1 mol/L时达到最大;当再生液浓度继续增大时,电流变化的RP%出现大幅度下降。此外,采用0.1 mol/L的浓度对电极进行再生后,其电流值可达到初始电流的85.23%。因此,我们选择了0.1 mol/L柠檬酸-柠檬酸钠作为再生液的最佳浓度。

图2 再生液浓度对电极电流响应的影响Fig.2 Influence of regenerated liquid concentration on electrode current response
2.1.2 柠檬酸-柠檬酸钠pH优化 pH对电极再生效果的影响如图3所示。由图可见,随着pH的增加,电极再生前后电流变化的RP%也增大,当pH达到2.4时,RP%达到最大;当pH进一步增加时,RP%急剧下降。pH主要影响抗原抗体之间的亲和力,进而影响Ag-Ab键的解离程度,当pH增大时,使抗原抗体亲和力下降的程度减小,致使免疫复合物的解离程度下降。且在pH2.4时,再生电极的电流达到其初始电流的CP%最大(86.63%),故此本文选取pH2.4为适宜的再生液pH。

图3 再生液pH对电极电流响应的影响Fig.3 Influence of regenerated liquid pH on electrode current response
2.1.3 柠檬酸-柠檬酸钠再生时间优化 图4为再生时间对电极电流响应的影响。在10~30 min内,随着时间的增加,再生前后电极电流变化的RP%整体上呈上升趋势,至30 min时达到最大,当时间继续增加时,变化基本持平,但在30 min下再生电极的电流达到其初始电流的CP%(84.28%)比较40 min(75.08%)下大。因此选取对电极再生处理30 min。

图4 再生时间对电极电流响应的影响Fig.4 Influence of regeneration time on electrode current response
2.2 氯金酸修饰条件的优化
氯金酸修饰量的优化结果如图5所示。在102.96~308.89 μg范围内,氯金酸修饰再生电极前后电流变化的RP%随着修饰量的增大而增大,至308.89 μg时达到最大,当继续增加时,RP%基本不再变化。由于氯金酸加入较多时,会在电极的表面形成结晶块,使修饰电极的比表面积减小[17]。且在308.89 μg的修饰量下,氯金酸修饰的再生电极的电流可达到其原始电流的144.6%,故选取308.89 μg的修饰量用于进一步的实验。

图5 氯金酸修饰量对电极信号的影响Fig.5 Inluence of modification amount of chloroauric acid on electrode signal
氯金酸修饰时间对再生电极电流响应的影响如图6所示。在30~90 min内,修饰前后再生电极电流变化的RP%成上升趋势,在90 min时达到最大,再增加修饰时间,RP%的变化基本保持不变,这主要是因为在一定量的氯金酸下,随着时间的增加氯金酸与电极之间的结合逐渐达到饱和。另外,在90 min时,相较于原始电流,氯金酸再生电极的电流增加到137.59%。故选取90 min为氯金酸的修饰时间。

图6 氯金酸修饰时间对电极信号的影响Fig.6 Inluence of chloroauric acid modification time on electrode signal
2.3 氯金酸修饰对再生电极检测性能的影响
两种免疫电极对单增李斯特菌的检测结果图7所示。氯金酸再生免疫电极在102~107cfu/mL范围内检测到目标菌为(R2=0.958),LOD为2.1×102cfu/mL。再生免疫电极的检测范围为103~107cfu/ml(R2=0.940),LOD为3.08×103cfu/mL,并与原始电极对单增李斯特菌的检测范围102~105cfu/mL(R2=0.993),LOD为1.07×102cfu/mL进行比较。由结果可知,电极经再生之后,对目标菌的检测灵敏度下降,但是经氯金酸修饰后,其检测灵敏度显著提高,并且接近原始电极的检测水平。这是由于氯金酸修饰到电极上之后,对信号起到增强作用,且氯金酸对抗体等蛋白质分子具有吸附能力,因此在同样的实验条件下氯金酸修饰的电极能够结合较多的抗体,信号响应较灵敏。此外,对单增李斯特菌的重现性分析及稳定性测试结果也显示氯金酸修饰后再生电极的性能得到了提高。

图7 氯金酸对再生电极检测灵敏度的影响Fig.7 The effect of chloroauric acid on detection sensitivity of regeneration electrode
25 d内免疫电极的稳定性测试结果如图8所示。再生免疫电极的电流在第15 d时已经下降至原始电流的74.68%;对于氯金酸-再生免疫电极,由于氯金酸的修饰加强了电极对抗体的结合、固定,在第15 d时,电流为其原始电流的84.55%,在20 d以后逐渐下降至原来的76.92%;并与15 d后电流下降至最初的91.69%的原始电极相比。由这些对比数据可以看出,氯金酸处理后对再生电极的电流性能恢复较为稳定,可应用于目标物的检测。

图8 氯金酸对再生电极稳定性的影响Fig.8 The effect of chloroauric acid on stability of regeneration electrode
在对单增李斯特菌的重现性实验中,再生免疫电极的RSD为7.92%,氯金酸-再生免疫电流的RSD为6.62%,原始电极的RSD为6.18%。从结果可知,氯金酸修饰再生电极后提高了对抗体结合的牢固度,提高操作平行性,且与原始电极的水平相近。综上所述,氯金酸修饰后的再生电极在检测灵敏度、稳定性和重现性方面都得到了显著提升,展现出较好的应用潜力。
3 结论
本文对电极的再生条件、氯金酸修饰条件及氯金酸对再生电极检测性能的影响进行了研究、分析。结果表明,在优化的再生条件(0.1 mol/L柠檬酸-柠檬酸钠、pH2.4、30 min)下,电极的再生效果较好,再生后电极电流恢复至其原始电流的近85.38%;在308.89 μg氯金酸量、90 min修饰时间下再生电极的信号增强近60%。氯金酸对再生电极的修饰使其在原有的检测范围103~107cfu/ml,增加至102~107cfu/mL,LOD提高了14.6倍,稳定性提升了近10%。氯金酸对再生电极的这些检测性能有显著提高,且氯金酸相较于纳米金而言较大的降低了成本,为再生电极的使用提供了应用潜力。
[1]TurnerAP.Biosensors--sense and sensitivity[J].Science,2000,290:1315-1317
[2]赵广英,马 超,励建荣.电沉积纳米金修饰4-SPCE电流型VP免疫传感器的研制[J].中国食品学报,2009,9(4):8-14
[3]Pei RJ,Cui XQ,Yang XR,et al.Real-time immunoassay of antibody activity in serum by surface plasmon resonance biosensor[J].Talanta,2000,53:481-488
[4]Gao ZX,Chao FH,Chao Z,et al.Detection of staphylococcal enterotoxin C2 employing a piezoelectric crystal immunosensor[J].Sensors Actuators B,2000,66(1-3):193-196
[5]高志贤,张 超,陶桂全,等.压电免疫传感器抗体固定方法研究[J].中华微生物学和免疫学杂志,1996,16(3):191-195
[6]李超凡,徐京宁,何 兵,等.免疫电化学方法测定γ干扰素[J].分析化学,1994,22(1):55-57
[7]姚春艳,府伟灵.基于碳纳米管修饰玻碳电极的唾液sIgA可再生免疫传感器[J].分析测试学报,2005,30(4):349-355
[8]Park IS,Kim WY,Namsoo K.Operational characteristics pf an antibody-immobilized QCM system detecting Salmonella spp[J].Biosens Bioelectron,2000,15(3-4):167-172
[9]Su X,Chew FT.Self-assembled monolayer-based piezoelectric trystal immunosensor for the quantification of total human immu—noglobulin E[J].Anal Biochem,1999,273(1):66-72
[10]王 艳,甄生航,朱 洋,等.纳米金自组装膜的IgM压电免疫传感器的研究[J].化学学报,2003,61(4):608-613
[11]Dai X,Nekrassova O,Compton RG.Anodic stripping voltammetry of arsenic(III)using gold nanoparlicle-modified electrodes[J].Anal Chem,2004,76(19):5924-5929
[12]Li Y,Shi GQ.Electrochemical growth of two-dimen-ional gold nanostructures polypyrrole film modifiedITO electrode[J].J Phys Chem B,2005,109(50):23787-23793
[13]Dai J,Guo L,Jiang Y.Preparation of gold nanoparticles modified with tetrathiafulvalene via direct sulfur bridge[J].J Nanosci Nanotechnol,2005,5(3):474-478
[14]Lei CX,Hu SQ,Yu RQ.An amperometric hydrogen peroxide biosensor based on immobilizing horseradish peroxidase to a nano-Aumonolayer supported by sol-gel derived carbon ccramic electrode[J].Bioelectro-chemistry,2004,65(1):33-39
[15]Goyal RN,Gupta VK,Oyama M.Simultaneous volta-mmetric determination of prednisone and prednisolone in human body fluids[J].Talanta,2007,72(3):976-983
[16]Zhuo Y,Yuan R,Chai YQ.A tris(2,2'-bipyridyl)co-balt(III)-bovine serum albumin composite membrane for biosensors[J].Biomaterials,2006,27(31):5420-5429
[17]楚 琳,张晓丽.纳米金修饰电极的制备及电化学性能研究[J].曲阜师范大学学报,2014,40(1):78-82
[18]Li L,Chen C,Xie J,et al.The preparation of carbon nanotube/MnO2composite fiber and its application to flexible micro-supercapacitor[J].Journal of Nanomaterials,2013(32):209-214
