2-氨基-3-新戊基-5-氯-3H-咪唑并[4,5-b]吡啶氢溴酸盐的合成研究*
2017-12-27喻明军
喻明军
(亳州学院)
0 引言
咪唑并吡啶类化合物在结构上具有和吲哚、氮杂吲哚的类似性,其在医药和农业工业上有着广泛的应用[1-3].咪唑并[4,5-b]吡啶衍生物是咪唑并吡啶类化合物中重要的一种,具有良好的抗微生物和杀菌作用,部分咪唑并[4,5-b]吡啶衍生物具有治疗癌症、糖尿病的作用[4-6].咪唑并[4,5-b]吡啶化合物的合成方法有2,3-二氨基吡啶与羧酸关环、二硫化碳或三光气关环[7-13],2-氯-3-氨基吡啶与芳胺关环[14-16]等,该文以2,6-二氯-3-硝基吡啶为原料经取代、还原,然后和溴化氰关环生成目标产物,其合成路线如图1所示.
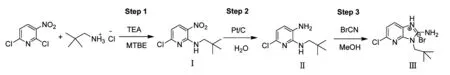
图1 2-氨基-3-新戊基-5-氯-3H-咪唑并[4,5-b]吡啶氢溴酸盐合成路线
1 实验部分
1.1 实验仪器与试剂
主要实验仪器:XPE205型电子天平,RE-2000旋转蒸发器,高效液相色谱仪(日本岛津,LC-20A),液质联用(日本岛津,LCMS2010EV),400 MHz核磁共振仪; 主要试剂:2,6-二氯-3-硝基吡啶(百灵威科技有限公司),Pt/C(10%)(宇瑞(上海)化学有限公司),溴化氰(湖北信康医药化工有限公司),辛戊胺盐酸盐(自制),溶剂为分析纯.
1.2 实验步骤
1.2.1 化合物Ⅰ的合成
在1 L的三口烧瓶中依次加入500 mL甲基叔丁基醚、2,6-二氯-3-硝基吡啶(38.6 g, 0.20 mol)和三乙胺(48.6 g,0.48 mol),然后控制温度在15~20℃之间分批加入辛戊胺盐酸盐(34.6 g,0.28 mol).加入完毕后在此温度下搅拌18 h.反应完后加入320 mL的水,分层,然后将有机层浓缩干,粗品用异丙醇重结晶.干燥后得到40.1 g的化合物Ⅰ,纯度为99.1%,收率为82.3%.
1.2.2 化合物Ⅱ的合成
在100 mL的三口烧瓶中依次加入20 mL水、2.5g的Pt/C和次磷酸(0.50g,7.6mmol),搅拌10 min后再加入乙酰丙酮氧钒(0.40 g,1.5 mmol).搅拌20 min后,将三口烧瓶中的物料转移到1L的高压釜中,然后将化合物Ⅰ(50.0 g, 205 mmol)和甲苯(500 mL)加入到高压釜中.将反应釜加热到70~80 ℃并控制氢气压力在50~55psi之间反应24 h.反应完毕后降温过滤,滤液浓缩至干得到43.2 g 的化合物Ⅱ,收率为98.5%.
1.2.3 化合物 Ⅲ的合成
在1 L的三口烧瓶中依次加入220mL的甲醇和化合物Ⅱ(43.2 g, 202 mmol),然后降温到10~20 ℃.控制温度在10~20 ℃之间分批加入溴化氰(22.5 g,205 mmol),并在此温度下反应24 h.反应完后,控制温度在10~20 ℃之间滴加440 mL的甲基叔丁基醚,滴加完毕后搅拌2~3 h后过滤,滤饼用甲基叔丁基醚洗涤.干燥后得到41.8g的化合物Ⅲ,纯度为99.1%,收率为64.7%.,MS(m / z, % ) : [M+1 ,238.9].
1.2.4 辛戊胺盐酸盐的制备
在1L的三口烧瓶中加入新戊醛(103 g, 1.2 mol),650 mL无水乙醇和50g无水硫酸镁,然后再加入苄胺(107 g, 1.0 mol),控制温度在25~35 ℃搅拌18 h.反应完后过滤,滤液转移到高压釜,加入10.7 g的Pd/C,控制压力在50~60psi和温度在20~30 ℃下搅拌20 h.反应完后过滤,滤液浓缩到200 mL,控制温度在20~30 ℃下,滴加5 mol/L的氯化氢甲醇溶液(220mL),然后在此温度下搅拌3 h后过滤.干燥得到99.5g的白色固体,收率为80.5%.
1.3 产物结构表征
图2为化合物Ⅲ的质谱图.MS(m / z, % ) : [M+1 ,238.9],和游离态目标产物一致.
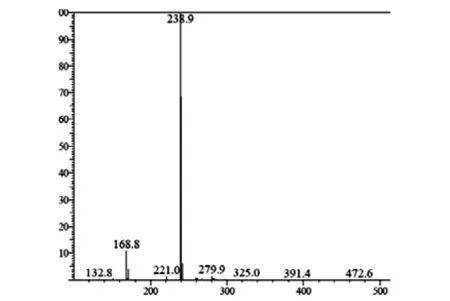
图2 C的MS谱图
图3 为化合物Ⅲ的1H-NMR谱图.1H NMR(DMSO):8.954(S,2H),7.777(d,1H),7.357(d,1H), 3.926(S,2H),0.960(S,9H).
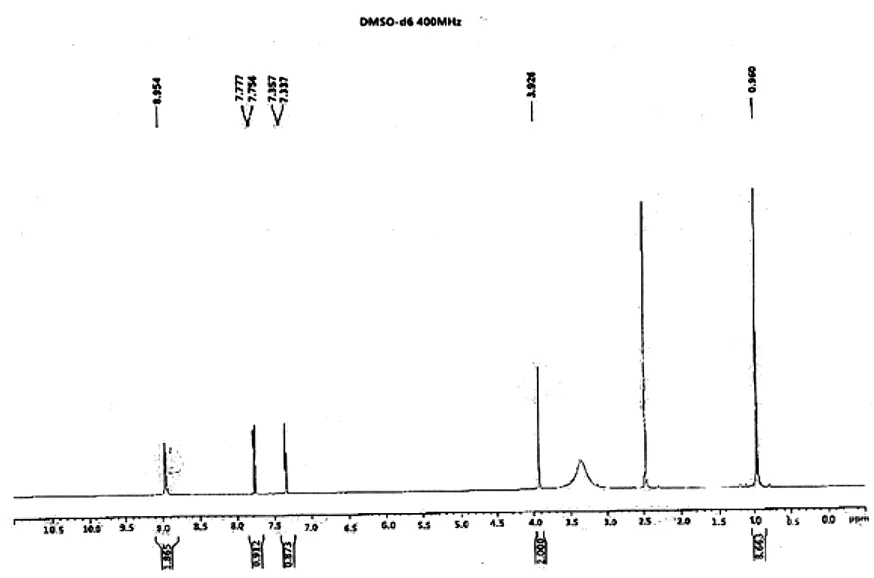
图3 化合物Ⅲ的1H-NMR谱图
2 结果与讨论
2.1 化合物Ⅰ反应条件确定
2.1.1 反应温度对取代反应的影响
在2,6-二氯-3-硝基吡啶、辛戊胺盐酸盐和三乙胺的物质的量比为1∶1.4∶2.0,反应时间为18h时,收率和纯度见表1.
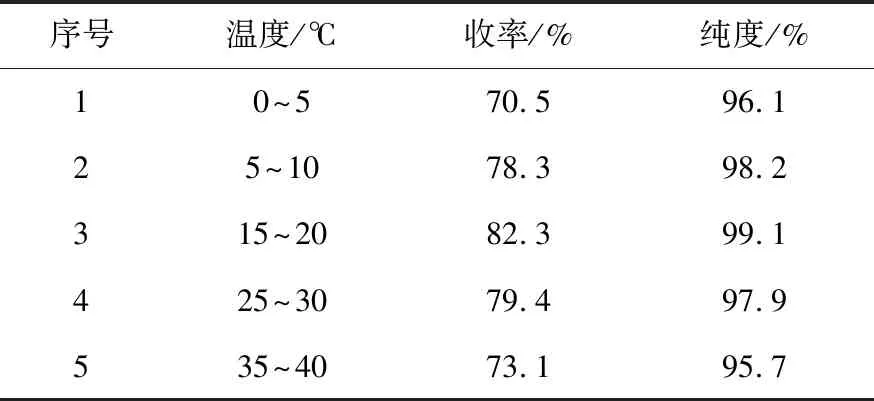
表1 反应温度对化合物Ⅰ的收率和纯度的影响
由表1可见,反应温度降低反应缓慢,原料反应不完,反应温度升高反应速度加快,但是当温度超过30 ℃时杂质明显增加,产品的纯度降低.从LCMS的结果上看是由2取代的产物生产造成了产品纯度降低.因此反应的理想温度是控制在15 ℃左右.
2.1.2 新戊酸盐酸的量对收率的影响
在2,6-二氯-3-硝基吡啶和三乙胺的物质的量比为1∶2.0,反应温度为15~20 ℃,反应时间为18h,收率见表2.

表2 辛戊胺盐酸盐的用量对化合物Ⅰ的收率的影响
由表2可以看出辛戊胺盐酸盐的用量在1.4mol/L时收率达到最大,再继续增加其用量,收率不再增加,甚至会有少许的降低.因此取代反应的条件确定为n(2,6-二氯-3-硝基吡啶)∶n(辛戊胺盐酸盐)∶n(三乙胺)=1∶1.4∶2.0,反应温度为15~20℃.
2.2 化合物Ⅱ反应条件的确定
2.2.1 压力对还原反应的影响
在Pt/C的用量为5.0%、反应温度为70~80 ℃,反应时间为24 h,考察了氢气压力对收率的影响,见表3.
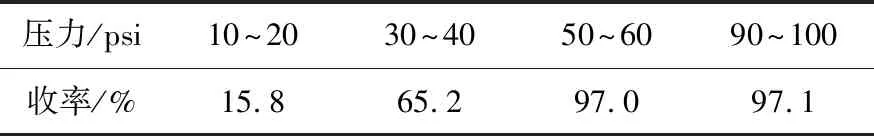
表3 氢气压力对收率的影响
由表3可以看出,随着压力的增加收率不断提高,当压力达到50~60psi后再继续增加压力不会再提高收率,因而压力确定在50~60psi比较合适.
2.2.2 Pt/C的用量对收率的影响
在氢气压力在50~60psi、反应温度在70~80 ℃、反应时间为24 h,考察了Pt/C的用量对收率的影响,见表4.

表4 Pt/C的用量对收率的影响
由表4可以看出,Pt/C的用量太少原料反应不完,随着Pt/C的用量增加收率也随着增加,当Pt/C的用量达到5.0%的时候原料已经反应完毕,再继续增加Pt/C的用量收率不会再继续增加.因此Pt/C的用量为5.0%.
2.2.3 反应温度对收率的影响
在氢气压力在50~60Psi、Pt/C的用量为5.0%、反应时间为24h,考察了反应温度对收率的影响,见表5.

表5 反应温度对收率的影响
*注:18h原料已经反应完.
由表5可以看出,升高反应温度收率也增加,当反应温度达到70~80 ℃后收率达到最大,如果再继续增加反应温度,反应时间会缩短但是收率会有所降低.因此反应温度确定在70~80 ℃.
2.3 化合物Ⅲ反应条件的确定
2.3.1 反应溶剂对关环反应的影响
在溴化氰的用量在1.1 mol/L、反应温度在10~20 ℃、反应时间为24 h下,考察了反应溶剂对收率的影响,见表6.

表6 反应溶剂对收率的影响
由表6可以看出,甲醇作为溶剂收率最高,因而选择甲醇作为反应溶剂.
2.3.2 溴化氰的用量对关环反应的影响
在甲醇作为反应溶剂、反应温度在10~20 ℃、反应时间为24h下,考察了溴化氰的用量对收率的影响,见表7.

表7 溴化氰的用量对收率的影响
由表7可以看出,当溴化氰的用量达到1.0 mol/L后继续增加其用量,对收率不会有影响,因而n(Ⅱ)∶n(BrCN)=1.0∶1.0.
2.3.3 纯化条件的确定
在纯度为83.2%粗品5.0g,考察了重结晶溶剂及溶剂体积对重结晶收率和纯度的影响,结果见表8.
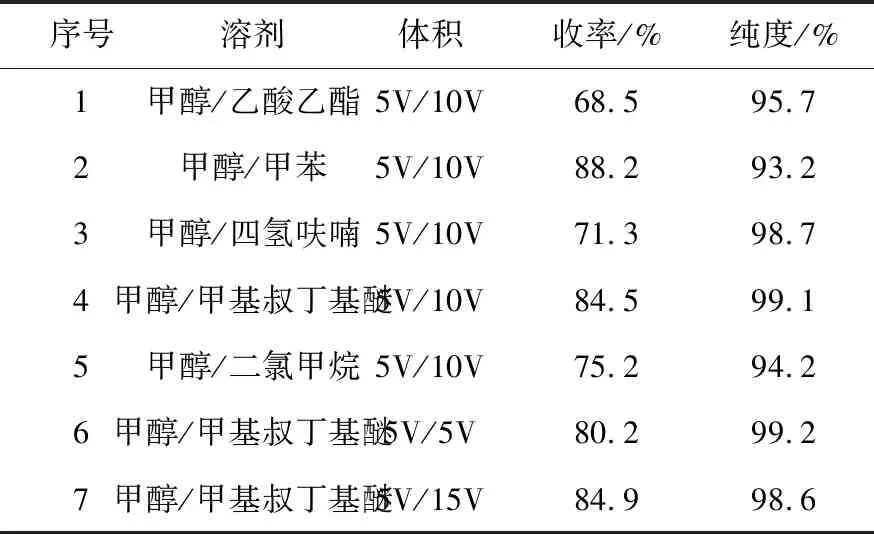
表8 溶剂对重结晶的收率和纯度的影响
由表8可以看出,甲醇/甲基叔丁基醚作为溶剂重结晶效果最好,增加甲基叔丁基醚的用量收率会增加同时产品纯度会随着降低,综合考虑收率和纯度,甲醇和甲基叔丁基醚的比例控制在1∶2比较合适.
3 结论
以2,6-二氯-3硝基吡啶为原料经取代、还原、环合步骤合成了2-氨基-3-新戊基-5-氯-3H-咪唑并[4,5-b]吡啶氢溴酸盐,纯度为99.1%,总收率为52.4%.
