Stanford B型主动脉夹层腔内隔绝术中导管校准法和标记导管校准法比较
2017-12-22张祥海闫红野王晓峰陈金华陆军军医大学大坪医院野战外科研究所放射科重庆400042
张祥海,周 林,闫红野,王晓峰,陈金华(陆军军医大学大坪医院野战外科研究所放射科,重庆 400042)
StanfordB型主动脉夹层腔内隔绝术中导管校准法和标记导管校准法比较
张祥海,周 林,闫红野,王晓峰,陈金华*
(陆军军医大学大坪医院野战外科研究所放射科,重庆 400042)
目的探讨导管校准和标记导管校法在Stanford B型主动脉夹层腔内隔绝术中测量主动脉直径的差异。方法收集30例接受经腔内隔绝术治疗的Standford B型主动脉夹层患者,分别以2种校准法测量左锁骨下动脉开口处主动脉直径,并将测量值与CTA测量结果进行对比。结果导管校准、标记导管校准、CTA测量值间差异有统计学意义(F=3.15,P<0.05)。两两比较显示,导管校准法与CTA、标记导管校准法间测量值差异均有统计学意义(P均<0.05),标记导管校准法与CTA间测量值差异无统计学意义(P>0.05)。以CTA测量值为金标准,Bland-Altman分析显示标记导管校准法与CTA测量法一致性较导管校准法更好。结论在Stanford B型主动脉夹层腔内隔绝术中,标记导管校准法的测量值接近CTA的测量值,优于导管校准法,可为支架的选择提供更加精准的数据。
动脉瘤,夹层; 腔内隔绝术;血管造影术,数字减影;测量
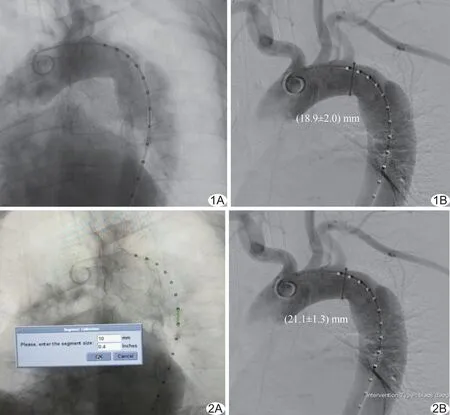
图1 导管校准法校准(A)及测量(B) 图2 标记导管校准法校准(A)和测量(B)
主动脉夹层病变死亡率高,是临床高度重视的大血管病变[1-2]。外科手术治疗主动脉夹层病变创伤大、死亡风险高[3-4];而主动脉夹层腔内隔绝术具有创伤小、安全性高、可以结合杂交手术治疗的优点,成为主动脉夹层的首选治疗方案[5-7]。进行主动脉夹层腔内隔绝术时,介入技师需精准测量血管直径、病变长度等,为手术医师选择手术方案、支架直径、锚定位置等提供依据[8-9]。目前,介入手术中主要测量方法有自动ISO校准法、自动TOD(床面和靶血管距离)校准法、导管校准法、标记导管校准法、球体校准法等,而不同测量方法各有优劣[10]。在Stanford B型主动脉夹层的介入测量中,综合考虑各测量方法的准确性、实用性、便捷性后,本研究选择导管校准法和标记导管校准法分别测量左锁骨下动脉开口处的主动脉直径,并将2组测量数据与CTA测量结果比较,旨在分析两种校准方法的差异性和准确率。
1 资料与方法
1.1 一般资料 收集2014年2月—2017年5月在本院确诊为Stanford B型主动脉夹层的患者30例,其中男19例,女11例,年龄32~65岁,平均(45.5±4.6)岁,均接受腔内隔绝术治疗主动脉夹层。
1.2 仪器与方法
1.2.1 CTA检查方法 采用GE 64排Lightspeed VCT,患者平卧,扫描范围自胸廓人口至耻骨联合。扫描参数:管电压120 kV,管电流400 mAs,层厚0.625 mm;增强扫描对比剂为碘克沙醇(320 mgI/ml),注射速率5 ml/s,剂量50~70 ml,采用团注对比剂追踪法监测主动脉腔内对比剂浓度,达到设定阈值(150 HU)时,嘱受检者屏气后开始扫描。
1.2.2 DSA引导介入治疗 采用GE Innova3100 DSA机为引导设备。全麻后穿刺患者的右股动脉或左肱动脉,将5F的黄金标记导管(COOK)送至升主动脉处,以20 ml/s注入40 ml对比剂(碘克沙醇,320 mgI/ml),在患者左侧位35°~48°暂停呼吸机下行胸主动脉造影,以显示左锁骨下动脉和夹层破口最佳的体位为手术操作位。透视下将覆膜支架输送装置导入降主动脉,定位支架位置,固定内鞘管,退出外鞘管,使覆膜血管支架自行打开释放。
1.3 介入影像测量 采用GE AW 4.4后处理工作站的Stenosis Analysis软件进行图像测量与分析。在图像中心区域,选择降主动脉段标记导管较平直的一段作为校准标尺[11],设定导管两侧壁间距离为5F(1.65 mm)及标记导管2个标记点间距离为10 mm作为校准长度分别校准后,测量左锁骨下动脉开口处的主动脉直径(图1、2)。由2名具有5年以上工作经验的介入技师各测量3次,取平均值。
1.4 CTA测量 CTA图像均能清晰显示血管主干及分支、血管夹层破口、血管真假腔等,符合临床影像诊断要求。将图像传至AW 4.4后处理工作站,观察冠状位、轴位、矢状位图像,由2名具有5年以上工作经验的CT技师测量左锁骨下动脉开口处的主动脉直径(图3),各自测量3次取平均值。
2 结果
导管校准法[(23.73±6.38)mm]、标记导管校准法[(27.07±5.88)mm]与CTA[(27.47±5.73)mm]测量主动脉直径的差异有统计学意义(F=3.15,P<0.05)。两两比较显示,导管校准法与CTA、标记导管校准法间测量值差异均有统计学意义(P均<0.05),标记导管校准法与CTA间测量值差异无统计学意义(P>0.05)。标记导管校准法与CTA测量值误差率为1.4%,导管校准法与CTA测量值误差率为13.6%。Bland-Altman分析显示,标记导管校准法的一致性界限(-9.09 vs -15.68)和偏差率[3.33%(1/30)vs 10.00%(3/30)]均小于导管校准法。在标记导管校准法测量数据的基础上增大15%~20%作为所选支架直径,术中支架均准确植入主动脉中,术后造影显示支架贴壁良好,覆盖近端夹层裂口,左锁骨下动脉和肾动脉等分支血管未受影响。
3 讨论
目前DSA是主动脉夹层疾病诊疗的金标准[12]。手术中,医师需找到夹层破口、分辨真假腔,定量测量病变长度,选择合适的支架以封闭夹层破口等[13],这些均需要对介入影像作精准测量来提供数据支持。但由受各类成像因素和设备参数设置的影响,图像存在失真、变形、放大等问题,而产生测量误差[14-15],给介入影像的准确测量带来困难。
既往关于Stanford B型主动脉夹层的研究[16-18]对测量方法的描述大多简略,或采用其他方法测量;对研究导管校准法和标记校准法的测量准确性和差异的报道鲜见。介入手术中,导管是最常用的造影器材,其走行于血管腔内,与血管病变有相似的影像放大率,因此常被作为校准标尺,计算出每个像素换算出的长度,成为介入测量的基础[19]。本研究在相同图像的中心区域,选取相同一段清晰显示的导管,按照导管两侧壁间距离和2个标记点间距离作为校准长度完成测量,减少了其他因素的干扰,使2种方法的测量值仅有校准标尺的差异。多种影像检查技术中,CTA能准确重建出血管细微形态结构,在其图像上测量血管直径、病变长度等参数的数值较精确,误差小,可作为测量的金标准[20-22]来评估其他测量方法的误差。本研究结果显示,标记导管校准法与CTA法对主动脉直径的测值更接近,2种测量技术差异性小,一致性较高,而常规导管校准法的测量值与CTA的测量值差异较大,在准确程度上逊于标记导管校准法,而在测量操作步骤和效率方面2种测量方法无明显区别。

图3 患者男,48岁,Stanford B型主动脉夹层,以冠状位图像测量左锁骨下动脉开口处主动脉直径作为标准值 A.冠状位图像; B.轴位图像; C.矢状位图像
标记导管校准法在主动脉夹层测量中具有准确、快捷、方便等优点,应用时辐射剂量和造影剂用量也较小,介入技师采用标记导管校准法测量病变血管,可获得更加精准的血管直径、病变长度等,为手术医师选择支架提供可靠依据,在主动脉夹层血管病变的治疗中具有重要的意义[23]。依据标记导管校准法测量主动脉值选取的支架释放后均能紧密贴合在血管壁上,较好封堵血管破口,未见支架移位、夹层破裂、对比剂明显外漏等问题,表明该测量法在测量、评估血管直径方面准确、可信。
总之,标记导管校准法测量动脉直径的准确性等同于CTA,在治疗即时性上优于CTA,可以替代CTA或导管校准法,运用于介入手术的精准化测量中。
[1] Thomas L, Jan B. Type B aortic dissection: A review of prognostic factors and meta-analysis of treatment options. Aorta, 2014,2(6):265-278.
[2] Nienaber A, Kische S, Rousseau H, et al. Endovascular repair of type B aortic dissection: Long-term results of the randomized investigation of stent grafts in aortic dissection trial. Circ Cardiovasc Interv, 2013,6(4):407-416.
[3] Khoynezhad A, Toluie S, Al-Atassi T. Treatment of the chronic type B aortic dissection: The pro-endovascular argument. Semin Thorac Cardiovasc Surg, 2017,29(2):131-136.
[4] 赵珺.导丝间歇式后拽法在Stanford B 型主动脉夹层腔内治疗中的价值.中国介入影像与治疗学,2006,3(3):214-216.
[5] Patel AY, Eagle KA, Vaishnava P. Acute type B aortic dissection: Insights from the international registry of acute aortic dissection. Ann Cardiothorac Surg, 2014,3(4):368-374.
[6] Parsa CJ, Williams JB, Bhattacharya SD, et al. Midterm results with thoracic endovascular aortic repair for chronic type B aortic dissection with associated aneurysm. Thorac Cardiov Sur, 2011,141(2):322-327.
[7] Chang YL. Endovascular repair in acute complicated type B aortic dissection: 3-year results from the valiant us investigational device exemption study. Korean J Thorac Cardiovasc Surg, 2017,50(3):137-143.
[8] 王会杰,黄光明.主动脉腔内隔绝术的DSA技术配合.中国现代医生,2011,49(20):94-95.
[9] 高宗恩,任晓萍,杭鹏,等.DSA测量技术误差与控制.中华放射学杂志,2005,39(10):1094-1097.
[10] 彭刚,曾勇明,李越.旋转DSA影像变形程度及测量误差的实验研究.中国医学影像技术,2010,26(1):33-35.
[11] 贲智进,盛红专.改良DSA测量技术在主腔内隔绝术中的应用.江苏医药,2010,36(20):2461-2462.
[12] 朱纯生,洪国斌,何强,等.运用自制模体定量评价三维数字减影血管造影测量误差的初步实验研究.中国医学影像学杂志, 2013,21(2):139-142.
[13] 谭延禄, 张红霞,张永杰.腔内隔绝术治疗胸主动脉夹层的临床应用.实用医技杂志,2007,14(2):147-148.
[14] 杨会军, 高斌,胡永胜.提高DSA测量精度方法的研究.安徽医学,2011,32(3):350-353.
[15] 张祖建,张勇,陈淑君.MSCTA、2D DSA和3D DSA对颈动脉狭窄测量差异比较的实验研究.重庆医学,2015,44(3):359-361,365.
[16] 王家平,杨达宽,杨青,等.带膜血管腔内支架植入术治疗Stanford B型胸主动脉夹层(附29例报告).中国介入影像与治疗学,2006,3(2):130-133.
[17] 肖志明.主动脉夹层影像解剖学分析与诊断及治疗评价.兰州:兰州大学,2010:19-24.
[18] 曾宪强, 郭广春,耿云平.CT断层和重建及DSA在主动脉腔内支架置入前的研究.医药论坛杂志,2008,29(19):110-111.
[19] 曾启龙,牡丹.3种不同测量技术在DSA中的应用与分析.医疗卫生装备,2010,31(10):92-93.
[20] Moritz JD, Rotermund S, Keating DP, et al. Infrarenal abdominal aortic aneurysms: Implications of CT evaluation of size and configuration for placement of endovascular aortic grafts. Radiology, 1996,198(2):463-466.
[21] Beebe HG, Jackson T, Pigott JP. Aortic aneurysm morphology for planning endovascular aortic grafts: Limitations of conventional imaging methods. J Endovasc Surg, 1995,2(2):139-148.
[22] 吴博云,杨卷红,田宏哲,等.MSCTA对Stanford B型主动脉夹层行腔内隔绝治疗的指导价值.实用放射学杂志,2015,31(2):305-308.
[23] 陈刚,李德生,王学刚,等.血管内覆膜支架介入治疗主动脉夹层6例分析.中国误诊学杂志,2009,9(7):1732.
ComparisonofcathetercalibrationmethodandcentimetersizingcathetercalibrationmethodinendovasculargraftexclusionforStanfordtypeBaorticdissection
ZHANGXianghai,ZHOULin,YANHongye,WANGXiaofeng,CHENJinhua*
(DepartmentofRadiology,ResearchInstituteofSurgery,DapingHospital,ArmyMedicalUniversity,Chongqing400042,China)
ObjectiveTo explore the differences of aortic diameter measured by catheter calibration method and centimeter sizing catheter calibration method in endovascular graft exclusion for Stanford type B aortic dissection.MethodsA total of 30 patients with Stanford B type aortic dissections treated with endovascular graft exclusion were measured with the two calibration methods to measure aortic diameters at left subclavicular artery position. The measurement parameters were compared with CTA measurement results.ResultsStatistical differences of measurement parameters were found among catheter calibration, centimeter sizing catheter calibration and CTA (F=3.15,P<0.05), and paired comparison showed statistical differences between catheter calibration method and CTA result (P<0.05), and between the results of catheter calibration method and centimeter sizing catheter calibration method (P<0.05), while no statistical difference was found between centimeter sizing catheter calibration method and CTA result (P>0.05). Taking CTA as golden standard method,Bland-Altmananalysis indicated that the centimeter sizing catheter calibration method exerted better consistency with CTA.ConclusionThe measurement value of centimeter sizing catheter calibration method is identical to the CTA measurement result, and superior to catheter calibration method for precise stent selection in Stanford type B aortic dissection.
Aneurysm, dissecting; Endovascular graft exclusion; Angiography, digital subtraction; Measurement
张祥海(1982—),男,重庆人,本科,技师。研究方向:介入影像技术。E-mail: ocean218@163.com
陈金华,陆军军医大学大坪医院野战外科研究所放射科,400042。E-mail: jhchenmri@163.com
2017-07-02
2017-10-12
10.13929/j.1672-8475.201707001
R543.1; R816
A
1672-8475(2017)12-0720-04
