心率变异性与磁导航指导下心房颤动射频消融术后复发的关系
2017-12-20承燕李库林郑杰刘晓宇张常莹李宗斌过瑾
承燕 李库林 郑杰 刘晓宇 张常莹 李宗斌 过瑾
赵晓溪 郁志明 王如兴
论著
心率变异性与磁导航指导下心房颤动射频消融术后复发的关系
承燕 李库林 郑杰 刘晓宇 张常莹 李宗斌 过瑾
赵晓溪 郁志明 王如兴
目的探索心率变异性与磁导航指导下心房颤动(atrial fibrillation,AF)射频消融术后复发的关系。方法顺序入选58例磁导航指导下AF射频消融术患者,随访心电图和动态心电图,分析心率变异性,观察AF复发情况。AF复发定义为:手术3个月后发生超过30 s的房速、房扑或AF。结果最终纳入50例AF患者,平均随访(15.56±4.60)个月,AF复发20例,平均复发时间(6.05±4.42)个月。AF复发组术后3个月相邻R-R间期差值的均方根、相邻R-R间期差值>50 ms的间期占总R-R间期的百分比和高频成分较未复发组显著高(P值分别为0.036、0.045和0.015),而低频/高频(LF/HF)显著低(P=0.015);COX生存分析显示LF/HF是AF复发的独立危险因素(P=0.010)。结论磁导航指导下AF射频消融术后3个月的LF/HF可作为AF复发的独立预测因子。
心房颤动;射频消融术;心率变异性;复发
自主神经系统功能紊乱通过增加心房电活动的异质性促发和维持心房颤动(atrial fibrillation,AF)[1]。心率变异性(heart rate variability,HRV)分析是目前定量分析自主神经功能的重要方法。组织病理学表明肺静脉前庭含有大量的自主神经,AF射频消融术后可引起HRV的变化。一些小样本量的研究通过分析HRV发现AF射频消融术后产生的心房去神经效应有助于提高阵发性AF的远期成功率[2-4]。然而,这些研究在手术方式上存在一定的差异,不同术者射频消融术后AF的复发率亦有差异。近年来磁导航系统应用于AF射频消融术后HRV分析尚无报道。本研究通过分析AF射频消融患者术后HRV并随访复发情况,探索HRV作为磁导航指导下AF射频消融术后AF复发预测因素的可行性。
1 资料和方法
1.1 研究对象
入选标准:2015年7月至2016年9月于我院行磁导航指导下AF射频消融术的患者。排除标准:术后3个月内发作持续性房颤、非首次射频消融术及术后行起搏器植入的患者。
1.2 AF射频消融围手术期处理
1.2.1 术前准备 术前华法林或达比加群酯抗凝、抗心律失常(包括β受体阻滞剂、胺碘酮或普罗帕酮)、保护食管胃黏膜(质子泵抑制剂),术前1 d行经食管心脏超声排除左心房血栓。
1.2.2 AF射频消融术 心脏三维标测系统(CARTO)指导下磁导航大头消融导管消融。局部麻醉,穿刺左右股静脉置入冠状窦电极和右心室电极。穿刺右侧股静脉置入Swartz鞘,穿刺房间隔一次进入左心房并分别行左右肺静脉造影。通过鞘管放入磁导航消融导管,固定在推送器上,磁头运行至导航位,结合心房造影和左心房建模,行左右肺静脉前庭电隔离术,温度43℃,功率前壁35~40 W,后壁30~35 W ,每点消融时间30~60 s或A波振幅下降80%,盐水灌注流量17 mL/min(消融)和2 mL/min(未消融)。LASSO电极确认肺静脉电隔离。持续性和长程持续性AF加行左心房顶部线性和二尖瓣峡部线性消融,消融后若AF仍持续发作,行体外电复律。
1.2.3 术后用药 术后常规华法林或达比加群酯抗凝2个月,2个月后CHA2DS2-Vasc≥2(男)或CHA2DS2-Vasc≥3(女)则继续抗凝治疗。术后抗心律失常药物至少服用3个月,质子泵抑制剂服用2周。
1.3 随访
无论有无AF复发,术后3个月、6个月、12 个月常规复查12导联心电图及24 h动态心电图,若有心悸症状随时行12导联心电图检查。无AF复发者12个月后每6个月电话随访一次,若患者有症状或AF复发,主动门诊随访。AF复发定义为:超过30 s的房速、房扑或AF。消融术后3个月内定义为空白期。根据随访结果,入选患者分为AF未复发组和AF复发组。
1.4 HRV分析
采用GE SeerLight动态数字心电记录仪,剔除早搏和其他非窦性心律后分析HRV指标,包括窦性心律的平均R-R间期(NN间期);时域分析参数:R-R间期的标准差(SDNN)、相邻R-R间期差值的均方根(rMSSD)和相邻R-R间期差值>50 ms的间期占总R-R间期的百分比(PNN50);频域分析参数:低频成分(LF,0.04~0.15 Hz)、高频成分(HF,0.15~0.4 Hz)及低频/高频(LF/HF)。
1.5 统计学处理

2 结果
2.1 患者的一般临床特征
2015年7月至2016年9月我科行磁导航指导下AF射频消融术患者58例,排除术后3个月内再发持续性AF、非首次射频消融术及术后起搏器植入患者共8例,最终纳入研究对象50例;其中男30例、女20例,年龄25~76(51.00±11.82)岁,合并原发性高血压患者33例,合并冠心病患者5例,合并脑卒中病史患者3例,阵发性AF 32例,持续性AF 10例,长程持续性AF 8例(阵发性AF:30 s≤持续时间≤7 d的AF;持续性AF:7 d<持续时间<1年的AF;长程持续性AF:持续时间≥1年的AF),无心力衰竭、糖尿病、甲状腺功能亢进以及心脏瓣膜病患者。术后平均随访12~27(15.56±4.60)个月,AF复发20例,平均复发时间3~19(6.05±4.42)个月。AF复发组和AF未复发组在性别、房颤类型、左心房内径、ACEI/ARB药物使用、原发性高血压、冠心病、脑卒中史方面差异无统计学意义(P>0.05);相比于AF未复发组,AF复发组年龄较小(P=0.003),BMI较高(P=0.028)。见表1。
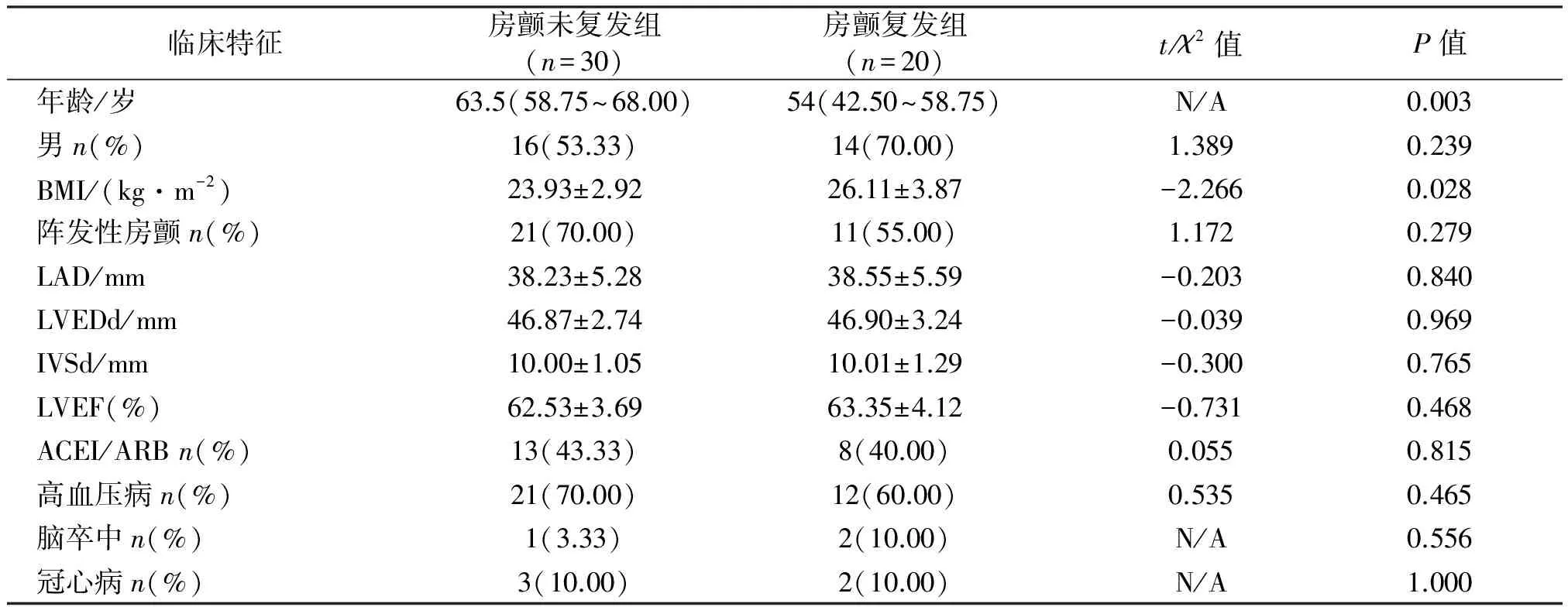
表1 房颤未复发组和房颤复发组患者一般临床特征
BMI:体质量指数;LAD:左心房内径;LVEDd:左心室舒张末内径;IVSd:室间隔厚度;LVEF:左心室射血分数;ACEI:血管紧张素酶抑制剂;ARB:血管紧张素受体拮抗剂
2.2 HRV分析
术后3个月的HRV分析显示,AF复发组与AF未复发组相比,NN间期、SDNN、LF差异无统计学意义(P>0.05),而rMSSD、PNN50、HF较高,LF/HF较低,且差异有统计学意义(P值分别为0.036、0.045、0.015和0.015)。见表2。Pearson相关性分析显示rMSSD、PNN50、LF/HF与AF复发的相关系数分别为0.298、0.284和-0.346,有统计学意义(P值分别为0.036、0.045和0.015);PNN50与rMSSD相关系数0.573,rMSSD与HF相关系数0.599,PNN50与HF相关系数0.690,有统计学意义(均为P=0.000)。COX生存分析提示术后3个月LF/HF和rMSSD是AF复发的独立危险因素[Exp(B)分别为0.185和1.089,95%CI分别为0.051~0.673和1.002~1.183,P分别为0.010和0.045]。见表3。LH/HF较rMSSD与AF复发相关性更高。
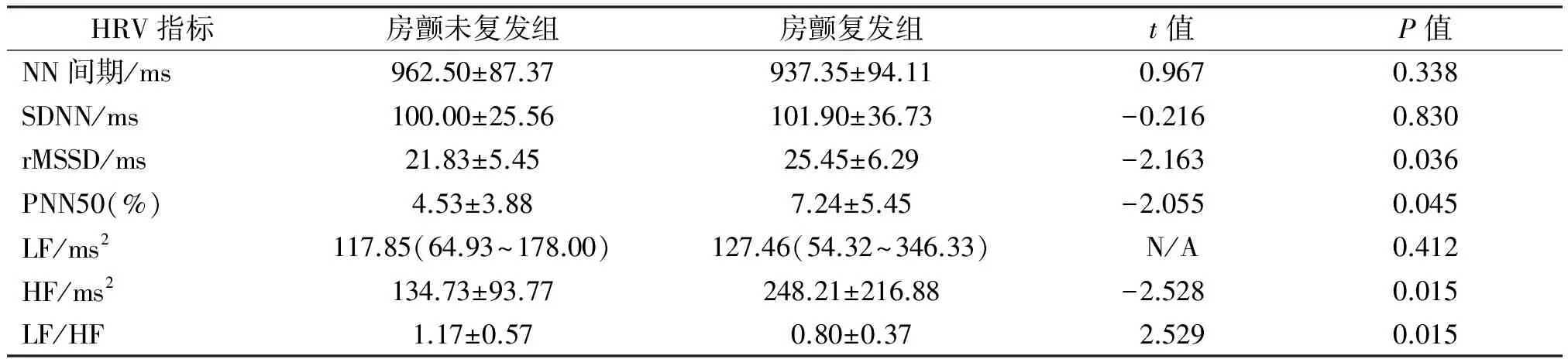
表2 房颤未复发组和房颤复发组HRV分析
NN间期:窦性心律的平均R-R间期;SDNN:R-R间期的标准差;rMSSD:相邻R-R间期差值的均方根;PNN50:相邻R-R间期差值>50 ms的间期占总R-R间期的百分比;LF:低频成分;HF:高频成分;LF/HF:低频/高频

表3 磁导航下房颤射频消融术后复发的COX生存分析
BMI:体质量指数;LAD:左心房内径;rMSSD:相邻R-R间期差值的均方根;PNN50:相邻R-R间期差值>50 ms的间期占总R-R间期的百分比;LF/HF:低频/高频
3 讨论
自主神经系统影响着心房的动作电位和不应期,约1/3的阵发性AF患者以及70%的年轻患者都存在明确的交感或迷走神经促发因素[5]。研究表明调节自主神经功能对AF的治疗有一定帮助,如神经节丛消融术、肾去交感神经术、刺激颈迷走神经术、压力反射刺激和皮肤刺激等[6]。目前AF主流手术方式还是环肺静脉电隔离术,肺静脉前庭含有大量的自主神经,AF射频消融术后可引起自主神经功能的变化。HRV分析通过研究逐次心动周期的时间变化反映自主神经功能,是目前公认的评估自主神经活动的定量指标之一。既往研究表明阵发性AF患者环肺静脉电隔离术后HRV降低,一定程度上达到左房去除迷走神经的作用,提示其可能为射频消融治疗AF的机制之一[7-8]。常栋等[2]发现AF射频消融术后HRV较术前降低,术后第2天SDNN可有效预测手术疗效。但是术后第2天存在心房局部急性损伤、炎症等因素的影响,均对自主神经功能有影响,此时评价HRV对AF复发的预测作用的有效性值得进一步论证。
研究表明AF术后使用抗心律失常药物可降低AF早期复发率[9]。临床工作中患者术后短期抗心律失常药物应用十分普遍,故不可避免地存在药物对HRV的影响(其中胺碘酮半衰期较长,要完全回避药物的影响很困难)。本研究中患者术前及术后3个月内均使用抗心律失常药物,而手术3个月后根据患者症状和心律失常情况停用或继续使用抗心律失常药物。考虑到手术3个月后用药情况差异较大,而手术3个月内有射频消融所致的损伤炎症及持续性房颤术后心房顿抑等因素的影响,故本研究仅分析术后3个月HRV对AF射频消融术疗效的预测价值。目前临床使用的HRV分析多为时域分析法和频域分析法。心脏对迷走神经的反应相对于交感神经迅速,一般刺激后400 ms内出现最大效应,刺激停止后5 s之内即可恢复,而交感神经起效延迟时间达5 s左右,并可持续20~30 s,故可通过研究心动周期的时间变化来反映交感和迷走神经的活动情况。rMSSD和PNN50通过计算相邻R-R间期差值的均方根和相邻R-R间期差值>50 ms的间期占总R-R间期的百分比来体现心率快速变化成分,反映迷走神经活动情况。HF阻断迷走神经活性时显著降低,也反映迷走神经活动。本研究分析HRV,反映迷走神经活动的指标(rMSSD、PNN50和HF)间均有相关性。本研究发现AF未复发组术后3个月rMSSD、PNN50和HF均较复发组低,提示成功的AF射频消融在术后3个月仍能维持其去迷走效应,并可能是其治疗AF的机制之一,这与非磁导航指导下AF射频消融术的研究结果一致[10]。COX生存分析提示术后3个月的LF/HF和rMSSD与AF复发独立相关,LF/HF预测AF射频消融术疗效的价值较rMSSD高,可以指导患者的随访,这在临床上有一定的应用价值。肺静脉前庭的免疫组化染色提示此处的神经丛同时有肾上腺素能纤维和胆碱能纤维[11]。LH/HF之所以比rMSSD的预测价值高,原因可能是环肺静脉电隔离不仅损伤胆碱能神经纤维,同时也损伤肾上腺素能神经纤维,所以反映交感迷走神经平衡情况的指标LH/HF更能预测术后AF复发,但其具体机制需要进一步研究。
随着科技的进步,“绿色”射频消融越来越受关注。磁导航指导下AF射频消融术能够减少射线曝光时间,有很好的安全性和有效性,且学习曲线较短,临床成功率与常规手动操作消融相似[12]。本研究提示磁导航指导下AF射频消融术后对HRV的影响与手动操作也相似。本研究不仅纳入了阵发性AF患者,同时也纳入了持续性和长程持续性AF患者,随访时间较长。既往研究提示阵发性AF的手术成功率远高于持续性AF。本研究中阵发性AF手术成功率66%,持续性AF为50%,两者未达统计学差异,考虑为样本量较小所致。研究人群的主要并发症为原发性高血压。患者药物控制血压良好,无明显室间隔增厚及高血压心脏病表现,故研究中高血压对AF复发并无显著影响。虽然传统认为高龄是AF复发的一个预测因素,但是既往研究结果并不一致,且均为小样本量研究,对高龄的定义也不同,而且一些研究表明高龄患者行AF射频消融术是安全有效的[13-14]。本研究中患者年龄基本小于75岁,AF未复发组的年龄反而较大,提示对于75岁以下的AF患者,术后复发可能并不与较大的年龄相关。
总之,磁导航指导下AF射频消融术对HRV的影响与手动操作相似。AF射频消融术后3个月可行HRV分析,LF/HF与AF复发独立相关,可作为手术疗效的独立预测因子。持续的去神经效应可能与AF射频消融术的成功相关。AF射频消融与心脏自主神经系统的关系仍需要大样本的临床研究进一步证实。
[1] Kirchhof P, Benussi S, Kotecha D, et al.2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS[J]. Eur Heart J, 2016, 37(38):2893-2962.
[2] 常栋,褚振亮,丛培鑫,等.去神经效应对环肺静脉消融治疗阵发性心房颤动远期疗效影响[J]. 中华心律失常学杂志, 2012, 16(2):87-92.
[3] Seaborn GE, Todd K, Michael KA, et al.Heart rate variability and procedural outcome in catheter ablation for atrial fibrillation[J]. Ann Noninvasive Electrocardiol,2014, 19(1):23-33.
[4] Kang KW, Kim TH, Park J, et al.Long-term changes in heart rate variability after radiofrequency catheter ablation for atrial fibrillation: 1-year follow-up study with irrigation tip catheter[J]. J Cardiovasc Electrophysiol, 2014, 25(7):693-700.
[5] Fabritz L, Guasch E, Antoniades C, et al.Expert consensus document: Defining the major health modifiers causing atrial fibrillation: a roadmap to underpin personalized prevention and treatment[J]. Nat Rev Cardiol, 2016, 13(4):230-237.
[6] Chen PS, Chen LS, Fishbein MC, et al.Role of the autonomic nervous system in atrial fibrillation: pathophysiology and therapy[J]. Circ Res, 2014, 114(9):1500-1515.
[7] 居维竹,陈明龙,杨兵, 等.左房线性消融治疗阵发性心房颤动对心率变异性的影响[J]. 中国心脏起搏与心电生理杂志, 2007, 21(3):233-235.
[8] 陶四明,郑甲林,李建美,等.环肺静脉前庭电隔离对阵发性心房颤动患者消融术后心率的影响[J]. 中国心血管病研究, 2012, 10(2):127-130.
[9] Leong-Sit P, Roux JF, Zado E, et al.Antiarrhythmics after ablation of atrial fibrillation (5A Study): six-month follow-up study[J]. Circ Arrhythm Electrophysiol, 2011, 4(1):11-14.
[10] 任春霖,陈志勇.阵发性房颤患者环肺静脉消融术前术后心率变异性变化及其与复发的关系[J]. 心血管康复医学杂志, 2017, 26(1):78-82.
[11] Tan AY, Li H, Wachsmann-Hogiu S, et al.Autonomic innervation and segmental muscular disconnections at the human pulmonary vein-atrial junction: implications for catheter ablation of atrial-pulmonary vein junction[J]. J Am Coll Cardiol, 2006, 48(1):132-143.
[12] 郑杰,李库林,刘晓宇,等.磁导航系统指导下心房颤动导管消融学习曲线期间有效性和安全性分析[J]. 实用心电学杂志, 2016, 25(2):96-100.
[13] Metzner I, Wissner E, Tilz RR, et al.Ablation of atrial fibrillation in patients≥75 years: long-term clinical outcome and safety[J]. Europace, 2016, 18(4):543-549.
[14] Nademanee K., Amnueypol M, Lee F, et al.Benefits and risks of catheter ablation in elderly patients with atrial fibrillation[J]. Heart Rhythm, 2015, 12(1):44-51.
Thecorrelationbetweenheartratevariabilityandoutcomeofradiofrequencycatheterablationguidedbymagneticnavigationsystemforpatientswithatrialfibrillation
ChengYan,LiKu-lin,ZhengJie,LiuXiao-yu,ZhangChang-ying,LiZong-bin,GuoJin,ZhaoXiao-xi,YuZhi-ming,WangRu-xing
(Department of Cardiology, Wuxi People’s Hospital Affiliated to Nanjing Medical University, Wuxi Jiangsu 214023, China)
ObjectiveTo explore the relationship between heart rate variability(HRV) and outcome of radiofrequency catheter ablation(RCA) guided by magnetic navigation system for patients with atrial fibrillation(AF).MethodsFifty-eight AF patients who had undergone RCA guided by magnetic navigation system were enrolled consecutively. ECG and Holter recordings were performed, and HRV was analyzed. The recurrence of AF was observed. AF recurrence was defined as recurrence of atrial tachycardia, atrial flutter or AF lasting longer than 30 seconds three months after the procedure.ResultsFifty patients were enrolled finally, and were followed up for an average of (15.56±4.60) months. AF recurrence was found in 20 patients and the mean recurrence time was (6.05±4.42) months after the procedure. In the AF recurrence group, the root mean square of successive R-R interval difference, proportion of R-R intervals differing from their neighbors by >50 ms, and high-frequency component three months after the procedure were significantly higher than those in the non-recurrence group(P=0.036, 0.045 and 0.015, respectively) while low-/high-frequency ratio(LF/HF) was significantly lower(P=0.015). COX survival analysis revealed that LF/HF was an independent risk factor of AF recurrence(P=0.010).ConclusionLF/HF three months after RCA guided by magnetic navigation system for AF patients may be an independent predictor of AF recurrence.
atrial fibrillation; radiofrequency catheter ablation; heart rate variability; recurrence
无锡市医院管理中心重点研究项目(YGZXZ1522);无锡市青年医学人才项目(QNRC010)
214023 江苏 无锡,南京医科大学附属无锡人民医院心内科
承燕,医学博士,主治医师,从事心血管内科临床工作。
王如兴,E-mail:ruxingw@aliyun.com
R541.7
A
2095-9354(2017)06-0408-05
10.13308/j.issn.2095-9354.2017.06.005
2017-10-31) (本文编辑:郭欣)
