有机物燃烧二十规律
2017-12-14宁夏王开山
宁夏 王开山
有机物燃烧二十规律

一、与耗氧量有关的规律
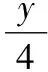

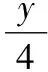
二、与气态烃燃烧前后压强变化有关的规律
规律4.温度不变(高于100℃),气态烃CxHy完全燃烧,反应前后密闭容器内压强大小的判断:
(1)当y<4时,反应后压强减小;
(2)当y=4时,反应后压强不变;
(3)当y>4时,反应后压强增大。
三、根据燃烧后CO2和H2O(g)的体积比确定有机物种类的规律
规律5.同温同压下,生成的CO2和H2O(g)的体积比为1∶1时,可能为环烷烃、烯烃、醛、酮、羧酸、酯、葡萄糖、果糖等C、H原子个数比为1∶2的物质。
规律6.同温同压下,生成的CO2和H2O(g)的体积比为1∶2时,可能为甲烷、甲醇、尿素等C、H原子个数比为1∶4的物质。
规律7.同温同压下,生成的CO2和H2O(g)的体积比为2∶1时,可能为乙炔、苯、苯乙烯、苯酚等C、H原子数相等的物质。
四、与C、H元素含量有关的规律
规律8.当有机物A、B以任意比例混合,若其总质量不变,完全燃烧产生的水或二氧化碳量也不变,则A和B中的所含H的质量分数或C的质量分数均相同。
规律9.当有机物A、B以任意比例混合,若其总物质的量不变,完全燃烧产生的水或二氧化碳量也不变,则相同物质的量的A和B中所含H的物质的量或C的物质的量均相同。
规律10.当有机物A、B以任意比例混合,若其总质量不变,完全燃烧时其耗氧量为定值,则两者互为同分异构体或两者的最简式相同。
五、与确定有机混合物组成有关的规律
规律11.总物质的量为1 mol的烃A和烃B以任意比例混合,燃烧生成CO2和H2O的物质的量分别为m和n,则有机物A、B的分子式可能为以下几种情况:
(1)C原子数都为m,H原子数一个大于2n一个小于2n。如C2H2和C2H6等。
(2)H原子数都为2n,C原子数一个大于m一个小于m。如CH4和C3H4等。
(3)C原子数一个大于m一个小于m,H原子数一个大于2n一个小于2n。如CH4和C3H8等。
六、与两种有机物相对分子质量之差有关的规律
规律12.完全燃烧等物质的量的烃或烃的含氧衍生物A和B,当消耗氧气的量相等时,A和B的分子量相差可能为8n或18n或44n(n为正整数)。
七、与有机物中C、H原子数有关的规律
A、B两种有机物,相对分子质量不同,不论以何种比例进行混合,只要总物质的量保持一定,则完全燃烧时根据耗氧量与生成的CO2和H2O的量之间的关系可得出以下关于两种有机物中C、H原子数的规律。
规律13.若生成的CO2的物质的量不变,则两者中的碳原子数必然相等,如:C2H4与C2H4O、C2H4O2等。
规律14.若生成的H2O的物质的量不变,则两者中的氢原子数必然相等,如:CH4、CH4O、C2H4O、C2H4O2等。
规律15.若生成的CO2和H2O的量不变,则两者中的碳、氢原子数都相等,如:CH4、CH4O;C2H4、C2H4O、C2H4O2等。
规律16.若消耗的氧气和生成的CO2的量保持不变,两者含碳原子数必相等,分子中必相差n个H2O,如:C2H4与C2H6O等。
规律17.若消耗的氧气和生成的H2O的量保持不变,则两者含氢原子数必相等,分子中必相差n个CO2,如:CH4与C2H4O2等。
八、根据耗氧体积与产生CO2体积的相对大小确定有机物分子式一般形式的规律
规律18.燃烧消耗氧气体积大于生成CO2的体积,其一般形式为(CxHy)m(H2O)n。
规律19.燃烧消耗氧气体积等于生成CO2的体积,其一般形式为Cx(H2O)n。
规律20.燃烧消耗氧气体积小于生成CO2的体积,其一般形式为(CxOy)m(H2O)n。
例题赏析
例1相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是
( )
A.C3H4和C2H6B.C3H6和C3H8O
C.C3H6O2和C3H8O D.C3H8O和C4H6O2
解析:根据规律1,A中C3H4的耗氧量多于C2H6的耗氧量;根据规律3,B和D中的C3H8O可改写为C3H6·(H2O),C中的C3H6O2可改为C3H2·(H2O)2,D中的C4H6O2可改为C3H6·(CO2),消耗氧气量相同的是B和D。
答案:B、D
例2等质量的下列各类烃,分别完全燃烧时,其耗氧量最大的是
( )
A.C6H6B.C7H8
C.C4H10D.C3H8

答案:D
例3两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中符合此条件的是
( )
A.CH4和C2H4B.CH4和C3H6
C.C2H4和C3H4D.C2H2和C3H6
解析:根据规律4,当反应后温度高于100℃时,气态烃氢原子数为4时,反应前后密闭容器内压强不变,即反应前后气体体积不变。符合此条件的是A和C。
答案:A、C
例4下列各组烃的混合物,只要总质量一定,无论按什么比例混合,完全燃烧后生成的CO2和H2O都是恒量的是
( )
A.C2H2和C2H4B.C2H4和C4H6
C.C3H8和C3H6D.C6H6和C2H2
解析:根据规律8,混合烃各组分中C和H的质量分数分别相同时,即两种烃的最简式是一样的。D选项符合题意。
答案:D
例5有机物A、B只可能为烃或烃的含氧衍生物,等物质的量的A和B完全燃烧时,消耗氧气的量相等,则A和B的分子量相差不可能为(n为正整数)
( )
A.8nB.14n
C.18nD.44n
解析:根据规律12,A和B的分子量相差不可能为14n。解答如下:
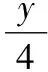
答案:B
例620 mL由分子中碳原子数相同的两种气态烃组成的混合物,与过量的氧气混合后完全燃烧,当产物通过浓硫酸时,体积减少30 mL,然后通过碱石灰,体积减少40 mL(气体体积均在同温同压下测得)。这种混合物的组成可能为
( )
A.CH4和C2H4B.C2H4和C2H6
C.C2H2和C2H4D.CH4和C2H2
解析:通过浓硫酸体积减少的气体为烃燃烧生成的水蒸气,通过碱石灰体积减少的气体为烃燃烧生成的二氧化碳。20 mL该烃完全燃烧生成二氧化碳40 mL、水蒸气30 mL,令烃的平均组成为CxHy,则:
根据C原子守恒有:20x=40,故x=2,
根据H原子守恒有:20y=30×2,故y=3,
故该烃的平均组成为C2H3。根据规律11,该烃一定含有C2H2,可能含有C2H4或C2H6。
答案:C
例7某有机物完全燃烧,消耗氧气体积等于生成CO2的体积,该有机物可能是
( )
A.C3H8O B.C2H4O2
C.C4H8O D.H2C2O4
解析:分别根据规律18、规律20、规律19可知,C3H8O和C4H8O完全燃烧时,消耗氧气体积大于生成CO2的体积;H2C2O4完全燃烧时,消耗氧气体积小于生成CO2的体积;C2H4O2完全燃烧时,消耗氧气体积等于生成CO2的体积。

宁夏育才中学)
