红麻液泡膜质子泵H+-PPase(Hcvp1)基因的克隆、序列分析和表达
2017-12-12李德芳陈安国唐慧娟李建军黄思齐
李 辉,李德芳,陈安国,唐慧娟,李建军,黄思齐
(中国农业科学院 麻类研究所,湖南 长沙 410205)
土壤的盐碱化是一个世界性的难题,全球盐渍土面积约10亿hm2,中国盐渍土面积约占世界盐渍土面积的10%[1-3]。随着人类活动的增加,环境的恶化,不合理的灌溉等因素使盐碱化土地的面积不断扩大。随着世界人口的不断增加,对粮食的需求也不断增加[4-5],人口、粮食、耕地的矛盾不断加剧,所以探索农作物的耐盐机理,培育耐盐品种是一项十分重要的任务。
植物在进化过程中形成了各种生理生化机制来适应盐胁迫,其中盐离子的转运和吸收是一个很重要的耐盐机制。液泡是成熟植物细胞中最大的细胞器,在细胞渗透压的调节、离子的吸收和转运、有毒离子的区域化以及信号转导系统的调控等方面具有重要作用[6-7],而液泡膜上的质子泵是实现这些生物功能的关键因素。定位于液泡膜上的H+-PPase的质子泵,能够利用焦磷酸(PPi)为底物,催化H+由细胞质进入液泡,形成电化学梯度,用于各种离子的运输和积累,维持细胞的离子平衡和渗透压,保证植物能够在盐胁迫下正常生长[8-9]。H+-PPase基因已经从多种植物中得到了克隆,如黄瓜、玉米、梭梭、陆地棉、费尔干猪毛菜、刚毛柽柳等[10-15]。大量的研究表明,通过对H+-PPase基因的遗传转化能够显著提高转基因作物的耐盐性。Gaxiola等[16]在2001年首次将AVP1 基因转入拟南芥中,结果发现,超表达AVP1 基因的转基因植株抗盐性得到增强。Duan等[17]通过在烟草中过量表达液泡膜H+-PPase基因,发现在盐胁迫下转基因烟草比野生型烟草叶肉细胞液泡中的Na+含量更高,耐盐性更强。
红麻(Hibiscuscannabinus)是一年生韧皮纤维作物。红麻纤维是重要的纺织原料,可以用于地毯,麻袋的生产,随着红麻多用途开发利用的研究,红麻还可以用于建筑板材、纸浆、饲料、麻骨炭等方面[18]。随着人们对粮食需求的不断增加,红麻的生产必须向盐碱地、滩涂、干旱坡地转移而避免与粮棉油争地。所以对红麻耐盐机理的探索,培育红麻耐盐品种对红麻产业的发展具有重要意义。目前,红麻的H+-PPase基因还未见报道,本研究从红麻耐盐转录组测序结果中发现了该基因,克隆了其全长cDNA序列,并对该基因进行了盐胁迫表达分析,这将为红麻耐盐分子设计育种奠定坚实的基础。
1 材料和方法
1.1 试验材料和试剂
中红麻16号的种子由中国农业科学院麻类研究所红麻育种课题组提供。选取籽粒饱满,大小均匀的种子,消毒,播种在发芽盒,置于光照培养箱,昼夜温度为28,26 ℃,光照13 h/d,培养7 d后,选取植株健壮,长势一致的红麻幼苗,移入1/2 Hoagland 营养液中继续培养,每天更换营养液。在营养液中培养5 d后进行NaCl胁迫处理,NaCl浓度梯度为0,75,150,250 mmol/L。每个处理设置3个重复,每个重复选用10株幼苗。NaCl胁迫处理5 d后取样,每个处理选取3株幼苗叶片,液氮速冻后保存在-80 ℃冰箱,用于总RNA的提取。
TRIzol购自Invitrogen 公司, Reverse Transcriptase、Rever Transcriptase inhibitor、Power2(SYBR Real-time PCR Premixture、pMD19-T载体购自TaKaRa 公司,DH5α感受态细胞购自天根生化科技有限公司;其余试剂为国产分析纯。
1.2 引物设计
依据红麻转录组序列利用Primer premier 5.0进行引物设计,NCBI Blast验证引物准确性,序列由上海生工合成。基因克隆的引物序列:Primer-F(5′-3′):ATGTCGGATCATGGATTTA;Primer-R(5′-3′):
TCATGGTTCGTGTTTAAGGA。
1.3 总RNA的提取
参照天根生化科技有限公司,植物总RNA提取试剂盒的说明书提取总RNA, 然后用1.0%的琼脂糖凝胶电泳检测提取总RNA的完整性和纯度。
1.4 Hcvp1基因的克隆
提取250 mmol/L NaCl胁迫下红麻幼苗叶片的总RNA,并进行反转录合成首链cDNA, 以1 μL反转录产物为模板进行PCR扩增。PCR反应体系:10×LA PCR Buffer(Mg2+plus) 2.5 μL,LATaq(TaKaRa) 0.25 μL, dNTP(2.5 mmol/mL)1 μL,F-primer(10 μmol/mL)0.25 μL,R-Primer(10 μmol/mL)0.25 μL,cDNA 1 μL,dH2O 补足25 μL。PCR反应程序:94 ℃ 2 min;94 ℃ 30 s,55 ℃ 30 s,72 ℃ 60 s,30个循环;72 ℃ 3 min,反应终止于4 ℃。反应结束后,取10 μL PCR产物进行琼脂糖凝胶电泳。PCR产物连接到pMD19-T载体上,转化DH5α感受态细胞,送华大基因进行测序。
1.5 Hcvp1基因的生物信息学分析
利用ORF Finder(http://www.ncbi.nlm.nih.gov/gorf/gorf.html)寻找Hcvp1基因的最大开放读码框;在NCBI网站((http://www.ncbi.nlm.nih.gov/blast)对Hcvp1基因的核苷酸序列进行BlastN序列比对,同时利用推测的氨基酸序列进行BlastP比对;利用ClustalW软件进行Hcvp1基因氨基酸序列同源性比对;用MEGA 6.0构建进化树,分析该基因的进化关系。用TMHMM-2.0(http://www.cbs.dut.dk/services/TMHMM-2.0/)预测Hcvp1基因编码蛋白质的跨膜结构,用(http://www.expasy.ch/tools/pi_tool.html)推测Hcvp1基因编码蛋白质的等电点和分子量。
1.6 Hvcp1基因在不同NaCl浓度胁迫下的表达特征分析
采用实时荧光定量PCR(qRT-PCR)技术分析Hvcp1 在不同的NaCl浓度胁迫下的表达特征。荧光定量PCR的引物Primer-F(5′-3′):GGTGCGGAGGAATTAGTA,Primer-R(5′-3′):ATGAAAGCAAATCGTGGT;内参基因为Actin, 引物为:Primer-F (5′-3′) CAGGCAGTTCTTTCTTTGT;Primer-R (5′-3′) ATCCTCCAATCCAGACACT。qRT-PCR的反应体系为(10 μL):Power 2×SYBR Real-time PCR Premixture 5 μL,正向引物(Forward primer)0.3 μL,反向引物(Reverse primer)0.3 μL,cDNA 2 μL,H2O 2.4 μL。qRT-PCR的反应程序为:95 ℃ 2 min; 95 ℃ 15 s, 61 ℃ 15 s, 72 ℃ 20 s,40个循环。
2 结果与分析
2.1 红麻叶片总RNA的提取
根据天根生化科技有限公司的植物总RNA提取试剂盒说明书提取250 mmol/L NaCl浓度胁迫的红麻幼苗叶片的总RNA, 然后用1.0%的琼脂糖凝胶电泳检测提取总RNA的完整性和纯度。结果如图1所示28S、18S和5S 3条带清晰可见,并且28S条带的亮度约是18S条带亮度的2倍,表明RNA结构完整,无污染和降解可以作为反转录的模板。
2.2 Hcvp1基因的克隆
以红麻耐盐转录组获得的Hcvp1基因的片段序列为基础,设计特异性引物,以cDNA为模板进行PCR扩增,扩增产物进行琼脂糖凝胶电泳检测结果如图2所示。经PCR获得产物连接到pMD19-T载体上,转化DH5α感受态细胞,经培养后提取质粒,送华大基因公司进行测序。将测序获得的cDNA序列,通过Blast比对发现,其与H+-PPase基因高度相似,将其命名为Hcvp1,在GenBank中的登录号为:KX687919。

图1 红麻叶片总RNA凝胶电泳图Fig.1 Agarose gel electrophoresis of total RNA of kenaf leaf
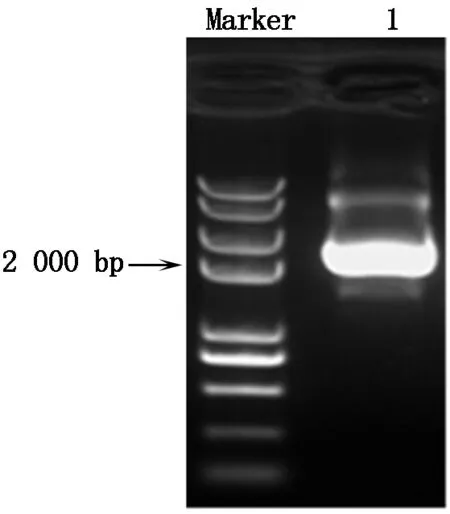
Marker.2k plus Ⅱ;1.PCR产物。Marker.2k plus Ⅱ; 1.PCR production.

图3 Hcvp1基因的核苷酸序列和氨基酸序列Fig.3 Nucleotides sequence and predicted amino acids sequence of Hcvp1 gene
2.3 Hcvp1基因的生物信息学分析
经过Sanger测序,该基因cDNA全长2 298 bp,开放阅读框为2 298 bp,推测其编码765个氨基酸的蛋白质(图3),推测其分子量和等电点分别为80.2 kDa和5.25。用TMHMM-2.0预测表明Hcvp1基因编码蛋白质具有13个跨膜结构(图4)。
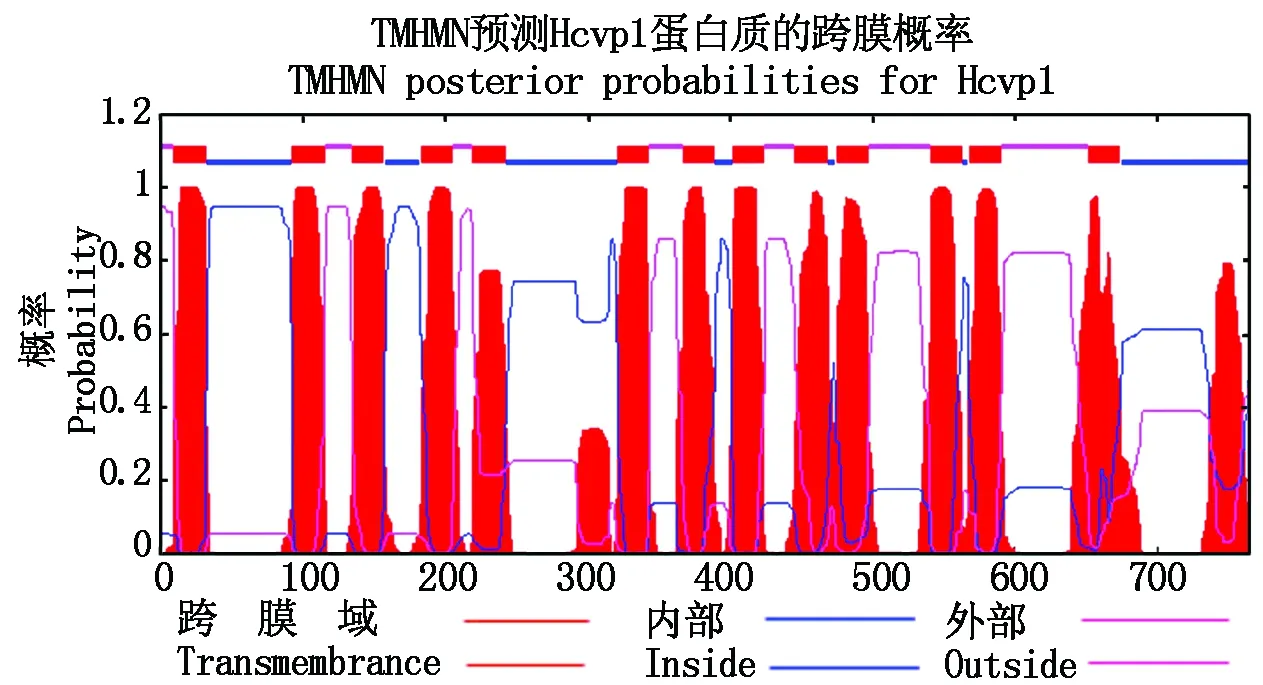
图4 Hcvp1 蛋白质的跨膜结构预测Fig.4 Transmembrane region prediction of Hcvp1
将该基因核苷酸序列通过BlastN 比对分析,发现其与雷蒙德氏棉(XM 012587702)、甜橙(XM 006492028 )、毛果杨(XM 006389360 )、烟草(NM001325218)、和大豆(XM 003528254)的H+-PPase基因核苷酸序列的相似性分别为90%,85%,85%,83%,83%,通过BlastP比对发现蛋白质序列的相似性分别为96%,93%,91%,93%,94%。
利用ClustalW软件分析Hcvp1基因氨基酸序列与具有代表性的雷蒙德氏棉(XM 012587702)、甜橙(XM 006492028 )、毛果杨(XM 006389360)、烟草(NM001325218)、红麻(KX687919)和大豆(XM 003528254)的H+-PPase基因氨基酸序列进行比对分析(图5)。结果表明,Hcvp1基因氨基酸序列与其他植物氨基酸序列的一致性为94.6%,保守的氨基酸多达738个,而非保守的氨基酸仅有27个。


多重比较采用ClustalW软件进行;不同的标记表示氨基酸残基不同的保守性;* .完全保守; :.75%以上;..50%以上和不足50%的保守。
利用MEGA 6.0软件分析Hcvp1基因的氨基酸序列与具有代表性的雷蒙德氏棉(XM 012587702)、甜橙(SM 006492028 )、毛果杨(XM 006389360 )、烟草(NM001325218)、红麻(KX687919)和大豆(XM 003528254)的H+-PPase基因氨基酸序列的进化关系(图6)表明,红麻与雷蒙德氏棉的距离最近,这可能是因为两者都是锦葵科的缘故。红麻与毛果杨的距离最远。

图6 Hcvp1 和其他H+-PPase基因的进化树分析Fig.6 Phylogenetic tree of Hcvp1 and other H+-PPase genes

图7 qRT-PCR分析Hcvp1基因在不同NaCl浓度胁迫下的表达Fig.7 Expression analysis of Hcvp1 under different concentration of NaCl by qRT-PCR
2.4 Hvcp1基因在不同NaCl浓度胁迫下的表达特征分析
分别提取0,75,150,250 mmol/L NaCl浓度胁迫下红麻幼苗叶片的总RNA,并反转录成cDNA作为qRT-PCR 反应的模板,以肌动蛋白做内参,进行qRT-PCR 分析,结果如图7所示。表明随着NaCl浓度的增加,Hvcp1基因的表达量不断增加。可见Hvcp1基因与NaCl胁迫直接相关。
3 讨论
根据红麻耐盐转录组测序获得的转录组序列设计引物[19],从红麻克隆得到Hcvp1基因,采用多种生物信息学的方法对Hcvp1基因进行分析,其cDNA全长为2 298 bp,开放阅读框为2 298 bp,编码765个氨基酸的多肽。同源序列比较发现,红麻的Hcvp1基因序列与雷蒙德氏棉、甜橙、毛果杨、烟草、和大豆的液泡膜H+-PPase 基因的序列高度同源,因此,推测获得的全长cDNA编码产物是红麻液泡膜H+-PPase。
液泡膜H+-PPase在植物耐盐抗旱、生长发育等方面具有重要的作用。液泡膜H+-PPase能够调节液泡的pH值,参与Na+、K+等溶质向液泡内运输;为Na+、Cl-液泡区域化提供运输动力,进而减轻盐害,降低细胞的渗透压[20-21],提高植物的耐盐能力。本研究通过qRT-PCR分析发现,随着NaCl浓度的提高,Hcvp1基因的表达量也随着升高。可见液泡膜H+-PPase基因的表达受NaCl胁迫的诱导,且表达量与NaCl浓度直接相关,所以液泡膜H+-PPase基因在红麻耐盐机制中具有重要的作用。
本研究克隆了红麻Hcvp1基因,并对其在不同NaCl浓度胁迫下的表达模式进行了qRT-PCR分析,这将为后续开展该基因的功能验证,揭示红麻耐盐机制奠定坚实的基础。
