液相色谱-串联质谱法检测大鼠血浆盐酸妥布特罗含量及其贴剂药代动力学的研究
2017-12-06李海涛王明明
曹 芳,李海涛,王明明
·药学研究·
液相色谱-串联质谱法检测大鼠血浆盐酸妥布特罗含量及其贴剂药代动力学的研究
曹 芳,李海涛,王明明*
目的建立测定大鼠血浆中盐酸妥布特罗浓度的方法,并对盐酸妥布特罗贴剂药代动力学进行研究。方法采用液相色谱-串联质谱法进行检测,以克仑特罗为内标,安捷伦氨基C18分析柱为色谱柱,A(0.1%甲酸+100%水)及B(甲醇)为流动相进行色谱分离。色谱条件为0~2.5 min,70%A→40%A;2.5~2.6 min,40%A→70%A;2.6~5 min,70%A。采用电喷雾电离源和多反应监测的方式进行正电荷检测,用作定量分析的盐酸妥布特罗和克仑特罗的离子反应对m/z分别为228.2→154.0和277.1→203.0。结果盐酸妥布特罗在0.5~100 ng/mL范围内线性关系良好;最低检测限分别为0.5 ng/mL;盐酸妥布特罗样本的日内及日间精密度和准确度均符合相关生物样品分析的要求,且RSD<10%。盐酸妥布特罗大鼠血浆样品在室温放置7 h、经历3次冷冻-解冻循环及在-80 ℃中放置120 d等条件下均可保持稳定;该方法成功运用于盐酸妥布特罗贴剂的药代动力学研究。结论该方法具有检测快速且灵敏性好等特点,可对其人体临床相关药动学研究展开探讨。
盐酸妥布特罗;贴剂;液相色谱串联质谱法;血药浓度;药代动力学
0 引言
盐酸妥布特罗是一种对支气管平滑肌具有持久且较强扩张作用的第3代选择性β2受体激动剂,主要应用于慢性阻塞性肺疾病、哮喘型支气管炎及慢性支气管炎等呼吸内科疾病的预防与治疗[1-2]。临床研究表明,盐酸妥布特罗除具有平喘作用之外,在止咳方面亦具有较好的药理活性[3-4]。目前临床针对妥布特罗的液相色谱-串联质谱法的相关研究较少,对该药物贴剂的药代动力学研究更是少见[5-6]。针对该问题,本研究利用大鼠模型,建立了一种快速、准确和灵敏的妥布特罗含量检测方法,并利用该方法对盐酸妥布特罗贴剂药代动力学进行研究,为后期该药物在人体临床药学及药动学研究提供了一定的借鉴。
1 材料
1.1 仪器 高效液相色谱仪(LC-20AD型,日本岛津公司);Techne氮吹仪(英国泰科尼公司);QTRAPTM4000型质谱仪(美国Applied AB Sciex公司);Analyst software 1.5.2分析软件(美国Applied AB Sciex公司)。
1.2 药品及试剂 盐酸妥布特罗标准品(Tulobuterol,中国食品药品检定研究院,纯度99.9%,批号:2015012173);盐酸妥布特罗贴剂由中国药科大学药学院制备并提供,陕西省疾病控制中心药物分析研究所完成其质量控制研究;克仑特罗作为本研究中内标(美国Sigma公司,纯度99.6%,批号:94330108);色谱甲醇,甲基叔丁醚及甲酸(美国Sigma公司,批号:15220171);其他试剂均为分析纯。质谱图及其化学结构见图1。

图1 质谱图及其化学结构注:A.盐酸妥布特罗(228.2→154.0);B.克仑特罗(277.1→203.0)
2 实验方法与结果
2.1 色谱条件 色谱柱:氨基C18分析色谱柱(100 mm×2.1 mm,3 μm,美国安捷伦公司)。流动相:A(0.1%甲酸+100%水),B(甲醇)。色谱条件:0~2.5 min,70%A→40%A;2.5~2.6 min,40%A→70%A。2.6~5 min,70%A。流速:0.4 mL/min,柱温:30 ℃,进样量:2 μL。进样方式为自动进样。
2.2 质谱条件 质谱条件为多反应监测(MRM),正电荷模式检测,电喷雾电离源(ESI)。离子喷雾电压:5 500 V;气体压力345 kPa;用于定量的盐酸妥布特罗及克仑特罗的离子反应对m/z分别为228.2→154.0、277.1→203.0;去簇电压(DP)分别为53、62 V;入口电压(EP)分别为10、7 V;碰撞能量(CE)分别为25、23 eV;碰撞室出口电压(CXP)分别为10、12 V。
2.3 对照品溶液的配制 分别用甲醇将盐酸妥布特罗及内标克仑特罗配成1.0 ng/mL和100 ng/mL的储备液,于-80 ℃冰箱中保存。对照品储备液的制备:将上述1.0 mg/mL的盐酸妥布特罗用甲醇稀释配成0.5、2.5、5、10、50、100 ng/mL的储备液。内标储备液质量浓度则为100 ng/mL。
2.4 血浆样品处理 所有血样均通过超临界萃取技术处理,于4 ℃条件下,取200 μL大鼠血样并向其中加入20 μL IS,20 μL甲醇,20 μL氨水(1 mol/L),涡旋混合30 s;加600 μL甲基叔丁醚于上述混合液中,涡旋混合3 min;处理后的上述血浆在4 000 r/min条件下高速离心(1 163 r/min)5 min,吸取上清液500 μL置于干燥离心管中,在氮气保护下于室温自然挥干;取残留物,加入50 μL甲醇复溶,并于12 000 r/min条件下高速离心(10 464 r/min)5 min后,进行LC-MS/MS分析。
2.5 专属性考察 在上述色谱及质谱条件下,分别得到大鼠空白血浆(图2A)、对照品血浆(图2B)及大鼠服药后3 h血浆(图2C)的典型多反应监测色谱图,见图2。盐酸妥布特罗和内标克仑特罗的保留时间分别为2.23、1.89 min,液质图峰形良好,血浆中存在的内源性物质不干扰上述药物的检测。
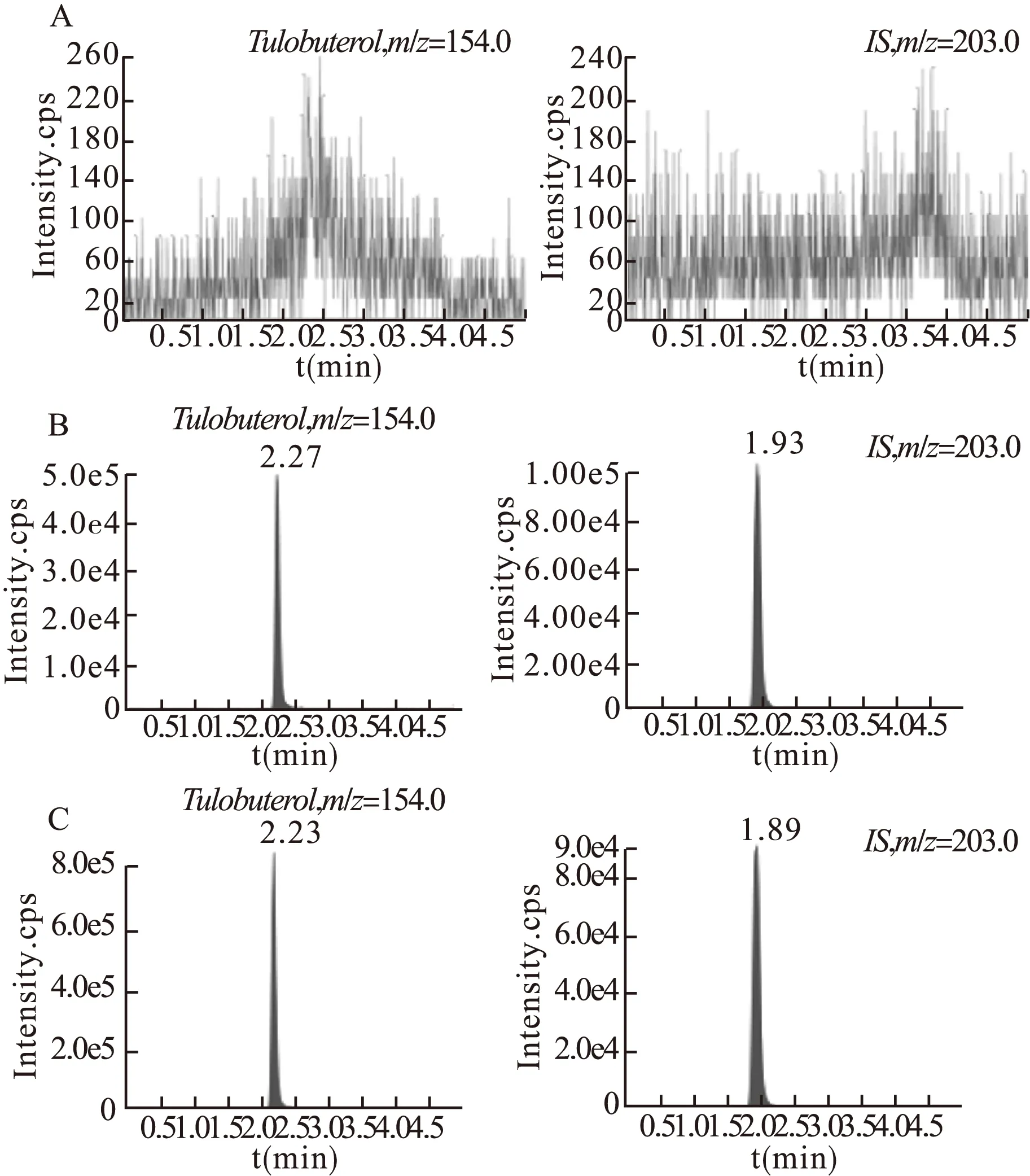
图2 色谱图
注:A.大鼠空白血浆;B.大鼠空白血浆+0.5 ng/mL盐酸妥布特罗(左),大鼠空白血浆+内标溶液(右);C.大鼠灌胃给予服用盐酸妥布特罗1 mg后3 h血浆(左),大鼠灌胃给予服用1 mg克仑
特罗1 mg后3 h血浆(右)
2.6 标准曲线和最低定量限(LLOQ)的考察 收集不含盐酸妥布特罗及内标的大鼠血浆,配置含有盐酸妥布特罗的对照品血浆,其质量浓度分别为0.5、2.5、5、10、50、100 ng/mL,并根据“2.3”和“2.4”项相关样品检测方法对相关样品进行测定。以盐酸妥布特罗峰面积比值(R)为纵坐标,以其浓度(c)为横坐标,计算该药物在血浆中的标准曲线,得其直线回归方程:Y=0.132 4 X+0.267 6 (r=0.996 7);结果表明,盐酸妥布特罗的LLOQ分别为0.5 ng/mL,其在0.5~100 ng/mL范围内线性关系良好。
2.7 精密度及准确度试验 取大鼠空白血浆,参照“2.3”及“2.4”项下方法,将盐酸妥布特罗配制成高、中、低浓度梯度QC样品(即1、20、80 ng/mL),上述浓度均分别连续测定3 d,且进行6样本分析。根据每日所检测的标准曲线计算血浆中盐酸妥布特罗的日内精密度,并在不同的日期重复操作,计算该药物的日间精密度。见表1。

表1 盐酸妥布特罗的精密度及准确度试验结果(%)
2.8 回收率、基质效应和稳定性检测 取大鼠空白血浆,参照“2.3”及“2.4”项下方法,将盐酸妥布特罗配制成浓度为1、20、80 ng/mL的高、中、低浓度梯度样品,分别取2 μL进样。取上述浓度下对应的峰面积,并计算其提取回收率(n=6)。结果显示,低、中、高浓度盐酸妥布特罗的回收率分别为95.6%±3.3%、93.7%±1.6%、97.4%±4.1%。按照上述操作,另配制100 ng/mL的内标进行回收率检测,结果显示,内标回收率为92.1%±1.0%。结果表明,该盐酸妥布特罗及内标的回收率均符合要求。
另取大鼠空白血浆,参照“2.3”及“2.4”项下方法,分别加入上述配制的1、20、80 ng/mL盐酸妥布特罗2 μL及内标2 μL进行LC-MS/MS分析,将上述得到的峰面积分别与直接进样的等浓度标准品溶液得到的峰面积相比较,对本研究中的基质效应进行考察。结果显示,上述浓度的盐酸妥布特罗基质效应分别为101.4%±5.5%、112.2%±3.1%、106.4%±2.2%。内标的平均基质效应为96.6%。结果显示,该盐酸妥布特罗和内标在本方法下均不存在基质效应。
考察不同的保存条件下盐酸妥布特罗的低、中、高质量浓度和内标(100 ng/mL)血浆样品的稳定性(n=6),结果显示,该药物及内标血浆样品于室温中放置7 h、3次冷冻-解冻循环处理及在-80 ℃条件下保存120 d后均稳定。结果见表2。
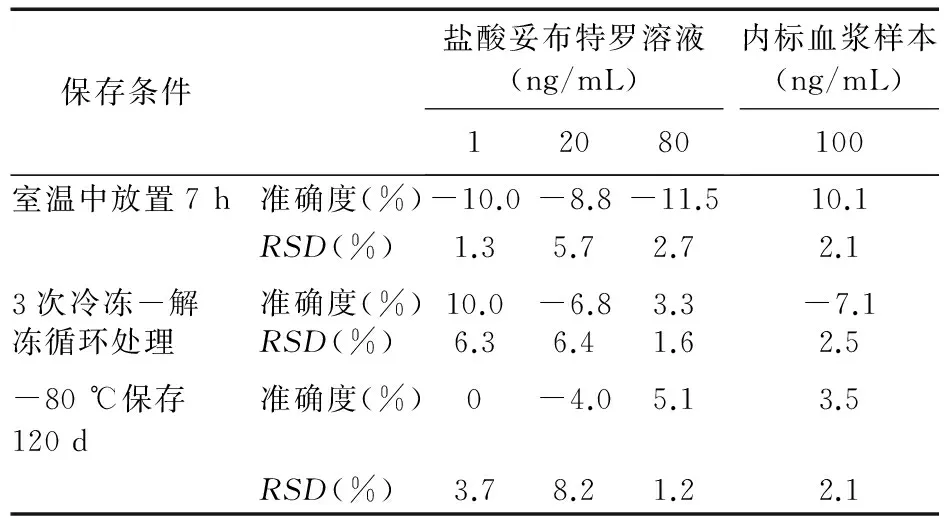
表2 稳定性检测结果(n=6)
2.9 药代动力学试验 18只雌性SD大鼠(300~350 g)购买于陕西省疾病控制中心,合格证号:SCXK(陕)2015-1113,由西安交通大学动物实验中心代饲养,饲养条件为标准饲养,日常光照及自由饮水,实验开始前上述大鼠均适应性喂养1周。
将上述大鼠随机分为高剂量组、中剂量组及低剂量组,对大鼠脖颈背部进行剃毛处理,并于实验日分别将0.5、1.0、2.0 mg盐酸妥布特罗贴片贴于大鼠脖颈处,贴片面积分别为2.5、5.0、10 cm2,给药完成后让大鼠自由活动,并于给药后0、0.5、1、2、2.5、3、5、7、9、12、20、24、48 h通过尾静脉取血法取0.5 mL大鼠静脉血,置于肝素管中,冰浴冷却后离心10 min(5 000 r/min)得到分离后的血浆,置于-80 ℃冰箱中保存待测。采用LC-MS/MS法检测给药后不同时间的盐酸妥布特罗血药浓度,利用DAS 2.1软件(中国药学会)对相关药-时数据进行分析,并得到主要药动学检测数据,见表3。盐酸妥布特罗药-时曲线见图3。
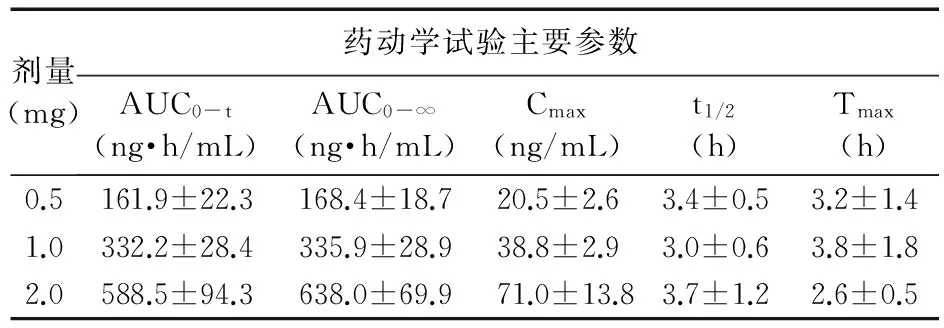
表3 药动学试验主要参数(n=6)
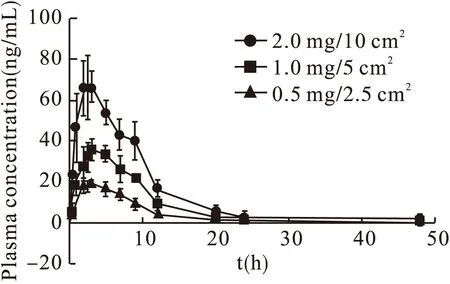
图3 盐酸妥布特罗药-时曲线
3 讨论
盐酸妥布特罗为选择性β2受体激动剂,对支气管平滑肌具有较好的扩张作用,但对心脏的兴奋作用较弱。动物实验证明,盐酸妥布特罗松弛支气管平滑肌的作用为氯喘通的2~10倍,药效维持时间为异丙肾上腺素的5~10倍,而对心脏的兴奋作用仅为异丙肾上腺素的1/1 000[7-8]。盐酸妥布特罗贴片为该药物的重要剂型之一,其给药较为持久且不良反应较小,因此,妥布特罗贴剂可能成为一种被广泛应用的呼吸内科药物[9]。但临床针对该药物贴剂的LC-MS/MS研究十分匮乏。因此,建立简便且准确的盐酸妥布特罗贴剂血药浓度检测方法具有十分重要的意义。Matsumura等[10]早在上世纪80年代已应用气相色谱-电子捕获检测器法对兔及人体血浆中妥布特罗的检测方法展开了初步研究,但由于实验技术限制等因素,其研究深度不够,且检测指标极为有限。徐福等[11]在上述研究的基础上,建立了一种兔血浆中盐酸妥布特罗口服制剂浓度的LC-MS/MS快速检测方法,尽管该研究是首次利用该方法对盐酸妥布特罗的含量进行检测,但其未对该药物的药代动力学展开深入讨论。Kim等[12]对比格犬中盐酸妥布特罗口服制剂的药代动力学展开了研究,但其研究对象仍未口服制剂,而未对该药物的贴剂进行研究。
针对上述研究的不足,本研究建立了一种灵敏且高效的LC-MS/MS检测方法,用于盐酸妥布特罗贴剂药代动力学研究,该方法的准确度、精密度及检测限均符合相关要求。尽管本课题得到较为科学的检测结果,但仍存在诸多问题。首先,本研究中药代动力学研究对象为大鼠,该方法是否适用于人体试验还需要进一步探讨;此外,本研究使用的盐酸妥布特罗贴剂为自制,尽管通过相关检测对其质量进行了较好的控制,但由于其缺乏普遍性,所以,在后续研究中还需选用市场中销售的相关药物对其展开深入论证;最后,由于临床对盐酸妥布特罗的代谢产物研究较少,因此,本研究未能对该药物的代谢产物进行同时检测,在后期研究中应对该问题进行进一步阐述。
综上所述,本方法可应用于盐酸妥布特罗贴剂的大鼠药动学及生物等效性研究,为其人体试验奠定一定的基础,对妥布特罗的应用研究具有重要意义。
[1] Yamaya M,Nishimura H,Nadine L,et al.Tulobuterol inhibits rhinovirus infection in primary cultures of human tracheal epithelial cells[J].Physiol Rep,2013,1(3):e00041.
[2] Ichikawa M,Kodama Y,Yoshimi K,et al.Effects of transdermal tulobuterol on dyspnea and respiratory function during exercise in patients with chronic obstructive pulmonary disease[J].J Thorac Dis,2015,7(4):687-696.
[3] Katsunuma T,Fujisawa T,Nagao M,et al.Effects of transdermal tulobuterol in pediatric asthma patients on long-term leukotriene receptor antagonist therapy:results of a randomized,open-label,multicenter clinical trial in Japanese children aged 4-12 years[J].Allergol Int,2013,62(1):37-43.
[4] Mochizuki H,Nanjo Y,Takahashi H.Better adherence to a transdermal tulobuterol patch than inhaled salmeterol in elderly chronic obstructive pulmonary disease patients[J].Geriatr Gerontol Int,2013,13(2):398-404.
[5] Tamura G,Ichinose M,Fukuchi Y,et al.Transdermal tulobuterol patch,a long-actingβ(2)-agonist[J].Allergol Int,2012,61(2):219-229.
[6] Sakamoto T,Fujimaki Y,Takada Y,et al.Non-destructive analysis of tulobuterol crystal reservoir-type transdermal tapes using near infrared spectroscopy and imaging[J].J Pharm Biomed Anal,2013,74:14-21.
[7] Kim KS,Park SJ.Influence of 1-D silica nanotubes as drug adsorbent on release behaviors of tulobuterol-loaded porous microcapsules[J].Colloids Surf B Biointerfaces,2012,92:240-245.
[8] Onari Y,Haruta Y,Mukaida K,et al.Clinical effects of budesonide/formoterol combination drug in elder patients with asthma compared with budesonide plus tulobuterol patch combination treatment[J].Arerugi,2012,61(6):820-831.
[9] Abe T,Setoguchi Y,Kono Y,et al.Effects of inhaled tiotropium plus transdermal tulobuterol versus tiotropium alone on impulse oscillation system (IOS)-assessed measures of peripheral airway resistance and reactance,lung function and quality of life in patients with COPD:a randomized crossover study[J].Pulm Pharmacol Ther,2011,24(5):617-624.
[10]Matsumura K,Kubo O,Sakashita T,et al.Determination of serum tulobuterol concentrations by mass fragmentography:comparison with an electron-capture gas chromatographic method[J].J Pharm Sci,1983,72(5):570-572.
[11]Xu F,Zhang Z,Tian Y,et al.High-performance liquid chromatography electrospray ionization mass spectrometry determination of tulobuterol in rabbit′s plasma[J].J Pharm Biomed Anal,2005,37(1):187-193.
[12]Kim JH,Kim TH,Park HJ,et al.The pharmacokinetics of the β2-adrenoceptor agonist,tulobuterol,in Beagle dogs following transdermal and intravenous administration[J].Vet J,2016,208:90-92.
SimultaneousdeterminationoftulobuterolinratplasmabyLC-MS/MSanditsapplicationinpharmacokineticstudyoftulobuterolpatch
CAO Fang,LI Hai-tao,WANG Ming-ming*
(Department of Pharmacy,Affiliated Hospital of Yan′an University,Yan′an 716000,China)
ObjectiveTo establish a method for simultaneous determination of tulobuterol in rat plasma and study the pharmacokinetics of tulobuterol patch.MethodsAfter plasma sample was treated with protein precipitation combined with extraction,the determination was performed on Angilent Venusil MP C18column with clenbuterol as the internal standard and 0.1% formic acid+100% water (A) and methanol (B) as the mobile phase (0~2.5 min,70%A→40%A;2.5~2.6 min,40%A→70%A;2.6~5 min,70%A).Tulobuterol (228.2→154.0) and clenbuterol (277.1→203.0) were detected by electrospray ionization(ESI)with positive ion in MRM mode quantitatively.ResultsThe linear range was 0.5~100 ng/mL for tulobuterol.The lower limits of quantitation was 0.5 ng/mL.The intra-day and inter-day precision and accuracy were all in line with the requirements of biological sample analysis.The plasma samples were stable after three freeze-thaw cycles and being stored for 7 h at room temperature and 120 days at -80 ℃.ConclusionThe method has the advantages of fast detection and good sensitivity,which can be used to investigate the pharmacokinetics of the human body in clinic.
Tulobuterol;Patch;LC-MS/MS;Plasma concentration;Pharmacokinetics
2017-03-22
延安大学附属医院药剂科,陕西 延安 716000
*
10.14053/j.cnki.ppcr.201711020
