芸香苷-羧甲基-β-环糊精包合物的制备及其表征
2017-11-21,,,,,*,,*
,,,,,*, ,*
(1.湖南省烟草科学研究所,湖南长沙 410007; 2.湖南农业大学生物科学技术学院,湖南长沙 410128)
芸香苷-羧甲基-β-环糊精包合物的制备及其表征
陈筠1,2,许诗豪2,罗井清1,杨红武1,彭曙光1,*,王征2,*
(1.湖南省烟草科学研究所,湖南长沙 410007; 2.湖南农业大学生物科学技术学院,湖南长沙 410128)
以包埋率为评价指标,在单因素实验基础上应用响应面法对芸香苷-羧甲基-β-环糊精包合物制备工艺条件进行优化并进一步用红外光谱、扫描电镜等方法对包合物进行了鉴定。结果表明芸香苷-羧甲基-β-环糊精包合物最佳制备工艺条件为包埋质量比1∶4,包埋温度60 ℃,包埋时间2 h,包埋率达62.92%,红外光谱、扫描电镜结果表明芸香苷已包埋在羧甲基-β-环糊精的内腔中。此条件下包合物的水溶解度得到明显提高,达到1760 mg/L。本实验采用的包埋方法和包埋材料可以改善芸香苷的水溶解性。
芸香苷,羧甲基-β-环糊精,包合物,溶解度
芸香苷又称芦丁(Rutin),是一种广泛存在于食用和药用植物的黄酮类化合物[1-2]。研究者发现芸香苷具有多种生物活性和功效,如吸收紫外线、抗骨质疏松[4]、清除自由基、抗氧化[3]、保护胃黏膜、增强免疫、抗衰老[5]、降低血糖、抗癌细胞[6]、抗病毒、抑菌、抗炎、镇痛等[7],在食品和药品等工业中具有良好的应用前景。但芸香苷的水溶性极差,限制了其在食品、药物、化妆品等行业中的广泛应用。若对芸香苷进行改性,增加其水溶性,可提高很多植物资源的经济附加值,提高生物利用度。
β-CD分子呈中空筒状,圆筒外侧分布大量羟基决定了其良好的水溶性,而圆筒内侧的非极性基团则在环糊精内部形成了一个疏水环境,它的疏水区可以与各种有机化合物发生作用,形成新的复合物,并且化合物的物理化学性质并未被改变[8]。若在β-环糊精中引入羧甲基,羧甲基的氧能与水分子的氢形成氢键,可以得到水溶性更好的羧甲基-β-环糊精[9-10]。目前,有一些关于利用β-CD及衍生物包埋木犀草素等活性物质的研究报道[11-13],包埋物仍然能较好地保持生物活性,这些研究为活性成分的有效应用提供了有意义的参考工艺和数据。而芸香苷和羧甲基-β-环糊精(carboxymethyl-β-cyclodextrin,CM-β-CD)之间相互作用还没有文献报道,所以本研究选取溶解度更好的CM-β-CD为壁材,对芸香苷进行包埋工艺条件研究,使其溶解度明显增加,拟进一步寻找芸香苷在功能食品应用中的新途径。
1 材料和方法
1.1材料和仪器
芸香苷 国药基团化学试剂有限公司;羧甲基-β-环糊精 上海伊卡生物技术有限公司;甲醇、乙腈 德国默克公司;无水乙醇 安徽安特食品股份有限公司。
安捷伦1260高效液相色谱仪、ZORBAX SB-C18色谱柱 美国Agilent公司;数学控温电热搅拌器 天津泰斯特仪器有限公司;VECTOR-22型傅立叶红外光谱仪 德国布鲁克公司;S-3700扫描电子显微镜 日本日立公司。
1.2实验方法
1.2.1 标准曲线 精密称取10 mg芸香苷加入到25 mL容量瓶中用80%乙醇定容得到标准溶液,分别取0.1,0.2,0.3,0.4,0.5,0.8,1.0 mL于10 mL容量瓶中,用80%乙醇定容,摇匀,用高效液相色谱法绘制出标准曲线。
1.2.2 芸香苷/CM-β-CD包合物制备 精密称取适量的芸香苷置于锥形瓶中,向其中加入乙醇溶液,超声使其完全溶解。按芸香苷与CM-β-CD的一定质量比称取CM-β-CD,并加水使其溶解。将CM-β-CD水溶液缓慢滴加入芸香苷-乙醇溶液中,在一定温度下,电热搅拌器搅拌一段时间,自然降温后继续搅拌,得到悬液,将悬液通过旋转蒸发仪除去乙醇后,得到的液体放入真空冷冻干燥机中干燥,得到包合物固体[14-15]。
1.2.3 包合物中芸香苷含量的测定 芸香苷含量测定采用高效液相色谱法。称取50 mg包合物,加入80 mL 50%乙醇溶解,电磁搅拌1 h,静置,得淡黄色液体。根据下式计算包埋率:
包埋率(%)=(包合物中芸香苷的量/投入到包埋反应体系中的芸香苷的量)×100
1.2.4 包合物的溶解度测定 称取100 mg的芸香苷和芸香苷/CM-β-CD包合物,分别用100 mL水溶解,摇床振荡72 h制成过饱和溶液,0.45 μm微孔滤膜过滤,取滤液稀释适当倍数,用高效液相色谱法测芸香苷的含量,再计算芸香苷的溶解度[16]。
1.2.5 红外光谱检测 分别取10 mg的芸香苷,CM-β-CD及芸香苷/CM-β-CD包合物,用KBr压片,于400~4000 cm-1范围进行红外光谱分析。
1.2.6 扫描电镜 分别取10 mg的芸香苷,CM-β-CD,芸香苷和CM-β-CD的物理混合物,芸香苷/CM-β-CD包合物进行扫描电镜分析。
1.2.7 包埋工艺条件的优化 包埋质量比的影响:以包埋率为评价指标,在包埋温度60 ℃、包埋时间2 h和乙醇浓度80%的条件下考察不同包埋质量比(1∶1、1∶2、1∶4、1∶6)对包埋率的影响。
乙醇浓度的影响:以包埋率为评价指标,在包埋质量1∶4,在包埋温度60 ℃,包埋时间2 h的条件下,考察不同乙醇浓度(60%、70%、80%、90%)对包埋率的影响。
包埋时间的影响:以包埋率为评价指标,在最适质量比1∶4和乙醇浓度80%,在包埋温度60 ℃条件下,考察不同包埋时间(1、2、3、4 h)对包埋率的影响。
包埋温度的影响:以包埋率为评价指标,包埋时间2 h、包埋质量比1∶4、乙醇浓度80%的条件下,考察不同包埋温度(50、60、70、80 ℃)对包埋率的影响。
响应面分析:由单因素实验结果中选择包埋温度,包埋时间,包埋质量比三个对包埋率影响较大的因素作为研究参数,分别用A、B、C表示,比包埋率为响应值(Y%),进行响应面设计,应用Box-Behnken中心组合设计原理对芸香苷-CM-β-CD包合物制备工艺进行优化[17-18]。
1.3数据处理
所有实验均重复3次取平均值,以平均值±标准差表示,通过SPSS 19.0软件进行比较分析,采用单因素方差分析组间差异(One-way ANOVA,LSD),p<0.05表示有显著性差异,p<0.01表示显著性差异极大。
2 结果和讨论
2.1芸香苷标准曲线绘制
按1.2.1可以得到芸香苷标准曲线方程为:y=43.499x+289.61,R2=0.9988,如图1所示,芸香苷在20~200 μg/mL浓度内线性关系良好。

图1 芸香苷标准曲线Fig.1 The standard curve of rutin
2.2包合物制备工艺的优化
2.2.1 单因素实验结果 由图2可看出,质量比为1∶4时,包埋率达到最大值,且与其它质量比相比有显著性差异(p<0.05),这可能是由于CM-β-CD的内腔有一定的空间[19],可以通过羟基与芸香苷上的活泼基团,如酚羟基或氢原子之间发生相互作用(见图9包合物的红外光谱酚羟基峰信号减弱)[20],在一定比例下,芸香苷进入CM-β-CD分子空穴,随其浓度增加会达到饱和状态,此时包埋率最大为61.11%。与CM-β-CD比较,如果芸香苷相对比例高,多余的芸香苷进入不了空穴,只能附着于包埋剂,容易离解。所以,我们推测 在1∶1或1∶2比例下,芸香苷比例相对较高,1∶6比例下,CM-β-CD空穴没有被饱和,1∶4比例下,包埋率最佳,说明此时两者相对浓度适合较适包埋比例。图3可看出,乙醇浓度为80%时,与其他乙醇浓度相比,包埋率的差别不大,说明四种乙醇浓度对包埋率的影响无明显差异(p>0.05),但由于乙醇浓度80%时芸香苷溶解效果好,且相对于乙醇浓度90%来说,节省乙醇,故选择乙醇浓度80%;图4可看出,包埋时间为2 h时,包埋率达到最大值59.56%,且与其它包埋时间相比有显著性差异(p<0.05),这可能是由于包埋时间的加长有利于包埋过程,但包埋时间过长,芸香苷的稳定性受到影响,降低了包埋率,故选择包埋时间2 h;由图5可看出,包埋温度为60 ℃时,包埋率达到最大值62.92%,且与其它包埋温度相比有显著性差异(p<0.05),这可能是由于温度升高有利于反应的进行,但温度过高,也加速了芸香苷从包埋物中释放,不利于其稳定性,且温度过高会消耗能量,故选择包埋温度60 ℃。

图2 质量比对包合物包埋率的影响Fig.2 Effect of mass ratio on the inclusion rate
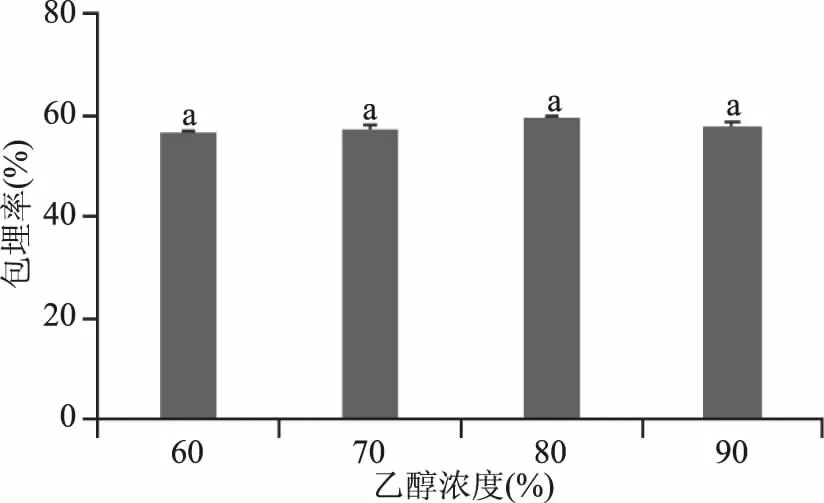
图3 乙醇浓度对包合物包埋率的影响Fig.3 Effect of ethanol concentration on the inclusion rate

图4 包埋时间对包合物包埋率的影响Fig.4 Effect of time on the inclusion rate
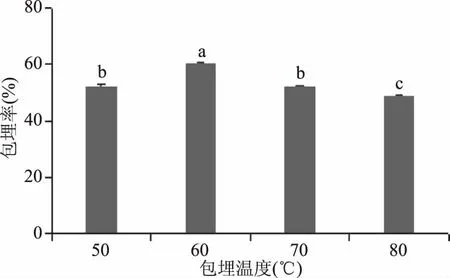
图5 包埋温度对包合物包埋率的影响Fig.5 Effect of temperature on the inclusion rate
2.2.2 BBD-RSM实验设计及显著性分析 利用单因素实验结果,根据Box-Behnken中心组合实验原则,选取三个对包合物包埋率影响显著的三个因素质量比,包埋温度,包埋时间,采用三因素三水平的响应面分析法对工艺方法进行优化。BBD方案结果见表1。
方差分析结果见表2。对各因素与响应值进行回归拟合得到模型对应的回归方程是y=63.03+0.39A+0.64B+0.39C+0.37AB+1.53AC+0.94BC+2.24A2+2.11B2-1.87C2
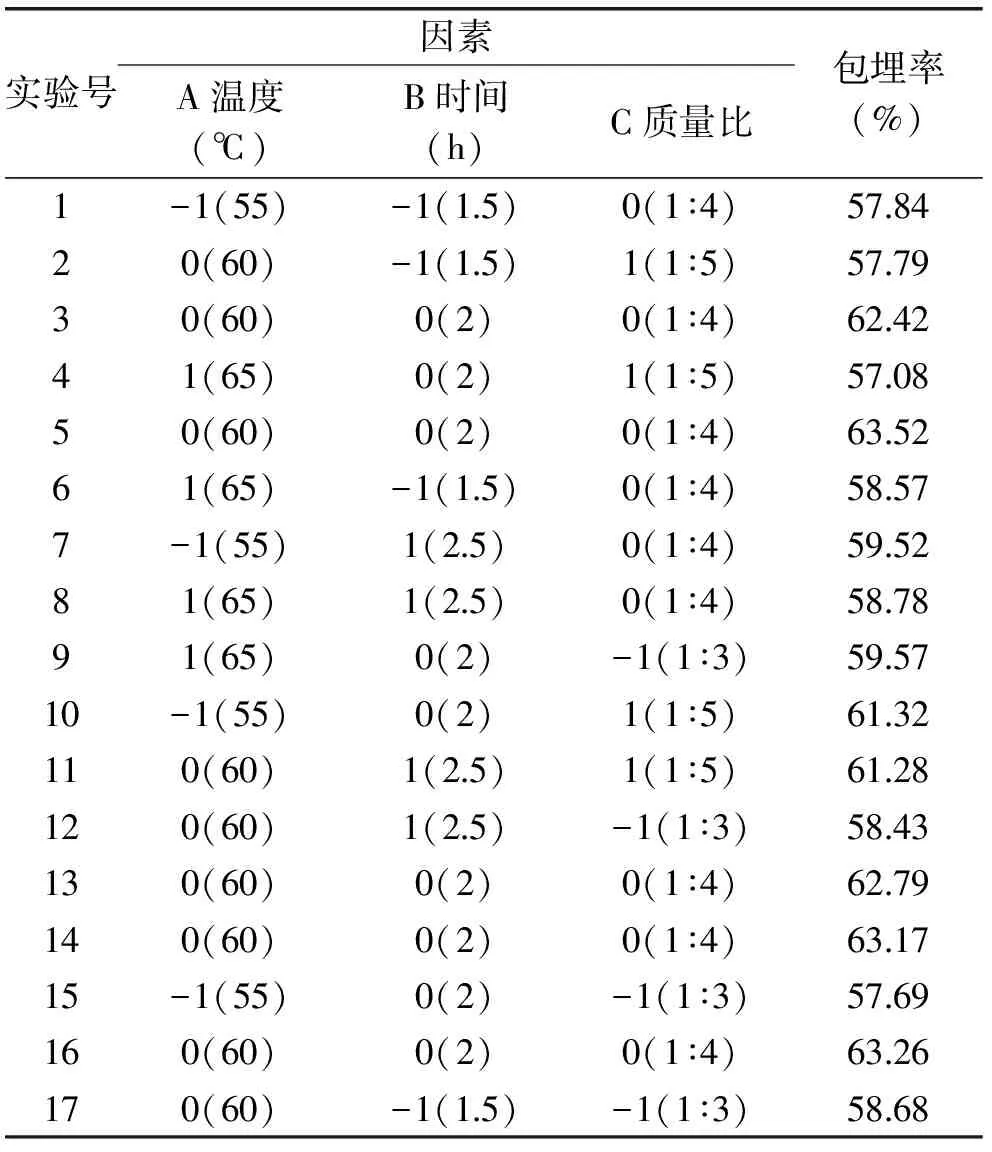
表1 BBD方案和结果Table 1 BBD matrix and results
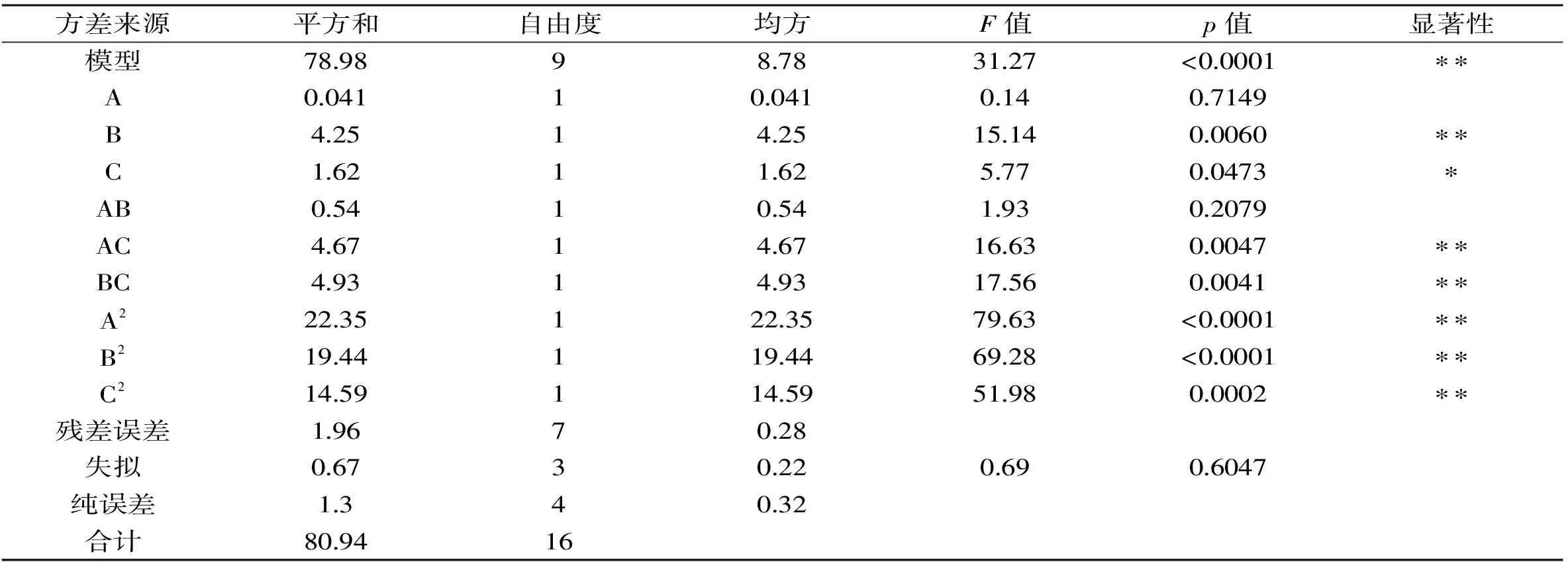
表2 方差分析Table 2 Variance analysis
注:*表示p<0.05为显著;**表示p<0.01为极显著。
由表2可以看出,模型p<0.01,表明回归方差模型极显著,该实验方法可靠,失拟项p=0.6047>0.05,不显著,说明实验所得的回归方程能够很好的对响应值进行预测。通过回归方程各项的方差系数可以看出,B,AC,BC,A2,B2,C2为差异极显著(p<0.01),C有显著差异(p<0.05),说明它们对影响值影响大,而其他变量的影响或交互影响都不显著(p>0.05)。
2.2.3 包埋工艺条件的响应面分析与优化 通过软件处理,得到三因素包埋温度(A),包埋时间(B),包埋质量比(C)交互作用的响应面及等高线图,图6~图8分别是固定其中一个因素,考察另外两个因素对包埋率的影响的响应面图,可直观的反映任意两个因素之间的相互作用及其对响应值(Y%)的影响。由图可以看出,各个交互作用的因素最佳作用点都落在了实验范围内,说明这个响应面实验设计合理。两个因素之间的交互作用可以清晰的反映包埋率(Y%)随着二元变量在三维空间上的变化情况,利用所得信息我们可以从理论上来对实验的优化方案解释。通过方程中的偏回归系数显著性分析可得,包埋质量比和包埋温度,包埋质量比和包埋时间相互作用影响大(p<0.01),而包埋时间和包埋温度相互作用影响不大(p>0.05),与之前的方差分析结果一致。

图6 包埋时间和包埋温度交作影响的响应面和等高线图Fig.6 Response surface and contour line of inclusion time and temperature
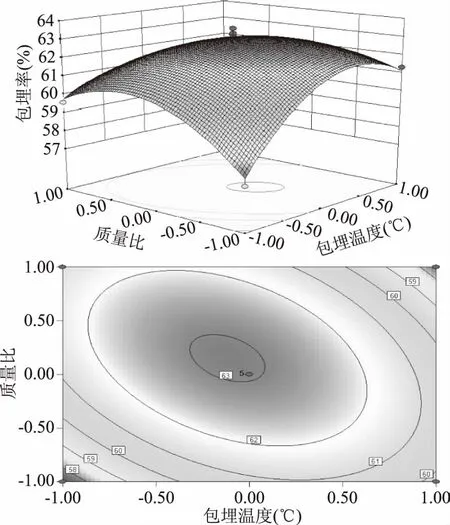
图7 质量比和包埋温度交作影响的响应面和等高线图Fig.7 Response surface and contour line of inclusion temperature and mass ratio
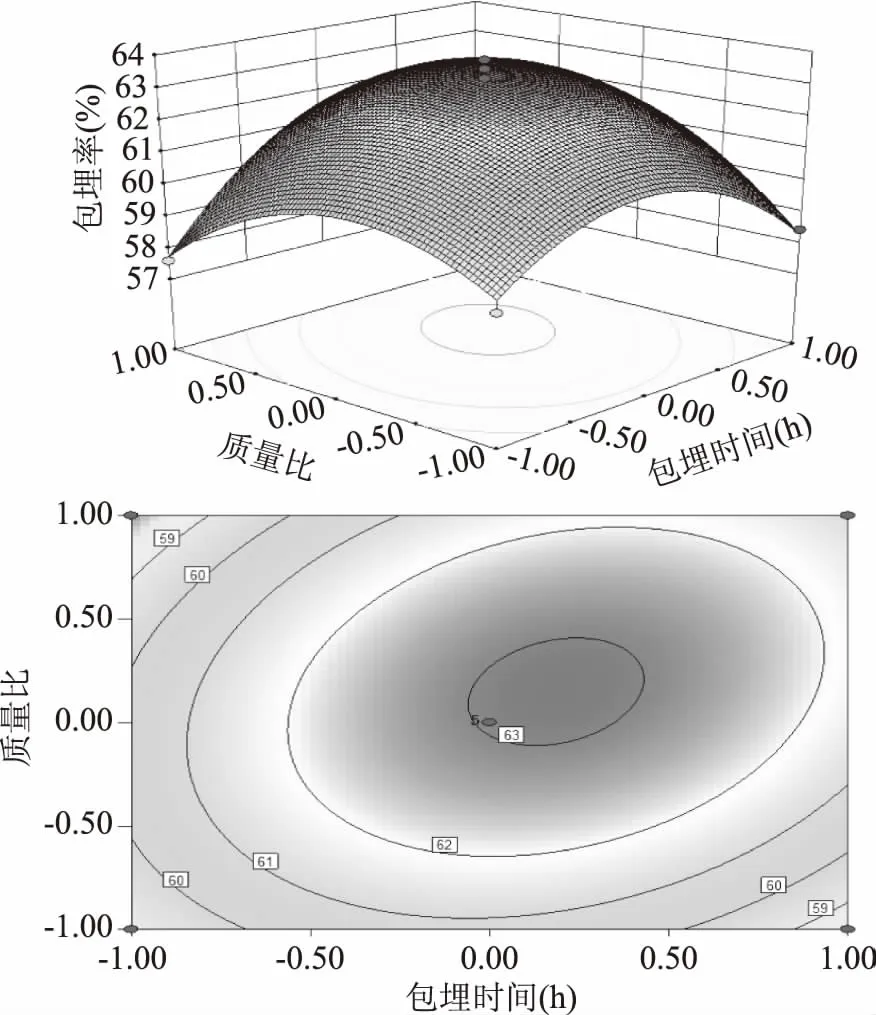
图8 质量比和包埋时间交作影响的响应面和等高线图Fig.8 Response surface and contour line of inclusion time and mass ratio
通过实验设计软件Design-Expert 7.1.6,依据单因素实验设计选取的对包合物包埋率影响较显著因素依次为包埋温度、包埋时间、包埋质量比,选取3因素的最佳水平范围,应用Box-Behnken中心组合设计原理对芸香苷包埋工艺进行优化,结果表明:此时最佳工艺条件为,包埋温度(X1)=59.34 ℃,包埋时间(X2)=120.78 min,包埋质量比(X3)=0.25,包埋率(Y)的最大预测值为62.73%。实际操作条件为:包埋温度(X1)=60 ℃,包埋时间(X2)=120 min,包埋质量比(X3)=0.25,在这个条件下进行实验得到包埋率为62.92%,得到的实验结果与预测结果十分吻合,优化效果显著,且回归模型有效可靠。
2.3红外光谱
分别测定芸香苷、包合物、环糊精单体的红外光谱,结果如图9所示,图中的a为芸香苷的红外光谱图,在3422 cm-1处是芸香苷羟基的伸缩振动峰,在2939 cm-1处是-CH2的反对称伸缩振动峰,在1655 cm-1处是α、β不饱和酮C=O的伸缩振动峰,而在1600~1400 cm-1是苯环的伸缩振动峰,在1063 cm-1则是-C-O-C的反对称伸缩振动峰。图中的c是CM-β-CD的红外光谱图,在3336 cm-1是其羟基的伸缩振动峰,在2928 cm-1是糖环骨架上的C-H伸缩振动峰,在1028 cm-1处是-C-O-C的反对称伸缩振动峰,在1420、1617 cm-1出现了羧甲基的特征峰,图中的b则为芸香苷-β-CD包合物的红外光谱图,可以看出来包合物与环糊精的红外光谱非常相似,只是芸香苷在500~1500 cm-1之间的一些小的吸收峰(1050.7、1203.5、1298.6 cm-1),表示酚羟基、Ar-O-R的基团特征峰在包合物的红外光谱中信号减弱或消失,说明这些基团几乎被环糊精掩盖。包合物有新的峰生成,也有峰的消失。这说明了芸香苷包进了CM-β-CD空腔中,而且包合作用过程是一个物理过程,主要作用是范德华力等,没有新化学键的形成,没有发生化学反应。

图9 样品红外光谱Fig.9 FTIR spectra of samples注:a. 芸香苷,b.包含物,c. CM-β-CD。
2.4扫描电镜分析
如图10A所示为CM-β-CD单体的电镜扫描结构图,可以看出CM-β-CD单体是个体单独存在的,形状为片状。如图10B所示为芸香苷单体的电镜扫描结构图,可以看出芸香苷单体是呈球状的,或单独或成簇存在的。由图10C所示的芸香苷和 CM-β-CD的物理混合物扫描结构图可以看出,混合物中既具有球状芸香苷形态,又有CM-β-CD的晶型,说明两者之间未发生包合。从图10D所示的芸香苷-CM-β-CD包合物的电镜扫描结构图可以看出包合物中芸香苷被包裹在CM-β-CD的内部,几乎看不到芸香苷的形态。说明芸香苷通过疏水作用以分子的形式进入CM-β-CD空腔,失去了芸香苷的形态。
2.5溶解度测定
在最优条件下制备芸香苷/CM-β-CD包合物,得到的包埋率为62.92%,溶解度为1760 mg/L,而纯芸香苷在水中的溶解度仅为50.34 mg/L,可见形成包合物后,芸香苷在水中的溶解度明显增加。
3 结论
芸香苷药理活性强,在植物界中广泛存在,但芸香苷溶水性差等缺点限制了其使用和发展。近年来,随着技术的进步,对芸香苷的改性研究有很多有意义的结果,这无疑提高了芸香苷的生物利用度[21-22]。邵伟等[16]用β-环糊精包埋芸香苷得到了溶解度增加13倍左右的包合物。艾凤伟等[8]用二甲基-β-环糊精包埋芸香苷得到了溶解度增加了14倍左右的包合物。本实验采用的是水溶性比β-环糊精和二甲基-β-环糊精更好的CM-β-CD,而且无毒无害,芸香苷用乙醇溶解而不是甲醇,通过溶液搅拌法制得的包合物溶解度比芸香苷单体溶解度增加了35倍左右。本实验将芸香苷、CM-β-CD、芸香苷-CM-β-CD包合物的红外光谱和电镜扫描图像进行了比较,验证了芸香苷已经包埋进环糊精的内腔中。研究结果为芸香苷水溶性改性和有效利用提供了有意义的参考数据。
芸香苷来源丰富,除了槐花等植物,很多农产品废弃物中芸香苷的含量也很高,例如烟草、蔬果加工废弃物等[23-25]。将芸香苷制成糊精包合物可极大增加芸香苷溶解度,对于废弃农产品的合理利用和开发,增加其经济附加值,节省自然资源有着积极的意义。

图10 样品的扫描电镜Fig.10 SEM of samples
[1]苏彩娟,王金水,刘本国,等. 芦丁/羟丙基-β-环糊精包合物的表征及其抗氧化能力研究[J]. 河南工业大学学报:自然科学版,2011,32(1):53-57.
[2]徐魁,孙兆伟,蔡艳丽. 荷花中芦丁含量测定方法研究[J].药学研究,2013,32(8):452-454.
[3]潘英明,梁英,朱志仁,等. 槐花米抗氧化成分的提取及其活性研究[J]. 林产化学与工业,2007,27(2):41-44.
[4]黄汉昌,姜招峰. 芦丁与人血清白蛋白相互作用的紫外可见光谱特性研究[J]. 天然产物研究与开发,2011,23(3):476-481.
[5]郭旭东,刁其玉,郭宇廷,等. 芦丁对大鼠免疫器官指数的影响[J]. 动物医学进展,2011,32(11):70-72.
[6]郑旭煦,胡应和. 神经介素U2受体激动剂芦丁的新用途:CN1615900[P]. 2005.
[7]王艳芳,王新华,朱宇同,等. 芦丁对甲型流感病毒抑制作用实验研究[J]. 中华中医药学刊,2005,23(5):827-827.
[8]艾凤伟,张加伟,钱楠,等. 芦丁-二甲基-β-环糊精包合物的制备、物理化学表征及体外溶出研究[J]. 药学研究,2015,34(11):650-653.
[9]宋全道,丁易,李新民,等. 羧甲基-β-环糊精的溶血作用及对槲皮素的增溶作用[J]. 山东大学学报医学版,2005,43(2):166-169.
[10]朱军峰,张光华,李楠,等. 羧甲基-β-环糊精的干法制备[J]. 应用化学,2008,25(6):681-684.
[11]Jullian C,Cifuentes C,Alfaro M,et al. Spectroscopic characterization of the inclusion complexes of luteolin with native and derivatized beta-cyclodextrin[J]. Bioorganic & Medicinal Chemistry,2010,18(14):5025.
[12]Yang L J,Chen W,Ma S X,et al. Host-guest system of taxifolin and native cyclodextrin or its derivative:Preparation,characterization,inclusion mode,and solubilization[J]. Journal of Agricultural & Food Chemistry,2011,85(3):629-637.
[13]Tsai Y,Tsai H H,Wu C P,et al. Preparation,characterisation and activity of the inclusion complex of paeonol withβ-cyclodextrin[J]. Food Chemistry,2010,120(3):837-841.
[14]初红涛,张晓会,苏立强. 槐花米中芸香苷的高效提取工艺[J]. 江苏农业科学,2013,41(9):239-240.
[15]周艳,唐亮,周咏梅. 芦丁-羟丙基-β-环糊精包合物的制备与验证[J]. 中国药学杂志,2011,46(16):1262-1264.
[16]邵伟,王大庆,米广太,等. 芦丁-β-环糊精包合物的研究[J]. 中药材,1998(1):31-33.
[17]徐向宏,何明珠. 试验设计与DESIGN-EXPERT、SPSS应用[M]. 科学出版社,2010.
[18]张玲,许薇,孙媛,等. 响应曲面法优化黄芩苷-β-环糊精包合物的制备[J]. 畜牧与兽医,2014,46(1):67-71.
[19]Kopecky F,Kopecká B,Kaclík P. Dissolution of nimodipine in an aqueous solution of hydroxyethyl-beta-cyclodextrin and a review of solubility of nimodipine with cyclodextrins[J]. Ceska a Slovenska Farmacie:Casopis Ceske Farmaceuticke Spolecnosti a Slovenske Farmaceuticke Spolecnosti,2003,52(1):33.
[20]Ai F,Ma Y,Wang J,et al. Preparation,Physicochemical Characterization andIn-vitroDissolution Studies of Diosmin-cyclodextrin Inclusion Complexes[J]. Iranian Journal of Pharmaceutical Research,2014,13(4):1115-1123.
[21]牛小花,陈洪源,曹晓钢,等. 芦丁的研究新进展[J]. 天然产物研究与开发,2008(b05):156-159.
[22]臧志和,曹丽萍,钟铃. 芦丁药理作用及制剂的研究进展[J]. 医药导报,2007,26(7):758-760.
[23]舒文将,刘金磊,邹蓉,唐健民,熊忠臣,蒋运生. 高效液相色谱法测定不同产地和采收期对槐米中芦丁含量的影响[J]. 时珍国医国药,2017,28(3):709-711.
Preparationandcharacterizationoftherutin-CM-β-CDinclusioncomplex
CHENYun1,2,XUShi-hao2,LUOJing-qing1,YANGHong-wu1,PENGShu-guang1,*,WANGZheng2,*
(1.Research Institute of Hunan Tobacco Science,Changsha 410007,China; 2. College of Bioscience and Biotechnology,Hunan Agricultural Universtity,Changsha 410128,China)
Based on the single factor experiments,the response surface methodology was utilized to obtain the optimum conditions by studying the factor of mass ratio,embedding temperature,embedding time with the embedding rate as the evaluation index,and rutin-CM-β-CD inclusion complex was identified by Sanning Electronic Microscopy(SEM),FI-IR. The rusults showed that the optimum ratio of Rutin and CM-β-CD was 1∶4,the embedding temperature was 60 ℃,the embedding time was 2 h,and the embedding rate was 62.92%. The results of SEM,FI-IR showed that rutin was contained in the inner cavity of CM-β-CD. Under these conditions,the solubility of inclusion complexes was about 1760 mg/L. The embedding method and material used in experiment could improve the solubility of rutin.
rutin;CM-β-CD;inclusion complex;solubility
2017-03-29
陈筠(1993-),女,硕士研究生,研究方向:天然产物的开发与利用,E-mail:714852160@qq.com。
*
彭曙光(1973-),男,博士,高级农艺师,研究方向:烟草科学与资源开发,E-mail:199166853@qq.com。 王征(1967-),女,博士,教授,博士生导师,研究方向:食物营养与药理,E-mail:wz8918@163.com。
中国烟草总公司湖南省公司科技项目(15-17Aa04)。
TS201.1
B
1002-0306(2017)21-0197-06
10.13386/j.issn1002-0306.2017.21.039
