水力空化对果胶粘度的影响及其凝胶色谱表征
2017-11-21,,,,*
, ,,,*
(1.广西科技大学生物与化学工程学院,广西柳州 545006;2.广西糖资源绿色加工重点实验室,广西柳州 545006;3.广西高校糖资源加工重点实验室,广西柳州 545006)
水力空化对果胶粘度的影响及其凝胶色谱表征
毛善巧1,2,3,杨锋1,2,3,黄永春1,2,3,黄承都1,2,3,*
(1.广西科技大学生物与化学工程学院,广西柳州 545006;2.广西糖资源绿色加工重点实验室,广西柳州 545006;3.广西高校糖资源加工重点实验室,广西柳州 545006)
为探明水力空化对果胶粘度及分子量分布的影响,通过空化装置产生空化效应并作用于果胶溶液,研究不同pH、温度、入口压力、初始浓度、作用时间下水力空化处理前后果胶粘度的变化,以粘度的下降率来衡量水力空化对果胶的作用效果,并采用凝胶色谱法(gel permeation chromatography,GPC)对空化处理前后的果胶分子量分布进行比较分析。结果表明,当溶液pH为5,温度为50 ℃,入口压力为0.1 MPa,果胶浓度为1 g/L,处理时间为60 min时,果胶粘度下降率达15.76%。经GPC分析发现,果胶相对平均分子量由70515 Da下降至57408 Da。所以用水力空化处理果胶可以有效降低果胶粘度及其分子量,为果胶降解提供了一个新方法。
水力空化,果胶,粘度,分子量分布
果胶是一种杂多糖[1],广泛存在于植物相邻细胞壁的中胶层[2-3]。因其具有良好的凝胶、增稠、稳定等性能而被广泛应用于食品工业[4];也因其能防止紫外线辐射,具有保护皮肤、养颜美容的作用被用于化妆品行业[5-6];除此之外,果胶还可用作造纸和纺织的施胶剂、制备超带离心膜和电渗析膜、制备铅蓄电池中的硫酸溶胶[7]等。因此对果胶的研究与开发具有良好的应用前景。
果胶作为大分子多糖,分子量是其重要指标之一,目前获取果胶分子质量及多分散性指数信息的分析方法有高效体积排阻色谱法[8]、凝胶法[9]、光散射法[10]等。与高分子量果胶相比,低分子量的果胶在其生物学活性的应用上具有独特的优势。因此,对果胶进行改性成为了近些年关于果胶的研究热点,而目前用于果胶改性的方法主要有化学方法和酶法[5-7],化学方法主要是依赖于高温、酸、碱等,既费时又污染环境;酶法比较昂贵且难以控制。因此,寻找对果胶的新的改性或者降解技术十分有意义。
水力空化是空化的一种[11],其对化工过程的强化原理与超声空化相同,但其能量利用率明显高于超声空化,更具工业化的优势[12]。超声波降解大分子物质的主要机理是机械性断键作用以及自由基的氧化还原反应[13-14],而张丽芬[15]等人的研究发现,超声波空化效应引起的自由基效应不是导致果胶降解的主要因素,机械效应是引起超声波降解果胶的主要原因。水力空化的降解机理[16]主要分为:“水相燃烧”反应机理、自由基反应机理以及机械作用。目前已有水力空化降解壳聚糖[17-19]的研究,但目前利用水力空化处理果胶的研究尚未见报道。本实验以粘度法测定水力空化对果胶的影响,并以凝胶色谱法比较分析空化处理前后果胶的分子量,为探索降解果胶的新方法提供参考依据,同时丰富水力空化技术的应用。
1 材料与方法
1.1材料与仪器
果胶 生化试剂(99%)CAS号:9000-69-5,成都市西亚化工股份有限公司;葡聚糖标准品系列 Waters公司;冰醋酸 分析纯,成都市科龙化工试剂厂;三水合乙酸钠 分析纯,台山市粤侨试剂塑料有限公司;盐酸 分析纯,西陇化工股份有限公司;氢氧化钠 分析纯,天津市科密欧试剂有限公司;实验室用水 为超纯水和去离子水。
DV-II+型Brookfield粘度计 美国Brookfield公司;Waters 1515pump系列高效液相色谱仪 具有针孔进样器,配Waters 2414示差折光检测,美国Waters公司;色谱柱:Ultrahydrogel 1000A,500A,250A(300 mm×7.8 mm)三根按排阻极限由大到小串联使用 美国Waters公司;空化装置 本实验室自制,如图1所示,水泵把液体输送到撞击流实验装置,产生强烈的物理效应,然后进入到空化器,空化器结构根据文献[17]设计,当液体流经空化器时因管径的变小使得流速随之增大,形成低压,当压强低于液体蒸气压时形成空化气泡,当进入压力较高区域后由于压强突然变大而使气泡溃灭,从而产生空化效应。通过调节阀门的大小,可控制流量和空化器入口的压力。

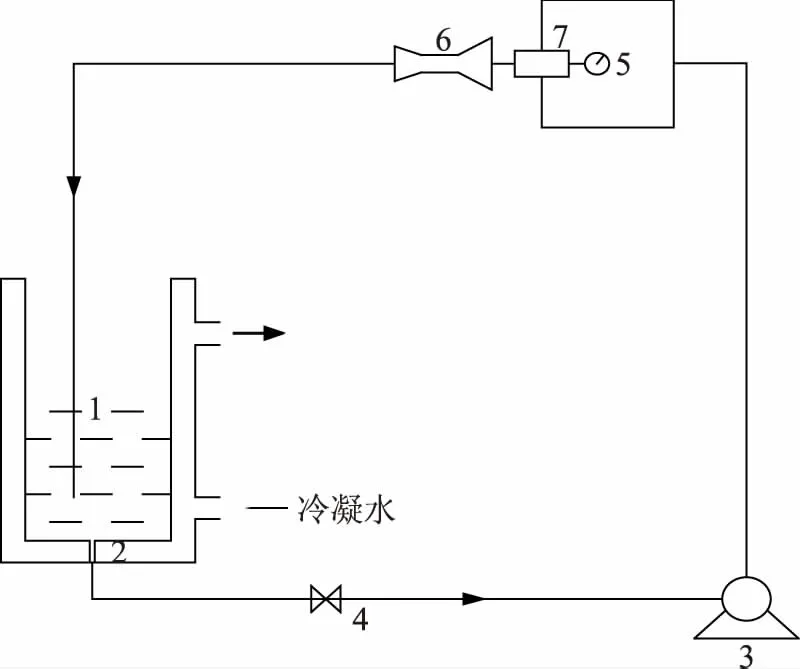
图1 空化装置示意图Fig.1 Diagram of homemade cavitation device注:1.溶液贮筒;2.循环水槽;3.水泵;4.阀门; 5.真空压力表;6.空化器;7.撞击实验装置。
1.2分析方法
1.2.1 果胶粘度下降率计算 参照刘雪[20]的方法,用Brookfield粘度计配2号转子在室温(25 ℃)、转速为100 r/min下测定果胶溶液粘度。并计算空化前后果胶粘度下降率,计算公式如下:

式中:ηr-粘度下降率,%;η0-空化前溶液黏度,mPa·s;ηt-空化后溶液黏度,mPa·s。
1.2.2 色谱条件 参照文献[21]中的色谱条件改进如下:按排阻极限由大到小将Ultrahydrogel 1000A,500A,250A(尺寸均为300 mm×7.8 mm)三根色谱柱串联;流动相为pH=5的乙酸乙酸钠缓冲液(V1 mol/L乙酸∶V1 mol/L乙酸钠∶V水=14.1∶5.9∶980);柱温30 ℃;检测池温度30 ℃;流速0.6 mL/min,进样量20 μL。流动相使用前经0.22 μm有机滤膜过滤。
1.3实验方法
1.3.1 溶液pH对果胶粘度的影响 称取2.00 g果胶,将果胶粉末平铺于2000 mL的烧杯底,缓慢加入去离子水,用玻璃棒将结块的果胶捣碎,再用磁力搅拌器搅拌至果胶完全溶解。用1 mol/L的盐酸和1 mol/L氢氧化钠溶液将得到的1 g/L的果胶溶液的pH调节至4、5、6、7、8,在0.4 MPa压力下,保持温度为50 ℃,通过空化装置循环60 min,测定空化处理前后各果胶溶液的粘度,计算粘度的下降率。
1.3.2 溶液温度对果胶粘度的影响 按上述方法配制浓度为1 g/L的果胶溶液,将果胶溶液的pH调节至5,在0.4 MPa压力下,控制温度分别为30、40、50、60、70、80 ℃,通过空化装置循环60 min,测定空化处理前后各果胶溶液的粘度,计算粘度的下降率。
1.3.3 入口压力对果胶粘度的影响 按上述方法配制浓度为1 g/L的果胶溶液,将果胶溶液的pH调节至5,分别在0.1、0.2、0.3、0.4、0.45 MPa压力下,保持温度为50 ℃,通过空化装置循环60 min,测定空化处理前后各果胶溶液的粘度,计算粘度的下降率。
1.3.4 初始浓度对果胶粘度的影响 按上述方法配制浓度分别为1、2、3、4、5 g/L的果胶溶液,将果胶溶液的pH调节至5,在0.1 MPa压力下,保持温度为50 ℃,通过空化装置循环60 min,测定空化处理前后各果胶溶液的粘度,计算粘度的下降率。
1.3.5 空化时间对果胶粘度的影响 按上述方法配制浓度为1 g/L的果胶溶液,将果胶溶液的pH调节至5,在0.1 MPa压力下,控制温度分别为50 ℃,分别通过空化装置循环10、20、30、40、50、60 min,测定空化处理前后各果胶溶液的粘度,计算粘度的下降率。
1.3.6 标准曲线的建立 将一系列不同分子量的葡聚糖标准样品:T1(Mw=5200),T2(Mw=11600),T3(Mw=23800),T4(Mw=48600),T5(Mw=148000),T6(Mw=273000),T7(Mw=410000),T8(Mw=668000)溶解于流动相中,各标准液的浓度均为0.5 g/L,在1.2.2中所述色谱条件下测定各标样,进样前均经 0.22 μm有机滤膜过滤。
1.3.7 凝胶色谱表征分析 将pH为5、温度为50 ℃、压力为0.1 MPa、浓度为1 g/L、空化处理60 min的果胶溶液与未经空化处理的果胶溶液均稀释至0.5 g/L,在1.2.2中所述色谱条件下,经 0.22 μm有机滤膜过滤后进样,根据保留时间以及回归方程分别计算果胶分子量,比较分析果胶分子量分布的变化。
1.4数据处理
色谱图和标准曲线来源于工作站Breeze Version 3.30;运用Origin 8.0处理数据并绘图。
2 结果与分析
2.1溶液pH对果胶粘度的影响
由图2可知,水力空化处理对果胶粘度的影响较大,这是因为果胶溶液在处理过程中,水力空化在大范围内形成一个比较均匀的空化强化场,并产生机械效应,在强大的剪切力和空化作用下[22],果胶的分子链发生断裂[15],致使溶液粘度降低。当溶液pH小于5时,果胶粘度下降率较大,当pH在5~7时,果胶粘度下降率明显变小,当pH为8时,果胶处于碱性环境,可能此时更有利于空化形成,使果胶的糖苷键发生断裂[17],导致粘度变得更低,粘度下降率稍微回升。本文考察pH的范围在4~8,发现pH为4时降解率最高。
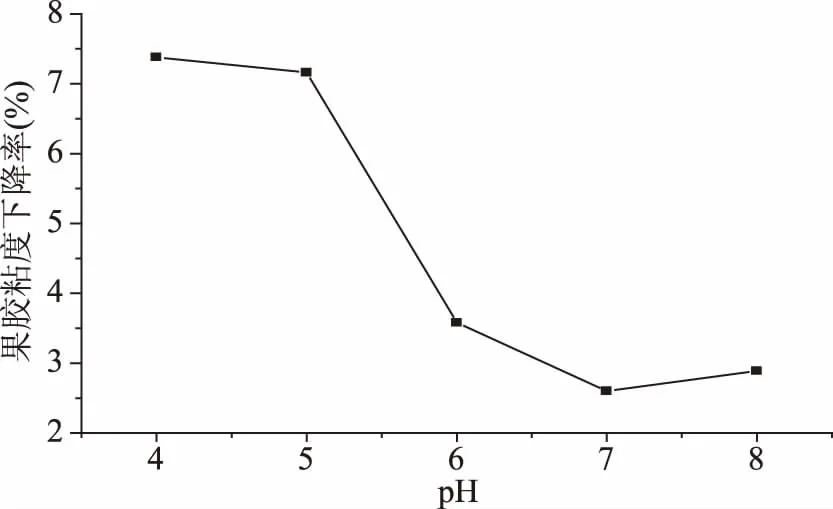
图2 pH对果胶粘度的影响Fig.2 Effect of pH on the viscosity of pectin
2.2溶液温度对果胶粘度的影响
由图3可知,溶液温度对果胶粘度有影响,果胶粘度下降率随温度升高而增大,这是因为当温度升高时,表面张力降低,空化变得容易[17],同时空化强度增大,果胶分子链断裂的几率也增大,分子量逐渐降低,溶液粘度下降。由图3可以发现,当温度小于50 ℃时,粘度下降率变化较快,虽然温度继续升高可以增加果胶粘度下降率,但50 ℃效率较高,可以节约能量。

图3 温度对果胶粘度的影响Fig.3 Effects of temperature on the viscosity of pectin
2.3入口压力对果胶粘度的影响
由图4可知,果胶粘度下降率随着入口压力的增大而降低,这是因为压力升高时,通过空化装置的流量降低,机械效应减弱,空化产生的剪切力也随之减弱[23],而机械效应是引起超声波降解果胶的主要原因[15],在水力空化处理过程中,其机理也是一致的,所以随着压力减小,通过空化装置的流量增大,果胶受到的剪切力越强,粘度下降越明显。在本实验考察的压力范围内,当入口压力为0.1 MPa时,果胶粘度下降率最大。
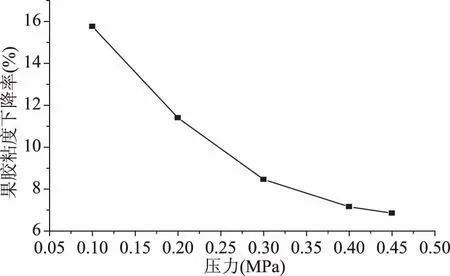
图4 压力对果胶粘度的影响Fig.4 Effect of pressure on the viscosity of pectin
2.4初始浓度对果胶粘度的影响
在一定浓度范围内,随着果胶浓度增大,果胶溶液本身的粘度也越大,在图5中可以发现,当果胶浓度增大时,果胶粘度下降率变小了,这是因为较高粘度的溶液导致空化产生困难,一定条件的空化作用产生的机械效应也是有限的。果胶浓度增大,相对来说,体系中大分子链总数较多,若空化作用剪切的分子链数量不变,则断裂的分子链比例变小,使得粘度下降率变小。本实验考察果胶初始浓度为1~5 g/L,发现浓度为1 g/L时,果胶粘度下降率最大。
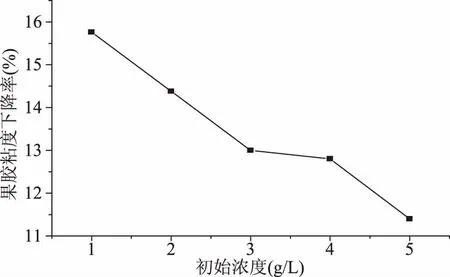
图5 初始浓度对果胶粘度的影响Fig.5 Effect of initial concentration on the viscosity of pectin
2.5空化时间对果胶粘度的影响
由图6可知,果胶粘度下降率随着时间增长而变大,在溶液空化60 min内,果胶粘度下降率上升缓慢,这是因为在一定范围内,处理时间越长,断裂的分子链数量积累量越多,但处理一定时间后,果胶粘度越来越小,水力空化对果胶大分子链的剪切效率降低,所以粘度下降率变化平缓。

图6 空化时间对果胶粘度的影响Fig.6 Effect of cavitation time on the viscosity of pectin
2.6标准曲线
将1.3.6中所述不同分子量葡聚糖标准品依次进样,在工作中将色谱图在同一坐标系重叠,重叠图如图7所示。根据凝胶渗透色谱分离原理[24-25]:当含有不同大小分子的样品通过具有多孔结构的凝胶构成的固定相时,大分子首先被洗脱出来,小分子后被洗脱出来,用于溶解样品的溶剂分子的分子量最小,可充分的进入凝胶的所有孔洞,因此最后从柱子中流出,使具有不同分子量大小的样品得以分离。所以图7中按保留时间从小到大,分别是T8~T1的葡聚糖标准品色谱图。根据葡聚糖标样分子量的对数Y与其对应的凝胶色谱的保留时间t的关系,经三阶线性拟合,得到回归曲线,如图8所示。回归方程为:Y=-0.0017t3+0.12t2-3.02t+30.9,R2=0.9994。
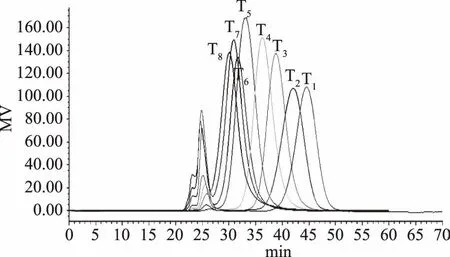
图7 葡聚糖标准品凝胶渗透色谱图Fig.7 Gel permeation chromatogram of dextran standard sample注:按保留时间从小到大依次为 T8、T7、T6、T5、T4、T3、T2、T1的色谱图。

图8 葡聚糖分子量标准曲线Fig.8 The standard curve of dextran molecular weight
2.7凝胶色谱表征
将pH为5、温度为50 ℃、浓度为1 g/L的果胶溶液在0.1 MPa压力下空化处理60 min后,粘度下降率达15.76%。按照1.3.7中所述方法取样并进行凝胶渗透色谱分析,果胶分子量分布色谱图如图9所示,色谱峰峰形良好,水力空化处理前后果胶的保留时间33.087 min延长至33.131 min,根据回归方程计算出果胶分子量由70515降低至57408,说明水力空化可有效降低果胶分子量。

图9 处理前后果胶凝胶渗透色谱图Fig.9 Gel permeation chromatography before and after pectin treatment
3 结论
本文采用一种新方法处理果胶,即通过水力空化装置产生空化效应并作用于果胶溶液。研究了不同pH、温度、入口压力、初始浓度、作用时间等条件下水力空化处理前后果胶粘度的下降率,并用凝胶色谱法对空化处理前后的果胶分子量分布进行比较分析。结果发现,当果胶溶液pH为5,温度为50 ℃,入口压力为0.1 MPa,浓度为1 g/L,处理时间为60 min时,果胶粘度下降率达15.76%,果胶相对平均分子量由70515下降至57408。
说明用水力空化处理果胶可以有效降低果胶粘度及其分子量,而且相比传统的化学法和酶法降解果胶,更有简单、环保、廉价等优势。
[1]Novosel’Skaya I L,Voropaeva N L,Semenova L N,et al. Trends in the science and applications of pectins[J]. Chemistry of Natural Compounds,2000,36(1):1-10.
[2]Kitajima J,Kimizuka K,Tanaka Y. Three new sesquiterpenoid glucosides of Ficus pumila fruit[J]. Chemical & Pharmaceutical Bulletin,2000,48(1):77-80.
[3]Shinohara K,Ohashi Y,Kawasumi K,et al. Effect of apple intake on fecal microbiota and metabolites in humans[J].
Anaerobe,2010,16(5):510-515.
[4]赵利,王杉. 果胶的制备及其在食品工业的应用综述[J]. 食品科技,1999(5):32-34.
[5]张学杰,郭科,苏艳玲. 果胶研究新进展[J]. 中国食品学报,2010,10(1):167-174.
[6]张雪娇,刘春叶,杨莉宁. 果胶含量测定方法研究现状[J]. 应用化工,2015(4):729-731.
[7]黄天斌. 果胶的提取方法与测定[J]. 文山学院学报,2004,17(4):380-381.
[8]张文博,高林,施秀芳,等. 高效体积排阻色谱法测定改性柑橘果胶的分子质量[J]. 色谱,2007,25(5):711-714.
[9]Takamine K,Abe J,Shimono K,et al. Physicochemical and gelling characterizations of pectin extracted from sweet potato pulp[J]. Journal of Applied Glycoscience,2007,54(4):211-216.
[10]Gidh A V,Decker S R,Vinzant T B,et al. Fungal-induced redistribution of kraft lignin molecular weight by multi-angle laser light scattering [J]. Chemical Engineering Communications,2006,193(12):1546-1561.
[11]Robert Talbot Knapp,James W Daily,F G Hammit. 空化与空蚀[M]. 水利水电科学研究院,译. 北京:水利出版社,1981:1-24.
[12]Kumar P Senthil,Kumar M Siva,Pandit A B. Experimental quantification of chemical effects of hydrodynamic cavitation[J]. Chemical Engineering Sinence,2000,55(9):1633-1639.
[13]李坚斌,李琳,李冰,等. 超声降解多糖研究进展[J]. 食品工业科技,2006(9):181-184.
[14]黄永春,马月飞,谢清若,等. 超声波辅助提取茶多糖及其分子量变化的研究[J]. 食品科学,2007,28(7):170-173.
[15]张丽芬. 果胶多糖超声波定向降解途径及机理研究[D]. 杭州:浙江大学.
[16]朱孟府,曾艳,邓橙,等.水力空化在水处理中的应用与研究进展[J]. 环境科学与技术,2010(S2):445-449.
[17]许佳丽,黄永春,袁媛,等. 基于文丘里管的水力空化降解壳聚糖的研究[J]. 食品工业科技,2016,37(2):244-248.
[18]何冰,张淑君,张德里. 水力空化联合H2O2降解壳聚糖的研究[J]. 三峡大学学报(自然科学版),2014(5):109-112.
[19]杨锋,刘婷,黄永春,等. 气体对涡流空化降解壳聚糖的影响[J]. 食品与机械,2015(2):47-51.
[20]刘雪,杨锋,任仙娥,等. 涡流空化对大豆分离蛋白黏度的影响[J]. 食品工业科技,2016,37(16):140-145.
[21]张帆,王鹏飞,黄永春. 水力空化降解壳聚糖产物分子量分布的研究[J]. 大众科技,2016,18(2):68-73.
[22]黄永春,吴修超,任仙娥,等. 水力空化对原糖溶液表面张力的影响[J]. 食品与机械,2012,28(6):16-18.
[23]戴干策. 化工流体力学[M]. 北京:化学工业出版社,1988:100-188.
[24]于世林. 高效液相色谱方法及应用[M]. 北京:化学工业出版社,2000:11-104.
[25]施良和. 凝胶色谱法[M]. 北京:科学出版社,1980:35-40.
Effectofhydrodynamiccavitationontheviscosityofpectinandcharacterizationbygelpermeationchromatography
MAOShan-qiao1,2,3,YANGFeng1,2,3,HUANGYong-chun1,2,3,HUANGCheng-du1,2,3,*
(1.Department of Biological and Chemical Engineering,Guangxi University of Science and Technology,Liuzhou 545006,China; 2.Guangxi Key Laboratory of Green Processing of Sugar Resources,Liuzhou 545006,China; 3.Key Laboratory for Processing of Sugar Resources of Guangxi Higher Education Institutes,Liuzhou 545006,China)
In order to find out the effect of hydraulic cavitation on the viscosity and molecular weight distribution of pectin,the cavitation effect was generated by the cavitation device and acted on the pectin solution. The change of pectin viscosity before and after hydrodynamic cavitation treatment was studied under different pH,temperature,inlet pressure,initial concentration and reaction time. The effect of hydrodynamic cavitation on pectin was evaluated by the decreasing rate of viscosity. The molecular weight distribution of pectin before and after treatment was analyzed by gel permeation chromatography(GPC). The results showed that when the pH of the solution was 5,the temperature was 50 ℃,the pressure of the population was 0.1 MPa,the concentration of pectin was 1 g/L and the treating time was 60 min,the viscosity of the pectin decreased by 15.76%. The GPC analysis showed that the relative average molecular weight of pectin decreased from 70515 to 57408. So the pectin treated by hydraulic cavitation can effectively reduce the viscosity of pectin and its molecular weight,which provided a new method for pectin degradation.
hydrodynamic cavitation;pectin;viscosity;molecular weight distribution
2017-04-18
毛善巧(1991-),男,硕士研究生,研究方向:糖资源加工技术及过程强化,E-mail:398019986@qq.com。
*
黄承都(1977-),男,博士,研究方向:糖资源加工技术及过程强化,E-mail:gx-hcd@163.com。
广西高等学校高水平创新团队及卓越学者计划资助(桂教人〔2014〕7号);广西科技大学创新团队支持计划资助;广西高校糖资源加工重点实验室开放课题(2015TZYKF04)。
TS202
A
1002-0306(2017)21-0065-05
10.13386/j.issn1002-0306.2017.21.013
