2-氰基-2,3-二烃基丁二酸酯类化合物的合成
2017-11-16周奇龙徐秀东
张 锐,谭 忠,周奇龙,徐秀东
(中国石油 化工股份有限公司 北京化工研究院 聚丙烯研究室,北京 100013)
2-氰基-2,3-二烃基丁二酸酯类化合物的合成
张 锐,谭 忠,周奇龙,徐秀东
(中国石油 化工股份有限公司 北京化工研究院 聚丙烯研究室,北京 100013)
开发了一种2-氰基-2,3-二烃基丁二酸酯类化合物的合成路线,并确定了最佳反应条件。该反应路线反应效率较高,并且能够避免废水的产生,极大地降低了后处理的成本。该路线在第二步通过换用不同的卤代烃,在基本相同的条件下可以制备不同结构的2-氰基-2,3-二烃基丁二酸酯化合物,尤其适合制备非对称烷基的2-氰基-2,3-二烃基丁二酸酯。该路线使得这类化合物的生产能够较容易的实现多样化,系列化和工业化,从而能够将使用该类化合物作为内给电子体的Ziegler-Natta聚丙烯催化剂产品差异化,系列化和高性能化。
2-氰基-2,3-二烃基丁二酸酯;内给电子体;聚丙烯催化剂
聚丙烯催化剂由主催化剂,助催化剂及外给电子体构成[1]。其中,主催化剂的性质主要取决于使用到的内给电子体。可以说,内给电子体的研发是聚丙烯催化剂的核心技术[2]。近年来,非邻苯二甲酸酯类内给电子体成为了学术界和工业界的研究热点,比较经典的有琥珀酸酯,1,3-二醚,二醇酯及2-氰基-2,3-二异丙基丁二酸酯等[3-6]。其中,2-氰基-2,3-二异丙基丁二酸酯是一种中国石化北京化工研究院开发的用于聚丙烯催化剂的新型内给电子体,使用该化合物作为内给电子体的催化剂制备得到的聚合物具有分子量分布宽,力学性能好等优点[7-10]。但目前只有2-氰基-2,3-二异丙基丁二酸二乙酯的合成路线被公开[11-13]。除此之外,没有公开的专利和文献对其它结构的2-氰基-2,3-二烃基丁二酸酯类化合物的合成进行报道。
本工作开发了一种2-氰基-2,3-二烃基丁二酸酯类化合物新的制备路线。该路线第二步中通过换用不同的卤代烃,可以在相同的条件下制备不同结构的2-氰基-2,3-二烃基丁二酸酯类化合物,尤其适合制备非对称烷基的2-氰基-2,3-二烃基丁二酸酯类化合物。该路线使得2-氰基-2,3-二烃基丁二酸酯类化合物的制备能够较容易的实现多样化,系列化和工业化,从而能够将使用该类化合物作为内给电子体的Ziegler-Natta聚丙烯催化剂产品差异化,系列化和高性能化。
1 实验部分
1.1 原料,试剂及仪器
溴代异戊酸乙酯99%,氰基乙酸乙酯99%,叔丁醇钾 99.5%,J&K Chemical公司;2-溴丙烷99.5%,1-溴正丁烷99%,溴代异丁烷99%,1-溴代正戊烷99.5%,溴代异戊烷99%,溴代环戊烷99%,Acros公司;KI 99%,NaH 60%(分散在矿物油中),Aldrich 公司;己烷,4分子筛干燥,含水量小于5×10-6。其他国产试剂均为北京化学试剂公司市售试剂,纯度为化学纯(CP)。二甲基甲酰胺(DMF)使用4分子筛干燥。
1H NMR谱图使用Brukerdmx核磁共振仪测定(300MHz,溶剂 CDCl3,内标 TMS,测定温度 300K)。化合物纯度及含量使用Agilent 7890 Series气相色谱和5977A质谱联用测定。
1.2 化合物的制备
1.2.1 2-氰基-3-异丙基丁二酸二乙酯(DCPS)
200g叔丁醇钾溶于500mL N,N'-二甲基甲酰胺中,待温度降至30℃以下,滴入氰基乙酸乙酯(ECA)181.4g和N,N'-二甲基甲酰胺的混合物100mL。控制温度不超过50℃,滴加完毕后加入KI 13.3g,滴加溴代异戊酸乙酯(EBiV)335.4g和N,N'-二甲基甲酰胺的混合物100mL,滴加时间4~5 h。滴加完毕后40℃反应3 h,80℃反应8h。停止反应,冷却,除去固体无机盐和溶剂。减压精馏得最终产物318.1g,产率 82.2%,纯度 99.0%(GC)。
1H NMR(CDCl3/TMS,300MHz)δ(×10-6):0.95~1.14(m,-CH(CH3)2),1.27~1.67(m,-OCH2CH3),2.15-2.22,2.29~2.30 (m,-CH(CH3)2),2.85~2.89,2.96-3.01(q,-CHCH(CH3)2),3.74~3.76,3.98~4.01(d,(NC)CH-),4.19~4.31(m,-OCH2CH3)。
1.2.2 2-氰基-2,3-二异丙基丁二酸二乙酯 33.2g 60%的NaH,加入到600mLDMF中。搅拌同时滴加200g 2-氰基-3-异丙基丁二酸二乙酯和100mL DMF的混合溶液。控制滴加温度为-25℃左右。滴加完毕后加入6.87gKI并自然升温至室温。随后升温至40℃,滴加122.3g2-溴丙烷和50 mLDMF的混合溶液。滴加完毕后40℃反应4h,80℃反应8h。停止反应,冷却,过滤,滤饼洗涤。蒸除溶剂,加入正己烷,冷却至室温并充分搅拌,过滤除去固体。旋除溶剂得粗品,减压精馏得最终产物160.2g,产率:68.2%,纯度96.3%(GC)。
1H NMR(CDCl3/TMS,300MHz)δ(×10-6):0.99~-1.04(t,-OCH2CH3),1.08~1.38(m,-CH(CH3)2),2.12~2.16(m,-CH (CH3)2),2.28~2.37 (m,- (NC)CCH(CH3)2),2.97~3.02(d,-CHCH(CH3)2),4.14~4.30(m,-OCH2CH3)。
1.2.3 2-氰基-2-正丁基-3-异丙基丁二酸二乙酯 使用相同的合成方法,将2-溴丙烷换为1-溴正丁烷制备得到2-氰基-2-正丁基-3-异丙基丁二酸二乙酯 185.1g,产率:75.1%,纯度 98.4%(GC)。
1H NMR(CDCl3/TMS,300MHz)δ(×10-6):0.86~1.02(t,-CH2CH2CH2CH3,m,-CH(CH3)2),1.29~1.38(t,-CH2CH2CH2CH3,m,-OCH2CH3),1.56~1.60(m,-CH2CH2CH2CH3),1.69~1.83(m,-CH2CH2CH2CH3),2.15~2.23(m,-CH(CH3)2),2.81~2.83(d,-CHCH(CH3)2),4.20~4.33(q,-OCH2CH3)。
1.2.4 2-氰基-2-异丁基-3-异丙基丁二酸二乙酯 使用相同的合成方法,将2-溴丙烷换为1-溴-2-甲基丙烷制备得到2-氰基-2-异丁基-3-异丙基丁二酸二乙酯193.5g,产率:78.5%,纯度98.0%(GC)。1H NMR(CDCl3/TMS,300MHz)δ(×10-6):0.86~1.09(t,-CH(CH3)2),1.30~1.36(m,-OCH2CH3),1.63~1.73(m,-CH2CH(CH3)2),1.80~1.91(m,-CH2CH(CH3)2),2.14~2.21 (m,-CHCH (CH3)2),2.77~2.81(d,-CHCH(CH3)2),4.14~4.33(q,-OCH2CH3)。
1.2.5 2-氰基-2-正戊基-3-异丙基丁二酸二乙酯 使用相同的合成方法,将2-溴丙烷换为1-溴正戊烷制备得到2-氰基-2-正戊基-3-异丙基丁二酸二乙酯 192.8g,产率:74.7%,纯度 98.1%(GC)。
1H NMR(CDCl3/TMS,300MHz)δ(×10-6):0.85~0.97(t,-CH2CH2CH2CH2CH3),0.99~1.10(m,-CH(CH3)2),1.21 ~1.37(t,-OCH2CH3,m,-CH2CH2CH2CH2CH3),1.58~1.61(m,-CH2CH2CH2CH2CH3),1.70~1.89(t,-CH2CH2CH2CH2CH3),2.15~2.22(m,-CHCH(CH3)2),2.80~2.83(d,-CHCH(CH3)2),4.16~4.32(m,-OCH2CH3)。
1.2.6 2-氰基-2-异戊基-3-异丙基丁二酸二乙酯 使用相同的合成方法,将2-溴丙烷换为1-溴-3-甲基丁烷制备得到2-氰基-2-异戊基-3-异丙基丁二酸二乙酯206.0g,产率:79.8%,纯度98.0%(GC)。
1HNMR(CDCl3/TMS,300MHz)δ(×10-6):0.85~1.10(t,-CH(CH3)2),1.30~1.37(t,-OCH2CH3,m,-CH2CH2CH(CH3)2),1.50~1.52(m,-CH2CH2CH(CH3)2),1.74~1.84(m,-CH2CH2CH(CH3)2),2.15-2.23 (m,-CH(CH3)2),2.81-2.84(d,-CHCH(CH3)2),4.17-4.28(q,-OCH2CH3)。
1.2.7 2-氰基-2-环戊基-3-异丙基丁二酸二乙酯 使用相同的合成方法,将2-溴丙烷换为溴代环戊烷制备得到2-氰基-2-环戊基-3-异丙基丁二酸二乙酯 154.1g,产率:60.1%,纯度 97.5%(GC)。
1H NMR(CDCl3/TMS,300MHz)δ(×10-6):0.86~1.08(t,-CH(CH3)2),1.22~1.38(t,-OCH2CH3),1.52~1.64(m,-CHCH2CH2CH2CH2-),1.85~1.89(m,-CHCH2CH2CH2CH2-),2.13~2.19(m,-CHCH2CH2CH2CH2-),2.36~2.42(m,-CH(CH3)2),2.89~2.92(d,-CHCH(CH3)2),4.16~4.32(q,-OCH2CH3)。
2 结果与讨论
在本工作中,首先使用σ-氰基乙酸乙酯(ECA)同σ-溴代异戊酸乙酯(EBiV)进行反应,得到2-氰基-3-异丙基丁二酸二乙酯(DCPS),再将其与不同的溴代烷进行反应得到一系列2-氰基-2,3-二烃基丁二酸二乙酯化合物(见图1)。这样,第一步反应中,由于溴代异戊酸乙酯的空间位阻相对较大,从而避免了氰基乙酸乙酯σ-位的双取代;第二步反应中,由于溴代烷体积较小,空间位阻较小,所以反应效率很高。
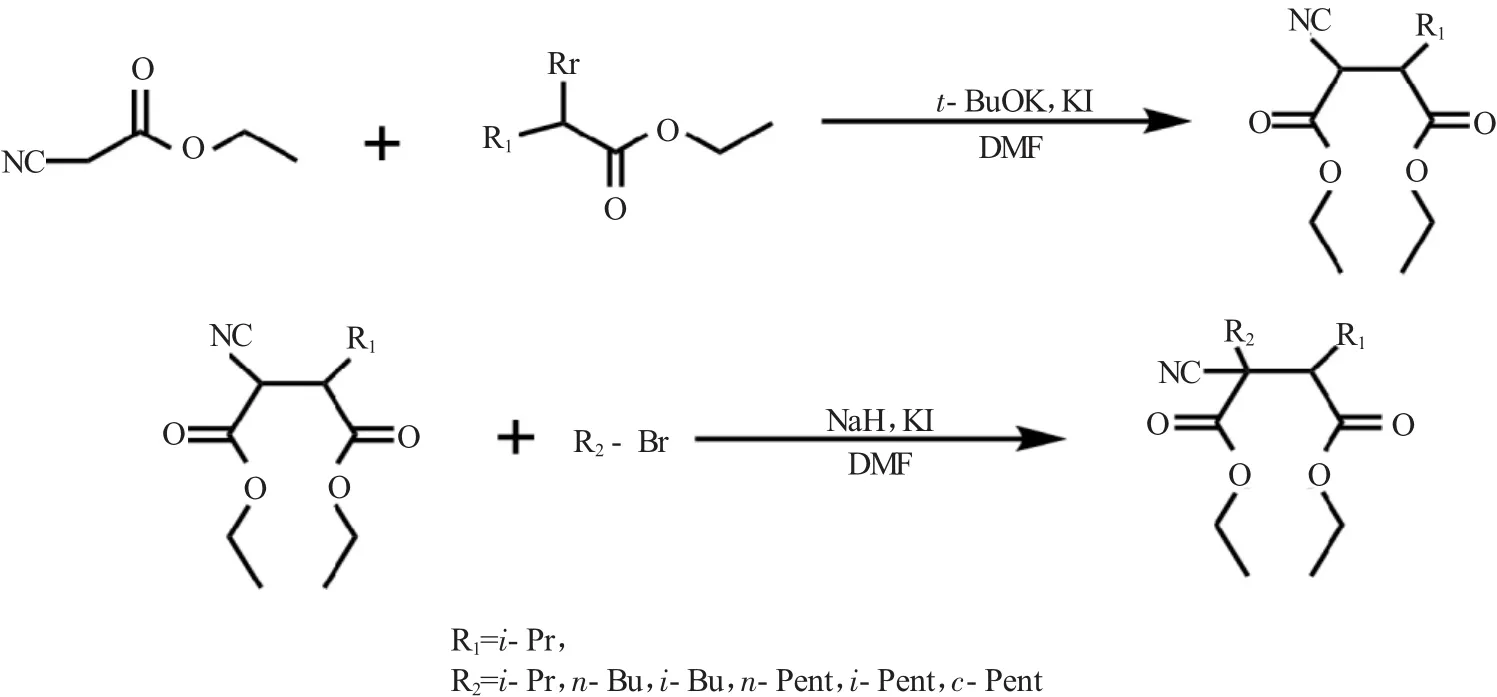
图1 2-氰基-2,3-二烃基丁二酸二乙酯类化合物的合成Fig.1 Synthetic route of 2-cyano-2,3-di-alkyl succinic acid diester
2.1 2-氰基-3-异丙基丁二酸二乙酯的合成
首先,考察了反应温度和时间对反应效率的影响,剩余原料和产物含量均为反应结束后,反应体系除去固体盐和溶剂后使用气相色谱测定。固定几种原料的比例和碱的种类,考察反应温度和反应时间对反应的影响,结果见表1。

表1 反应温度和时间对反应效率的影响Tab.1 Effects of reaction temperature and time on reaction efficiency
由表1可见,反应温度由50℃提高到80℃,延长反应时间由4~8h,都能很明显的提高溴代酯的转化率和最终产物的含量。当温度由80℃提高到100℃,对反应转化率没有进一步的提高。所以,我们固定反应条件为40℃,3h→80℃,8h。
接下来,考察了3种原料(碱,ECA,EBiV)的投料比例及碱的种类对反应的影响。当碱的用量较少或等量时,平行对比试验结果见表2。
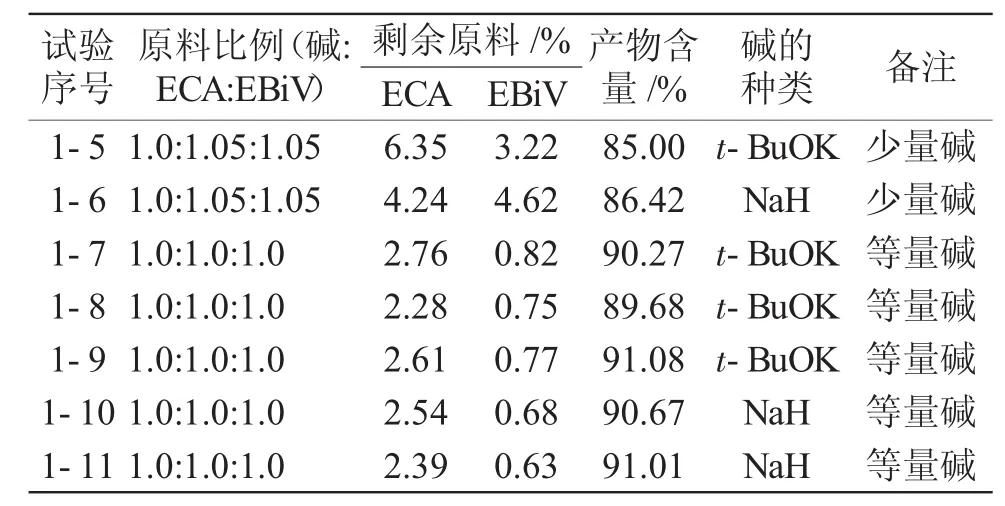
表2 碱用量较少和等量时对反应效率的影响Tab.2 Effects of less and equivalent amount of base on reaction efficiency
试验中选取了两种有代表性的碱:空间位阻较大的有机碱叔丁醇钾以及空间位阻很小的无机碱NaH。当碱用量较少时(试验1-5,1-6),两种原料都有较多的剩余,产物含量在85%左右。由试验6~10结果可知,当碱,ECA和EBiV三者用量相同时(试验1-7~1-11),两种原料剩余量明显减少,产物含量也提高至90%左右。当碱少量和等量时,两种碱的效果基本相同。
由表2可见,增加碱的用量可以提高反应效率,我们继续增加碱的用量(表3),当碱用量和EBiV相同,都大于ECA时(试验1-12,1-13),两种原料都有较多的剩余,产物含量不到90%。当碱用量和ECA相同,都大于EBiV时(试验1-14,1-15),产物含量提高到93%,反应体系中没有EBiV剩余,但是ECA剩余较多。
当碱用量比ECA和EBiV都多时,分为3种情况:ECA和 EBiV等量(试验1-16~1-19),ECA过量(试验1-20,1-21),EBiV过量(试验1-22,1-23)。当碱∶ECA∶EBiV为1.0∶0.9∶0.9时,反应效率较高,产物含量达到了96%左右,且EBiV没有剩余(试验1-17~19);同时提高ECA,EBiV用量(试验1-16),产物含量有所降低,EBiV出现剩余。只提高ECA用量(试验1-20,21),ECA剩余量增加,且产物含量降低;只提高EBiV用量(试验1-22,23),产物含量较高,但是EBiV剩余量较多。ECA和本步反应产物的沸点相差较大,粗产物直接减压蒸馏纯化即可。
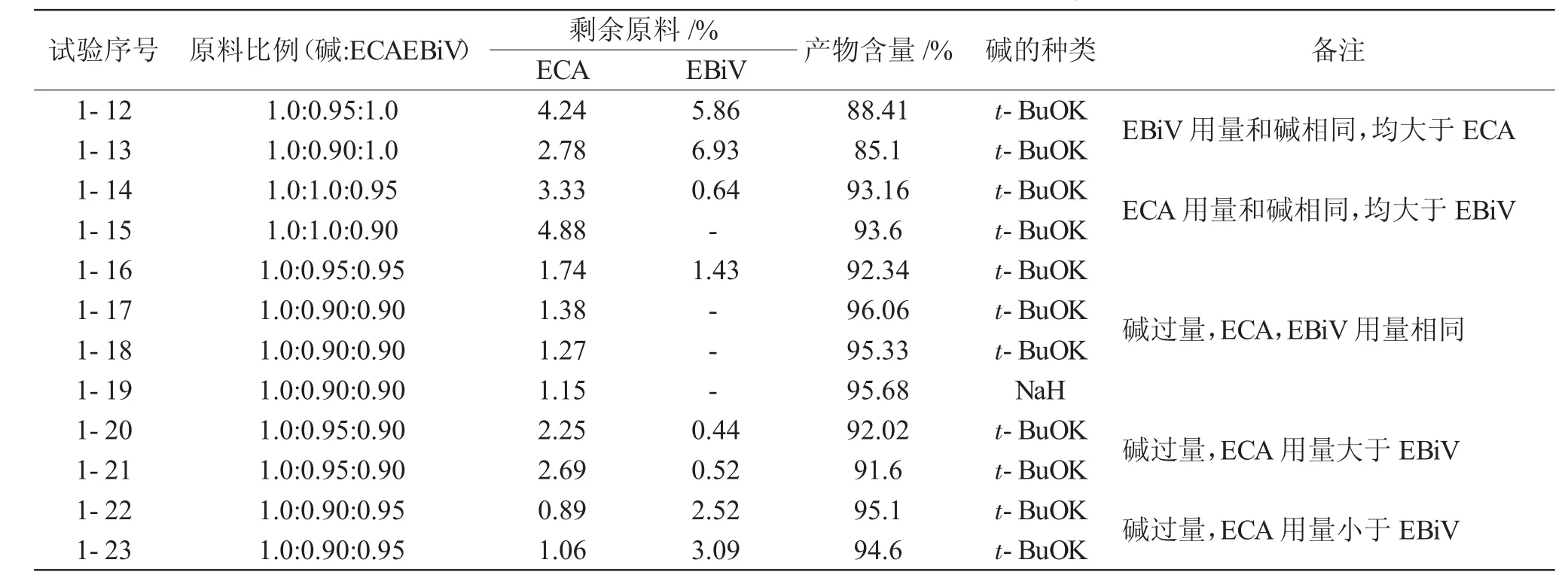
表3 碱过量时对反应效率的影响Tab.3 Effects of excess base on reaction efficiency
综合以上试验结果发现,固定反应温度和时间后,碱和两种有机原料的投料比例非常关键。当碱用量稍多时,ECA反应的最完全,EBiV反应程度不仅取决于其与碱和ECA的投料比例,还和ECA的反应程度(ECA和碱的用量比)有关系,当EBiV用量少于碱和ECA,且ECA反应程度较高时,EBiV在粗产物中基本上没有剩余。
综上所述,第一步最优的反应条件为40℃,3h→80℃,8h,反应物之比为碱:ECA:EBiV=1.0:0.9:0.9,该条件下,EBiV基本上没有剩余,ECA也剩余的很少,产物含量能达到96%左右。NaH和叔丁醇钾这两种碱的实际使用效果基本相同,考虑到叔丁醇钾和NaH的价格及使用时操作的难易程度,选取了较便宜且危险性较小的叔丁醇钾。
2.2 2-氰基-2,3-二烃基丁二酸二乙酯的合成
第二步反应中,由于反应底物2-氰基-3-异丙基丁二酸二乙酯(DCPS)空间位阻较大,所以选取了空间位阻较小的氢化钠,氢化钠和σ-位氢原子反应生成氢气,从反应体系中逸出,使反应不可逆且进行的比较完全。首先,考察了DCPS的滴加温度对反应效率的影响,实验结果见表4。
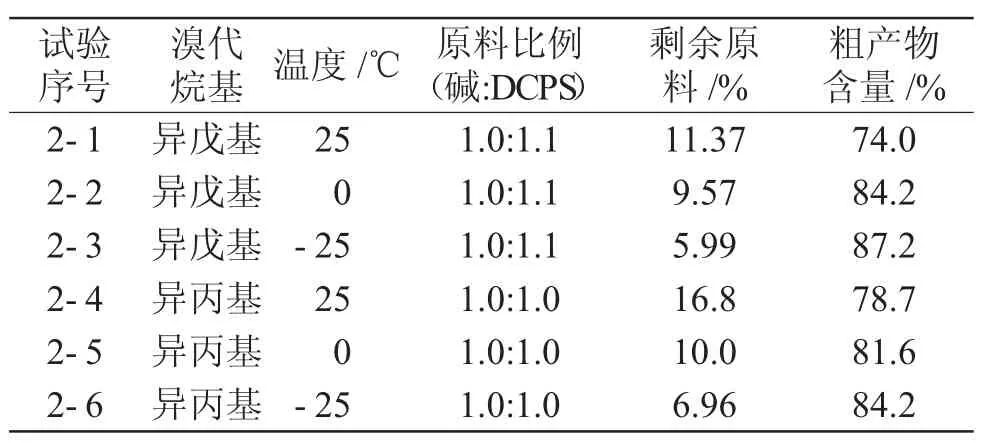
表4 滴加温度对反应效率的影响Tab.4 Effects of dropping temperature on reaction efficiency
表4结果表明,降低DCPS的滴加温度能够很明显的提高反应效率,随着温度的降低,反应效率在不断提高。DCPS上与氰基相连的碳和与异丙基相连的碳上的氢原子都可以与氢化钠进行反应,降低滴加温度有助于进一步扩大两个氢原子的反应活性,所以降低温度能够提高第二步反应的效率。
同第一步反应类似,碱用量也是个很关键的因素(表5)。以2-氰基-2,3-二异丙基丁二酸二乙酯为例,当碱用量小于DCPS时,反应结束后原料DCPS的量剩余较多,反应效率也相对较低(试验2-7)。当碱用量和DCPS等量时,DCPS剩余量有了明显减少,反应效率也提高了很多(试验2-8),继续增大碱的用量(试验2-9),原料DCPS的剩余量和粗产物的含量没有显著的变化,但是气相色谱证明在产物的后面又出现了杂质峰,表明过量的氢化钠可以同DCPS上与异丙基相连的碳上的氢原子反应生成碳负离子,进而同卤代烷反应生成杂质。所以,第二步反应中,氢化钠的用量不能超过DCPS。在不同结构的2-氰基-2,3-二烃基丁二酸二乙酯的制备中,也有着相同的规律(试验2-10~2-19),当碱用量和DCPS等量时,反应效率最佳。
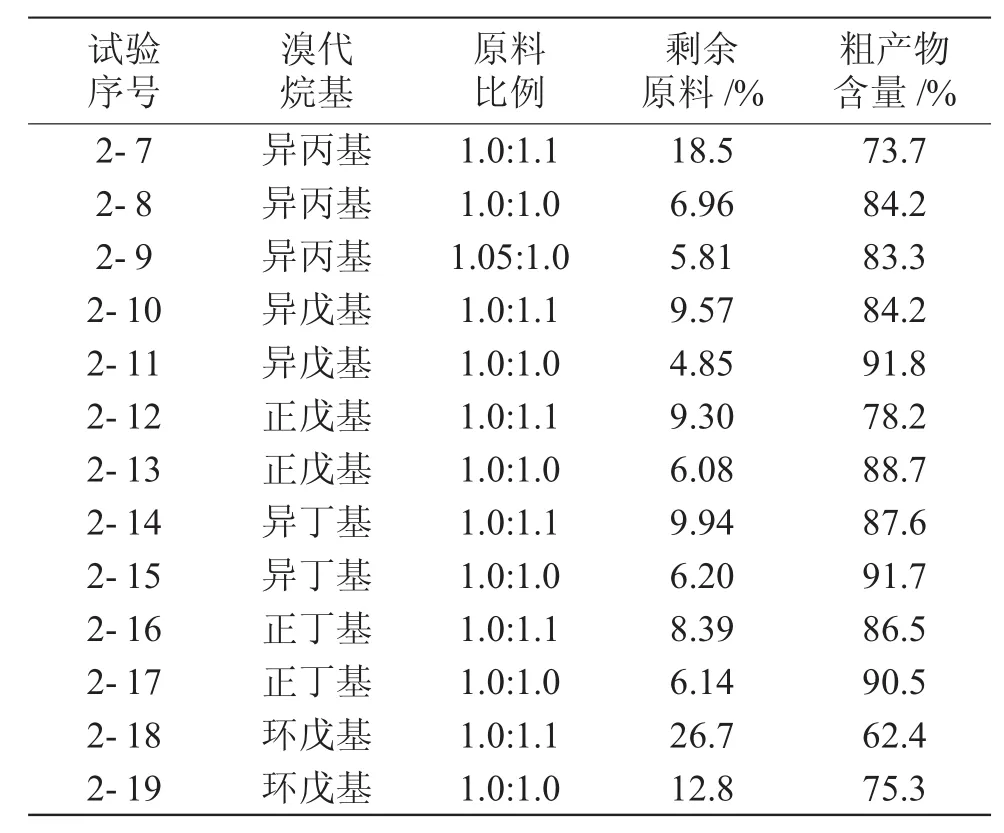
表5 碱用量对反应效率的影响Tab.5 Effects of the amount of base on reaction efficiency
第二步中,不同的卤代烷对反应效率也有影响,在试验2-9的条件下,将溴代异丙烷换为碘代异丙烷,原料DCPS剩余6.3%,产物含量为86.0%,也略有提高。但是,本工作中涉及到的卤代烷,碘代烷的价格是溴代烷的2~150倍不等,出于控制成本的考虑,均使用溴代烷。
除了不同类型的卤代烷,不同结构的溴代烷也会影响到反应的效率(表5)。同样条件下,当卤代烷反应位点为二级碳原子时,如2-溴丙烷和溴代环戊烷,反应效率较低,尤其是空间位阻较大的溴代环戊烷,仅为75.3%。当卤代烷反应位点为一级碳原子时,由于空间位阻较小,所以反应效率较高。当碳原子数相同时,支链溴代烷的反应效率略高于直链溴代烷,直链溴代烷分子链较长,末端空阻较小,分子柔性较大,分子链蜷曲将反应位点部分包裹起来,造成了反应效率较低。所以,不同结构的溴代烷中,溴代正戊烷反应效率最低,其次是分子链稍短的溴代正丁烷,而两个末端位阻较大,分子刚性较强的溴代异戊烷和溴代异丁烷反应效率最高。
本步反应在除去固体盐和溶剂后加入极性较小的正己烷,可以使粗产物中极性较大的杂质沉淀出来,进一步富集目标产物,便于减压精馏。并且正己烷可以回收利用,这样在整个反应路线中,就完全避免了废水的产生,极大地降低了后处理成本。
3 结论
本工作开发的2-氰基-2,3-二烃基丁二酸酯的合成路线分为两步,分别确定了最佳反应条件:第一步中使用叔丁醇钾(t-BuOK)作为碱,3种原料最佳的投料摩尔比为 t-BuOK∶ECA∶EBiV=1.0∶0.9∶0.9,反应温度和时间为 40℃,3h→80℃,8h。第二步中使用氢化钠(NaH)作碱效果较好,最佳投料摩尔比为NaH∶DCPS=1.0∶1.0。
该路线具有以下优势:首先,这两步反应使用的原料都是一般的工业原料,便宜易得。反应条件温和,不需要高温高压。并且,这两步反应的效率都很高,基本没有副反应的发生,第一步中,减压精馏前粗产物中目标产物的含量在96%左右;第二步中,根据使用到的不同卤代烃,减压精馏前粗产物中目标产物的含量在75~92%之间。
其次,整个反应的后处理过程中不产生废水,极大的降低了后处理成本。最后,也是最重要的,该合成方法可以在第二步中通过简单的换用不同的卤代烃,来制备不同的2-氰基-2,3-二烃基丁二酸酯化合物。使得该类化合物的生产能够较容易的实现多样化,系列化和工业化,从而能够将使用该类化合物作为内给电子体的Ziegler-Natta聚丙烯催化剂产品差异化,系列化和高性能化。
[1] 李玉芳.聚丙烯催化剂研究开发进展及其发展趋势[J].化工文摘,2008,(2):22-24.
[2] 杨渊,姚军燕,党小飞,等.内给电子体对Ziegler-Natta催化剂性能的影响[J].高分子学报,2013,(4):511-517.
[3] 钟赤锋,高明智,毛炳权.丙烯聚合用TiCl4/MgCl2催化剂的研究-内给电子体的作用[J].高分子学报,2003,(2):266-271.
[4] 温笑菁,冀棉,逯丽,等.丙烯等规聚合Ziegler-Natta催化剂体系中给电子体化合物的研究进展[J].高分子通报.2010,(6):53-60.
[5] 丁伟,张微,曲广淼.丙烯聚合Ziegler-Natta催化剂中给电子体的作用[J].化学工程师,2004,109(10):42-44.
[6] Zhong TAN,Lunjia Xie,Xiudong Xu,et al.SOLID CATALYST COMPONENT AND CATALYST FOR OLEFIN POLYMERIZATION[P].US:2013/0324682 A1,2013-12-05.
[7] 中国石油化工股份有限公司,中国石油化工股份有限公司,北京化工研究院.SOLID CATALYST COMPONENT AND CATALYST FOR OLEFIN POLYMERIZATION[P].WO,2012/097680 A1,2012-07-26.
[8] 中国石油化工股份有限公司,中国石油化工股份有限公司北京化工研究院.烯烃聚合用固体催化剂组分及催化剂[P].CN:102603932 A,2012-07-25.
[9] 中国石油化工股份有限公司,中国石油化工股份有限公司北京化工研究院.烯烃聚合用固体催化剂组分及催化剂[P].CN:102603933 A,2012-07-25.
[10] 中国石油化工股份有限公司,中国石油化工股份有限公司北京化工研究院.烯烃聚合用固体催化剂组分及催化剂[P].CN:102603931 A,2012-07-25.
[11] 中国石油化工股份有限公司,中国石油化工股份有限公司北京化工研究院.2,3-二异丙基-2-氰基丁二酸二酯类化合物的制备方法[P].CN:101811983 A,2010-08-25.
[12] 中国石油化工股份有限公司,中国石油化工股份有限公司北京化工研究院.PROCESS FOR PREPARING2,3-DI-NONSTRAIGHT-ALKYL-2-CYANO SUCCINIC ACID DIESTERS[P].WO:2010/094211 A1,2010-08-26.
[13] 田宇,谢伦嘉,凌永泰,等.2,3-二异丙基-2-氰基丁二酸二酯类化合物的制备方法及其应用[J].应用化学,2011,28:20-23.
Preparation of 2-cyano-2,3-di-alkyl succinic acid diester compound
ZHANGRui,TANZhong,ZHOUQi-long,XUXiu-dong
(Polypropylene Research Department,Beijing Research Institute of Chemical Industry,China Petroleum&Chemical Corporation,Beijing 100013,China)
A synthetic route of 2-cyano-2,3-di-alkyl succinic acid diester compounds was developed and the optimum reaction conditions were determined.This route has high reaction efficiency and no waste water was produced during the refinement,thus greatly reduce the cost of treatment.The 2-cyano-2,3-di-alkyl succinic acid diester derivatives of different structures can be easily prepared in the same condition by using different alkyl halide in the second reaction step especially the asymmetric 2-cyano-2,3-di-alkyl succinic acid diester.The diversified,serialized and industrialized of the production can easily achieved through this synthetic route and then the Ziegler-Natta polypropylene catalyst products with these compounds as an internal donor can be differentiated,serialized and with high performance.
2-cyano-2,3-di-alkyl succinic acid diester;internal donor;ziegler-natta polypropylene catalyst
TQ325.1
A
10.16247/j.cnki.23-1171/tq.20171073
2017-08-03
张 锐(1983-),男,高级工程师,毕业于北京大学化学与分子工程学院,博士学位,研究方向:聚丙烯催化剂的开发,内给电子体研发。
