3D打印技术在儿童腹膜后肿瘤手术规划中的应用
2017-11-15段光琦随帮志
段光琦 王 啸 刘 洁 唐 睿 随帮志 王 彭
3D打印技术在儿童腹膜后肿瘤手术规划中的应用
段光琦1王 啸1刘 洁1唐 睿1随帮志1王 彭2
目的 探讨3D打印技术在儿童腹膜后肿瘤手术规划及医患沟通中的应用价值。 方法选取2015年2月至2016年9月收治的11例腹膜后肿瘤患儿的全腹部CT平扫+增强DICOM格式的原始数据,使用Mimics软件对CT图像进行阈值选取、区域增长、模具处理、多层编辑修饰等建模过程,最终获得完整的肿瘤3D模型,通过3D打印机打印出患儿的肿瘤模型。术前将得到的肿瘤3D模型通过计算机进行分析并与患儿家属谈话。采用3D模型使用情况调查表分别对患儿家属及手术助手进行问卷调查。 结果 本研究成功建立11例腹膜后肿瘤的3D模型,肿瘤与周围临近脏器、血管的情况显示清晰。其中8例成功施行肿瘤切除术,3例患儿家属要求转院治疗。患儿家属较谈话前对病情掌握程度明显提高(P<0.05),手术助手满意度调查评分(9.1±1.5)分。 结论 通过3D打印出的肿瘤模型可清晰显示儿童腹膜后肿瘤复杂的解剖关系,有助于术前规划出合理的手术方式,并可提高患儿家属对于手术方式的认知,有利于增进家属对于治疗的配合。
3D打印技术;腹膜后肿瘤;外科手术;儿童
腹膜后肿瘤(retroperitoneal tumor,RT)是指起源于腹膜后间隙的肿瘤,广义上可包括腹膜后脏器如肾、肾上腺等实质性脏器肿瘤[1]。在小儿恶性肿瘤中,腹膜后肿瘤仅次于白血病及中枢神经系统肿瘤而居第三位,是威胁小儿健康和生命的严重疾病[2]。由于其位置深在,且症状隐匿,组织学类型繁多,缺乏特异性临床表现,难以早期发现,以至于确诊时往往肿瘤已较大。治疗原则以手术治疗为首选[3]。由于肿瘤常累及腹膜后血管、神经及脏器,解剖关系复杂,致使手术难度增大。目前通过增强CT可以在断层结构上进一步明确瘤体与周围组织血管的解剖关系,然而,由于医师阅片水平的不同,对影像学数据信息的理解也存在很大差异,一定程度上会影响医疗小组的诊断,更有甚者会影响术者对整个病情的判断。如果能够最大程度应用影像学手段明确肿瘤周围解剖关系,对于实施个性化的手术方案具有重大意义,并且可以提高医患沟通的效率。近年来3D打印技术和医学影像学技术不断发展,3D打印技术逐步应用于一些复杂手术的术前规划及手术操作训练中,尤其在骨科、口腔科及颅颌面外科手术中应用较多[4-6]。根据患者术前的三维影像学资料,如CT、MRI等,应用3D打印技术可直接、精确地打印手术区域的解剖结构。术者可在此基础上做出更准确的诊断,制定更详细的手术方案,评估术中可能存在的风险,并可在实物模型上操作、练习手术,预演手术结果等,从而缩短了手术时间,提高了手术成功率。然而,其在腹部外科中,尤其实体肿瘤方面应用相对较少。有文献报道在肝、肾肿瘤方面有初步的应用,但其仅仅局限于组织脏器的分割,对脏器周围的解剖结构缺乏全面的分析[7]。主要原因在于周围血管的复杂、脏器的变异等等使得构建肿瘤三维重建模型的复杂性和专业性高,图像分割建模的难度大大增加,限制了3D打印技术的应用。本研究应用Mimics软件进行3D建模,获取腹膜后肿瘤3D模型,通过3D打印机打印出肿瘤模型,探讨3D打印技术在儿童腹膜后肿瘤手术规划及医患沟通中的应用价值。
材料与方法
一、研究对象
选取2015年2月至2016年9月本院收治的11例术前经腹部彩超及全腹增强CT诊断为腹膜后肿瘤患儿,其中肾母细胞瘤4例,神经母细胞瘤3例,腹膜后畸胎瘤4例,均拟行肿瘤切除术。其中男4例,女7例,年龄12~65个月,平均年龄(44.9±12.3)个月,CT检查提示肿瘤直径6.3~15.8 cm,平均(10.5±2.7)cm。手术助手调查对象:4名从事小儿普外、泌尿外科工作1年以上的住院医师。
二、设备以及软件
双源64层CT机(Siemens,Somatom Definition),三维重建软件:Mimics R17.0,Magics 18.0(Materialise),3D打印机:CONNECX 350;SLA300(江苏舟可医疗器械科技有限公司)。
三、建立腹膜后肿瘤3D模型
患儿家属签署CT检查同意书后行全腹部增强CT检查。扫描范围:膈顶至耻骨联合,由头侧向足侧扫描。分别采集动脉期、静脉期、延迟期三项数据,扫描结束后进行薄层重建,重建层厚0.625 mm、间隔0.625 mm,取得DICOM格式的CT数据,将其导入Mimics R17.0软件进行三维重建。对增强CT的3期依次使用阈值选取、区域增长、多层编辑修饰等技术进行三维重建,人工去除肿瘤周围脂肪组织,保留并重建肿瘤周围大动脉、静脉、其他邻近脏器,区分正常组织和肿瘤组织,对模型进行360°全方位旋转观察,以显示肿瘤部位及其与周围结构的关系。
四、模型3D打印
模型打印采用两种方式:①光固化成型法,将重建数据以stl格式保存导入到Magics软件中,进行数据预处理,检查水密性无误后,进行支撑设计,切片处理,将切片数据导入SLA设备进行快速光固化成型。打印完成后,检查模型无缺损,采用95%酒精浸泡去除支撑,二次固化,然后打磨,抛光,进行后期上色处理,最后进行烘干。②多喷头喷射法。将重建数据以彩色stl格式导入CONNECX EDEN 350自带软件,选择合适的摆放位置、切片厚度以及包裹方式,进行自动切片以及快速成型。加工结束后,应用高压水枪将水溶性支撑冲洗去除。
五、满意度调查
术前同一术者应用3D模型与患儿家属进行术前谈话,使其了解肿瘤及其周围器官的解剖特点、位置、手术方式、手术可能出现的并发症等。患儿家属于交代病情前后两次回答手术相关问题(共20个问题),对谈话效果及3D打印模型用于交流的认可度进行调查。
术后使用满意度调查表对4名从事小儿普外、泌尿科工作时间1年以上的住院医师进行调查,内容包括:模型对肿瘤大小、血管关系的理解是否有帮助;模型对手术方案理解是否有帮助;模型对减少手术并发症是否有帮助。评分从高到低依次为1~10分,1分为根本没用,10分为非常有用。
六、统计学处理
结 果
本研究中所有患儿家属对手术安排及3D打印知情,并同意参与这一单中心前瞻性观察。所有患儿均接受CT扫描确诊后拟行肿瘤切除术。均用软件行数字建模后,使用三维重建软件和3D打印机对肿瘤模型进行分色打印(如图1,图2)。所有患儿家属术前对病情特点、手术方案及风险的了解均通过术者用患者CT资料和3D打印模型进行交流获取,应用3D模型交代病情后11例患儿家属对肿瘤病变特点、肿瘤与周围器官血管的分布情况及手术方案的认知程度较交代病情前显著提高(P<0.05,表1)。
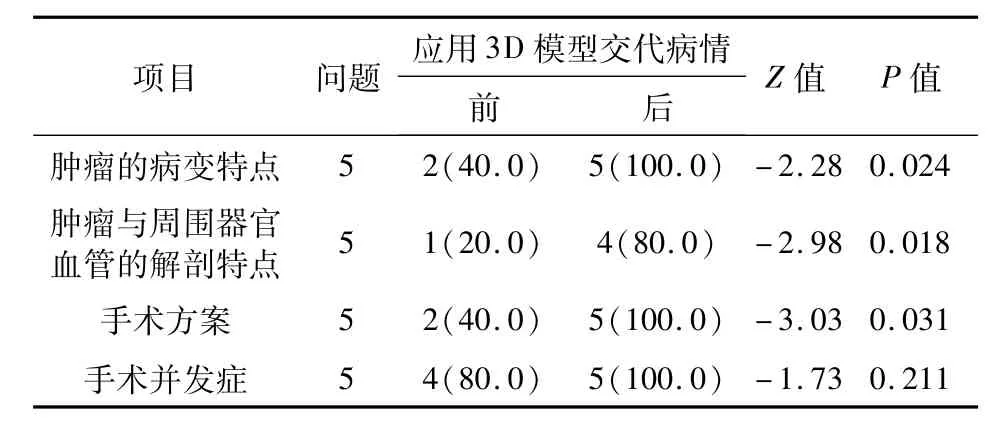
表1 11例腹膜后肿瘤患者家属应用3D打印模型交代病情前后正确回答手术相关问题结果[个,中位数(%)]Table 1 Results of correctly answering operative questions before and after history-knowing in parents of 11 RT children and after during the application of 3D printingmodel[n,median(%)]
11例患儿中,有8例成功施行肿瘤切除术,3例患儿家属要求转院治疗。4位初级职称医师认为3D打印模型精确显示了患者肿瘤大小及周围组织、血管的情况,有利于术前预知手术切除范围、应该规避的血管及手术的难点,根据3D打印模型进行术前规划对手术的帮助很大,对3D打印模型的使用满意度详见表2。两种不同的快速成型加工方法的比较,详见表3。

表2 4名低年资医师对于肿瘤3D模型的满意度(分)Table 2 Satisfaction level of3D tumormodeling for 4 junior physicians(points)
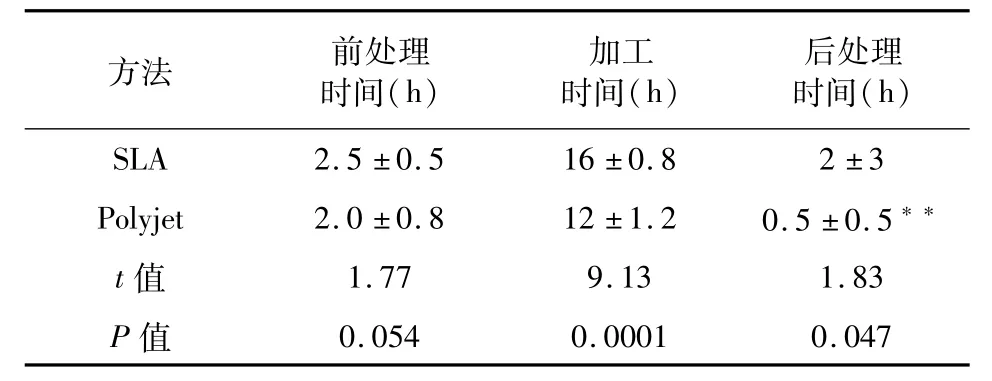
表3 SLA与Polyjet两种快速成型加工方法的比较Table 3 Comparison of two fast prototyping Methods SLA versus Polyjet
11例患儿的3D肿瘤模型成功建立,平均耗时245 min,模型清晰地反映了肿瘤与周围脏器、血管的毗邻关系(图1,图2)。
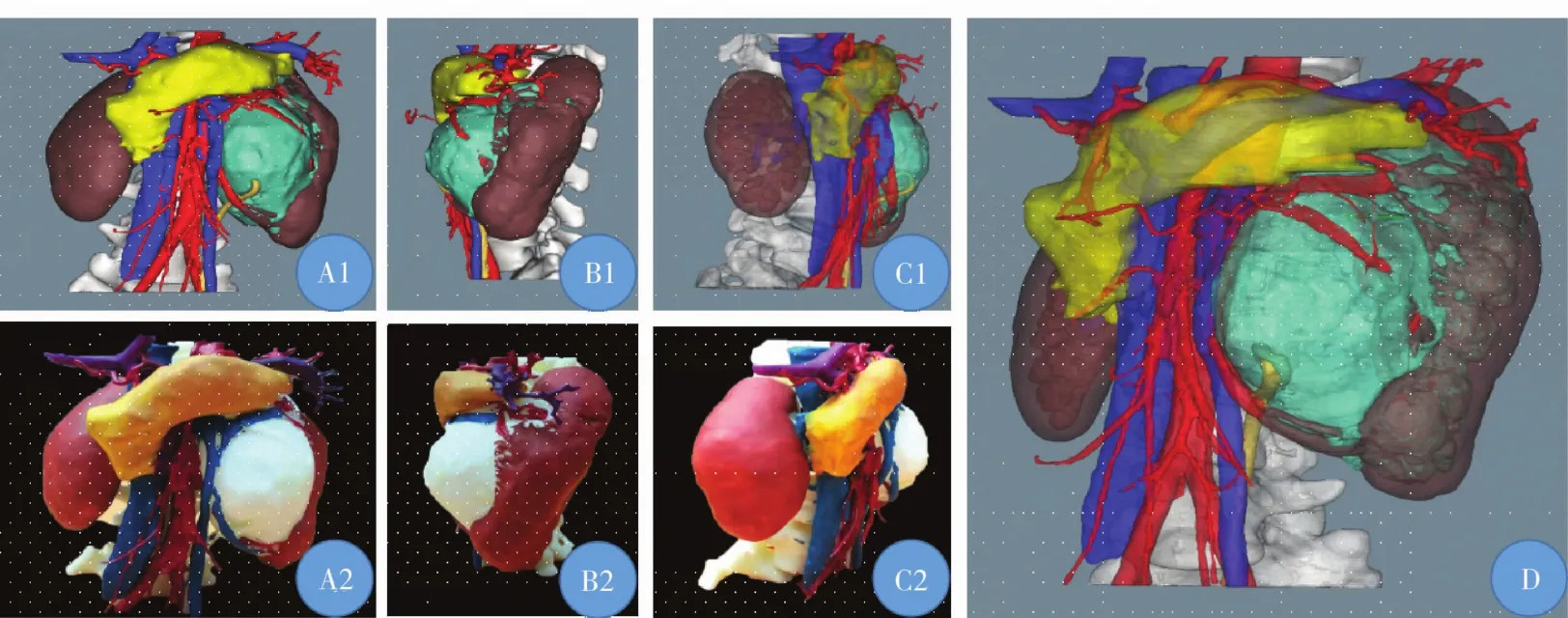
图1 肾母细胞瘤3D肿瘤模型图Fig.1 Nephroblastoma illustration of3D model
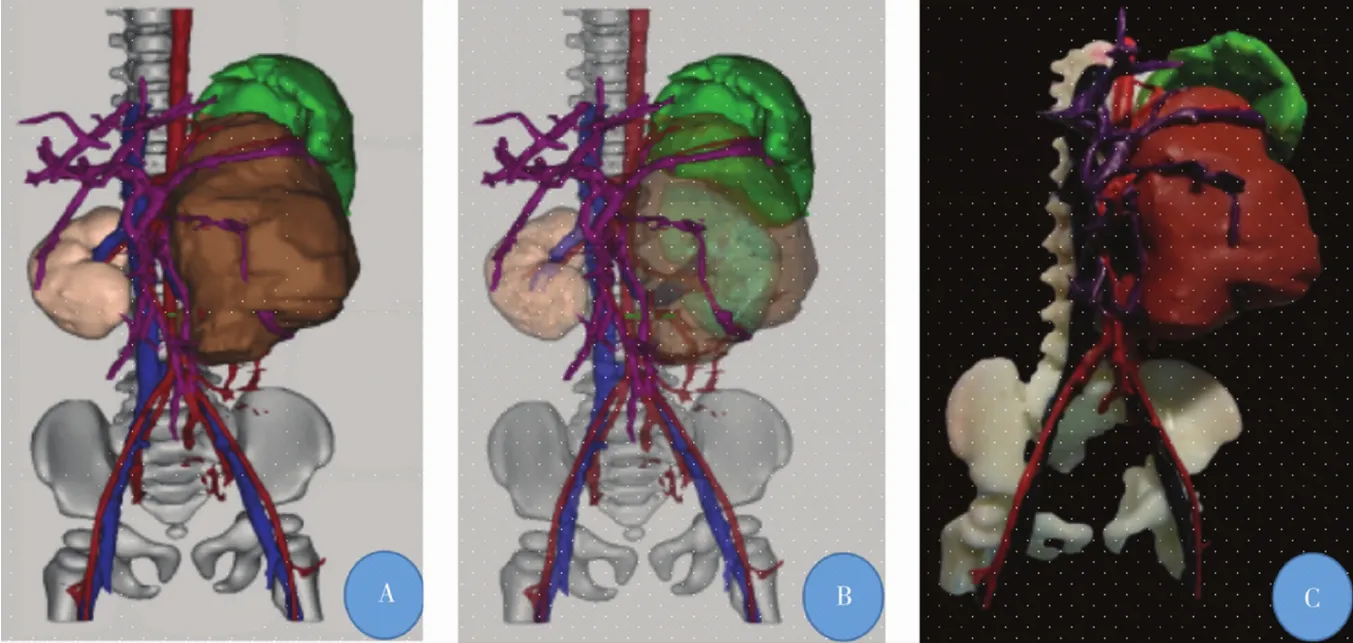
图2 神经母细胞瘤3D肿瘤模型图Fig.2 Neuroblastoma
讨 论
一、重建方法的区别
目前主流的重建方法以CT设备自带的重建模块为基础,采用多种重建方法,比如最大密度投影、最小密度投影等进行三维重建[8]。但仅仅在工作站中使用,临床医生无法通过PACS在终端进行三维成像,并对图像进行个体化的虚拟手术预演[9]。商业软件的出现,结合医生的阅片经验,采用多种算法结合,对瘤体以及周围血管、组织进行分割,不仅可以在个人电脑中实现,而且可以多方位全角度地实现对瘤体结构的观察,并且可以模拟投影至2D断面的解剖结构,与此同时,由于采用了通用的标准保存格式,可以轻松地将数字模型通过快速成型的方式转化为实物模型,让医患双方更为直接地了解病变的程度以及解剖关系[10]。
二、不同3D打印技术的比较
腹膜后血管变异较多,同时由于肿瘤的侵占,血管以及其他组织的移位,如果对肿瘤周围组织结构没有充分认识而贸然手术,将有可能产生灾难性的后果[11]。目前对于此类模型的彩色打印主要有3种方法,第1种,光敏树脂光固化成型后期上色处理,第2种石膏粉末彩色打印,第3种多色光敏树脂喷射打印。有文献报道,采用粉末粘结技术对肾脏模型进行3D打印,虽然能反映组织的解剖结构关系,但是粉末粘结的表面颗粒感很强,而且石膏粉末成型质硬较脆容易破损,在本研究中被排除在外[12]。本研究第1种方法选用的是高韧性的光敏树脂,通过后期处理打磨抛光后去除台阶纹理效应,然后进行上色处理,最终能清晰地还原瘤体周围解剖结构,整个打印过程的重点在于前期数据处理、支撑设计以及后期的支撑去除、上色工艺等环节[13]。但由于材料的局限性,无法获得对模型内部结构的直观认识。不过,最大的优势在于费用相对低廉[14-15]。相比而言,多色树脂喷射打印,模型仿真度较高,透明化处理可以让医患双方清楚地观察到模型内部的结构,而且工艺处理简单,但是费用相对昂贵,临床应用推广会受到很大的局限[16]。
三、本技术的关键点
如何评价一个模型的优劣,除了本身的加工工艺之外,精准的图像分割,建模是实现优秀模型的基础和必要条件。只有做到精准的分割与建模,才可能做到精准的打印。如果分割出现问题,严重者可能导致整个手术方案的失败。尽管目前的商用医学图像重建软件已经可以做到模块化,但是对于软组织的分割依然是一个难题,一方面在于组织的变异,尤其是腹膜后组织、血管错综复杂,没有一定的临床经验基础,很难将血管组织结构分割完全[17]。只有对断层结构有了充分的认识,形成了空间解剖结构,才能做到分割准确。同时,在分割过程中,必要时结合图谱以及多平面的交互分割,最终确保模型分割的可靠性[18]。
四、模型的临床意义
3D模型的使用使术前与患儿家属的沟通变得容易,患儿家属对病情、手术方案的理解会明显提高[19]。以往无论对患儿家属如何详细介绍CT情况或用文字方法介绍病情及手术方案,患者的理解程度都不高。本研究结果显示,数字建模有利于明显提高患儿家属对肿瘤病变特点及手术方案的理解,增加了医患之间的相互理解,由于患儿家属对肿瘤位置特点更加熟悉,针对肿瘤切除术可能出现的特异性并发症就会有所理解,减少了医疗纠纷的发生。本研究参与调研的初级资质医师认为,3D数字模型能够精确显示患儿肿瘤的大小及周围组织和血管的情况,有利于术前规划手术切除范围、预知应该规避的血管及手术的难点,满意度较高。传统的影像学资料需要术者有丰富的阅片经验才能达到完全了解,而3D数字模型弥补了初级资质外科医师阅片经验的不足,从而增加了医生对手术成功的把握。
本研究应用3D打印技术,将儿童腹膜后肿瘤等比例还原,清晰显示儿童腹膜后肿瘤复杂的解剖关系,用于手术预演以及医患沟通,有助于术前规划出合理的手术方式,并可提高患儿家属对于手术方式的认知,有利于家属对于治疗的配合。
1 Tseng WW,Madewell JE,WeiW,et al.Locoregional disease patterns in well-differentiated and dedifferentiated retroperitoneal liposarcoma:implications for the extent of resection?[J].Ann Surg Oncol,2014,21(7):2136—2143.DOI:10.1245/s10434—014—3643—4.
2 Solovyov AE,Morgun VV,Paholchuk AP.Neuroblastoma in pediatric patients[J].Klin Khir,2015,(6):59—61.
3 Rajeev R,Patel M,Jayakrishnan TT,et al.Retroperitoneal solitary fibrous tumor:surgery as first line therapy[J].Clin Sarcoma Res,2015,5(5):19.DOI:10.1186/s13569—015—0034—y.
4 Wang J,Yang M,Zhu Y,et al.Phage nanofibers induce vascularized osteogenesis in 3D printed bone scaffolds[J].Adv Mater,2014,26(29):4961—4966.DOI:10.1002/adma.201400154.
5 Mironov V,Boland T,Trusk T,et al.Organ printing:computer-aided jet-based 3D tissue engineering[J].Trends Biotechnol,2003,21(4):157—161.DOI:10.1016/S0167—7799(03)00033—7.
6 Boland T,Mironov V,Gutowska A,et al.Cell and organ printing 2:fusion of cell aggregates in three-dimensional gels[J].Anat Rec A Discov Mol Cell Evol Biol,2003,272(2);497—502.DOI:10.1002/ar.a.10059.
7 Fang CH,Tao HS,Yang J,et al.Impact of three-dimensional Reconstruction technique in the operation planning of centrally located hepatocellular carcinoma[J].J Am Coll Surg,2015,220(1):28—37.DOI:10.1016/j.jamcollsurg.2014.09.023.
8 Mironov V,Boland T,Trusk T,etal.Organ printing:computer-aided jet-based 3D tissue engineering[J].Trends Biotechnol,2003,21(4):157—161.DOI:10.1016/S0167—7799(03)00033—7.
9 Lee V,Singh G,Trasatti JP,etal.Design and fabrication of human skin by three-dimensional bioprinting[J].Tissue Eng Part C Methods,2014,20(6):473—484.DOI:10.1089/ten.TEC.2013.0335.
10 Rengier F,Mehndiratta A,von Tengg-Kobligk H,etal.3D printing based on imaging data:review ofmedical applications[J].Int JComput Assist Radiol Surg,2010,5(4):335—341.DOI:10.1007/s11548—010—0476—x.
11 牛爱国,时保军,温哲,等.小儿腹膜后肿瘤切除术涉及重要血管的处理[J].中华小儿外科杂志,2001,22(01):8—9.DOI:10.3760/cma.j.issn.0253—3006.2001.01.003.Niu AG,Shi BJ,Wen Z,et al.Management of major blood vessels involved in retroperitoneal neoplasms in children[J].Chinese Journal of Pediatric Surgery,2001,22(01):8—9.DOI:10.3760/cma.j.issn.0253—3006.2001.01.003.
12 贺超良,汤朝晖,田华雨,等.3D打印技术制备生物医用高分子材料的研究进展[J].高分子学报,2013,10(06):722—732.DOI:10.3724/SP.J.1105.2013.12430.He CL,Tang ZH,Tian HY,etal.Advances in the development of biomedical polymermaterials fabricated by 3-dimensional printing technology[J].Acta Polymerica Sinica,2013,10(06):722—732.DOI:10.3724/SP.J.1105.2013.12430.
13 方驰华,方兆山,范应方,等.三维可视化、3D打印及3D腹腔镜在肝肿瘤外科诊治中的应用[J].南方医科大学学报,2015,16(05):639—645.DOI:10.3969/j.issn.1673—4254.2015.05.04.Fang CH,Fang ZS,Fan YF,et al.Application of 3D visualization,3D printing and 3D laparoscopy in the diagnosis and surgical treatment of hepatic tumors[J].Journal of Southern Medical University,2015,16(05):639—645.DOI:10.3969/j.issn.1673—4254.2015.05.04.
14 黄沙,姚斌,付小兵.3D打印技术在医学领域的应用与发展[J].中华创伤杂志,2015,31(01):7—9.10.3760/cma.j.issn.1001—8050.2015.01.003.Huang S,Yao B,Fu XB.Application and development of 3-dimensional technology in medical fields[J].Chinese Journal of Trauma,2015,31(01):7—9.10.3760/cma.j.issn.1001—8050.2015.01.003.
15 Waran V,Narayanan V,Karuppiah R,et al.Utility of multimaterial3D printers in creatingmodelswith pathological entities to enhance the training experience of neurosurgeons[J].JNeurosurg,2014,120(2):489—492.DOI:10.3171/2013.11.JNS131066.
16 李永欣,黄文华.3D打印技术在人体器官方面的应用研究及展望[J].医学研究杂志,2015,44(06):119—127.DOI:10.11969/j.issn.1673—548X.2015.06.002.Li YX,Huang WH.Application and prospective of threedimensional printing for human organs[J].Journal ofMedical Research,2015,44(06):119—127.DOI:10.11969/j.issn.1673—548X.2015.06.002.
17 杜宇雷,孙菲菲,原光,等.3D打印材料的发展现状[J].徐州工程学院学报(自然科学版),2014,7(01):3—5.DOI:10.3969/j.issn.1674—358X.2014.01.004.Du YL,Sun FF,Yuan G,etal.Currentstatus ofmaterials for three-dimensional printing[J].Journal of Xuzhou Institute of Technology(Natural Sciences Edition),2014,7(01):3—5.DOI:10.3969/j.issn.1674—358X.2014.01.004.
18 Tam MD,Laycock SD,Bell D,etal.3-D printout of a DICOM file to aid surgical planning in a 6 year old patient with a large scapular osteochondroma complicating congenital diaphyseal aclasia[J].J Radiol Case Rep,2015,6(1):31—37.DOI:10.3941/jrcr.v6i1.889.
19 葛宏伟,张弋,李宁忱,等.3D打印技术在肾肿瘤手术规划中的应用研究初探[J].中华泌尿外科杂志,2014,35(9):659—663.DOI:10.3760/cma.j.issn.1000—6702.2014.09.007.Ge HW,Zhang Y,Li NC,et al.Application of 3D-printing technology in surgical planning for renal tumor:a preliminary report[J].Chinese Journal of Urology,2014,35(9):659—663.DOI:10.3760/cma.j.issn.1000—6702.2014.09.007.
App lication of 3-dimensional printing in surgical planning for pediatric retroperitoneal tumor
.
Duan Guang-qi1,Wang Xiao1,Liu Jie1,Tang Rui1,Sui Bang-zhi1,Wang Peng2.1.Department of Pediatric Surgery,Gejishan Hospital,Wannan Medical College,Wuhu 241001,China;2.Jiangsu Zhouke Medical Device Technology Co.,Ltd,Nantong 226000,China.Email:duangq453@sina.com
Objective To explore the application of 3-dimensional(3D)printing in surgical planning for pediatric retroperitoneal tumor(RT)and communication between doctor and patients.Methods From February 2015 to September 2016,11 RT children
enhanced computed tomography(CT)scanning of whole abdomen.The imaging data were saved in DICOM format.3Dmodelwas reconstructed by MIMICSsoftware by threshold,region growingmorphology operation and multi-layer edition.Meanwhile,the data ofmodel were sent to 3D printer.Finally themodel was used for surgical planning and doctor-patient communications.Questionnaire was distributed at the same time.Results Clinical3Dmodelswere successfully established by 3D printing.Based upon thesemodels,tumors,adjacent organs and vessels were distinctly delineated.With the assistance of printing models,8 cases underwent tumorectomy successfully and another 3 cases opted for hospital transfer.On average,the questionnaire results of patient satisfaction were higher than before(P<0.05).And the satisfaction results of surgeon assistants were 9.1±1.5 points.Conclusion Complex relationship between tumor and adjacent tissuemay be distinctly delineated by 3D printingmodels.Moreover,this technique allows for rational individualized surgical planning,improved understanding of disease and better therapeutic compliance.
3D Printing;Retroperitoneal Neoplasms;Surgical Procedures,Operative;Child
10.3969/j.issn.1671—6353.2017.05.004
皖南医学院弋矶山医院引进人才科研基金(YR201403)
1.皖南医学院弋矶山医院小儿外科(安徽省芜湖市,241001);2.江苏舟可医疗器械科技有限公司(江苏省南通市,226000),Email:duangq453@sina.com
2017—03—21)
本文引用格式:段光琦,王啸,刘洁,等.3D打印技术在儿童腹膜后肿瘤手术规划中的应用[J].临床小儿外科杂志,2017,16(5):430—435.
10.3969/j.issn.1671—6353.2017.05.004.
Citing this article as:Duan GQ,Wang X,Liu J,et al.Application of 3D printing in surgical planning for pediatric retroperitoneal tumor[J].JClin Ped Sur,2017,16(5):430—435.DOI:10.3969/j.issn.1671—6353.2017.05.004.
