溶胶凝胶-自蔓延燃烧法中焙烧温度对CuFe2O4晶体结构的影响
2017-11-09薛锐王永强臧萌陈曦刘敏敏
薛锐,王永强,2,臧萌,陈曦,刘敏敏
(1中国石油大学(华东)化学工程学院,山东 青岛 266580;2中国石油大学(华东)石油石化污染物控制与处理国家重点实验室,山东 青岛266580)
溶胶凝胶-自蔓延燃烧法中焙烧温度对CuFe2O4晶体结构的影响
薛锐1,王永强1,2,臧萌1,陈曦1,刘敏敏1
(1中国石油大学(华东)化学工程学院,山东 青岛 266580;2中国石油大学(华东)石油石化污染物控制与处理国家重点实验室,山东 青岛266580)
通过溶胶凝胶-自蔓延燃烧法制备了纳米尖晶石CuFe2O4材料,采用TG-DTA、XRD、FTIR、N2-吸附脱附、SEM等技术对样品进行表征,探究溶胶凝胶-自蔓延燃烧法的机理及焙烧温度对尖晶石CuFe2O4材料晶体结构的影响。结果表明,前体溶胶中金属离子与柠檬酸—COOH形成三维网状的柠檬酸络合物,使金属离子分散于溶胶体系中;200~230℃时柠檬酸络合干凝胶自蔓延燃烧,大量络合物发生原位分解,放出大量的热,生成正式CuFe2O4尖晶石晶型,并有明显正四面体和正八面体亚晶格出现,晶粒尺寸约25.6nm;经400℃焙烧后,不完全燃烧形成的碳残留物分解,同时正式CuFe2O4尖晶石晶型发生转变,形成片状的Fe[CuFe]O4反式尖晶石晶型;随着焙烧温度升高,晶格尺寸从13.9nm增长到58.2nm,反式尖晶石晶型结晶程度逐渐增强,片状结构逐渐融合,形成层状整体,比表面积逐渐减小。
尖晶石;合成;纳米材料;粒子形成;焙烧温度
尖晶石结构通式为AB2O4,通常A位元素占据正四面体亚晶格,B位元素占据正八面体亚晶格。其中CuFe2O4尖晶石材料具有稳定的晶体结构,其化学稳定性好、结构强度大、结晶程度高,广泛应用于催化、陶瓷、光学元件、合金等领域。在CuFe2O4的制备过程中,焙烧温度对其晶体类型、微观结构和化学性能的影响较大[1]。RISTIĆ等[2]通过固相反应法制备了CuFe2O4尖晶石材料,当焙烧温度为400℃时,体系中没出现尖晶石结构;焙烧温度升高到800℃时,体系中开始出现正方晶系和立方晶系的CuFe2O4尖晶石结构,并伴有少量CuO和α-Fe2O3物种;当焙烧温度大于1000℃时,随焙烧温度升高,正方晶系尖晶石结构、CuO和α-Fe2O3晶体逐渐消失,立方晶系逐渐增加。固相反应法合成尖晶石材料时,原料混合不均,产物粒径较宽且有团聚现象,严重影响材料性能。LAOKUL等[3]通过溶胶-凝胶法制备CuFe2O4尖晶石材料,焙烧温度小于800℃时,体系以正方晶系的CuFe2O4尖晶石结构为主,且有少量CuO和α-Fe2O3;当焙烧温度大于800℃时,α-Fe2O3物种消失,CuFe2O4尖晶石晶型发生变化,形成立方晶系CuFe2O4尖晶石结构,此时CuFe2O4尖晶石材料的磁性明显增强。但溶胶-凝胶法的凝胶中存在大量微孔,在其干燥过程中络合物体系收缩,孔径继续缩小,使材料的比表面积大大减小。SAID等[4]通过共沉淀法制备了Cu-Fe材料,焙烧温度小于500℃时,体系中的结晶以CuO为主,当焙烧温度大于500℃时,出现了CuFe2O4尖晶石晶型和少量Fe2O3,且CuO含量明显减少。随焙烧温度升高,体系中尖晶石晶体的结晶程度逐渐增强,且该材料对CO氧化活性影响较大。共沉淀法制备尖晶石材料时,沉淀剂的加入会使沉淀局部浓度过高,产生团聚或局部沉淀,影响材料的结晶程度。不同的制备方法中,焙烧温度对CuFe2O4尖晶石材料的结晶类型及性能的影响显著。故分析焙烧温度对CuFe2O4尖晶石材料的影响是其制备过程中首要的考虑因素。
由于传统的制备方法存在较多问题,近年来溶胶凝胶-自蔓延燃烧法、微波法等新的材料制备方法逐渐被人们关注。其中溶胶凝胶-自蔓延燃烧法在溶胶-凝胶法的基础上,将干凝胶点燃,使其发生自蔓延燃烧。再经过焙烧,形成相应的晶体结构。该方法在形成凝胶时,络合剂与金属离子结合形成三维网状结构,可使金属离子分散于体系中,有利于材料中相应晶体的形成。同时避免了干凝胶直接干燥及高温焙烧引起的比表面积减小的缺点;另外,干凝胶一经点燃,整个体系便会在低温下发生自蔓延燃烧,节约制备成本。该方法是较有潜力的材料制备方法[5-8]。
本文采用溶胶凝胶-自蔓延燃烧法,在不同焙烧温度下制备CuFe2O4尖晶石材料,并通过TG-DTA、XRD、FTIR、N2-吸附脱附、SEM等技术分析该尖晶石材料在制备过程中的变化、干凝胶组成、晶体结构、孔性质、微观结构等,在探索溶胶凝胶-自蔓延燃烧法的反应机理的基础上,进一步分析不同焙烧温度对CuFe2O4尖晶石材料晶体结构的影响。
1 实验部分
1.1 CuFe2O4材料的制备
通过溶胶凝胶-自蔓延燃烧法,以柠檬酸作络合剂,制备纳米尖晶石型CuFe2O4材料。按照摩尔比n(Cu)∶n(Fe)=1∶2分别将Cu(NO3)2·3H2O和Fe(NO3)3·9H2O加入装有去离子水的烧杯中,搅拌使之溶解形成金属硝酸盐前驱溶液A。按照摩尔比n(金属离子)∶n(柠檬酸)=1∶1,将一水合柠檬酸加入装有去离子水的烧杯中,搅拌使之溶解形成柠檬酸前驱溶液B。将B液缓慢加入A液中,用氨水调pH至7±0.5,并在70℃±5℃下加热搅拌5h,待溶液呈溶胶状态。室温下静置2h,溶胶老化成凝胶。将凝胶在130℃下鼓风干燥12h,形成干凝胶。将干凝胶研成粉末,在干凝胶表面用木棒点燃,火焰从表面向内部发生自蔓延燃烧,放出大量气体,干凝胶燃烧形成蓬松的树状粉末。待自蔓延燃烧完成后,将燃烧产物冷却、研磨,分别于400℃、500℃、600℃、700℃马弗炉中焙烧2h,制成相应纳米尖晶石粉末。
1.2 CuFe2O4材料的表征
热分析(TG-DTA)采用HCT-2型差示扫描量热仪(北京恒久科学仪器厂),称取前体干凝胶3.75mg。测试温度为室温~1000℃;升温速率10℃/min;升温气氛为空气。
X射线衍射(XRD)分析采用X’PertPro MPD型X射线粉末衍射仪(荷兰Panalytical)。采用Ni金属为滤波片、CuKα为光源,管电压40kV,管电流50mA,扫描范围2θ=5°~75°,扫描速度为4°/min。
傅里叶变换红外光谱分析(FTIR)采用NEXUS-FTIR型傅里叶变换红外光谱仪(美国Nicolet),用KBr锭片法测定前体干凝胶样品,采用DTGS检测器,测试温度为室温,波数范围4000~400cm–1。
孔结构分析采用ASAP2020M型比表面积及微孔物理吸附分析仪(美国Micromeritics),样品先在300℃下抽真空处理5h,然后在液氮温度(–196℃)下进行N2吸附-脱附实验。
扫描电子显微镜分析(SEM)采用MERLIN Compact型超高分辨率场发射扫描电镜(德国Carl Zeiss Jena),镜筒内光轴采用InLens二次电子探头,加速电压15kV。
2 结果与讨论
2.1 CuFe2O4前体干凝胶的TG-DTA分析
图1为CuFe2O4前体干凝胶在20~1000℃的TG-DTA谱图。由图1可知,20~135℃段,DTA曲线缓慢上升,表明干凝胶在该温段持续吸热,前体干凝胶共失重0.21mg,占干凝胶样品的5.6%,可能是干凝胶中吸附水解析导致。135~200℃段,DTA曲线出现了矮且宽的吸热峰,质量损失0.34mg,失重10.17%,QI等[9]将该质量损失归结于结合水的解析和柠檬酸中羧基的缩合。200~230℃段,DTA曲线出现了高且窄的放热峰,前体质量损失2.34mg,失重约73.58%,此时硝酸根作氧化剂,柠檬酸作还原剂[10-11],前体干凝胶发生自蔓延燃烧,反应速率快,且放出大量的热,这些热量是前体干凝胶在低温下发生自蔓延燃烧的主要能量来源。
BIABANI-RAVANDI等[12]认为220~230℃温度下只能形成无定形或弱结晶的金属氧化物,但结合下文所示自蔓延燃烧产物的XRD谱图可以看出,此时正式尖晶石晶型的衍射峰非常尖锐,晶格尺寸为25.6nm,说明尖晶石结构已经形成,且结晶度较高。233~423℃段,DTA曲线出现了明显的放热峰,失重0.40mg。SUKPANISH等[13]认为柠檬酸络合物在自蔓延燃烧过程中发生原位分解,其中不完全燃烧形成的炭残留物在该温度段内燃烧。由下文XRD分析发现,该温段正式尖晶石晶型发生Jahn-Teller效应[14],形成反式Fe[CuFe]O4尖晶石结构,这也是样品在该温段放热的原因之一。423℃以后,TG-DTA曲线较平坦,没有明显热量变化,说明自蔓延燃烧产物在423℃后处于较稳定状态。

图1 CuFe2O4干凝胶的TG-DTA谱图
2.2 CuFe2O4的FTIR分析
图2为自蔓延燃烧前后CuFe2O4在4000~400cm–1的FTIR谱图,图3为干凝胶中柠檬酸络合物结构图。从图2可以看出,自蔓延燃烧前干凝胶在3149cm–1处,出现了羧基(—COOH)中C—H键的伸缩振动峰[15-16]。在1768cm–1处出现了该官能团中C==O键的伸缩振动峰[17-18],且在1384cm–1处出现了其C—O键的伸缩振动特征峰。同时-COOH中各吸收峰面积较大,结合图3络合物的结构图,发现柠檬酸络合物中有大量—COOH出现,说明该官能团在前体凝胶形成干凝胶时没有被分解。在3418cm–1处出现了少量结晶水的O—H键和大量柠檬酸络合后O—M键[19]的伸缩振动峰,在2858cm–1和2912cm–1处出现了—CH2中反对称的和对称的C—H键在碳链上的振动峰[20],可见前体溶液形成络合物时,金属离子取代—COOH中的H+,碳链连接形成了网状结构,与图3中络合物的结构一致。

图2 自蔓延燃烧前后CuFe2O4的FTIR谱图

图3 干凝胶中柠檬酸络合物结构图
该结构的出现,使金属离子分散于干凝胶络合物体系中,保证了自蔓延燃烧时金属粒子相互结合形成尖晶石结构。在指纹区出现了较多吸收峰,SANJAY等[21]认为,642cm–1和690cm–1分别为NO3–中N—O键的不对称和对称弯曲振动,851cm–1和1107cm–1分别为该键的水平摇动峰和对称伸缩振动峰[22-23]。NO3–吸收峰的出现,说明NO3–没有在加热搅拌、老化和干燥等过程中分解和转化,保证了自蔓延燃烧时氧化性物质存在。在3444cm–1处出现了NH4+中N—H键的伸缩振动峰,且在1619cm–1处为该键的弯曲振动峰,说明体系中部分NH4+在制备过程中没有分解。另外在2357cm–1和2334cm–1处出现了明显的吸收峰,MUSTAFA等[24]认为此峰为氰化物中C—N键的特征峰,可能是NO3–和NH4+中的N在加热、老化过程中与柠檬酸中的C结合形成了少量氰化物。
自蔓延燃烧后,柠檬酸络合物和硝酸根等物质没有出现,结合干凝胶的TG-DTA分析,说明自蔓延燃烧反应时,大量的柠檬酸络合物和硝酸根等物质通过自蔓延燃烧可以基本分解。燃烧产物分别在416cm–1和600cm–1处出现了明显的α吸收峰和β吸收峰。其中α峰为尖晶石晶体中Cu元素占据的正四面体亚晶格,β峰为尖晶石晶体中Fe元素占据的正八面体亚晶格[25]。LAOKUL等[3]认为由于金属氧化物中金属—氧键(M—O)键长不同,两个亚晶格的吸收峰出现在不同的波数,其中正四面体中Cu—O键长较短,正八面体中Fe—O键长较长,与本文吸收峰波数相对位置一致。
2.3 CuFe2O4的XRD分析

图4 不同焙烧温度CuFe2O4的XRD谱图
图4为不同焙烧温度CuFe2O4的XRD谱图。从图4可知,自蔓延燃烧后的产物在18.3°、30.17°、35.54°、37.18°、43.25°、53.60°、57.14°、62.75°分别出现了CuFe2O4(JCPDS 72-0010)立方晶系Fd-3m型晶群(111)、(220)、(311)、(222)、(400)、(422)、(511)、(440)晶面的特征峰。说明柠檬酸络合物干凝胶自蔓延燃烧后,已生成明显的尖晶石结构,这与LIU等[26]的研究结果一致。尖晶石晶型衍射峰相对尖锐,通过Scherre公式[27]计算其(311)晶面的晶格尺寸为25.6nm,说明自蔓延燃烧时,尖晶石结构结晶程度较高。此时Cu占据正四面体,Fe占据正八面体,为正式尖晶石结构,结合FTIR分析中正四面体和正八面体亚晶格的出现,进一步证明了正式尖晶石结构的产生。自蔓延燃烧产物经不同温度焙烧2h后,在18.34°、29.87°、30.75°、34.51°、36.04°、37.17°、41.43°、44.05°、52.48°、54.14°、54.99°、57.13°、58.174°、62.14°、64.06°、74.83°处均出现了CuFe2O4(JCPDS 72-1174)正方晶系I41/amd型晶群的(101)、(112)、(200)、(103)、(211)、(202)、(004)、(220)、(204)、(312)、(105)、(303)、(321)、(224)、(400)、(413)晶面。可见正式尖晶石结构CuFe2O4在高温和晶体场稳定能的作用下,产生了Jahn-Teller效应,A位上Cu2+的3d轨道发生畸变,由正四面体转向正八面体,Fe离子则分别以正四面体和正八面体存在,形成更稳定的反式尖晶石晶型,该晶型应写成Fe[CuFe]O4[14]。由图4可知,当焙烧温度升高时,反式尖晶石Fe[CuFe]O4晶体的衍射峰逐渐变尖锐,通过Scherre公式计算(211)晶面的晶格尺寸,400℃、500℃、600℃、700℃焙烧后晶格分别为13.9nm、32.9nm、44.5nm、58.2nm。可见随焙烧温度升高,反式尖晶石结晶程度逐渐增强,但均为纳米材料。
由自蔓延燃烧后产物的XRD谱图知,在43.25°、50.43°、74.18°处出现了Cu(JCPDS 04-0836)单质的特征峰,可能是自蔓延燃烧时,柠檬酸络合物分解反应速率较快,羧基结合的部分Cu没有进入尖晶石晶体,以Cu单质的形式存在于体系中。另外,在38.76°处出现了CuO(JCPDS 89-5899)的特征峰,说明还有少量无法进入尖晶石结构的Cu在高温下与O结合形成Cu-O物种。该产物经400℃焙烧2h后,大量Cu单质消失;在33.164°、35.64°、43.47°处出现了α-Fe2O3(JCPDS 84-0306)斜方六面体晶系的特征峰;在30.24°、62.93°处产生了少量的α-Fe2O3(JCPDS 39-1346)立方晶系的特征峰。说明在产生Jahn-Teller效应时,A位上的Cu形成正八面体,部分正八面体中的Fe没有及时转换成正四面体,形成Fe2O3物种析出尖晶石结构;此时,部分Cu单质在高温下被氧化,进入反式尖晶石晶型。当焙烧温度从500℃升高到700℃时,α-Fe2O3物种逐渐消失,LI等[28]认为,随着焙烧温度增加,Fe2O3逐渐转向反式尖晶石结构中。可见随着焙烧温度的增加,反式尖晶石晶型结晶程度逐渐增强。
2.4 CuFe2O4的孔结构分析
图5为CuFe2O4干凝胶前体自蔓延燃烧产物和不同焙烧温度CuFe2O4的N2等温吸附-脱附曲线。由图5可以看出,CuFe2O4干凝胶自蔓延燃烧后产物的N2等温吸附-脱附曲线在Ⅱ型和Ⅳ型曲线之间(BDDT分类),说明有大孔和介孔结构存在。可能是前体干凝胶在自蔓延燃烧时放出大量气体,使材料形成有大孔结构。当P/P0为0.45~1.0时,该曲线出现了明显回滞环,说明自蔓延燃烧后有大量介孔结构形成,N2在材料中发生了毛细凝聚现象。该回滞环属于H3型(IUPAC分类),说明该介孔结构分布不均匀,有较多片状颗粒出现[29-30]。结合TG-DTA、XRD和FTIR分析,自蔓延燃烧后仍有柠檬酸络合物燃烧的炭残留物,且此时已出现了明显的CuFe2O4尖晶石晶型,说明该介孔结构是由正式CuFe2O4尖晶石晶体和一些剩余络合物组成,与图6(a)中自蔓延燃烧后产物SEM分析结果一致。
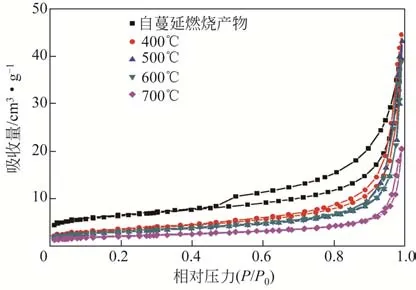
图5 不同焙烧温度CuFe2O4的N2等温吸附-脱附曲线
400~700℃焙烧2h后,样品的等温吸附曲线符合Ⅳ型。说明经焙烧后,该材料主要由介孔结构组成。进一步分析发现,该回滞环为IUPAC分类中的H4型,说明样品中同时出现了微孔和介孔结构,且含有狭窄的裂隙孔。随着焙烧温度增加,回滞环逐渐减小,且N2吸附量逐渐减小,计算400℃、500℃、600℃、700℃焙烧后样品的BET比表面积,分别为12.28cm2/g、10.424cm2/g、10.537cm2/g、7.190cm2/g。说明在焙烧过程中,裂隙孔结构和大孔结构随焙烧温度升高逐渐变小,比表面积明显减小。结合XRD分析,进一步说明反式尖晶石Fe[CuFe]O4晶体的结晶程度逐渐增强。

图6 不同焙烧温度CuFe2O4的SEM图
2.5 CuFe2O4的SEM分析
图6为不同焙烧温度CuFe2O4的SEM图。由图6(a)可知,CuFe2O4干凝胶自蔓延燃烧后,在样品表面出现了较多100nm左右的蘑菇状凸起,结合TG-DTA和孔结构分析,可能是自蔓延过程中干凝胶中柠檬酸络合物没有完全燃烧,局部剩余物存在于样品表面所致。但在该凸起中,仍可看到较多晶粒,且在产物表面也出现了大量晶粒,该晶粒在20~30nm,与XRD分析的正式CuFe2O4尖晶石晶型的晶格尺寸相近。400℃焙烧后,剩余柠檬酸络合物基本燃尽,样品主要由反式尖晶石结构组成,且出现了大量孔结构。同时样品表面出现了不完全结晶的片状晶粒,该晶粒与图6(a)中晶粒的形貌完全不同,结合XRD分析,正式尖晶石晶型在焙烧时产生了Jahn-Teller效应,形成不规则的Fe[CuFe]O4反式尖晶石晶粒。随着焙烧温度的升高,晶粒开始融合,大量晶体结构逐渐清晰,反式尖晶石晶体结晶程度逐渐增强。由图6(e)可知,当温度升高到700℃时,小的片状尖晶石晶体开始融合,片状结构融合成高度结晶的层状整体,这也是比表面积逐渐减小的原因。
3 结论
本文研究了溶胶凝胶-自蔓延燃烧法制备CuFe2O4材料中焙烧温度对晶体结构的影响,并对前体干凝胶和不同温度焙烧的样品进行了表征,主要得到以下结论:CuFe2O4前体形成柠檬酸络合物时,金属离子取代柠檬酸—COOH官能团中的H+,形成三维网状结构,使金属离子分散于干凝胶体系中,保证了自蔓延燃烧时金属粒子之间相互结合形成尖晶石结构。CuFe2O4前体干凝胶在200~230℃时发生自蔓延燃烧,柠檬酸络合物发生原位分解,此时已产生了正式CuFe2O4尖晶石晶型,并有明显正四面体和正八面体亚晶格出现,结晶程度较高。经过不同温度焙烧,自蔓延燃烧中不完全燃烧形成的炭残留物完全分解,同时正式CuFe2O4尖晶石晶型发生转变,A位上Cu2+的3d轨道发生正四面变形,转向正八面体中,Fe离子在正四面体和正八面体中均存在,形成更稳定的片状反式Fe[CuFe]O4尖晶石晶型。随着焙烧温度增加,α-Fe2O3物种逐渐进入反式尖晶石结构,尖晶石晶型的结晶程度逐渐增强,同时片状结晶逐渐融合,形成层状整体。
[1] 叶明泉,刘竹波,韩爱军. 溶胶凝胶自蔓延燃烧法制备钴蓝颜料[J]. 化工进展,2010,29(5):927-931.YIE M Q,LIU Z B,HAN A J. Sol-gel self-propagating combustion synthesis of cobalt blue pigment[J]. Chemical Industry and Engineering Progress,2010,29(5):927-931.
[2] RISTIĆ M,HANNOYER B,POPOVIĆ S,et al. Ferritization of copper ions in the Cu-Fe-O system[J]. Materials Science and Engineering:B,2000,77(1):73-82.
[3] LAOKUL P,AMORNKITBAMRUNG V,SERAPHIN S,et al.Characterization and magnetic properties of nanocrystalline CuFe2O4,NiFe2O4,ZnFe2O4powders prepared by the Aloe vera extract solution[J]. Current Applied Physics,2011,11(1):101-108.
[4] SAID A E A,ABD EL-WAHAB M M M,GODA M N. Synthesis and characterization of pure and (Ce,Zr,Ag) doped mesoporous CuO-Fe2O3as highly efficient and stable nanocatalysts for CO oxidation at low temperature[J]. Applied Surface Science,2016,390:649-665.
[5] ANSARI F,SOBHANI A,SALAVATI-NIASARI M. Facile synthesis,characterization and magnetic property of CuFe12O19nanostructuresviaa sol-gel auto-combustion process[J]. Journal of Magnetism and Magnetic Materials,2016,401:362-369.
[6] SHAHRI Z,SOBHANI A,SALAVATI-NIASARI M. Controllable synthesis and characterization of cadmium molybdate octahedral nanocrystals by coprecipitation method[J]. Materials Research Bulletin,2013,48(10):3901-3909.
[7] TORKIAN S,GHASEMI A,RAZAVI R S. Magnetic properties of hard-soft SrFe10Al2O19/Co0.8Ni0.2Fe2O4ferrite synthesized by one-pot sol-gel auto-combustion[J]. Journal of Magnetism and Magnetic Materials,2016,416:408-416.
[8] ANSARI F,SOBHANI A,SALAVATI-NIASARI M. Green synthesis of magnetic chitosan nanocomposites by a new sol-gel auto-combustion method[J]. Journal of Magnetism and Magnetic Materials,2016,410:27-33.
[9] QI L,YU Q,DAI Y,et al. Influence of cerium precursors on the structure and reducibility of mesoporous CuO-CeO2catalysts for CO oxidation[J]. Applied Catalysis B:Environmental,2012,119/120:308-320.
[10] LERTPANYAPORNCHAI B,YOKOI T,NGAMCHARUSSRIVICHAI C. Citric acid as complexing agent in synthesis of mesoporous strontium titanatevianeutral-templated self-assembly sol-gel combustion method[J]. Microporous and Mesoporous Materials,2016,226:505-509.
[11] HANKARE P P,SANADI K R,GARADKAR K M,et al. Synthesis and characterization of nickel substituted cobalt ferrite nanoparticles by sol-gel auto-combustion method[J]. Journal of Alloys and Compounds,2013,553:383-388.
[12] BIABANI-RAVANDI A,REZAEI M,FATTAH Z. Study of Fe-Co mixed metal oxide nanoparticles in the catalytic low-temperature CO oxidation[J]. Process Safety and Environmental Protection,2013,91(6):489-494.
[13] SUKPANISH P,LERTPANYAPORNCHAI B,YOKOI T,et al.Lanthanum-doped mesostructured strontium titanates synthesizedviasol-gel combustion route using citric acid as complexing agent[J].Materials Chemistry and Physics,2016,181:422-431.
[14] TASCA J E,QUINCOCES C E,LAVAT A,et al. Preparation and characterization of CuFe2O4bulk catalysts[J]. Ceramics International,2011,37(3):803-812.
[15] AHMED I S. A simple route to synthesis and characterization of CoAl2O4nanocrystallineviacombustion method using egg white(ovalbumine) as a new fuel[J]. Materials Research Bulletin,2011,46(12):2548-2553.
[16] KHALIL K M S,ELHAMDY W A,SAID A E A,et al. Porous LaFeO3/Silica Nanocompositesviasol-gel mixing involving citric acid[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2016,506:840-848.
[17] MI F-L,WU S-J,CHEN Y-C. Combination of carboxymethyl chitosan-coated magnetic nanoparticles and chitosan-citrate complex gel beads as a novel magnetic adsorbent[J]. Carbohydrate Polymers,2015,131:255-263.
[18] ESCOBAR J,BARRERA M C,GUTIÉRREZ A W,et al.Benzothiophene hydrodesulfurization over NiMo/alumina catalysts modified by citric acid. Effect of addition stage of organic modifier[J].Fuel Processing Technology,2017,156:33-42.
[19] TODOROVSKY D S,GETSOVA M M,VASILEVA M A. Thermal decomposition of lanthanum-titanium citric complexes prepared from ethylene glycol medium[J]. 2002,37(18):4029-4039.
[20] KURTAN U,TOPKAYA R,BAYKAL A,et al. Temperature dependent magnetic properties of CoFe2O4/CTAB nanocomposite synthesized by sol-gel auto-combustion technique[J]. Ceramics International,2013,39(6):6551-6558.
[21] SANJAY KUMAR D,ANANTHASIVAN K,VENKATA KRISHNAN R,et al. Bulk synthesis of nanocrystalline urania powders by citrate gel-combustion method[J]. Journal of Nuclear Materials,2016,468:178-193.
[22] YANG L,XI G,LIU J. MnZn ferrite synthesized by sol-gel auto-combustion and microwave digestion routes using spent alkaline batteries[J]. Ceramics International,2015,41(3):3555-3560.
[23] KHOSHBIN R,HAGHIGHI M,MARGAN P. Combustion dispersion of CuO-ZnO-Al2O3nanocatalyst over HZSM-5 used in DME production as a green fuel:effect of citric acid to nitrate ratio on catalyst properties and performance[J]. Energy Conversion and Management,2016,120:1-12.
[24] MUSTAFA G,ISLAM M U,ZHANG W,et al. Temperature dependent structural and magnetic properties of cerium substituted Co-Cr ferrite prepared by auto-combustion method[J]. Journal of Magnetism and Magnetic Materials,2015,378:409-416.
[25] BOBADE D H,RATHOD S M,MANE M L. Sol-gel auto-combustion synthesis,structural and enhanced magnetic properties of Ni2+substituted nanocrystalline Mg-Zn spinel ferrite[J].Physica B:Condensed Matter,2012,407(18):3700-3704.
[26] LIU T,WANG L,YANG P,et al. Preparation of nanometer CuFe2O4by auto-combustion and its catalytic activity on the thermal decomposition of ammonium perchlorate[J]. Materials Letters,2008,62(24):4056-4058.
[27] DERBAL A,OMEIRI S,BOUGUELIA A,et al. Characterization of new heterosystem CuFeO2/SnO2application to visible-light induced hydrogen evolution[J]. International Journal of Hydrogen Energy,2008,33(16):4274-4282.
[28] LI N H,LO S L,HU C Y,et al. Stabilization and phase transformation of CuFe2O4sintered from simulated copper-laden sludge[J]. Journal of Hazardous Materials,2011,190(1-3):597-603.
[29] CAO J,WANG Y,YU X,et al. Mesoporous CuO-Fe2O3composite catalysts for low-temperature carbon monoxide oxidation[J]. Applied Catalysis B:Environmental,2008,79(1):26-34.
[30] ZHAO S,LI K,JIANG S,et al. Pd-Co based spinel oxides derived from Pd nanoparticles immobilized on layered double hydroxides for toluene combustion[J]. Applied Catalysis B:Environmental,2016,181:236-248.
Effect of calcination temperature on crystal structure of CuFe2O4in sol-gel auto-combustion
XUE Rui1,WANG Yongqiang1,2,ZANG Meng1,CHEN Xi1,LIU Minmin1
(1College of Chemical Engineering,China University of Petroleum(East China),Qingdao 266580,Shandong,China;2State Key Laboratory of Petroleum Pollution Control,China University of Petroleum(East China),Qingdao 266580,Shandong,China)
The spinel CuFe2O4were prepared by sol-gel auto-combustion method. The mechanism of the preparation method and the effect of the calcination temperature on the structure of the CuFe2O4spinel crystal,were investigated by characterizing the samples with TG-DTA,XRD,FTIR,N2-adsorption desorption and SEM. It was found that the metal ions were evenly dispersed in the precursor sol system,when the citric acid complex compound was formed. The auto-combustion occurred at 200—230℃,and the citric acid complex compound decomposed by releasing lots of heat. The CuFe2O4formal spinel crystal with tetrahedron and octahedron sublattice was formed and the grain size was about 25.6nm. The carbon residue formed by incomplete combustion was decomposed,when calcinated at 400℃. The CuFe2O4formal spinel crystal transformed to lamellar trans-spinel crystal Fe[CuFe]O4at the same time. As the rising of the calcination temperature,the size of the lattice group increased from 13.9nm to 58.2nm,and the lamellar trans-spinel crystal gradually merged to entirety.
spinel;synthesis;nanomaterials;particle formation;calcination temperature
TQ426.6
A
1000–6613(2017)11–4182–07
10.16085/j.issn.1000-6613.2017-0445
2017-03-17;修改稿日期2017-07-23。
国家自然科学基金(21505156)及山东省自然科学基金(ZR2014EEM011)项目。
薛锐(1991—),男,硕士研究生。E-mail:haorenxuerui@qq.com。联系人王永强,博士,副教授。E-mail:wyqupc@163.com。
