铝合金表面预处理及其镀镍工艺优化
2017-11-01,,,
,, ,
(西北农林科技大学理学院,陕西 杨凌 712100)
铝合金表面预处理及其镀镍工艺优化
唐田田,党沛琳,赵倩,王芳
(西北农林科技大学理学院,陕西杨凌712100)
本实验分别采用打磨、混合碱处理、水合肼处理和电晕处理四种方式对AA5052铝合金基体表面进行预处理,探讨了预处理方式对铝合金表面润湿性和表面形貌的影响,并在此基础上对铝合金表面镀镍工艺参数进行优化。通过接触角仪和扫描电子显微镜对镀层润湿性以及表面形貌进行表征,得到最佳化学镀镍条件:镀液温度为75℃,镀液pH值在6.2~6.4之间,化学镀时间40min。通过循环伏安法(CV)探索得到了最佳电化学镀镍条件:电镀时间为240s,电流密度为5 mA/cm2,镀液温度为60℃。实验表明,该实验条件下可以得到理想的镍镀层,且该方法可以广泛应用于其他相关的材料研究领域。
预处理; 化学镀镍; 铝合金; 电沉积
1 引 言
铝合金与铜、钢铁等常见金属材料相比,具有质轻、比强度高、塑性好、成型性好、硬度小、导热性和导电性良好等特点,是一种综合性能优良的有色金属材料,因而被广泛应用于汽车、航空航天、电子通讯、机械制造以及化学工业等领域[1-4]。然而铝合金在腐蚀介质中易受到腐蚀从而限制了它的应用。铝合金的腐蚀防护问题已得到了广泛的关注并发现了很多行之有效的方法,例如用铬酸盐钝化,磷酸盐转化以及利用表面复合涂层技术处理等[5-9]。
金属表面复合涂层技术是指利用表面涂层工艺方法,如电镀、化学镀、阳极氧化、气相沉积、热化学反应法、溶胶-凝胶法[10-14]等技术,在金属表面形成一层或数层具有复合材料结构和性质,并与金属表面结合良好的薄膜[15]。其中,最常用的方法有化学镀和电镀。化学镀无须电流通过而是借助还原剂在溶液中发生氧化还原反应,使金属离子还原沉积在金属表面上的一种镀覆方法,是一种可控制的、自催化的化学还原过程。化学镀可镀铜、钴、金、银等金属,而化学镀镍是化学镀工业中发展最快的行业。它以其优异的性能被广泛应用于石油、化工、能源、机械、电子信息、航空航天及军事装备等领域,并向着多功能性和应用性的方向发展。金属表面复合涂层作为新材料研究的一个重要方向,具有广阔的应用前景[16]。
然而金属基底表面一般都覆盖有一层氧化膜,直接沉积薄膜的效果并不理想,因此需要对基底表面进行预处理以除去氧化膜。不同的预处理方法对基底表面性能有很大的影响,进而也会影响沉积层的性质,目前尚没有文章系统地介绍不同预处理方法对沉积薄膜效果的影响。
本文以AA5052铝合金为基底,通过抛光剂打磨,混合碱处理,水合肼处理,电晕处理四种方法对其进行预处理,探讨了四种预处理方法对铝合金表面润湿性和表面形态的影响,在此基础上对铝合金表面镀镍工艺参数进行优化,并对处理后表面进行表征分析,探索铝合金表面最佳镀镍条件。
2 实 验
2.1材料与试剂
铝合金(型号:AA5052;规格:50×20×0.3mm;组分含量:Cu:0.1%,Si:0.2%,Fe:0.4%,Mn:0.1%,Mg:2.8%,Zn:0.1%,Cr:0.3%,其它组分:0.15%);镍片(99.98wt.%;规格:50×20×0.3mm);石墨电极(50×30×3mm)等。无水碳酸钠、磷酸钠、碱式碳酸镍、柠檬酸、硫化铵、次磷酸钠、氨水、氯化镍、氯化钴、盐酸乙二胺、硼酸、氯化钠均为分析纯,6-N-烯丙基-N-1,1,2,2-四氢氟代癸烷基胺-1,3,5-三嗪-2,4-硫醇单钠盐(AF17N)为自合成[17],结构式如图1所示。

图1 AF17N的分子结构Fig.1 Molecular structure of AF17N
2.2前处理方法
基底为AA5052铝合金,对其进行不同的前处理,方法如下:
(1)金相抛光剂打磨法:将铝合金依次用5μm、2.5μm和0.5μm的金相抛光剂打磨,去离子水冲洗后丙酮超声并烘干。
(2)电晕处理法:对丙酮超声处理后的铝合金基体进行电晕处理,正反两面分别进行。电晕时间为20s。根据电极放电火花的均匀程度,放电工作电压控制在50V,电流控制在(1.90±0.1)A。
(3)混合碱处理法:称取1.00g无水碳酸钠固体,1.00g磷酸钠固体置于100mL烧杯中,加入100mL蒸馏水用玻璃棒搅拌后置于磁力加热搅拌器上加热至60℃,将丙酮超声处理后的铝合金放入其中处理1.5min。
(4)水合肼处理法:配制体积分数为5%的水合肼溶液,置于磁力加热搅拌器上加热至55℃,将丙酮超声处理后的铝合金放入其中处理15s。
2.3化学镀镍
在优化进行前处理工艺的基础上,对合金表面进行化学镀镍。化学镀镍液组成为:10g/L NiCO3·2NiO2H2·4H2O,5g/L C6H7O8·H2O(柠檬酸),0.001g/L(H4N)2S,20g/L NaH2PO2·H2O,30mL/L NH3·H2O。实验采用单因素法对化学镀时间、镀液温度以及pH值进行了探究。
2.4电化学镀镍
在化学镀镍的基础上,再通过CHI 660C电化学工作站进行电镀镍。采用三电极体系,阳极为高纯镍片(99.98wt.%),阴极为化学镀镍后的AA5052铝合金,参比电极选用饱和甘汞电极(SCE)。电镀液组成为:11.3g/L NiCl2·6H2O,0.8g/L CoCl2·6H2O,10g/L EDA·2HCl,1.5g/L H3BO3。实验采用正交法对电镀液温度、电镀时间以及电流密度进行了探究。
2.5化学修饰
为了提高金属的防腐能力,电镀镍后需在金属表面修饰低表面能物质6-N-烯丙基-N-1.1.2.2-四氢氟代癸烷基胺-1,3,5-三嗪-2,4-硫醇单钠盐(简称AF17N)。将电镀后的金属于室温下浸泡在1mmol/L的AF17N溶液中2h,并于150℃的烘箱中固化15min。
2.6测定与表征
使用HARKE-SPCAX1系列静态接触角仪测量蒸馏水在不同试样表面的接触角,每个试样测5个点并取其平均值,所使用的蒸馏水滴的体积均为1 μL。利用场发射扫描电子显微镜(FESEM)观察预处理铝合金表面及化学镀镍层的表面形态。
通过CHI 660C电化学工作站进行电化学测试,在0.1mol/L NaOH溶液中对AA5052基体表面复合薄膜进行致密性测定。采用三电极体系,参比电极为饱和甘汞电极,辅助电极为不锈钢片,扫描范围为-0.7~0.7V,扫描速率为20mV/s。所有电化学测试均在相同条件下重复进行三次以保证其准确性。
3 结果与讨论
3.1不同前处理对接触角及表面形貌的影响
借助静态接触角仪测定了4种不同预处理后铝合金表面的接触角,结果如图2。由图2可以看出,铝合金经不同前处理后表面接触角大小顺序为:电晕(14.4°)<碱处理(24.2°)<打磨(51.1°)<肼处理(89.3°)<空白(91.6°)。

图2 不同预处理方法对铝合金表面接触角的影响Fig.2 Effect of different pretreatments on the contact angle of AA5052 aluminum alloy
经电晕处理的铝合金表面接触角最小,铝合金表面经电晕放电处理后,通过等离子体中粒子流与中性粒子流碰撞以及活性离子的辐射,金属表面分子被氧化和极化。同时离子电击并侵蚀表面,增加了表面的附着力,从而使铝合金表面呈现出良好的亲水性,为镍离子提供了结合位点,并为铝合金表面形成致密的镍镀层提供了条件,电晕处理后的金属表面均匀完好(图3(a))。经碱处理后的铝合金表面接触角降低值仅次于电晕法,由图3(b)可以看到铝合金被混合碱腐蚀后,表面粗糙度增加,这种凹凸不平的粗糙结构有利于基底与化学镀镍层发生物理啮合作用,有利于镍镀层的形成。打磨处理后表面接触角降低较多,表明抛光剂打磨后的表面粗糙度增加,但均匀程度欠佳(图3(c))。肼处理后的铝合金表面接触角较空白下降最少,并且该操作过程复杂且温度控制范围较严格,温度一旦超过60℃,样品表面可观察到颜色不均匀的痕迹,由图3(d)可知样品表面也有一定程度的破坏。因此,与肼处理和打磨处理相比,推断电晕处理和碱处理后的铝合金表面化学镀镍效果会更佳。为了保证实验结果的统一性,后续探索中均采用碱处理作为样品的前处理方式。

图3 不同前处理后铝合金的表面形貌图(a) 电晕; (b) 碱处理; (c) 打磨; (d) 肼处理Fig.3 SEM images of AA5052 surface for different pretreatment methods (a) corona treatment; (b) alkali treatment; (c) polish; (d) hydrazine hydrate treatment
3.2化学镀镍液温度、pH值以及化学镀时间对镍镀层的影响

图4 不同镀镍温度下铝合金的表面形貌;右上角为该温度对应的接触角图 (a) 65℃; (b) 75℃; (c) 85℃; (d) 95℃Fig.4 SEM and corresponding contact angle images of the samples after nickelplating under different temperature (a) 65℃; (b) 75℃; (c) 85℃; (d) 95℃
3.2.1镀液温度 化学镀镍层的沉积速度取决于镀液温度,故酸性化学镀镍都在较高温度下进行。为了确定最佳化学镀镍液温度,控制时间和pH值不变,取镀液温度分别为:65、75、85及95℃进行试验。图4为在不同镀镍温度下铝合金表面镍镀层的表面形貌图。由图可以看出,温度为65℃时,镍颗粒直径较小且分布不连续,表面镍层覆盖率低且不完整;温度为75℃时,镍颗粒大小均匀并将铝合金表面完全覆盖,镍层光亮均匀;温度升高至85℃时,镍颗粒直径增大,但由于温度过高导致镀速过快,使得表面镍层疏松不均匀;温度继续上升至95℃时,镍颗粒大小不均,镍层的结合力与光亮度均较差。综合微观形貌与表观分析,确定化学镀镍最佳温度为75℃。
图5为镀镍温度对样片表面接触角的影响,由图5可以看出镀液温度对样片接触角影响显著。接触角的均值越大,镀层表面疏水性越强,意味着样品对空气中的水分及腐蚀性粒子的阻挡能力越强,对基底起到的防腐蚀效果越好。随着温度的升高,样片表面接触角先增大再减小,于75℃时接触角达到最大值122.3°,呈现疏水性。温度继续升高,接触角持续下降。

图5 化学镀镍温度对样片表面接触角的影响Fig.5 Variation of contact angles of the sample surface with different nickel plating temperature

图6 不同镀镍时间下铝合金的表面形貌;右上角为该时间对应的接触角图 (a) 30min; (b) 35min; (c) 40min; (d) 45minFig.6 SEM and corresponding contact angle images of the samples after nickelplating under different time (a) 30min; (b) 35min; (c) 40min; (d) 45min
3.2.2化学镀时间 为了确定最佳化学镀时间,控制温度75℃和pH值不变,设定化学镀时间分别为:30、35、40及45min进行实验。图6为不同化学镀时间下铝合金表面镍镀层的表面形貌图,由图可以看出从30min开始,铝合金表面已完全被镍颗粒覆盖,但镍颗粒大小不均,镍镀层较薄无光亮。化学镀时间为40min时,金属表面镍颗粒均匀致密,此时镀层光亮、均匀、完整,形成了结合较好的连续镀层。化学镀时间增至45min时,部分镍颗粒直径增大,大小不均,同时沉积的镍层过厚出现鼓包现象,结合力变差。综合微观形貌与表观分析,确定化学镀镍最佳时间为40min。
图7为镀镍时间对样片表面接触角的影响曲线。由图可以看出,化学镀时间对样片接触角影响同样显著。随着化学镀时间的增加,样片表面接触角逐渐上升,在40min时达到最大值120.5°,呈现疏水性。此后化学镀时间继续增加,接触角基本维持不变。

图7 化学镀镍时间对样片表面接触角的影响Fig.7 Variation of contact angles of the sample surface with different nickel plating time

图8 不同pH值下化学镀镍后铝合金的表面形貌;右上角为该pH对应的接触角图 (a) 5.0; (b) 5.5; (c) 6.0; (d) 6.5Fig.8 SEM and corresponding contact angle images of the samples after nickelplating under different pH (a) 5.0; (b) 5.5; (c) 6.0; (d) 6.5
3.2.3化学镀液pH值 为了保证镀液稳定、镀层质量及沉积速率,镀液的pH值应控制在6.5以下,否则镀液内的Ni2+会发生水解而生成Ni(OH)2沉淀。为了确定镀液最佳pH值,控制温度和化学镀时间不变,镀液pH值分别为:5.0、5.5、6.0、6.5。图8为不同pH值时所制备镍镀层的表面形貌图。由图可知,在探讨的pH值范围内,镍颗粒均将金属表面完全覆盖,当pH值为6.0和6.5时,镍颗粒大小更为均匀。表观上,镍镀层均完整致密,结合力较好,而pH值为6.0和6.5的镀层较其余两组更加均匀光亮。综合微观形貌与表征分析,确定化学镀镍最佳pH值在6.0~6.5之间。
图9为镀镍pH值对样片表面接触角的影响曲线。由图可以看出,在一定范围内镀镍液pH值对样片接触角影响有限,随着镀液pH值的增加,样片表面接触角略微增大,在pH值为6.0~6.5时达到最大值(116.7°)并趋于稳定。在探讨的pH值范围内,样片表面接触角均呈疏水性。

图9 化学镀镍液pH值对样片表面接触角影响Fig.9 Variation of contact angles of the sample surface with different nickel plating pH
3.3电镀镍的条件优化
化学镀后实施电镀处理。实验对电镀液温度、电镀时间以及电流密度三个主要影响因素进行了正交试验,结果如表1所示。

表1 3因素3水平正交试验设计
由于不考虑几个因素之间的交互作用,实验采用L9(34),9次试验后的结果如表2所示。由于得到的镀层质量均较好,实验以循环伏安法(CV)测得的数学积分面积为指标来分析实验结果(如图10所示)。通过循环伏安法考察了不同电沉积条件下AA5052基体表面复合镀层的致密性,并与未修饰AF17N的样片进行对比。由CV图可以看到未经AF17N修饰的样片存在明显的氧化峰(0.37V)和还原峰(0.3V),而经过AF17N修饰的正交组其氧化峰和还原峰均消失,说明实验中制得的复合薄膜具有较强的钝化作用,可以有效阻碍AA5052基体表面电子的转移,从而抑制其表面氧化还原反应的进行。在正交试验组中不同条件下制备的样片其电流变化均不一致,循环伏安曲线所围成的面积也不尽相同。当施加一定范围的电压时,AA5052基体表面的电流变化越不明显,循环伏安曲线所围成的数学积分面积越小,表明经修饰后的镍镀层可以更加有效地抑制AA5052铝合金被氧化或腐蚀。
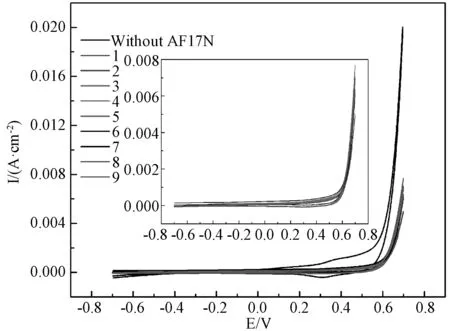
图10 不同电镀条件下制备的样片在0.1mol/L NaOH溶液中的CV曲线图Fig.10 Cyclic voltammetry curves of the samples in 0.1mol/L NaOH solution under different electroplating conditions

RunsABCCVMathematicArea11111.773×10-421222.164×10-431332.342×10-442132.004×10-452212.302×10-462322.528×10-473121.356×10-483231.141×10-493311.603×10-4K16.2795.1335.715K26.8345.8805.771K34.3736.4736.000k12.0931.7111.905k22.2781.9601.934k31.4382.1582.000R0.8400.4470.095
根据表2数学积分面积和极差值可以看出,用循环伏安曲线的致密性结果作为试验指标时,各因素对应的极差表明电镀液温度对镀层性能影响最显著,电镀时间影响次之,电流密度影响最小。通过该试验指标得出的电化学镀镍最优条件为:电镀液温度60℃,电镀时间240 s,电流密度5 mA/cm2。
4 结 论
对AA5052型铝合金最优的前处理方式为电晕处理和混合碱处理。通过单因素法确定的最佳化学镀镍条件是:镀液温度为75℃,化学镀时间为40min,镀液pH值在6.2~6.4之间。通过正交试验确定的最佳电镀镍条件是:电镀液温度为60℃,电镀时间为240s,电流密度为5mA/cm2。此工艺制备的镍镀层均匀致密、光亮完整、结合力强,经过AF17N修饰后耐腐蚀性显著提高,可以更加有效地抑制AA5052铝合金被氧化或腐蚀。
[1] F. Wang, H. Luo, et al. Preparation of Superhydrophobic Polymeric Film on Aluminum Plates by Electrochemical Polymerization[J]. Molecules, 2009, 14(11): 4737~4746.
[2] J.M.Hu,L. Liu, J. Q. Zhang, C.N.Cao. Effects of Electrodeposition Potential on the Corrosion Properties of Bis-1,2-[triethoxysilyl] Ethane Films on Aluminum alloy[J]. Electrochimica Acta, 2006, 51(19): 3944~3949.
[3] 余美琼. 铝及铝合金表面处理技术新进展[J]. 化学工程与装备, 2008, (06): 84~95.
[4] 胡吉明, 刘倞, 张金涛,等. 铝合金表面BTSE硅烷化处理研究[J]. 金属学报, 2004, 40(11): 1189~1194.
[5] N. Tang, W.J. van Ooij, G. Gorecki. Comparative EIS Study of Pretreatment Performance in Coated MetalsProg[J]. Progress in Organic Coatings, 1997, 30(4): 255~263.
[6] A.M. Cabral, W. Trabelsi, et al. The Corrosion Resistance of Hot Dip Galvanised Steel and AA2024-T3 Pre-Treated with Bis-[triethoxysilylpropyl] Tetrasulfide Solutions Doped with Ce(NO3)3[J]. Corrosion Science, 2006, 48(11): 3740~3758.
[7] T. Prosek, D. Thierry. A Model for the Release of Chromate from Organic Coatings[J]. Progress in Organic Coatings, 2004, 49(3): 209~217.
[8] J. Sinko. Challenges of Chromate Inhibitor Pigments Replacement in Organic Coatings[J]. Progress in Organic Coatings, 2001, 42(3-4): 267~282.
[9] F Deflorian, S Rossi, L Fambri, PL Bonora. Study of the Corrosion Behaviour of Phosphatized and Painted Industrial Water Heaters[J]. Progress in Organic Coatings, 2001, 42(1~2): 65~74.
[10] 易笃钢, 田宗军, 沈理达,等. 铝合金表面喷射镀镍的结合力与硬度[J]. 材料科学与工程学报, 2013, 31(06): 877~880.
[11] 闫洪, 杜强, 徐亚飞,等. 全光亮和高耐蚀性非晶态合金层的制备新工艺[J]. 材料科学与工程学报, 2003, 21(03): 371~374.
[12] W. Liu, Y. Luo, L. Sun, R. Wu, H. Jiang, Y. Liu. Fabrication of the Superhydrophobic Surface on Aluminum Alloy by Anodizing and Polymeric Coating[J]. Applied Surface Science, 2013, (264): 872~878.
[13] 宋瑞利, 刘平, 张柯,等. 铜箔表面化学气相沉积少层石墨烯[J]. 材料科学与工程学报, 2016, 34(1): 96~100.
[14] S. Lu, Y. Chen, W. Xu, W. Liu. Controlled Growth of Superhydrophobic Films by Sol-Gel Method on Aluminum Substrate[J]. Applied Surface Science, 2010 (256): 6072~6075.
[15] 宣天鹏. 材料表面功能镀覆层及其应用[M]. 北京: 机械工业出版社, 2008, 7~16.
[16] 肖蔚鸿. 非金属材料表面金属化的方法[J]. 矿产保护与利用, 2004, (3): 28~31.
[17] K. Mori, H. Hirahara, Y. Oishi, N. Kumagai. Effect of Triazine Dithiols on the Polymer Plating of Magnesium Alloys[J]. Materials Science Forum, 2000, (350~351): 223~234.
DifferentPretreatmentsandOptimizationofElectrolessNickelPlatingonAluminumAlloy
TANGTiantian,DANGPeilin,ZHAOQian,WANGFang
(Collegeofscience,NorthwestA&Funiversity,Yangling712100,China)
We studied the effects of surface morphologies and wettabilities with different pretreatments (polishing treatment, mixed alkali treatment, hydrazine hydrate treatment, corona treatment) on AA5052 aluminum alloy surface and finalize the optimum pretreatment method. On the basis of comparison tests, the optimum process conditions of nickel plating on AA5052 surface were determined. The surface morphologies and wettabilities were characterized by using scanning electron microscopy (SEM) and telescopic goniometer. The results show that the best electroless nickel plating conditions in this study are as follows: the temperature of the plating bath is 75℃, the pH value is 6.2-6.4 and the plating time is 40 minutes. By cyclic voltammetry, the best nickel plating was obtained under the conditions of 240s nickel plating time, current density of 5 mA/cm2at 60℃. The results show that an ideal nickel plating can be prepared under the optimum experiment conditions, and this method is also meaningful for other relevant material engineering fields.
pretreatment; electroless nickel plating; aluminum alloy; electrodeposition
TG174.4
A
10.14136/j.cnki.issn1673-2812.2017.05.026
2016-06-02;
2016-08-16
国家自然科学基金资助项目(21203152)
唐田田(1991-),女,硕士研究生,研究方向为金属材料的表面改性。E-mail: tangtiantian1020@foxmail.com。
王 芳,副教授,博士生导师。E-mail: wangfang4070@nwsuaf.edu.cn。
1673-2812(2017)05-0820-06
